Здравствуйте, дорогие читатели. Что такое гиперплазия молочной железы ? Это исключительно женское заболевание или встречается оно у сильной половины человечества? Насколько это серьезно и страшно? Этой теме и посвящена наша статья.
Hyperplasia — что это такое ? Медицинский термин латинского происхождения, первая его часть нам знакома («гипер» — «сверх»), вторая же «плазия» означает «формирование» или «образование». И означает, что клетки грудной железы активны, больше чем нужно, размножаются и создают новые тканевые структуры.
На начальном этапе это доброкачественные изменения фиброзной, жировой или железистой ткани . Но доброкачественная гиперплазия может переродиться в рак. Чаще с такими изменениями бюста сталкиваются женщины менопаузального возраста. Но не исключено начало процесса пролиферации и в юном возрасте.
Гиперплазия — это увеличение числа структурных элементов клеток или тканей. Есть еще один похожий термин, с которым пациенты сталкиваются нередко — гипертрофия. Это патологическое состояние, при котором железы также будут увеличиваться в размере, но в этом случае за счет увеличения размеров клеток и тканей.
Еще вы можете спросить аденоз — это тоже самое, что и гиперплазия? Если речь идет о пролиферации железистых тканей молочной железы, то да и это всего лишь один из ее видов.
Встречается патология у 8 из 10 женщин, у мужчин , у детей. Это действительно «женская» болезнь, мужчины болеют в исключительных случаях. Но болеют.
Пролиферация тканей грудных желез считается предвестницей рака (по-крайней мере, атипичная) у 10% пациенток с таким диагнозом через десять лет диагностируется рак. Через 25 лет этот показатель достигает 30%.
Если при рассмотрении тканей под микроскопом лаборант медицинской лаборатории может увидеть не только рост количества клеток, но и их структурные изменения. При структурных изменениях (в цитоплазматической сети, митохондриях) говорят о внутриклеточной гиперплазии или регенерации
Если же речь идет о количественном росте клеток (в результате размножения делением) — о пролиферации. Избыточная пролиферация — это и есть причина гиперплазии тканей. А вот факторы подталкивающие клетки к пролиферации разнообразны:
- нервные расстройства (депрессия, неврозы);
- постоянное или интенсивное воздействие стрессоров;
- постоянный контакт с антисептиками и бытовой химией;
- экологически неблагоприятная обстановка;
- генетическая предрасположенность;
- травмы;
- длительный неконтролируемый прием ОК (гормональные таблетки для контрацепции);
- эндокринные патологии.
Некоторые специалисты считают, что длительное (до 3-лет и более) кормление ребенка грудью может стать причиной пролиферации клеток молочной железы.
Заподозрить пролиферативные изменения можно по косвенным признакам:
- боль (ее может и не быть);
- нарушение менструации;
- выраженный предменструальный синдром;
- деформация желез;
- узелки при прощупывании;
- выделение секрета из соска.
Эти признаки сопровождают большинство проблем с грудью и требуют консультации маммолога.
Классифицировать болезнь можно по нескольким критериям:
- степени пролиферации;
- по виду разрастающейся ткани;
- по локализации очага.
Если пролиферация тканей носит гормонозависимый характер, болезнь называют мастопатией или дисгормональной гиперплазией, или болезнью Реклю (Шиммельбуша), фиброаденоматозом, склерозирующим аденоматозом бюста.
Гормональная пролиферация или фиброзно-кистозная болезнь может протекать в узловой, очаговой или диффузной форме.
Узловая форма предполагает образование одного реже нескольких ограниченных округлых, эластичных «шариков» внутри железы. Для очаговой формы характерно образование нескольких не сливающихся очагов. При этой форме есть риск малигнизации. При диффузной форме очаги буквально «пропитывают» ткани. Между здоровыми участками обнаруживаются мелкие, размером с зернышко очажки гиперплазии.
Пролиферативные изменения характеризуются 3 составляющими:
- интенсивным ростом соединительной ткани;
- очагами роста рыхло расположенных железистых клеток, окруженных стромой;
- образованием мелких кист, заполненных прозрачным секретом.
Гистологически мастопатия протекает в кистозной , фиброзной, железистой и папиллярной ( внутрипротоковой ) форме.
По классификации американских проктологов гиперпластические изменения делят на 5 степеней:
- 1 степень — норма;
- 2 степень — гиперплазия;
- 3-4 степень — атипичная гиперплазия;
- 5 степень — карцинома на месте (in situ).
Атипичная гиперплазия (атипия) опасное изменение тканей. Клеток не только больше по количеству, но и сами они изменены. При этой форме болезни возрастает риск озлокачествления очага.
По виду активно растущей ткани изменения в грудной железе делят на жировую, железистую и стромальную гиперплазию.
Жировая пролиферация — это активное деление адипоцитов (структурных единиц жировой ткани). Разрастание обычно диагностируется как плотный шарик. При биопсии в материале обнаруживают капельки жира
Железистые образования подвижны, эластичны, похожи на сплюснутый шар (диск). Их не сразу выявляют при пальпации и они далеко не всегда сопровождаются болью и тем более деформацией бюста.
Стромальное разрастание знакомо женщинам в посменопаузе. Это разрастание соединительной (фиброзной) ткани , из которой формируются связки, фасции. Морфологическим признаком стромальных изменений является обнаружение миофибропластов в очаге.
Выделяют гиперактивный рост протоков и долек . Для дольковой формы характерно избыточное деление клеток эпителия , выстилающего альвеолы. При этом просветы альвеол сужены (облитерированы), но проходимы. Этим (проходимость протока) дольковая гиперплазия отличается от рака долек на месте (in situ). Ведущим морфологическим признаком этого типа пролиферации считается клеточный полиморфизм. При изучении биоматериала обнаруживают 2 типа клеток по цвету цитоплазмы:
Они как будто налазят друг на друга. Для дольковой формы изменений характерно наличие множественных очагов (мультицентричность).
Для пролиферации протокового этителия характерно обнаружение разного типа клеток в очаге (сосочковые, железистоподобные и другие).
Важным диагностическим критерием протоковой гиперплазии считается обнаружение в биоматериале не только эпителиальных клеток, но и миоэпителиальных. Причем при наличии миоэпителия процесс считается доброкачественным. Увеличение клеток в млечных протоках идет лавинообразно, но если диагноз поставлен на ранних этапах, лечение не представляет труда. И может остановиться на консервативных мерах.
Гиперплазия грудных желез или развитие железистой ткани по женскому типу у мальчиков и мужчин называется гинекомастией. Гинекомастия новорожденных — припухлость желез у ребенка до года, не зависимо от пола, связана с избытком материнских гормонов в крови новорожденного или младенца. Лечения не требует.
У девочек бывает раннее телархе (рост груди) в допубертатном возрасте, связано это с приемом продуктов питания, содержащих гормоны, чувствительностью к собственным гормонам и обычно это наследственное явление. Если на УЗИ развитие железы не имеет отклонений, лечение не требуется.
У мальчиков в возрасте 12-17 тоже могут быть проблемы с грудной железой. Она увеличивает, припухает, из соска сочится секрет. Это связано с пиковыми концентрациями эстрадиола в крови, которые накапливаются раньше тестостерона, и превышают содержание мужского полового гормона в 30 раз. Чуть более четверти случаев подобного увеличения грудной железы у юношей — это ювенильная гиперплазия или гинекомастия — лечения не требует.
Истинная гиперплазия у мальчиков и у мужчин или гинекомастия связана с гормональными сбоями, лечится оперативно.
При диагностике данного заболевания врач осматривает и ощупывает грудь, назначает анализ крови (общий и биохимический), и аппаратные исследования (КТ, МРТ, рентгенографию, УЗИ). При необходимости — забор биоматериала из очага пролиферации.
Иногда в результате УЗИ вы можете получить описание изменений, где наряду с обнаружением очагов пролиферации врач-диагност определяет увеличенный лимфоузел ( гиперплазию аксиллярных лимфоузлов). Если рост очага пролиферации не наблюдается и размер лимфоузла в пределах нормы, ничего страшного в этом нет. Визуализируется он при онкозаболеваниях, в том числе доброкачественных. Лимфоидная ткань реагирует на изменения молочной железы.
Лечение болезни может быть консервативным и оперативным. В зависимости от формы гиперплазии и опасности ее перерождения в рак.
На этом мы прощаемся с вами. И надеемся, вы поделитесь статьей с друзьями через социальные сети.
источник
В Европейской клинике ведёт консультативный приём и выполняет операции известный российский хирург-маммолог, доктор медицинских наук Сергей Михайлович Портной (автор более 300 печатных работ, член правления Российского общества онкомаммологов, автор трех патентов на изобретения).
Сергей Михайлович выполняет весь объем оперативных вмешательств на молочной железе, включая органосохраняющие и реконструктивные пластические операции.
До 25% всех случаев рака у женщин приходится на рак молочной железы (РМЖ). Часто его возникновению предшествуют доброкачественные изменения в молочной железе — мастопатия. У мастопатии есть много синонимов: фиброзно-кистозная болезнь, мастодиния, доброкачественная дисгормональная дисплазия, доброкачественная гиперплазия, аденоз и др.
Мастопатия — доброкачественный процесс, при котором в ткани молочной железы нарушается правильное соотношение между клетками железистого эпителия и соединительной ткани. Незначительные изменения обнаруживаются также на уровне строения клеток.
По статистике, женщины с доброкачественной дисплазией молочных желез заболевают РМЖ в 3–4 раза чаще, чем здоровые. Если же процесс сопровождается размножением клеток эпителия с образованием узелков, то риск развития рака увеличивается в 30–40 раз.
До 60–90% женщин репродуктивного возраста имеют те или иные признаки мастопатии. Основная причина развития этого заболевания — гормональный дисбаланс. При доброкачественной дисплазии отмечается избыток эстрогенов на фоне дефицита прогестерона. К такому дисбалансу приводят:
- хронические гинекологические заболевания;
- ожирение;
- некоторые общесоматические болезни (сахарный диабет, гипотиреоз, артериальная гипертензия и др.);
- отдельные методы контрацепции;
- нарушения менструального цикла;
- постоянный стресс и др.
Различают диффузную и узловую мастопатию. Для диффузной формы характерно равномерное разрастание эпителия и соединительной ткани в молочной железе. При узловой мастопатии обнаруживают один или несколько уплотненных узелков с четкой границей — это результат местного разрастания фиброзной ткани и расширения протоков. По данным исследований, узловая мастопатия, будучи локальной формой заболевания, протекает легче, кроме того, она более благоприятна в плане прогноза.
При мастопатии на микроскопическом уровне обнаруживается увеличение количества и размеров клеток эпителия — это явление называют гиперплазией. Различают дольковую (разрастание долек молочной железы) и протоковую (разрастание эпителия протоков) гиперплазию. Если при гиперплазии изменяется также форма клеток, ее расценивают как атипичную и склонную чаще других перерождаться в рак.
Аденоз молочных желез — это форма мастопатии с преобладанием гиперплазии железистого эпителия долек. Если преобладает гиперплазия эпителия молочных протоков, то отмершие в большом количестве эпителиальные клетки забивают просвет протоков, вызывая их расширение. Это явление называют эктазией протоков молочных желез.
Гиперплазия, аденоз и эктазия молочных желез обладают типичными симптомами мастопатии и часто используются в качестве ее синонимов.
В ряде случаев пациентки годами живут, даже не догадываясь о наличии у них мастопатии. Неприятные симптомы отмечаются лишь в 38–50% случаев, они зависят от формы заболевания и фазы менструального цикла.
Боли появляются обычно за 7–10 дней до менструации, они могут быть ноющими, тупыми или распирающими, разными по интенсивности. Неприятные ощущения усиливаются при движении и пальпации (ощупывании). В начале заболевания боли начинаются незадолго до и проходят сразу после менструации, но со временем они становятся продолжительнее и интенсивнее.
Отек и увеличение размеров молочных желез при мастопатии выражены сильнее, чем их физиологическое нагрубание перед менструацией. Иногда пациентки замечают прозрачные, молочные или зеленоватые выделения из соска. При узловой мастопатии все эти симптомы выражены незначительно или отсутствуют вовсе.
При мастопатии важно регулярно наблюдаться у маммолога и уметь самостоятельно обследовать грудь. Врачи рекомендуют проводить самообследование ежемесячно, на 5–12 день цикла.
Вас обязательно должны насторожить:
- асимметрия и разная форма желез;
- узлы и уплотнения;
- втяжения соска;
- пигментации;
- выделения из соска;
- втяжения кожи;
- увеличение и уплотнение подмышечных лимфоузлов.
При обнаружении хотя бы одного из таких симптомов необходимо обратиться к гинекологу, маммологу или онкологу. При мастопатии врач в любом случае назначает дополнительное обследование.
Маммография — рентгенологическое исследование молочных желез, которое используют в качестве метода скрининга (массовой диагностики). Маммографию проводят на 8–10 день цикла. В идеале данное обследование должно назначаться всем женщинам с 35 до 50 лет 1 раз в 2 года, после 50 лет — ежегодно, по показаниям — чаще. Маммография не требует специальной подготовки и с высокой точностью позволяет обнаружить патологические признаки. Благодаря повсеместному распространению маммографов смертность от РМЖ снизилась на 30%.
При мастопатии на маммограмме могут быть обнаружены контурированные тяжистые, округлые сливающиеся или множественные мелкоочаговые тени. Чаще всего изменения носят смешанный характер.
Ультразвуковое исследование (эхография) молочных желез рекомендуется в качестве скрининга женщинам до 35 лет, оно менее информативно, нежели маммография. Точность результатов эхографии определяется размерами образования и разрешением аппаратуры, поэтому его относят к вспомогательным методам.
Пункционная дуктография применяется при подозрении на поражение протоков молочной железы — в проток вводят раствор метиленового синего и выполняют маммографию.
Перед лечением мастопатии независимо от сроков предыдущего исследования обязательно проводят маммографию или УЗИ молочных желез и, по показаниям, — пункционную дуктографию. Если их результаты позволяют заподозрить наличие злокачественного новообразования, врач может назначить более точные методы диагностики, проведение которых возможно лишь в специализированных центрах:
- пункционную биопсию с цитологией,
- тонкоигольную аспирационную биопсию под контролем УЗИ,
- исследование гормонального фона (эстрогены, пролактин).
Они исключают или подтверждают онкологический диагноз со 100%-ной вероятностью.
Важно помнить, что даже если в груди обнаружены уплотнения, или на маммографии зафиксированы узелки — о раке думать еще рано. До 80% пункций новообразований молочной железы в итоге выявляют доброкачественную природу узелков. Тем не менее, при наличии любой формы мастопатии важно регулярно наблюдаться у специалиста и вовремя проходить назначаемые доктором исследования.
источник
Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Гиперплазия молочной железы — это болезнь груди, вызванная избыточным разрастанием ее тканей. Встречается очень часто, по статистике 8 женщин из 10 подвержены этому заболеванию. Имеет еще одно название — мастопатия. Возникает обычно на фоне гормональных нарушений в организме женщины. Эта болезнь не является исключительно женской. Гиперплазия молочной железы встречается и у мужчин, правда это крайне редкие случаи и причины возникновения, возраст и протекание болезни отличается от такой же проблемы у женщин.

Гиперпластические процессы в молочной железы у женщин в последнее время достаточно распространенное заболевание, возраст людей страдающих данной патологией от 20 до 70 лет, встречается у 2/3 женщин в разной форме.
Основной причиной гиперплазии молочной железы является гормональное нарушение в организме. Также сюда можно отнести генетическую предрасположенность женщины, стрессы, продолжительные периоды грудного вскармливания, заболевания эндокринной системы, механические травмы груди и работа с вредными химическими веществами. Иногда сбой в организме может быть вызван приемом других гормональных медикаментозных препаратов, предназначенных для лечения других заболеваний, поэтому после приема таких лекарств необходимо обязательно пройти обследование на предмет обнаружения данной патологии.

Конечно же, точно определить симптомы гиперплазии молочной железы может только доктор, но первые признаки при самостоятельном осмотре можно заметить самому. К ним относится:
- отечность и боль в груди;
- узелковые образования в груди;
- боль в груди переходящая в плечо, или в подмышечную впадину;
- выделения из соска различной консистенции и цвета;
- нарушения менструального цикла;
- деформация формы груди;
- образования в груди могут быть твердыми, или мягкими, находиться в одном и том же месте, или быть подвижными.
К сожалению, некоторые формы гиперпластических процессов в молочных желез протекают бессимптомно, поэтому только врачебный осмотр может их выявить.

Встречается большое количество видов данного заболевания, они делятся за причинами возникновения, то есть в зависимости от того, нарушение каких именно гормонов в организме женщины произошло. Ниже приводятся основные виды этого заболевания.

Возникает на фоне развития гормонального дисбаланса в организме женщины, обычно носит характер доброкачественных изменений в структуре тканей груди и лечится гормонами, подобранными врачом, после детального изучения результатов исследования.

Это избыточные образования железистой ткани груди, в основном имеют дисковидную форму и очень подвижны, поэтому при самостоятельном осмотре их довольно трудно нащупать. Каких-либо болезненных симптомов обычно не наблюдается. Эта форма болезни имеет еще одно название — аденоз. Правда, со временем аденоз прогрессируют, новообразования становятся более заметны, они расширяются. В этом и состоит опасность заболевания, так как самостоятельно его сложно определить на ранних стадиях.
Это разрастание клеток эпителия груди в избыточном количестве. Чаще всего встречается у беременных женщин, так как в этом состоянии ее гормональный фон изменяется. Лечиться непродолжительно и относительно легко, а в некоторых случаях, после родов, когда гормоны успокаиваются и тело возвращается в привычное состояние, гиперплазия эпителия проходит сама по себе. Но ждать, что болезнь уйдет сама не рекомендуется, следует в обязательном порядке проконсультироваться с врачом и пройти обследование.
Это одна из форм патологии, для которой характерно появления мелких, похожих на зернышки, опухолей и узелков в груди. Основный симптомом является болезненность груди перед началом менструации, на которую большинство женщин не обращают внимания на протяжении долгих лет, тем самым запуская развитие патологии, которая впоследствии может привести к раку груди.

Через некоторое время, новообразования при диффузной форме растут в размере и превращаются в плотные узлы, размером с вишню. Тогда болезнь переходит в стадию узловую форму патологии. Боли в груди становятся сильнее и интенсивнее, появляются кровянистые, молочные или прозрачные жидкие выделения из сосков, а с началом менструации симптомы не проходят. Выделяют также фиброзную и кистозную виды болезни, они отличаются структурой новообразования, при фиброзной — образования грубые, тяжелые, с четко определенной структурой, не двигаются и их можно легко нащупать. При фиброзно-кистозном виде появляется киста в груди.
Свое название эта форма получила из-за разрастания тканей эпителия в протоках груди. Симптомы и протекание болезни довольно типичные, на ранних стадиях полностью излечивается, на поздних переходит в предраковое состояние. Без надлежащего лечения может трансформироваться в злокачественную опухоль.
Это появление уплотнений не кучно, а в виде отдельных новообразований в тканях, так называемых очагов. По сути это любой из видов болезни, с расположением одиночных опухолей в разных местах. Может быть даже сразу несколько типов патологии, как фиброзная, так и диффузная, например. Опасность этой формы болезни состоит в том, что она наиболее склонна к перерождению в злокачественную форму.

Это мышечно-фиброзная опухоль, встречается довольно редко, имеет доброкачественный характер. Выражается в виде щелей в мышечной ткани груди, которые устелены миофибробластами (перерожденными клетками фибробластами, которые обычно находятся в мышечной ткани и способствуют заживлению ран). Чаще всего этот вид патологии встречается у женщин в возрасте перед или во время менопаузы, у молодых девушек крайне редко.
Это опухоль, которая образуется в груди из жировой ткани. Развивается в шаре подкожной соединительной ткани, обычно легко обнаруживается, имеет средний размер и легко излечивается при помощи медикаментозного лечения, или методом хирургического удаления. При игнорировании проблемы, может перерасти в липосаркому — рак груди, который отличителен тем, что очень быстро развивается и поражает обе груди.

Отличается от обычной гиперплазии тем, что кроме чрезмерного образования тканей, происходят структурные изменения в самих клетках. Этот процесс является более запущенной формой патологии, по сути, даже предраковым состоянием. Эта форма болезни поддается медикаментозному лечению, но чаще используется хирургическое вмешательство.

Данная патология делится на 2 вида. При первом, увеличивается количество мелких протоков аденоз, в самой дольке появляются альвеолярные узелки из двухслойного эпителия. Они очень подвижны. При втором виде дольковой гиперплазии, атипичном, кроме возникновения самих опухолей, изменяется из клеточная структура.
Появления такого вида патологии значительно увеличивает риск появления рака груди, особенно у женщин в возрасте от 40 до 60 лет, в других случаях риск ниже, но все же присутствует.
Диагностика гиперплазии молочной железы состоит из целого комплекса исследований. В первую очередь, это самостоятельный осмотр женщиной себя, не реже раза в месяц, то есть проверка груди на наличие узелков, уплотнений, болевых ощущений при прикосновениях. Нужно обращать внимание на состояние груди до, во время и после менструации. При малейших изменениях, болях, новообразованиях следует обратиться к маммологу, для проведения дальнейших анализов. Врач проведет маммографию (рентген груди), и в случае, если найдет опухоль, возьмет анализ на цитологию, то есть проверит доброкачественность.

Лечение гиперплазии молочной железы очень разнообразно и зависит исключительно от типа заболевания и стадии развития.
Если болезнь не атипичная и на ранней стадии развития, то проводится медикаментозное лечение, направленное на устранение самой гиперплазии и возможных причин ее появления, таких как гормональное нарушение, стресс, физические травмы.
Для лечения назначаются следующие гормональные препараты.
- Ременс – препарат, способствующий устранению дисбаланса гормонов, нормализации работы гипоталамуса, гипофиза. Их нарушенная работа вызывает сбой гормональной системы, который является причиной патологии. Препарат при данной болезни принимают по 20 капель два раза в сутки, на протяжении трех месяцев. Побочным эффектом может быть аллергическая реакция на компонент препарата (при индивидуальной чувствительности).
- Этинилэстрадиол – гормональный препарат, предназначен для лечения гиперплазии молочной железы, вызванной недостатком эстрогенов. Показанием для применения является неатипичная форма болезни, вторичная эстрогенная недостаточность и другие заболевания. Принимают препарат от 0,05мг до 0,1 мг за один прием, трижды в день. Курс лечения обычно длительный (2-4 месяца). Побочными эффектами приема данного препарата можно считать гиперпигментацию кожных покровов, тошноту, рвоту, увеличение веса и другие расстройства со стороны нервной, эндокринной систем.
- Линдинет 20, 30 — гормональный препарат, содержащий в соответствующих пропорциях этинилэстрадиол и гестоден. Этот препарат подавляет рост разнообразных новообразований, регулирует уровень гормонов. Показанием к применению есть образования в груди диаметром до одного сантиметра, профилактика рецидивов после хирургического удаления образований. Принимают Линдинет с первого дня менструации одна таблетку в день, в один и тот же час. После 21 таблетки – семидневный перерыв. Дальнейшие указания делает лечащий врач, исходя из анализов. Побочными действиями данного препарат можно считать – аллергическую реакцию, тошноту, сыпь, воспалительные процессы влагалища и другие.
Кроме гормонов выписывают еще йодосодержащие и седативные препараты.
Йодосодержащие назначают следующие:
- Кламин – препарат, содержащий йод и другие активные вещества, выделенные морской водорослью ламинарией. Кламин рекомендуют для улучшения функционального состояния груди и для общеукрепляющего эффекта. Принимают одну таблетку (или две капсулы в зависимости от формы выпуска) во время приема пищи три раза в день. Побочными эффектами можно считать аллергические реакции на компоненты средства.
- Калий йодистый – йодосодержащий препарат. Показаниями для его приема являются нарушение образования гормонов щитовидной железы, которые могут стать причиной патологии, другие заболевания. Калий йодистый принимают от 100 до 200 мкг за один прием, раз в сутки. Продолжительность приема определяет лечащий врач. Побочным эффектом есть аллергия.
- Йод-актив – препарат, соединяющий йод и молочный белок, что позволяет впитывать организму только необходимое количество йода. Показания для применения данного препарата – это снижение рисков появления заболеваний, которые связаны с йододефицитом. Применяют по одной или две таблетки во время приема пищи один раз в день. Побочные эффекты могут проявляться в виде аллергических реакций.
Рекомендуемые седативные препараты:
- Сибазон – препарат, оказывающий спазмолитическое, антиаритмическое и другие действия. Показанием для его приема есть следующие недомогания: невротические расстройства, бессонница, миозит, невроз и другие. Дозы и кратность приема определяется врачом, зависит от болезни и стадии. Побочными действиями препарата могут быть – сонливость, астения, отдышка и др.
- Амизил – успокаивающий препарат, который рекомендуют при неврозах и расстройствах нервной системы. Принимают по один — два миллиграмма 4 р. в день, на протяжении четырех – шести недель. Побочные действия Амизила проявляются сухостью (во рту), тахикардией, судорогами.
- Грандаксин – препарат, выступающий в роли психовегетативного регулятора. Рекомендуют при – депрессии, климактерических синдромах, неврозах и др. Чаще всего доза – одна или две таблетки от одного до трех раз в день, определяется врачом. Побочные действия проявляются в виде головных болей, тошноты, зуда кожи и других изменения состояния человека.
Если гиперплазия молочной железы атипичная, или на поздней стадии, когда новообразований большое количество, применяют хирургическое удаление опухолей.
При доброкачественной опухоли операция называется «секторальной резекцией», так как образование удаляют вместе с частью груди. Если опухоль недоброкачественная, обычно происходит «экстирпация», то есть полное удаление груди, иногда даже с лимфатическими узлами и грудными мышцами, для пресечения дальнейшего распространения заболевания.
источник
Опухоли молочной железы встречаются довольно часто у женщин всех возрастных групп, а наибольшее их число составляют доброкачественные, в числе которых и фиброаденома.
С узловыми образованиями в молочной железе маммологи сталкиваются едва ли не ежедневно. На прием приходят как молодые девушки и женщины, так и дамы преклонных лет. Современной женщине, ведущей активный образ жизни, часто не до походов к врачу, поэтому, обнаружив у себя опухоль, она может откладывать визит к специалисту на неопределенно долгое время. Хорошо, если опухоль окажется доброкачественной, но за время выжидания она может достигнуть больших размеров или в ней появятся клетки с признаками злокачественности, а значит, и лечение будет более сложным.
Осмотр врача и ультразвуковое исследование в большинстве случаев бессимптомных опухолей показывает наличие фиброаденомы молочной железы. Это новообразование чаще поражает девушек и молодых женщин 20-30 лет, но и в более зрелом возрасте, в том числе, в климактерическом периоде, эта опухоль также может быть диагностирована.

Часто опухоль путают с фиброаденоматозом, но эти процессы имеют отличия. Фиброаденома – локализованное новообразование, в то время как фиброаденоматоз характеризуется разрастанием железистой и соединительной ткани по всей железе. Кроме того, фиброаденоматоз хорошо поддается консервативной терапии, чего практически не наблюдается при доброкачественных опухолях.
Фиброаденома, как правило, не проявляется никакими симптомами, а единственной жалобой пациентки может быть наличие узлового образования в груди. Чаще всего опухоль обнаруживается при самостоятельном ощупывании груди либо при прохождении профилактического осмотра.
У большинства женщин имеется один опухолевый узел в одной из грудных желез, хотя случается и двустороннее поражение. Это новообразование имеет плотную консистенцию, хорошо смещается при ощупывании, безболезненно, с четкими контурами, не связано с окружающими тканями. Кожа в зоне роста неоплазии не изменяется. Размеры опухоли колеблются от нескольких миллиметров до 7-9 см, но чаще 2-3 см бывает достаточно для того, чтобы женщина пришла к врачу.
Крупные опухоли благодаря своевременному выявлению сегодня диагностируются довольно редко. У большинства женщин перед менструациями происходит некоторое набухание молочных желез, что может создать ложное впечатление роста опухоли, которого на самом деле не происходит.
Основу фиброаденомы составляет железистая ткань с прослойками соединительной, придающей ей плотную консистенцию. У молодых женщин опухоль может быть более мягкой и склонной к быстрому росту, в то время как у женщин старшего поколения она увеличивается очень медленно или практически не растет, плотная, с хорошо выраженной капсулой (зрелая фиброаденома).
В зависимости от характера роста и особенностей гистологического строения принято выделять:
гистологическое строение фиброаденом
Интраканаликулярную фиброаденому, растущую преимущественно в просвет протоков;
Особое клиническое значение имеет листовидная фиброаденома, имеющая слоистое строение и склонная к быстрому увеличению. Такая опухоль нередко диагностируется у молодых пациенток и в 10% случаев перерождается в рак молочной железы. В отличие от других вариантов опухоли, заподозрить листовидную аденому можно по ее величине, которой неоплазия достигает за небольшой промежуток времени.
Длительность заболевания и размеры опухоли не имеют четкой связи с риском озлокачествления. Так, рак способен развиться из неоплазии в 1-2 см, а крупные узлы у пожилых женщин могут длительное время оставаться абсолютно доброкачественными. Считается, что обнаружение атипических клеток или атипической гиперплазии эпителия повышает вероятность рака молочной железы в 8-9 раз. Момент, когда фиброаденома станет злокачественной опухолью, предсказать невозможно, поэтому специалисты чаще всего настаивают на радикальном лечении заболевания.
Причины появления фиброаденомы, как и любой другой опухоли, продолжают обсуждаться, однако достоверно известно, что гормональный дисбаланс имеет решающее значение среди всех остальных факторов риска. По этой причине опухоль чаще диагностируется в периоды наибольших гормональных колебаний: в подростковом периоде, во время беременности и кормления грудью, в пременопаузе, особенно на фоне проводимой заместительной гормонотерапии.
Помимо нарушений гормонального фона, возникновению фиброаденомы весьма способствуют:
- Бесконтрольное, длительное, не согласованное с врачом применение оральных контрацептивов и препаратов, содержащих высокую дозу эстрогенов (средства экстренной контрацепции);
- Частые аборты;
- Непродолжительный период лактации, отказ или невозможность кормления грудью;
- Наличие сопутствующей патологии – ожирение, заболевания щитовидной железы, надпочечников и др.
Рост опухоли происходит под влиянием женских половых гормонов, всплеск уровня которых возможен в подростковом возрасте, когда только устанавливается менструальный цикл, в пременопаузе, когда на фоне постепенного снижения гормонпродуцирующей функции яичников происходят периодические выбросы большого количества эстрогенов. Если женщина решилась на аборт, то она должна знать, что резкое падение уровня половых гормонов за счет прекращения беременности может вызвать у нее появление и мастопатии, и фиброаденомы.
При наличии другой эндокринной патологии и нарушения функции щитовидной железы, надпочечников, гипофиза, яичников изменяется общий гормональный баланс, а у половины таких больных возможно обнаружение опухолей молочных желез.
Поскольку фиброаденома гормонозависима, то не удивителен факт ее роста в период беременности, что нужно обязательно иметь в виду пациенткам, планирующим завести детей. Опухоль может достигнуть таких размеров, что приведет к сдавливанию млечных протоков и нарушению лактации, а в худшем случае к этому присоединится еще и воспаление.
Роль наследственного фактора в развитии фиброаденомы отвергается. Если женщина здорова, имеет правильный менструальный цикл, то опухоль почти наверняка ей не грозит, даже в том случае, если у мамы или у бабушки были такие образования. С другой стороны, если у пациентки имеется неблагоприятный семейный анамнез в отношении рака груди, вероятность озлокачествления фиброаденомы выше, поэтому она нуждается в повышенном внимании маммолога.
Симптомы фиброаденомы молочной железы сводятся к наличию плотного узлового образования, видимого невооруженным глазом при довольно крупных размерах и прощупываемого в ткани железы. Опухоль хорошо смещается, безболезненна, не связана с кожей. Как правило, единственным беспокойством женщины становится само наличие плотного узла, который не болит. Самой частой локализацией фиброаденомы считают верхненаружный квадрант железы.
В случаях, когда пациентка отмечает изменения кожных покровов в проекции роста опухоли, втяжение соска или выделения из него, увеличение подмышечных лимфоузлов, врач всегда заподозрит рак молочной железы, так как внешних изменений и поражения окружающих тканей при фиброаденоме не происходит.

Для постановки диагноза при наличии любого узлового образования следует обязательно отправиться к специалисту. Маммолог осмотрит и пропальпирует железу, и часто диагноз выставляется уже на этом этапе обследования. В целях его подтверждения женщине предлагают пройти ультразвуковое исследование, которое дает информацию о местонахождении, размерах, структуре новообразования. УЗИ позволяет отличить фиброаденому от узловой формы мастопатии, кисты, что очень важно при определении тактики лечения в последующем. При необходимости, УЗИ дополняется маммографией, которая предпочтительна у пациенток более старшего возраста.
способы диагностики фиброаденом
При обнаружении узлового образования в молочной железе обязательным этапом диагностики будет пункционная биопсия, позволяющая исключить или подтвердить злокачественный характер неоплазии. Стоит отметить, что это исследование дает лишь приблизительный результат, так как злокачественные клетки могут в исследуемый материал попросту не попасть. Применение трепан-биопсии дает больше шансов правильной диагностики. Процедура проводится под местной анестезией, поэтому бояться ее не стоит. Окончательный диагноз ставится на основании гистологического исследования ткани опухоли, полученной после ее удаления.
Лечение фиброаденомы, как правило, хирургическое. Поскольку фиброаденома – опухоль, хоть и доброкачественная, то консервативная терапия вряд ли даст хоть какой-то эффект. В некоторых случаях, когда размер новообразования не превышает 5-8 мм, может быть назначена консервативная терапия в течение 4-6 месяцев под контролем УЗИ. Положительный результат наблюдается крайне редко и часто в тех случаях, когда сам факт наличия опухоли сомнителен, то есть высока вероятность, что у пациентки была не опухоль, а фиброаденоматоз, хорошо поддающийся консервативному лечению. По истечении этого времени стоит рассматривать вариант хирургического лечения, пока время не упущено, и опухоль не достигла больших размеров.
Молодые пациентки, принимающие гормональные препараты, должны быть особенно осторожны, ведь гормоны могут ускорить рост опухоли, а значит, в таких случаях лучше ее удалить. Женщинам же менопаузального возраста можно предложить наблюдение при небольших размерах новообразования.
Делать операцию или нет – решает врач в зависимости от клинической ситуации. Предлагая пациентке с небольшой опухолью выжидательную тактику, маммолог может обречь ее на постоянное беспокойство и переживания: вдруг за время наблюдения фиброаденома переродится в рак? Такое возможно, и никто не сможет точно определить момент, когда клетки опухоли станут злокачественными, ведь любое, даже доброкачественное новообразование – своего рода мина замедленного действия. Исходя из этих позиций, большинство специалистов склоняется к необходимости хирургического лечения как единственно правильного.
Если диагноз фиброаденомы был установлен по результату пункционной биопсии и сомнений не вызывает, а размер опухоли исчисляется сантиметрами, то выход один – удалять опухоль.
Показаниями для удаления фиброаденомы могут быть:
- Быстрый рост опухоли;
- Подозрение на возможный злокачественный характер роста;
- Отсутствие эффекта от консервативного лечения;
- Листовидный вариант фиброаденомы;
- Размер свыше 2 см либо наличие косметического дефекта при меньшем диаметре опухоли;
- Желание пациентки удалить новообразование;
- Планируемая беременность.

Беременным женщинам рекомендуют удаление фиброаденомы при сроке беременности свыше 3 месяцев. Если опухоль удалена не будет, то к вопросу ее хирургического лечения стоит вернуться, как только женщина перестанет кормить ребенка грудью, при условии стабильного течения заболевания.
Фиброаденома не возникает сама по себе, причинами ее могут быть различные эндокринные расстройства, патология яичников, наследственная предрасположенность. Удаляя один узел и не устранив первопричину опухоли, не стоит ждать стойкого излечения, ведь может вырасти новая опухоль. В связи с этим, пациенток с установленным диагнозом фиброаденомы должны лечить и другие смежные специалисты – гинеколог, эндокринолог. Только после устранения всех возможных факторов риска опухоли можно рассчитывать на стойкий положительный результат после удаления опухоли.
Итак, вопрос лечения решен: нужна операция. При выборе места ее проведения, стоит ориентироваться не на цену услуги и внешний вид палаты медицинского центра, а на квалификацию и опыт хирурга, от руки которого будет зависеть конечный результат. Оперативное лечение фиброаденомы лучше проводить в медицинских центрах или отделениях, специализирующихся именно на патологии молочной железы. Большинство пациенток волнует не только полное удаление опухоли, но и последующий хороший косметический эффект лечения, который достигается применением органосохраняющих методик и наложением косметических швов. В части случаев необходима помощь пластических хирургов.
На сегодняшний день при фиброаденоме молочной железы может быть проведено два вида операций:
- Секторальная резекция;
- Энуклеация узла.
Секторальная резекция проводится в случаях, когда врач не может полностью исключить вероятность злокачественной трансформации клеток опухоли. При этой операции производится удаление новообразования с окружающей тканью самой железы в пределах 1-3 см вокруг неоплазии. Поскольку удаляется значительный объем тканей, то и косметический дефект после операции, скорее всего, будет. На помощь могут прийти пластические хирурги, а пациентке может быть предложена имплантация или замещение недостающего объема железы за счет собственных тканей, в зависимости от конкретной клинической ситуации. Секторальную резекцию проводят под общим наркозом.
секторальная резекция: операция при фиброаденоме молочной железы
Энуклеация подразумевает удаление только узла фиброаденомы (вылущивание). Такой подход оправдан в случае доказанной абсолютной доброкачественности опухоли. Операция может быть проведена под местной анестезией. Идеальным доступом считается разрез по границы ареолы околососкового поля, тогда шов будет практически незаметен, и лишь в случаях, когда через такой разрез опухоль извлечь невозможно, врач прибегает к удалению через кожу другой зоны железы, над местом расположения образования.
Длительность удаления опухоли, как правило, не превышает часа, а пациентка может быть отправлена домой уже к вечеру. Послеоперационный период протекает легко и безболезненно, швы снимают на 7-10 день после операции, но возможно и на пятый день после вмешательства.
Хороший косметический результат достигается наложением внутрикожных швов, которые после окончательного заживления становятся незаметными для окружающих. Если разрез был произведен в коже над опухолью и был достаточным для удаления крупного узла, то после заживления может остаться небольшой рубец. Чтобы избежать такого явления, лучше проводить операцию тогда, когда новообразование не достигло больших размеров.
Рецидивов после лечения фиброаденомы не происходит, но опухоль может вырасти в другом участке груди, что связано с наличием не устраненных причин роста новообразования. В этой связи больная должна находиться под пристальным вниманием маммолога, гинеколога, эндокринолога.
При значительном объеме удаленной ткани железы возникает вопрос реконструктивного лечения для замещения образовавшегося дефекта. Пациентке могут быть предложены:
- Введение гиалуроновой кислоты при небольшом дефекте;
- Замещение недостающего объема за счет собственной жировой ткани, которую обрабатывают предварительно специальным способом. Возможно, этот метод вскоре будет дополнен введением стволовых клеток, и соответствующие исследования уже проводятся;
- Установка грудных имплантов.
Имплантация возможна не только при больших дефектах грудной железы, но и при желании женщины удалить фиброаденому с одновременной коррекцией формы и размера груди. Кроме того замечено, что женщины с имплантами живут дольше и меньше подвержены риску рака. Это связано отнюдь не с благотворным действием установленных протезов, а с тем, что такие пациентки более тщательно контролируют состояние своей груди и значительно чаще появляются на приеме у маммолога.
Беременных женщин и тех, кто только планирует обзавестись потомством, беспокоит вопрос последующей лактации. После операции удаления опухоли кормление грудью возможно, но при больших размерах неоплазии могут быть определенные трудности, связанные с удалением значительного объема паренхимы железы. В этом вопросе, как и в случае необходимости реконструктивных операций, помочь может раннее обращение к специалисту и своевременное удаление новообразования.

Своевременное обращение к грамотному и опытному специалисту позволяет избежать травматичных операций, необходимости пластики и риска злокачественной трансформации опухоли. После лечения наблюдение у маммолога является обязательным и служит залогом сохранения женского здоровья, профилактики повторного роста доброкачественной опухоли и рака молочной железы.
Автор: врач-онколог, гистолог Гольденшлюгер Н.И. (OICR, Toronto, Canada)
источник
Наиболее сложным в патологической анатомии является вопрос дифференциальной диагностики гиперпластических процессов, которые возникают па фоне гормональной стимуляции, прежде всего гиперэстрогении, и начальных форм рака молочной железы (РМЖ).
Дольковая неоплазия наиболее часто развивается у женщин впредменопаузальный период (в возрасте 45-47 лет) и составляет 1-3,8% всех эпителиальных патологических процессов молочной железы.
В 0,5-4% материала биопсий, взятых по поводу доброкачественных заболеваний молочной железы, выявляют дольковую неоплазию разной степени дифференцировки. В 85% случаев дольковая неоплазия возникает мультицентрично и в 30-67% — билатерально.
Для лобулярной неоплазии характерна пролиферация мелкого эпителия, расположенного в просвете долек, со слабым межклеточным соединением, с педжетоидной реакцией или без нес.
Происходит дольковая неоплазия из эпителия концевой (терминальной) протоково-дольковой единицы молочной железы. Выраженность атипии, степень пролиферации, количество атипических митозов зависят от степени дифференцировки неоплазии.
Выделяют два типа клеток дольковой неоплазии: тип А и тип В. Тип А состоит из мономорфных эпителиальных клеток, тип В — из крупных полиморфных клеток с выраженными признаками атипии. Хотя клетки крупные, они гораздо мельче эпителия протоков.
Может быть смешанный тип, представленный сочетанием в разной пропорции клеток типа А и В.
Термины «атипическая дольковая неоплазия» и «рак in situ» используют, чтобы подчеркнуть их важное прогностическое значение и для указания степени атипии клеток в очаге поражения. Однако известны публикации, свидетельствующие об отсутствии разницы клинического течения атипической дольковой неоплазии и рака in situ, а также разницы в прогнозе дальнейшего развития на их фоне инвазивного рака.
Согласно Классификации РМЖ ВОЗ (2003) рекомендуется пользоваться термином «дольковая неоплазия», подразделяя ее на три степени и термин «дольковый ракшей».
Деление на степени дифференцировки дольковой неоплазии происходит в зависимости от выраженности клеточного полиморфизма, наличия некрозов, признаков атипии и количества митозов.
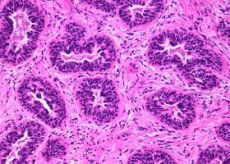
Легкая степень дольковой неоплазии (первая степень неоплазии) характеризуется сохранением альвеолярной архитектоники, пролиферацией в одной или нескольких дольках мелких мономорфных эпителиальных клеток, слабо сцепленных между собой (клетки типа А). Как правило, клетки в очаге пролиферации имеют округлое, нечетко отграниченное ядро и скудную цитоплазму.
Некрозы, митозы и кальцинаты редки. Иногда отмечают очаги пролиферации и полиморфизма клеток, появляются скопления крупных клеток, но эти признаки представлены незначительно. В единичных дольках могут быть признаки апокриновой неоплазии (фото 3).
Фото 3. Легкая степень дольковой неоплазии. Общее строение дольки сохранено, однако количество долек значительно увеличено, отмечается выработка секрета, эпителий мелкий мономорфный. Гематоксилин-эозин, х 100
Умеренная дольковая неоплазия (вторая степень неоплазии) характеризуется нарастанием полиморфизма эпителия долек, появлением большего количества крупных клеток с неправильной формой ядра и обильной цитоплазмой, отмечают единичные митозы и отдельные перстневидные клетки.
Миоэпителиальные клетки чаще располагаются вдоль базальной мембраны, но могут вытесняться из обычного места расположения и примешиваться к эпителиальному пролиферату. Базальная мембрана сохранна на всем протяжении (фото 4, 5).
Фото 4. Умеренная степень дольковой неоплазии. Отмечается пролиферация и формирование многорядного эпителия, очаги секреции. Гематоксилин-эозин, х 200
Фото 5. Умеренная степень дольковой неоплазии. Эпителий полиморфный, формирует сосочки, миоэпителиальные клетки местами вытесняют эпителиальные. Гематоксилин-эозин, х 400
Тяжелая дольковая неоплазия (третья степень неоплазии) представлена в основном полиморфными клетками, заполняющими почти полностью просвет долек, чаще, чем в предыдущей стадии, выявляют митозы, в том числе атипические митозы, очаги некроза (фото 6).
Фото 6. Тяжелая степень дольковой неоплазии. Дольки расширены, просвет полностью заполнен эпителиальными клетками. Гематоксилин-эозин, х 100
Данную дольковую неоплазию трудно дифференцировать от рака in situ. Основное отличие тяжелой дольковой неоплазии и рака in situ в том, что последний представлен малигнизированным эпителием, по клеточному составу не отличается от долькового рака и характеризуется сохранной базальной мембраной.
Для описания атипической дольковой неоплазии часто используют термин «дольковый рак in situ». Все эти процессы имеют один морфологический код в Международном классификаторе онкологических заболеваний — 8520/2.
Рак in situ часто ассоциирован с микроинвазивным раком в окружающих участках, поэтому его исследование требует особой ответственности и внимания при установлении диагноза. Необходимо изучить большое количество срезов и края резекции. В сложных случаях для исключения инвазивного рака необходимо исследовать базальную мембрану для выявления ее целостности и доказать отсутствие нарушения миоэпителиального слоя и базальной мембраны.
Важным условием диагностики дольковой неоплазии является отсутствие инвазии опухолевыми клетками базальной мембраны. Для исключения инвазии применяют антитела, выявляющие коллаген IV типа и гладко-мышечный актин.
Рецепторы эстрогена по данным большинства авторов и нашим наблюдениям выявляют в 60-90% случаев долькового рака in situ, а рецепторы прогестерона редко.
В низкодифференцированном дольковом раке in situ может быть определена экспрессия HER2/neu и белка р53, однако это нетипично для данной патологии.
Фото 7. Дольковый рак in situ. Атипичные клетки заполняют просвет долек. Гематоксилин-эозин, х 100
Фото 8. Дольковый рак in situ. Видны микроочаги некроза в опухолевом инфильтрате. Гематоксилин-эозин, х 100
Типичным для дольковой неоплазии тяжелой степени и рака in situ является отсутствие экспрессии цитокератина СК 5/7 и Е-саdherin.
Но цитокератин высокой молекулярной массы (HMW СК 34ВЕ12) присутствует в цитоплазме клеток долькового рака in situ. Это является важным дифференциальным признаком для диагностики протокового и долькового рака.
Черездовольно длительный промежуток времен и у некоторых женщин на фоне рака in situ возникают инвазивные формы рака, но следует отметить, что дольковый рак in situ не обязательно является предраком инфильтративных форм.
К ним относят простую протоковую гиперплазию, гиперплазию со слабо выраженной пролиферацией эпителия, атипическую протоковую гиперплазию и протоковый рак in situ (трех степеней дифференцировки).
Существуют два классификационных подхода к оценке эпителиальных пролиферативных поражений протоков. Касательно молочной железы одновременно используют две классификационные схемы.
Таблица 1. Классификационные схемы оценки эпителиальных пролиферативных поражений протоков