Киста представляет собой тонкостенный мешочек, заполненный жидкостью, который может образовываться в тканях различных органов. Обычно кисты хорошо поддаются лечению не перерождаются и на начальном этапе не имеют каких бы то ни было симптомов.
В зависимости от того, в каком органе образовалась киста, ее содержимое может существенно отличаться в одних случаях это может быть секрет органа (например, в случае кисты слюнных желез), слизь или жидкость с высоким содержанием белка (например, паровариальная киста, коллоидные кисты щитовидной железы и мозга).
- Врожденными (такие кисты появляются в результате сбоя во время внутриутробного развития плода);
- Приобретенными, то есть возникшими у человека уже после рождения.
Причины появления кист с белковым содержимым во многом зависят от того, в каком органе они развиваются, но если обобщить причины, то можно выделить:
- Перенесенные травмы соответствующего органа или его повреждения в результате операции или других действий;
- Вирусные и бактериальные заболевания органа;
- Плохая экологическая обстановка;
- Неправильное питание;
- Вредные привычки;
- Гормональные сбои;
- Генетическая предрасположенность и др.
Обычно на начальных этапах, когда киста еще относительно небольшая, они не дает практически никаких симптомов и обнаружить ее можно только случайно, на осмотре у врача или при проведении инструментальных обследований органа.
На более поздних стадиях, когда киста вырастет до больших размеров и начнет оказывать давление на органы (головной мозг, щитовидную железу и др.) возникает целый ряд неврологических (если киста расположена в головном мозге) и гормональных (отклонение уровней соответствующих гормонов в крови от нормы).
Кроме того, могут возникнуть неприятные ощущения и боли в местах появления кист.
- Осмотр пациента врачом, который собирает жалобы на самочувствие и определяет возможные причины их возникновения. Сложность состоит в том, что на этом этапе врач редко может определить, какова недомогания. Ведь это может быть не только киста, но и опухоль или какое-то другое заболевание.
- Комплекс анализов, позволяющих определить уровень гормонов в крови и ряд других показателей, что дает возможность уточнить диагноз.
- УЗИ, электроэнцефалограмма.
- Компьютерная томография (КТ) и магнитно-резонансная томография (МРТ).
При этом наибольшей информативностью обладает МРТ.
КТ представляет собой исследование организма, во время которого томограф при помощи рентгеновского излучения делает ряд снимков органа, а компьютер затем собирает полученные снимки в объемную модель этого органа или участка тела. Метод предоставляет точную информацию о расположении кист с высоким содержанием белка, а также может дать информацию относительно содержимого кисты. Периодическое проведение КТ позволяет отследить динамику развития кисты и принять решение о необходимости оперативного вмешательства.
При проведении МРТ томограф регистрирует реакцию ядер водорода на воздействие магнитного поля определенной частоты. Так как при обследовании не используется рентгеновское излучение этот метод имеет меньше противопоказаний, а возможность проведении МРТ с использованием контрастов дает возможность получить точную информацию о характере образования. Учитывая то, что снимки делаются через каждые 2 мм, МРТ обнаруживает даже очень маленькие кисты, пока не дающие никаких симптомов. Также томография определяет не только наличие белка в жидкости кисты, но и его концентрацию.
Нередко и людей возникает вопрос: Зачем нужно второе врачебное мнение, если МРТ и КТ дают настолько ясную картину.
- Объективная. Любой томограф имеет свои ограничения по разрешению и возможностям, особенно это касается старых устройств, установленных много лет назад. Также нужно всегда понимать, что при некоторых заболеваниях картина на томограмме может выглядеть практически также, как и киста.
- Субъективная. Увы, но особенно в небольших городах врачи зачастую не имеют большого опыта анализа полученных в ходе КТ или МРТ снимков. Особенно это касается заболеваний, встречающихся реже, чем остальные. В этом случае имеет смысл говорить о возможной врачебной ошибке.
Для того, чтобы снизить риск такой ошибки до минимума (к сожалению, мы не можем сказать «до нуля» из-за перечисленных объективных причин) и избежать ненужного или неправильного лечения, необходимо получить второе мнение от врача с высокой квалификацией и большим опытом анализа результатов МРТ и КТ.
Национальная телерадиологическая сеть (НТРС) позволяет получить второе мнение от лучших специалистов ведущих клиник и институтов страны. При этом совершенно не важно, как далеко вы находитесь от этих институтов. Все, что вам нужно – это доступ к сети интернет и возможность загрузить результаты КТ/МРТ на наш сервер. Не более, чем через сутки вы будете иметь авторитетное второе мнение, которое подтвердит или опровергнет первичный диагноз.
источник
В связи с широким внедрением в клиническую практику УЗИ и КТ значительно возросло количество пациентов с паразитарными и непаразитарными кистами печени (НКП). Результаты их лечения зависят от этиологии кистозных образований, их связи с желчевыводящими путями и наличия осложнений. Большинство хирургов уделяют внимание только макроскопической оценке содержимого кист печени, описывая его, в большинстве, как прозрачную жидкость без цвета и запаха [4, 6, 8]. Иногда отмечают коричнево-зеленый оттенок кистозной жидкости [2], желеобразную ее консистенцию, наличие мутного с хлопьями содержимого, что свидетельствует об их связи с желчевыводящими протоками, инфицировании или кровоизлиянии в их просвет [2, 9, 14].
По данным литературы, при биохимическом исследовании в кистозной жидкости находят белок, глюкозу, холестерин, билирубин, муцин, эпителиальные клетки. При определении уровня эстрогена в кистозной жидкости выявлены некоторые механизмы его влияния на рост непаразитарных кист печени [15]. Изучение содержимого кист перспективно для выбора адекватного метода их лечения, в то же время работ, посвященных исследованию биохимического, цитологического, гормонального состава кистозной жидкости, недостаточно.
Цель – сравнить биохимический состав содержимого при солитарных и множественных непаразитарных кистах печени.
Материалы и методы исследования
В Пермской краевой клинической больнице за последние 6 лет обследовано и оперировано 34 чел. по поводу солитарных кист печени и 36 чел. – по поводу поликистозной болезни (ПК), что составило 10 % от всех пациентов с заболеваниями печени и желчевыводящих протоков.
Перед операцией всем больным были проведены общеклинические обследования, ультразвуковое исследование органов брюшной полости и компьютерная томография. Для дифференциальной диагностики с гидатидными кистами определяли антитела к эхинококку методом иммуноферментного анализа. При наличии толстой стенки, внутренних перегородок в полости кисты и плотного содержимого (более 20 НU), определяли уровень онкомаркеров: АФП, РЭА, СА-199, СА-242. Пациенты были оперированы «открытым» (15,5 %) и мини-инвазивным способами (84,5 %), при этом выполняли лапароскопические или мини-ассистированные фенестрации кист печени с деэпитализацией, а также чрескожные пункции, дренирование и склерозирование под контролем УЗИ.
Перед фенестрацией кист для биохимического исследования их содержимого производили пункцию с аспирацией иглой 1,4 Fr. Оценивали количество общего белка, альбумина, общего билирубина, активность АСТ и АЛТ, уровень содержания глюкозы, мочевины, креатинина, натрия, калия, кальция и хлоридов. Проводили сравнение полученных результатов с дооперационными и нормальными биохимическими показателями сыворотки крови, а также определяли их взаимосвязь с течением раннего послеоперационного периода.
Результаты исследования и их обсуждение
Среди больных преобладали лица женского пола (90 %) в возрасте от 23 до 69 лет. Средний возраст составил 59 лет. Основной жалобой при кистах печени больших размеров (диаметром от 5 см и более) была тяжесть, ноющая или распирающая боль в правом подреберье, усиливающаяся после физической нагрузки (42 %). У двух пациенток в анамнезе отмечен подъем температуры тела до 39 °С.
Гепатомегалия обнаружена у 44 % больных поликистозом. У половины больных с солитарными кистами дополнительно диагностирована желчнокаменная болезнь.
В то же время при исследовании биохимического состава крови у больных все показатели в среднем были в пределах нормы. У некоторых больных при наличии поликистоза печени и солитарных кист более 15 см в диаметре в биохимическом анализе крови отмечали признаки цитолиза с повышением активности трансаминаз в 1,5–2 раза (10 чел.) и слабые – холестаза (4 чел.). У 10 % пациентов уровень общего белка в сыворотке крови находился на нижней границе нормы, либо был чуть ниже. У одной больной поликистозом печени 3 типа по J.F. Gigоt в сочетании с поликистозом почек обнаружено значительное повышение показателей очищения крови, активности трансаминаз и общего билирубина в 1,5 раза в связи с нарастающей печеночно-почечной недостаточностью. Пациентка в течение 6 лет находится на программном диализе.
У 12 человек при наличии толстой капсулы и перегородок в полости кисты уровень онкомаркеров – АФП, РЭА, СА-199, СА-24 ‒ был в норме. Антитела к эхинококку определяли у 28 больных, у всех результат был отрицательным.
Размеры кист колебались от 5 до 20 см: в 53 % – 5–10 см, в 29 % – 10–15 см, в 18 % – 15–20 см. В большинстве случаев (83 %) кисты были тонкостенными с однородным содержимым низкой плотности до 15 HU. У остальных обнаружены неровные контуры, толстые стенки, гетерогенность содержимого с повышенной плотностью. До операции у 34 больных диагностированы солитарные непаразитарные кисты печени и у 36 пациентов – поликистоз, причем в половине случаев в сочетании с поликистозом почек. Среди осложнений до хирургического вмешательства только у двоих диагностировано инфицирование содержимого. Уровень лейкоцитов и температура тела при этом были в пределах нормы.
Интраоперационно при макроскопической оценке инфицирование содержимого кист выявлено у 9 чел. (13 %), геморрагический характер – у троих (4,3 %), примесь желчи – у 10 (14,3 %), в том числе у четверых при поликистозе печени. Лишь у одной из них обнаружен свищевой ход между кистой и желчным пузырем. Пациентке лапароскопическая фенестрация кист печени дополнена холецистэктомией. При наличии инфицированной жидкости в полости кисты количество лейкоцитов в периферической крови колебалось от 5,5∙109 до 20,4∙109, в среднем составило 12,0∙109 ± 5,9∙109.
При статистической обработке обнаружена слабая положительная корреляция между уровнем лейкоцитов до операции и наличием инфицирования содержимого кист (r = 0,136, p = 0,048).
Биохимическое исследование кистозного содержимого проведено у 35 пациентов, из них у 15 – с солитарными непаразитарными кистами, у 19 – с поликистозом печени, у одной – с эхинококковой кистой. В одном случае при фенестрации предположительно ретенционной кисты установлен ее паразитарный (эхинококковый) характер, что было подтверждено результатом гистологического исследования.
Содержание калия и натрия у всех пациентов НКП соответствовало нормальным показателям сыворотки крови, а уровень хлоридов несколько превышал норму и в среднем составлял 118,7 ± 2,1 ммоль/л.
У 86,7 % пациентов в содержимом НКП находили глюкозу, уровень которой колебался от 0,1 до 1,4 ммоль/л, что было достоверно ниже нормальных показателей сыворотки крови.
Общий белок обнаружен в 73 %, его показатели варьировались от 1,0 до 22,0 г/л. Обнаружена прямая, слабая, статистически достоверная корреляция между уровнем общего белка сыворотки крови, количеством белка и альбумина в кистозной жидкости (r = 0,28, p = 0,0098; r = 0,35, p = 0,006). Чем выше было содержание общего белка в сыворотке крови, тем выше уровень белка и альбумина в кистозной жидкости (r = 0,92, p
источник
Магнитно-резонансная томография в диагностике новообразований почек, мочевых путей и предстательной железы (стр. 5 )
 | Из за большого объема этот материал размещен на нескольких страницах: 1 2 3 4 5 |
Кроме визуальной оценки зависимости интенсивности сигнала от гистологического типа гиперплазии мы провели количественный анализ ИС, используя встроенное программное обеспечение томографа. Для дифференциации получаемых данных на низко – и высокоинтенсивные в качестве эталона проводили измерение ИС от желтого костного мозга головки бедренной кости, так как сигнал от нее является промежуточным между ИС от гладкомышечных и железистых элементов простаты. На Т2-взвешенных изображениях (TR=4000 мсек, TE = 97мсек) выделяя центральную зону железы и головку бедренной кости, получали гистограмму и определяли среднее значение интенсивности сигнала. Отношение ИС костного мозга головки бедренной кости к ИС центральной зоны равное 1 и более свидетельствовало о преобладании в ней железистых элементов — высокоинтенсивная простата. Значение менее 1 свидетельствовало о преобладании стромальных и мышечных элементов. По данным проведенного нами исследования достоверной корреляции между типами гистологического строения гиперплазии и изменением интенсивности МР-сигнала (p>0,05) выявлено не было.
При проведении динамической простатовезикулографии после введения контрастного препарата отмечалось, быстрое повышение интенсивности МР-сигнала в узлах гиперплазии в раннюю фазу. Скорость повышения интенсивности и её пиковое значение в узловых образованиях диаметром более 20мм превосходили таковые в узлах меньшего размера. Нами была прослежена тенденция, заключающаяся в том, что при железистой и фиброзно-мышечной формах гиперплазии контрастное вещество активно накапливается всей тканью узла, в отличие от железисто-фиброзной формы, при которой накопление определяется преимущественно по периферии. Однако исследования достоверной корреляции между типами гистологического строения гиперплазии и изменением интенсивности МР-сигнала после введения контрастного препарата выявлено не было (p>0,05). Приведем клиническое наблюдение комплексного анализа доконтрастных изображений и результатов перфузии простаты.
Использование программ в режиме быстрого спин-эхо дало нам возможность выявить все основные признаки ДГПЖ предстательной железы. Применение данных последовательностей в различных проекциях позволило нам оценить не только форму и размеры железы, но и направление роста центральной зоны, ее соотношение к мочевому пузырю, прямой кишке, задней уретре. В случаях оперативного вмешательства данная информация позволяла, выстроит план предстоящей операции, судить о ходе задней уретры.
Таким образом, для ДГПЖ было характерно: увеличение всех размеров железы, неоднородность МР-сигнала, которая обусловлена преобладанием в узлах гиперплазии фиброзного или железистого компонентов, а также возможность наличия очагов хронического воспаления. В тех случаях, когда периферическая зона, истончена за счет компрессии её узлами гиперплазии, оценка ее структуры затруднена как визуально, так и с помощью количественной оценки изменения интенсивности МР-сигнала. По результатам проведенного динамического исследования предстательной железы было выявлено, что в узлах гиперплазии контрастный препарат накапливается в раннюю артериальную фазу. А окружающие ткани, включая воспалительный компонент (при наличии у пациента в сопутствующих заболеваниях хронического простатита), контрастируются заметно позднее.
В 18 наблюдениях с динамическим контрастированием были проанализированы МР-данные после ТУР с целью оценки степени радикальности вмешательства, визуализации остаточной ткани железы, шейки мочевого и задней стенки уретры. В 6 случаях была выявлен остаточный фрагмент ткани, выступающий в просвет шейки пузыря. При этом шейка мочевого пузыря и ложе удаленной простаты не определялись как единый конус. Во всех 6 случаях при динамическом контрастировании отмечалось ранее накопление препарата в участках подозрительных на остаточную ткань.
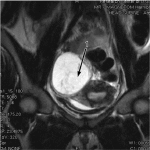
С целью демонстрации возможностей МРТ в диагностике кист простаты и семенных пузырьков, описания, характерных для этих состояний МР-признаков, позволяющих дифференцировать простатические кисты между собой и отличать их от других кистозных образований, локализующихся в полости малого таза у мужчин проанализировали МР-данные 16 пациентов. В 14 наблюдениях они сопутствовали гиперплазии простаты.
Из 16 у 7 пациентов срединно-расположенное кистозное образование в проекции простаты было выявлено также и при ультразвуковом исследовании, и для уточнения диагноза была рекомендована МРТ органов малого таза. У 8 пациентов по данным УЗИ было диагностировано локальное расширение одной из ячеек семенных пузырьков. У 7 пациентов в проекции семявыбрасывающего протока визуализировалась расположенная по срединной линии, над уровнем простатической маточки дополнительная структура округлой формы, с четкими ровными контурами. Из них в 2 случаях описанная структура имела высокую интенсивность сигнала как на Т1-, так и на Т2-взвешенных изображениях (что свидетельствует о высокобелковом содержимом, или примеси крови), и определялось локальное расширение нескольких ячеек семенных пузырьков.
В 5 наблюдениях сигнал от содержимого кист был характерен для серозной жидкости, т. е. был гиперинтенсивным на Т2-взвешенных изображениях, МР-урограммах и гипоинтенсивным в режиме Т1. Во всех случаях когда (n=9), когда кисты были выявлены в латеральных отделах простаты сигнал от их содержимого также, был типичным для простой кисты.
Таким образом, полученные у всех обследуемых данные указывали на то, что вышеописанные структуры являются простатическими кистами: в 2 наблюдениях киста имела повышенное содержание белка или примесь крови, на что указывала высокая интенсивность сигнала как на Т2-, так и на Т1-взвешенных изображениях. Во всех остальных 14 случаях содержимое кист было серозным (высокая интенсивность МР-сигнала на Т2-взвешенных изображениях, низкая в режиме Т1). В 5 случаях, при срединном расположении кист над уровнем простатической маточки, было сделано предположение о наличие кист семявыбрасывающего протока, в 11 случаях, при латеральном расположении кистозных структур, был поставлен предварительный диагноз кист мюллерова протока. Диагноз наличия утрикулярной кисты простаты ни одному из пациентов поставлен не был.
Всем пациентам была рекомендована процедура диагностической транспромежностной аспирации содержимого кисты под контролем ультразвука с дальнейшим микроскопическим исследованием аспирата с целью обнаружения в нем сперматозоидов.
Были определены наиболее характерные МР-признаки различных видов простатических кист. Кисты семявыбрасывающего протока обычно располагаются медиально (редко парамедиально), над простатической маточкой, имеют округлую форму или форму слезы, обычно гипоинтенсивные на Т1-взвешенных изображениях, гиперинтенсивные в режиме Т2 – серозные кисты. В случаях высокобелкового содержимого кисты, или при наличии геморрагического компонента, МР-сигнал гиперинтенсивный как на Т1-, так и на Т2-взвешенных изображениях. Кисты семявыбрасывающего протока часто сочетались с локальным престенотическим расширением ячеек семенных пузырьков на ипсилатеральной стороне. Кисты мюллерова протока, располагались латерально от верхних отделов простаты, с распространением к основанию железы по эмбриональному ходу протока Мюллера. Хотя кисты обычно случайно выявлялись при проведении ультразвукового исследования, МРТ благодаря мультипроекционности более точно определяет органную принадлежность.
Результаты МРТ позволили не только точно визуализировать отсутствие связи выявленного образования с простатой, но также на основании характеристик МР-сигнала, определить наличие геморрагического компонента в его содержимом и в семенных пузырьках.
Таким образом, хотя магнитно-резонансная томография не является методом первой линии при изолированной доброкачественной объемной патологии предстательной железы, в случае их сочетания с раком по нашим данным является высокоинформативным дифференциально-диагностическим методом. Так же, как и в случае рака, Т2-взвешенные изображения были наиболее информативными импульсными последовательностями позволяющими выявлять узлы гиперплазии при аденоме. Многопроекционность метода, позволяет точно оценить объем железы, направление роста центральной зоны при ДГПЖ, отношение к прямой кишке, степень протрузии в мочевой пузырь, состояние простатической части уретры. Все это, в целом является необходимой информацией в случае оперативного вмешательства, в частности определения внешних границ оперируемого органа, что затруднительно при распространенных в настоящее время трансуретральных вмешательствах. Безусловно, часть этой информации может быть получена при ультразвуковом исследовании, но столь четкая анатомическая визуализация возможна только при выполнении МРТ. Также как и при раке предстательной железы, МРТ может быть инструментом для анализа результатов оперативного вмешательства. Высокая межтканевая дифференциация позволяет оценить, насколько полно удалось удалить гиперплазированную ткань простаты и каково состояние задней уретры.
1. Комплексный анализ диагностических возможностей МР-томографии в уроонкологии показал, что метод дает высокоточные и воспроизводимые данные в отношении линейных и объемных характеристик изучаемых структур. При правильно выбранных в соответствии с клиническим статусом показаниях и оптимизированном протоколе формирования изображений применение МР-томографии повышает точность диагностики, сокращает сроки обследования, способствует выявлению метастазов и сопутствующих поражений. Достоинствами МРТ являются неинвазивность, широкое поле изображения, мультипроекционность, возможность варьировать контрастностью изображений.
2. При ретроспективном анализе верифицированного материала получены данные о чрезвычайной гетерогенности МР-картины рака почки. Несмотря на это, метод позволяет провести дифференциальный диагноз данной патологии от доброкачественных образований и от широкого круга других, имитирующих опухоль состояний. С учетом многопроекционности, при адекватном выборе импульсных последовательной, МРТ позволяет не только выявить новообразование почек, мочевого пузыря, предстательной железы, но и оценить распространенность процесса, выработать тактику ведения, а при необходимости оперативного лечения определить объем вмешательства.
3. При диагностике опухоли почки чувствительность и специфичность МРТ составляют 96,2% и 95,9% соответственно. Магнитно-резонансная томография может быть рекомендована для уточнения природы образования, стадирования или устранения сомнений, возникших при анализе результатов УЗИ или МСКТ.
4. Магнитно-резонансная томография с динамическим контрастированием в сочетании со сверхбыстрыми методиками наиболее точный метод в выявлении инвазии опухоли мочевого пузыря в стенку детрузора (стадия Т2 и выше) и оценке экстравезикальной инвазии. Чувствительность метода — 97,9%, специфичность — 95,8%, точность – 96,7%.
5. Магнитно-резонансная томография с динамическим контрастированием является высокоинформативным методом первой линии в диагностике и стадировании рака предстательной железы у пациентов с повышенным уровнем ПСА и сомнительными или негативными данными ТРУЗИ. Чувствительность метода – 89,3%, специфичность – 85,7%, точность – 87,7%. МРТ является методом выбора в выявлении рецидивирования рака предстательной железы и оценке состояния после оперативного лечения и всех видов консервативной терапии.
6. При определении объема и последовательности применения различных методик МРТ следует отметить значительную их вариабельность в зависимости от уровня поражения и поставленных задач. Тем не менее, для извлечения максимума информации и расширения возможностей метода у пациентов с опухолями мочеполового тракта необходим комбинированный подход, включающий в себя МРТ, МР-ангиографию и МР-урографию. Применение комбинированного подхода оправдано также и у пациентов с ХПН.
7. МР-томография является высокоинформативным, неинвазивным диагностическим методом, который возможно использовать в уроонкологической практике, как при первичном обследовании, так и для уточнения данных, полученных с помощью других методов исследования. Оценка результатов МРТ вкупе с другими клиническими данными повышает адекватность выбора методов лечения, в случаях хирургического вмешательства способствует планированию и обоснованию техники операции. Метод может использоваться для динамического контроля в качестве критерия оценки эффективности лечения (консервативного и различных видов оперативного).
1. Новообразования почек: МРТ или МСКТ? Как в диагностике, так и в предоперационном стадировании опухоли почки эффективность МРТ и МСКТ практически одинакова, но процесс венозной инвазии в виде опухолевых тромбов, псевдокапсула опухоли все же лучше выявляются при МРТ. Метод МРТ обладает превосходством в отношении возможности выявить проникновение опухолевого процесса за пределы фасции Герота. Однако МСКТ имеет преимущества по простоте применения, скорости обследования и объему визуализации анатомических областей, возможности построения наглядных для хирургов трехмерных реконструкций. МРТ имеет специфическое клиническое преимущество, поскольку не требует применения йодсодержащих контрастных препаратов, которые многим пациентам могут быть противопоказаны. Применение МРТ предпочтительно у больных после нефрэктомии с пограничным состоянием функции почки. Таким образом, мы считаем, что МРТ представляет собой резервный метод, который рекомендуем применять в случаях, когда результаты УЗИ или МСКТ малоинформативные.
2. Применяемый протокол получения МР-изображения почек должен имеет двойное назначение: в сущности, если выявленная структура не является простой кистой, необходимо корректное установление плотного характера образования и получение информации о распространенности процесса для оптимизации предоперационного планирования. Для этого, мы рекомендуем следующий набор импульсных последовательностей: быстрые спин-эхо последовательности в режиме Т1 и Т2 для получения начальных (доконтрастных) томограмм. Эти изображения несут морфологическую информацию о наличии жировой ткани (высокоинтенсивный Т1 и Т2 сигнал), кровоизлияний (высокоинтенсивный Т1 сигнал) или кистозных структур (высокоинтенсивный Т2 сигнал). Далее уточнения наличия жидкостного компонента возможно применение бесконтрастной МР-урографии, а для дифференциации жировой составляющей от кровоизлияния использование последовательности в режиме подавления сигнала от жировой ткани. Для выявления нарушений кровотока в почечной вене и НПВ обусловленных опухолевым тромбом, наряду с МР-флебографией рекомендуется использование быстрых градиентных эхо-последовательностей со «светлым» сигналом от кровотока. Эффект притока на этих последовательностях максимальный в поперечной плоскости. Иногда возможны артефакты потока, и в этих случаях возможно применение кардиосинхронизации, поскольку при наличии тромба имеет место стойкий дефект наполнения в течение всего сердечного цикла. Все схемы визуализации опухоли почки должны включать динамическую многосрезовую последовательность в режиме Т1.
4. Считаем целесообразным для диагностики, стадирования и определения тактики лечения включение МРТ в комплексное урологическое обследование больных с подозрением на рак мочевого пузыря и предстательной железы.
5. При раке мочевого пузыря выполнение МРТ показано в первую очередь для оценки процесса в стадиях Т2-Т4. Дифференциальная диагностика Т1 и Т2 стадий методом МРТ не всегда возможна. Рекомендуется применение МРТ для исключения рецидива после резекции в случае отсутствия опухоли (или неопределенных результатах) цистоскопии.
6. Для оценки степени инвазии опухоли в мышечный слой при раке мочевого пузыря исследование рекомендуется выполнение Т2-взвешенных быстрых спин-эхо последовательностей в трех ортогональных проекциях. Получение изображений в трех плоскостях обычно гарантирует, что, по меньшей мере, одна проекция позволит оптимально оценить взаиморасположение опухоли и подлежащего детрузора. Для этой же цели, а также оценки степени экстравезикальной инвазии и состояния лимфатических узлов необходимым является проведение контрастного динамического исследования с использованием трехмерных Т1-взвешенных импульсных последовательностей с подавлением сигнала от жировой ткани.
7. При подозрении на рак предстательной железы считаем необходимым применение МРТ для выявления заболевания (в том числе при отрицательных данных ТРУЗИ и биопсии), уточнения зон для прицельной биопсии, стадирования процесса и отбора пациентов для различных методов лечения. Кроме этого, метод показан для наблюдения в динамике после радикальной простатэктомии, на фоне лучевой (в том числе брахитерапии), химиотерапии, гормональной терапии.
8. Оптимизированный протокол импульсных последовательностей, который показан не только для выявления неопластического процесса, но и для адекватной оценки железы в целом как минимум включает в себя Т2-ввзешенные изображения в трех проекциях и Т1-взвешенные изображения в поперечной плоскости. При необходимости доконтрастный протокол может быть расширен за счет поперечных Т2-взвешенных изображений с подавлением сигнала от жировой ткани и фронтальных Т1-взвешенных изображений. Необходимым рекомендуемым компонентом данного протокола на завершающем этапе обследования является динамическое контрастное исследование и комплексный анализ пре — и постконтрастных томограмм.
Список основных научных работ, опубликованных по теме диссертации.
1. Магнитно-резонансная томография в диагностике опухоли почки. //В сборнике материалов I республиканского съезда урологов Узбекистана, Ташкент, 1992, C.182. Авторы: Клычева C. Ш.,
2. Magnetic resonance imaging renal cysts and tumors. //In book of abstracts of XI Annual Scientific Meeting of European Society of Magnetic Resonance in Medicine, Berlin, 1992, P. 323. Авторы: Ternovoj S. K., Belichenko O. I., Sharia M. A.
3. Клиническое применение МР-томографии почек при их кистозных поражениях, опухолях и гидронефротической трансформации у больных артериальной гиперотнией. //Автореф. дисс… канд. мед. наук. М., 1994, 26С. Автор:
4. Клиническое применение МР — томографии с парамагнитным контрастным средством «МАГНЕВИСТ» у больных с почечными кистами, опухолями и гидронефротической трансформацией. //Вестник рентгенологии и радиологии, 1994, №1, C.26-30. Авторы: , ,
5. Clinical using of magnetic resonance imaging in patients with renal cysts and tumors. //In book of abstracts «The European society for Magnetic Resonance in Medicine and Biology», XI Annual Scientific Meeting, Vienna, 1994, P. 371. Авторы: Sharia M. A., Belichenko O. I., Mikailov D. V., Abramova N. N.
6. Clinical possibilities of MRI with paramagnetic contrast medium Magnevist in patients with renal, tumors and hydronephrosis. //In book of abstracts «The Eureopean society for Magnetic Resonance in Medicine and Biology», XI Annual Scientific Meeting, Vienna, 1994, P. 370. Авторы: Belichenko O. I., Ternovoj S. K., Sharia M. A.
7. Магнитно-резонансная томография с повышенным контрастированием у больных с объемными поражениями почек и надпочечников (препарат Магневист). //Визуализация в клинике, 1994, №5, C.39-46. Авторы: , ,
8. МР-томография при гидронефротической трансформации, кистозных поражениях и опухолях почек у больных артериальной гипертонией. //Терапевтический архив, 1995, №4, C. 21-26. Авторы: , Беличенко О. И
9. MRI of renal tumors, cysts and hydronephrosis in patients with arterial hypertension. //In book of abstracts of 13th International Congress of Nephrology, Madrid, 1995, P. 325. Авторы: Belichenko O. I., Sharia M. A., Mikhailov D. V.
10. Computed tomography of renal cysts, stones and hydronephrotic transformations in patients with arterial hypertension. //In book of abstracts of 13th International Congress of Nephrology, Madrid, 1995, P. 326. Авторы: Sharia M. A., Mikhailov D. V.
11. Магнитно-резонансная томография почек и магнитно-резонансная ангиография почечных артерий в диагностике реноваскулярной гипертонии. //В сборнике материалов научно-практической конференции «Магнитно-резонансная томография в клинической практике» Санкт-Петербург, 1996, C.76-78. Авторы: , Абрамова И. В).
12. Магнитно-резонансная томография с применением парамагнитных контрастных средств у больных с опухолями почек и надпочечников. //В сборнике материалов научно-практической конференции «Магнитно-резонансная томография в клинической практике» Санкт-Петербург, 1996, C.79-80. Авторы: Михайлов О. И.,
13. MR-angiography of renal arteries and MR-imaging of kidneys in patients with renovascular hypertension. //In book of abstracts of 13th Annual meeting European Society for Magnetic Resonance in Medicine and Biology, Prague, 1996, P.221. Авторы: Sharia M. A., Belichenko O., Abramova N., Sergienko I.
14. Объемные поражения почек. //В сборнике «Клиническое применение магнитно-резонансной томографии с контрастным усилением (Опыт использования парамагнитного средства «Магневист»»), Москва, «Видар», 1996, С.88-95. Авторы: , ,
15. Магнитно-резонансные томо — и ангиография в оценке состояния почечных артерий и почек у больных реноваскулярной гипертонией. //Медицинская радиология и радиационная безопасность, №2, 1997, C.42-47. Авторы: , , ,
16. Магнитно-резонансная томография с контрастным усилением при опухолях почек и надпочечников. //Медицинская визуализация, 1997, №1, C.21-26. Авторы: , ,
17. MRI with paramagnetic contrast medium in patients with renal and adrenal tumors. //In book of abstracts of 14th Annual Meeting European Society for Magnetic Resonance in Medicine and Biology, Brusseles, 1997, P. 237. Авторы: Belichenko O., Sharia M., Mikhailov D., Kiseleva O.
18. Магнитно-резонансная томография и ангиография в оценке состояний почек и почечных артерий у больных артериальной гипертонией. //Вестник рентгенологии и радиологии, 1998, №4, C.50-59. Авторы: , ,
19. Функциональная магнитно-резонансная томография почек. //Медицинская визуализация, 1998, №2, С.56-59. Авторы: , ,
20. Магнитно-резонансная томография при объемных образованиях почек. //Медицинская визуализация, 1998, №3, C.12-17. Автор:
21. Функциональная магнитно-резонансная томография у здоровых лиц. //В книге материалов научно-практической конференции по лучевой диагностике. Санкт-Петербург, 1998, С.45-48. Авторы: , , Ходарева Е. Н,
22. MRI in patients with renal developmental anomalies and arterial hypertension. //Book of abstracts of 9th European Meeting on Hypertension, Milan, 1999, P.212. Авторы: Belichenko O., Sharia M., Kiseleva. O.
23. МР-томография при объемных образованиях почек. Актуальные проблемы хирургии. //Сборник трудов ММСУ им. , 2000, С.35-39. Автор:
24. МР-томография в диагностике патологии мочевого пузыря (случай из практики). //Медицинский бизнес, 2000, №4, , С.21-22. Автор:
25. Магнитно-резонансная томография в диагностике и стадировании рака мочевого пузыря //Урология, 2000, №1, С.43-45. Авторы: , , ,
26. Магнитно-резонансная томография почек у больных артериальной гипертонией. //М.: Издательский дом “Русский врач”, 2000, 196С. Авторы: , ,
27. The using of MRI in dynamic control in p-ts with renal cysts, tumors and hydronephrotic transformation and arterial hypertension. //In book of abstracts of 10th European Meeting on Hypertension, Milan, 2001, P.254. Авторы: Sharia M. A., Belichenko O., Mikhailov D., Abramova N., Mazaev A.
28. Prostatic cysts: diagnosis with magnetic resonance imaging. //In book of abstracts «The European society for Magnetic Resonance in Medicine and Biology» of 19th Annual Meeting, Cannes,, 2002, P.266. Авторы: Sharia M. A., Zaitseva E. V., Ternovoy K. S., Belichenko O. I., Mazaev A. A.
29. Диагностика кист предстательной железы методом магнитно-резонансной томографии. //Визуализация в клинике, 2002, №20, C.32-35. Авторы: , ,
30. Возможности магнитно-резонансной томографии в диагностике псевдокапсулы почки. //Визуализация в клинике, 2003, №4, C. 71-76. Авторы: , , , , , , ,
31. МРТ в диагностике кист предстательной железы. //В книге материалы Невского радиологического форума, Санкт-Петербург, 2003, C.227-228. Автор:
32. Магнитно-резонансная томография в диагностике опухолей почки. //В книге «Магнитно-резонансная томография в урологии», 2005, С. 30-62. Авторы: , , ,
33. Магнитно-резонансная томография в диагностике рака предстательной железы. //В книге «Магнитно-резонансная томография в урологии», 2005, С. 160-189. Авторы: , , ,
34. Методы томографии в диагностике опухоли почки. //Здравоохранение и медицинские технологии, 2007, №2, C.34-38. Автор:
35. Magnetic resonance imaging in patients with renal tumors and arterial hypertension. //In book of abstracts of 18 Scientific Meeting of the European Society of Hypertension and the 22 Scientific Meeting of the International Society of Hypertension, Berlin, 2008, P.284. Авторы: Sharia M. A, Ansheles A., Belichenko O. I.).
36. Экскреторная урография. //Глава в руководстве по амбулаторно-поликлинической инструментальной диагностике. Под ред. , 2008, C.400-413. Авторы: ,
37. Магнитно-резонансная и мультиспиральная компьютерная томография в комплексной диагностике опухолей почек. //Труды научно-практической конференции Центрального Федерального округа РФ, 2008, С.79-85. Автор:
источник
Карман Ратке ([КР] или гипофизарный ход) представляет собой анатомическую структуру, которая образуется в процессе эмбрионального развития и со временем формирует воронку, переднюю и заднюю части гипофиза. Это карман, как правило, исчезает (облитерируется, заполняясь развивающимся гипофизом) на раннем этапе развития плода, но некоторые клетки кармана нередко остаются в виде щели или небольших заполненных коллоидом кист, которые у детей выражены четче, чем у взрослых.
Киста кармана Ратке (ККР) представляет собой доброкачественную четко отграниченную анатомическую структуру округлой или овальной формы, формирующуюся в результате аномальной инволюции КР с развитием кист (располагающиеся [чаще] интраселлярно или супраселлярно) между адено- и нейрогипофизом (т.е. между передней и задней долями гипофиза) или кпереди от воронки гипофиза. Патогенетически ККР схожи с краниофарингиомами. Размеры ККР варьируют от нескольких миллиметров до 4 — 5 см, содержимое, как правило, незначительно по объему и обычно мукозное (смесь белка и холестерина), реже она заполнена серозной жидкостью или остатками десквамированных клетоки. ККР — вторая по распространенности патология гипоталамо-гипофизарной области после аденом гипофиза, популяционная частота по данным аутопсий составляет от 13 — 33% (соотношение женщин и мужчин приблизительно 2 : 1).

В большинстве случаев ККР гормонально неактивны и клинически асимптомны и являются случайной находкой при аутопсии). Кисты становятся симптоматичными только тогда, когда они, вследствие своего большого размера, компримируют ткань гипофиза, структуры кавернозного синуса или хиазму (перекрест) зрительных нервов, вызывая соответствующую симптоматику: головные боли (33 — 81%), нарушение зрения (33 — 75%), гипофизарную дисфункцию (19 — 81%). В ряде случаев первым клиническим проявлением ККР являются: кровоизлияние в полость ККР или апоплексия гипофиза (сопровождающиеся выраженными головными болями, нарушением зрительной функции, тошнотой или рвотой). Среди эндокринных нарушений наиболее распространены гипопитуитаризм, гиперпролактинемия, водно-электролитные расстройства.

Осложнением ККР может быть ее трансформация в краниофарингиому [КФ] (то есть в доброкачественную эпителиальную опухоль), когда остатки КР (и/или фарингеального эпителия) претерпевают опухолевую трансформацию в процессе развития аденогипофиза. Полагают, что именно так формируются адамантиноподобные КФ, чаще проявляющиеся в детском возрасте. КФ сходны с ККР по возрастным и демографическим признакам, но, в отличие от ККР, обычно имеют обызвествления и супраселлярное распространение образования. Также ККР необходимо дифференцировать от кистозных аденом гипофиза, эпидермоидных кист, а также от арахноидальных кист.
Диагностика кисты кармана Ратке включает в себя: обследование неврологом и офтальмологом на наличие симптомов давления на структуры головного мозга, консультация эндокринолога (в том числе, лабораторные исследования гормональной функции гипофиза), [обязательно] нейровизуализацию: магнитно-резонансную томографию (МРТ) и/или рентгеновскую компьютерную томографию (КТ), а при необходимости ангиографию сосудов головного мозга (в некоторых случаях необходима консультация онколога для исключения злокачественного перерождения кисты).
Общепринятым и стандартным способом диагностики ККР является метод МРТ. Данный способ позволяет определить место локализации кисты, ее размеры и контакты с функционально значимыми зонами мозга, а также основными магистральными сосудами. В зависимости от состава содержимого ККР представлены гипо-, изо- или гиперинтенсивными на Т1- и Т2-ВИ. Кальцификация стенок кисты встречается крайне редко. При болюсном введении парамагнетика эти образования не накапливают контрастное вещество. ККР с мукозным содержимым представляются гиперинтенсивными как на Т2-ВИ, так и на Т1-ВИ; серозное содержимое ККР соответствует сигналу ликвора, т. е. гипоинтенсивный сигнал на Т1-ВИ и гиперинтенсивный сигнал на Т2-ВИ. Однако ККР с высоким содержанием белка являются гиперинтенсивными на Т1-ВИ и гипоинтенсивными на Т2-ВИ. На основе многочисленных МР-исследований и гистологических верификаций кистозных образований гипофиза можно предположить, что наличие внутрикистозного муцинозного включения патогномонично для ККР в 70 — 80% случаев. Также часто совместно с МРТ применяется КТ — метод, который позволяет обеспечить лучшую визуализацию костных структур черепа. Используя трехмерную спиральную КТ (СКТ), можно уточнить топографические соотношения ККР со структурами черепа и сосудами головного мозга. Когда в качестве первичной диагностики невозможно применить МРТ (например, у больного с кардиостимулятором), то применяют КТ и КТ с контрастированием.


Принципы лечения. Небольшие по размеру ККР с асимптоматическим течением не требуют лечения. Наличие эффектов компрессии (гиперпролактинемия, гипофизарный дефицит, сдавление зрительных нервов) является показанием к выполнению хирургического вмешательства (обязательно: в специализированных центрах нейрохирургии). Как правило, задача операции сводится к дренированию содержимого кисты или разрушению ее стенки эндоназальным транссфеноидальным доступом (малоинвазивный метод с применением высокоточной эндоскопической техники): оптико-волоконный эндоскоп вводится через носовую полость и под визуальным компьютерным наблюдением достигает области турецкого седла; с помощью специальных манипуляторов специалисты-нейрохирурги выполняют удаление структур кисты и аспирацию ее содержимого, освобождая окружающие ткани от механического давления ([ . ] содержимое кисты и удаленные ткани отправляются на гистологический анализ с целью исключения наличия злокачественных клеток). Этот метод применяется как при лечении впервые обнаруженной кисты, так и при рецидиве заболевания.
Эффективность оперативного лечения в достижении нормопролактинемии составляет практически 100%, ослабление головных болей и восстановление зрительных нарушений наблюдается в 40 — 100% и 33 — 100% соответственно. Частичный гипо-питуитаризм регрессирует в 14 — 50%, полного восстановления гормональной функции при пангипопитуитаризме, как правило, добиться не удается.


статья «Эндокринные нарушения при наличии кисты кармана Ратке: представление клинического случая» Воротникова С.Ю., Дзеранова Л.К., Пигарова Е.А., Воронцов А.В., Владимирова В.П., Аверкиева Е.В.; ФГБУ «Эндокринологический научный центр» Минздрава России, Москва (журнал «Ожирение и метаболизм» №13(4), 2016) [читать];
статья «Магнитно-резонансная диагностика кисты кармана Ратке» В. Мандал, Н.И. Ананьева; Санкт-Петербургский психо-неврологический институт им. В.М. Бехтерева, Санкт-Петербург, Россия (журнал «Лучевая диагностика и терапия» №3(2) 2011) [читать];
статья «Магнитно-резонансная томография в диагностике условно патологических изменений структур хиазмально-селлярной области (обзор литературы и собственные наблюдения)» Е.В. Аверкиева, В.П. Владимирова, А.В. Воронцов, Ю.В. Новолодская, Н.А. Шувахина; ФГУ Эндокринологический научный центр Минздравсоцразвития России, Москва (журнал Медицинская визуализация №5, 2011) [читать];
источник
Опухоли головного мозга. Классификация опухолей головного мозга. КТ-семиотика опухолей головного мозга. Компьютерная томография нейроэпителиальных опухолей головного мозга , страница 15
На краниограммах при пинеобластоме к моменту обращения больного за помощью, как правило, определяются выраженные гипертензионно-гидроцефальные изменения, обусловленные большими размерами опухоли, блокирующей ликворные пространства.
В атипичных случаях с большим количеством обызвествлений в опухоли на краниограммах могут быть выявлены участки обызвествления – прямой признак опухоли
Гемангиобластомы (ангиоретикуломы) (ГМБ) – доброкачественные сосудистые опухоли неясного происхождения. ГМБ составляют от 1 до 2.5% всех первичных опухолей ЦНС и около 7% опухолей задней черепной ямки у взрослых (68). Более чем у 40% больных ГМБ сочетаются с синдромом Гиппель-Линдау (69). Эти опухоли в 80-85% случаев локализуются в мозжечке, 2-3% в продолговатом мозге и в 3-13% — в спинном мозге. ГМБ – четко отграниченные опухоли. Более чем в 60% они представляют собой гладкостенную кисту с небольшим опухолевым узлом опухоли, расположенный на одной из ее стенок (В.Н. Корниенко с соавт., 2000). В 40% случаев эти опухоли представляют мягкотканный узел без распада и кровоизлияния. В опухолевом узле выявляется большое количество разнокалиберных сосудов.
По результатам МРТ и КТ исследования различают три формы опухоли: узловую, «узел с кистой» и кистозную. Может наблюдаться значительная диспропорция между размерами массивной кисты и очень небольшой величиной пристеночного узла. Как правило, опухолевый узел располагается в том участке кисты, который наиболее близко подходит к поверхности мозжечка.
На КТ киста ГМБ имеет низкую плотность (8-14 Ед.H). При введении контрастного вещества плотность кисты и ее стенок не изменяется; узел опухоли прилежащий к стенке кисты, проявляется четко в виде повышенной, чаще зернистой, плотности (60-85 Ед.H).
На церебральных ангиограммах сосудистая сеть опухолевого узла гемангиобластомы контрастируется, по данным различных авторов в 90% случаев, что соответствует и нашим данным. Сосудистая сеть представлена на ангиограммах обильным количеством равномерных, с четкими контурами сосудов, максимальное ее контрастирование в конце артериальной фазы, прослеживается до 6-7 сек. венозной фазы. Ангиография у больных с кистозной ГМБ выявляет безсосудистую зону, на границе которой определяется небольшая сосудистая сеть опухоли. Иногда наблюдается раннее венозное дренирование.
Эпидермоидные (холестеатомы) и дермоидные опухоли относятся к доброкачественным, медленно растущим образованиям, которые встречаются как интракраниально, так и интраспинально. Эпидермоиды составляют приблизительно от 0.2 до 1.8% всех первичных интракраниальных опухолей; дермоиды встречаются приблизительно в пять раз реже (0.04-0.06%) (Корниенко В.Н., 2000). Считается, что эти опухоли являются результатом включения в другие тканевые структуры эктодермального эпителия во время закрытия нейрональной трубки на 3-5 неделе эмбриогенеза.
Интракраниальные эпидермоиды представляют собой кистозные образования. Эпидермоидные кисты могут быть врожденными и приобретенными. Врожденные кисты имеют интрадуральное расположение с преимущественной локализацией на основании мозга. Приобретенные эпидермоидные кисты – чаще всего травматического генеза, когда возможно проникновение эпидермиса в глубоколежащие ткани, где он образует кисту, в просвете которой происходит постепенное накопление кератина. От 40 до 50% эпидермоидных кист располагается в области мостомозжечкового угла, занимая по частоте третье место после неврином, менингиом. Они также могут располагаться в хиазмально-селлярной области, III желудочке, редко — в стволе головного мозга, мозжечке. Около 10% эпидермоидных кист располагается в диплоическом слое костей свода черепа.
Внутренняя часть кисты образована воскообразным материалом из слущенных кератиновых производных ее стенки и твердых кристаллов холестерина. В отличие от дермоидной кисты, эпидермоид не содержит волосяных фолликулов потовых и жировых желез.
На КТ эпидермоид в большинстве случаев выявляется в виде мелкодольчатого объемного образования, по плотности ниже ликвора (до – 20-10Ед.H), не накапливающего КВ. Обызвествление в эпидермоиде определяется в 10-25% (В.Н. Корниенко с соавт., 1999). В случае перенесенных кровоизлияний и высокого содержания белка на КТ эпидермоид определяется в виде очага повышенной плотности.
Дермоиды локализуются обычно по средней линии, чаще в параселлярной области, реже – в задней черепной ямке. Для супраселлярных опухолей характерны зрительные расстройства, сочетающиеся с головной болью, редко выявляются гипопитуитаризм, несахарный диабет, поражение черепно-мозговых нервов.
В стенках дермоида содержатся различные дермальные придатки, такие как волосяные фолликулы, потовые и жировые железы. Для этих опухолей характерен медленный экспансивный рост. Дермоиды, содержащие жировые включения, хорошо визуализируются на МРТ и КТ.
На КТ дермоидные опухоли имеют типично округлую форму, четко отграниченную от мозговой ткани, с неоднородно пониженной плотностью (от -20 до -60 Ед.H), что зависит от содержания жира в опухоли. Плотность их не изменяется после контрастирования. Небольшие образования, близкие по плотности к цереброспинальной жидкости, расположенные на основании мозга, трудно отличить от расширенных цистерн. В этих случаях необходимо проведение КТЦГ с омнипаком для выявления дефектов наполнения, либо МРТ. Часто наблюдается обызвествление капсулы опухоли. В желудочковой системе и субарахноидальном пространстве при разрывах дермоидных опухолей могут наблюдаться мелкие очаги снижения плотности, представляющие собой капельки жира. Высокоплотные дермоиды наблюдаются редко.
Тератомы происходят из герминогенных клеток. Они встречаются чаще в пинеальной области, реже в боковых, III желудочках, в селлярной области. Опухоль содержит различные компоненты, развивающиеся из трех эмбриональных компонентов, включая и зубы.
На КТ для тератом характерна гетерогенность строения, опухоль с множеством участков повышенной плотности.
Липома относится к мезенхиазмальным неменинготелиальным опухолям. Липома локализуется в различных отделах мозолистого тела:
источник
Киста — патология в виде опухоли, которая состоит из стенок и содержимого. Подобное образование возможно в различных тканях и местах организма, бывает врожденным или приобретенным. Само содержимое кисты и строение ее стенки различается в зависимости от способа образования и места расположения патологии.
- 1 Киста истинная, с внутренней поверхностью, устланной эпителием или эндотелием
- 2 Киста ложная, без особой подстилки
- 1 Киста ретенционная — образуется обычно в тканях и железистых органах в результате закупоривания протока железы.
- 2 Киста рамолиционная — образование происходит по причине омертвения органа или тканевого участка.
- 3 Киста травматическая — следствие травмирования мягких тканей.
- 4 Киста паразитарная — тело паразита в оболочке.
- 5 Киста дизонтогенетическая — врожденное образование, возникающее при нарушениях в процессе формирования тканей и органов на ранней стадии развития.
возникновение больших ложных кист поджелудочной железы может сопровождаться тупыми ноющими болями в верху живота, диспепсией, нарушением общего состояния, периодическим повышением температуры, появлением опухолеобразного формирования в животе.
При кисте яичника нарушается менструальный цикл, появляется тупая боль в низу живота, боли при менструации, ощущение тошноты. Увеличивается объем живота, возможны боли в районе влагалища.
Так как киста образуется в различных местах организма, нет общей, стандартной диеты при данном заболевании. Приводятя некоторые виды болезни, с рекомендованными и запрещенными продуктами.
Киста поджелудочной железы — разрешенные продукты:
мучные изделия из муки первого и второго сорта, несладкое печенье, несвежий хлеб, сухари, пресная отварная или приготовленная на пару рыба, мясо кролика или птицы, нежирная говядина, телятина (мясо нужно измельчать), суп с добавлением сметаны, нежирные кисломолочные продукты, молоко, пресный сыр, вареные яйца, рис, гречка, перловка, овес, ограниченно — манка и пшеничная каша.
- выжатый сок листьев лопуха при кисте почки принимают два месяца трижды в день до еды, также используется кашица из лопуха;
- настойка из суставчиков золотого уса на водке, принимать натощак утром, вечером за сорок минут до еды;
- порошок из осиновой коры, принимается трижды в день по половине столовой ложки;
- зеленый чай с добавкой меда и молока, пить дважды в день;
- отвар корней колючего шиповника, принимается по половине стакана дважды вдень;
- свежая брусника вместе с сливками, сметаной, медом;
- красный корень настаивается в термосе, и принимается трижды в день за час до приема еды;
- настойка девясила с добавлением дрожжей. Принимается три раза в день после принятия пищи;
- отвар следующих растений: двудомная крапива, трехраздельная череда, трехцветная фиалка, полынь, зверобой, корень большого лопуха, песчаный бессмертник, листья грецкого ореха, малый золототысячник, плоды жостера, спорыш, обыкновенная душица, корень лекарственной валерианы, корень конского щавеля; заваривать в термосе, принимать несколько раз в день до еды;
- настойка петрушки принимается в течение дня понемногу;
- спиртовая настойка цветков акации белой, или ее коры, принимать три раза в день по одной столовой ложке;
- отвар из перегородок грецких орехов, принимать трижды вдень по полстакана;
- настой следующих трав: рябина обыкновенная, лекарственная ромашка, манжетка, пастушья сумка, калиновая кора, розовая родиола, пустырник, настаиваются в термосе, трижды в день принимается по четверти стакана;
- настойка из стеблей и головок клевера – готовится вечером, выпивается днем;
- настойка изюма на водке, прием ведется по столовой ложке перед приемом пищи;
- луковый рецепт: средняя луковица заливается медом целиком, затем из нее делается тампон на ночь (рецепт используется для лечения кисты влагалищ);
- настойка, приготовляемая из белых грибов готовится на водке или спирте, и принимается два раза в день по чайной ложке.
копченые изделия, мясо и рыба, обработанные химикатами овощи, продукты с пищевыми добавками (тартразин E 102, борная кислота Е284, амарзант Е123, тетракарбонат натрия Е 285, глюконовая кислота Е574, хлорид олова Е512, полидекстроза Е1200, экстракт Quillaja Е999, эритрозин Е127), заплесневелый хлеб, подгнившие яблоки, облепиха, другие фрукты, плоды, овощи, ягоды, соки, джемы или варенья, которые приготовлены из заплесневелого сырья, несколько раз кипяченная вода, соевый соус, генномодифицированные орехи, уксус, консервы, фаст-фуд.
Ограничить употребление кофе, маргарина и масла из растительных жиров, жирного мяса и печень, алкоголя, сахар, соль, дрожжевой хлеб,
Киста почки: умеренное потребление белковой пищи, исключить из рациона раков, крабов, креветок, бобы, говядину и морскую рыбу – при метаболизме этих продуктов образуется большое количество мочевины, гуанидина, полиамина, креатинина. Диета аналогична применяемой при болезнях почек.
Киста поджелудочной железы: все разновидности бобовых (возникающие газы приносят боль при давлении на окружающие органы), белокочанная капуста и груши (опасны для железы содержанием древовидной клетчатки), пшено (содержит много углеводов, частично откладывающегося в виде жира), табак, специи, томаты, алкоголь (раздражают слизистую, провоцируя возникновение осложнения, опухоли, повышенное выделение сока).
источник
Магнитно-резонансная томография в диагностике новообразований почек, мочевых путей и предстательной железы (стр. 5 )
 | Из за большого объема этот материал размещен на нескольких страницах: 1 2 3 4 5 |
Кроме визуальной оценки зависимости интенсивности сигнала от гистологического типа гиперплазии мы провели количественный анализ ИС, используя встроенное программное обеспечение томографа. Для дифференциации получаемых данных на низко – и высокоинтенсивные в качестве эталона проводили измерение ИС от желтого костного мозга головки бедренной кости, так как сигнал от нее является промежуточным между ИС от гладкомышечных и железистых элементов простаты. На Т2-взвешенных изображениях (TR=4000 мсек, TE = 97мсек) выделяя центральную зону железы и головку бедренной кости, получали гистограмму и определяли среднее значение интенсивности сигнала. Отношение ИС костного мозга головки бедренной кости к ИС центральной зоны равное 1 и более свидетельствовало о преобладании в ней железистых элементов — высокоинтенсивная простата. Значение менее 1 свидетельствовало о преобладании стромальных и мышечных элементов. По данным проведенного нами исследования достоверной корреляции между типами гистологического строения гиперплазии и изменением интенсивности МР-сигнала (p>0,05) выявлено не было.
При проведении динамической простатовезикулографии после введения контрастного препарата отмечалось, быстрое повышение интенсивности МР-сигнала в узлах гиперплазии в раннюю фазу. Скорость повышения интенсивности и её пиковое значение в узловых образованиях диаметром более 20мм превосходили таковые в узлах меньшего размера. Нами была прослежена тенденция, заключающаяся в том, что при железистой и фиброзно-мышечной формах гиперплазии контрастное вещество активно накапливается всей тканью узла, в отличие от железисто-фиброзной формы, при которой накопление определяется преимущественно по периферии. Однако исследования достоверной корреляции между типами гистологического строения гиперплазии и изменением интенсивности МР-сигнала после введения контрастного препарата выявлено не было (p>0,05). Приведем клиническое наблюдение комплексного анализа доконтрастных изображений и результатов перфузии простаты.
Использование программ в режиме быстрого спин-эхо дало нам возможность выявить все основные признаки ДГПЖ предстательной железы. Применение данных последовательностей в различных проекциях позволило нам оценить не только форму и размеры железы, но и направление роста центральной зоны, ее соотношение к мочевому пузырю, прямой кишке, задней уретре. В случаях оперативного вмешательства данная информация позволяла, выстроит план предстоящей операции, судить о ходе задней уретры.
Таким образом, для ДГПЖ было характерно: увеличение всех размеров железы, неоднородность МР-сигнала, которая обусловлена преобладанием в узлах гиперплазии фиброзного или железистого компонентов, а также возможность наличия очагов хронического воспаления. В тех случаях, когда периферическая зона, истончена за счет компрессии её узлами гиперплазии, оценка ее структуры затруднена как визуально, так и с помощью количественной оценки изменения интенсивности МР-сигнала. По результатам проведенного динамического исследования предстательной железы было выявлено, что в узлах гиперплазии контрастный препарат накапливается в раннюю артериальную фазу. А окружающие ткани, включая воспалительный компонент (при наличии у пациента в сопутствующих заболеваниях хронического простатита), контрастируются заметно позднее.
В 18 наблюдениях с динамическим контрастированием были проанализированы МР-данные после ТУР с целью оценки степени радикальности вмешательства, визуализации остаточной ткани железы, шейки мочевого и задней стенки уретры. В 6 случаях была выявлен остаточный фрагмент ткани, выступающий в просвет шейки пузыря. При этом шейка мочевого пузыря и ложе удаленной простаты не определялись как единый конус. Во всех 6 случаях при динамическом контрастировании отмечалось ранее накопление препарата в участках подозрительных на остаточную ткань.
С целью демонстрации возможностей МРТ в диагностике кист простаты и семенных пузырьков, описания, характерных для этих состояний МР-признаков, позволяющих дифференцировать простатические кисты между собой и отличать их от других кистозных образований, локализующихся в полости малого таза у мужчин проанализировали МР-данные 16 пациентов. В 14 наблюдениях они сопутствовали гиперплазии простаты.
Из 16 у 7 пациентов срединно-расположенное кистозное образование в проекции простаты было выявлено также и при ультразвуковом исследовании, и для уточнения диагноза была рекомендована МРТ органов малого таза. У 8 пациентов по данным УЗИ было диагностировано локальное расширение одной из ячеек семенных пузырьков. У 7 пациентов в проекции семявыбрасывающего протока визуализировалась расположенная по срединной линии, над уровнем простатической маточки дополнительная структура округлой формы, с четкими ровными контурами. Из них в 2 случаях описанная структура имела высокую интенсивность сигнала как на Т1-, так и на Т2-взвешенных изображениях (что свидетельствует о высокобелковом содержимом, или примеси крови), и определялось локальное расширение нескольких ячеек семенных пузырьков.
В 5 наблюдениях сигнал от содержимого кист был характерен для серозной жидкости, т. е. был гиперинтенсивным на Т2-взвешенных изображениях, МР-урограммах и гипоинтенсивным в режиме Т1. Во всех случаях когда (n=9), когда кисты были выявлены в латеральных отделах простаты сигнал от их содержимого также, был типичным для простой кисты.
Таким образом, полученные у всех обследуемых данные указывали на то, что вышеописанные структуры являются простатическими кистами: в 2 наблюдениях киста имела повышенное содержание белка или примесь крови, на что указывала высокая интенсивность сигнала как на Т2-, так и на Т1-взвешенных изображениях. Во всех остальных 14 случаях содержимое кист было серозным (высокая интенсивность МР-сигнала на Т2-взвешенных изображениях, низкая в режиме Т1). В 5 случаях, при срединном расположении кист над уровнем простатической маточки, было сделано предположение о наличие кист семявыбрасывающего протока, в 11 случаях, при латеральном расположении кистозных структур, был поставлен предварительный диагноз кист мюллерова протока. Диагноз наличия утрикулярной кисты простаты ни одному из пациентов поставлен не был.
Всем пациентам была рекомендована процедура диагностической транспромежностной аспирации содержимого кисты под контролем ультразвука с дальнейшим микроскопическим исследованием аспирата с целью обнаружения в нем сперматозоидов.
Были определены наиболее характерные МР-признаки различных видов простатических кист. Кисты семявыбрасывающего протока обычно располагаются медиально (редко парамедиально), над простатической маточкой, имеют округлую форму или форму слезы, обычно гипоинтенсивные на Т1-взвешенных изображениях, гиперинтенсивные в режиме Т2 – серозные кисты. В случаях высокобелкового содержимого кисты, или при наличии геморрагического компонента, МР-сигнал гиперинтенсивный как на Т1-, так и на Т2-взвешенных изображениях. Кисты семявыбрасывающего протока часто сочетались с локальным престенотическим расширением ячеек семенных пузырьков на ипсилатеральной стороне. Кисты мюллерова протока, располагались латерально от верхних отделов простаты, с распространением к основанию железы по эмбриональному ходу протока Мюллера. Хотя кисты обычно случайно выявлялись при проведении ультразвукового исследования, МРТ благодаря мультипроекционности более точно определяет органную принадлежность.
Результаты МРТ позволили не только точно визуализировать отсутствие связи выявленного образования с простатой, но также на основании характеристик МР-сигнала, определить наличие геморрагического компонента в его содержимом и в семенных пузырьках.
Таким образом, хотя магнитно-резонансная томография не является методом первой линии при изолированной доброкачественной объемной патологии предстательной железы, в случае их сочетания с раком по нашим данным является высокоинформативным дифференциально-диагностическим методом. Так же, как и в случае рака, Т2-взвешенные изображения были наиболее информативными импульсными последовательностями позволяющими выявлять узлы гиперплазии при аденоме. Многопроекционность метода, позволяет точно оценить объем железы, направление роста центральной зоны при ДГПЖ, отношение к прямой кишке, степень протрузии в мочевой пузырь, состояние простатической части уретры. Все это, в целом является необходимой информацией в случае оперативного вмешательства, в частности определения внешних границ оперируемого органа, что затруднительно при распространенных в настоящее время трансуретральных вмешательствах. Безусловно, часть этой информации может быть получена при ультразвуковом исследовании, но столь четкая анатомическая визуализация возможна только при выполнении МРТ. Также как и при раке предстательной железы, МРТ может быть инструментом для анализа результатов оперативного вмешательства. Высокая межтканевая дифференциация позволяет оценить, насколько полно удалось удалить гиперплазированную ткань простаты и каково состояние задней уретры.
1. Комплексный анализ диагностических возможностей МР-томографии в уроонкологии показал, что метод дает высокоточные и воспроизводимые данные в отношении линейных и объемных характеристик изучаемых структур. При правильно выбранных в соответствии с клиническим статусом показаниях и оптимизированном протоколе формирования изображений применение МР-томографии повышает точность диагностики, сокращает сроки обследования, способствует выявлению метастазов и сопутствующих поражений. Достоинствами МРТ являются неинвазивность, широкое поле изображения, мультипроекционность, возможность варьировать контрастностью изображений.
2. При ретроспективном анализе верифицированного материала получены данные о чрезвычайной гетерогенности МР-картины рака почки. Несмотря на это, метод позволяет провести дифференциальный диагноз данной патологии от доброкачественных образований и от широкого круга других, имитирующих опухоль состояний. С учетом многопроекционности, при адекватном выборе импульсных последовательной, МРТ позволяет не только выявить новообразование почек, мочевого пузыря, предстательной железы, но и оценить распространенность процесса, выработать тактику ведения, а при необходимости оперативного лечения определить объем вмешательства.
3. При диагностике опухоли почки чувствительность и специфичность МРТ составляют 96,2% и 95,9% соответственно. Магнитно-резонансная томография может быть рекомендована для уточнения природы образования, стадирования или устранения сомнений, возникших при анализе результатов УЗИ или МСКТ.
4. Магнитно-резонансная томография с динамическим контрастированием в сочетании со сверхбыстрыми методиками наиболее точный метод в выявлении инвазии опухоли мочевого пузыря в стенку детрузора (стадия Т2 и выше) и оценке экстравезикальной инвазии. Чувствительность метода — 97,9%, специфичность — 95,8%, точность – 96,7%.
5. Магнитно-резонансная томография с динамическим контрастированием является высокоинформативным методом первой линии в диагностике и стадировании рака предстательной железы у пациентов с повышенным уровнем ПСА и сомнительными или негативными данными ТРУЗИ. Чувствительность метода – 89,3%, специфичность – 85,7%, точность – 87,7%. МРТ является методом выбора в выявлении рецидивирования рака предстательной железы и оценке состояния после оперативного лечения и всех видов консервативной терапии.
6. При определении объема и последовательности применения различных методик МРТ следует отметить значительную их вариабельность в зависимости от уровня поражения и поставленных задач. Тем не менее, для извлечения максимума информации и расширения возможностей метода у пациентов с опухолями мочеполового тракта необходим комбинированный подход, включающий в себя МРТ, МР-ангиографию и МР-урографию. Применение комбинированного подхода оправдано также и у пациентов с ХПН.
7. МР-томография является высокоинформативным, неинвазивным диагностическим методом, который возможно использовать в уроонкологической практике, как при первичном обследовании, так и для уточнения данных, полученных с помощью других методов исследования. Оценка результатов МРТ вкупе с другими клиническими данными повышает адекватность выбора методов лечения, в случаях хирургического вмешательства способствует планированию и обоснованию техники операции. Метод может использоваться для динамического контроля в качестве критерия оценки эффективности лечения (консервативного и различных видов оперативного).
1. Новообразования почек: МРТ или МСКТ? Как в диагностике, так и в предоперационном стадировании опухоли почки эффективность МРТ и МСКТ практически одинакова, но процесс венозной инвазии в виде опухолевых тромбов, псевдокапсула опухоли все же лучше выявляются при МРТ. Метод МРТ обладает превосходством в отношении возможности выявить проникновение опухолевого процесса за пределы фасции Герота. Однако МСКТ имеет преимущества по простоте применения, скорости обследования и объему визуализации анатомических областей, возможности построения наглядных для хирургов трехмерных реконструкций. МРТ имеет специфическое клиническое преимущество, поскольку не требует применения йодсодержащих контрастных препаратов, которые многим пациентам могут быть противопоказаны. Применение МРТ предпочтительно у больных после нефрэктомии с пограничным состоянием функции почки. Таким образом, мы считаем, что МРТ представляет собой резервный метод, который рекомендуем применять в случаях, когда результаты УЗИ или МСКТ малоинформативные.
2. Применяемый протокол получения МР-изображения почек должен имеет двойное назначение: в сущности, если выявленная структура не является простой кистой, необходимо корректное установление плотного характера образования и получение информации о распространенности процесса для оптимизации предоперационного планирования. Для этого, мы рекомендуем следующий набор импульсных последовательностей: быстрые спин-эхо последовательности в режиме Т1 и Т2 для получения начальных (доконтрастных) томограмм. Эти изображения несут морфологическую информацию о наличии жировой ткани (высокоинтенсивный Т1 и Т2 сигнал), кровоизлияний (высокоинтенсивный Т1 сигнал) или кистозных структур (высокоинтенсивный Т2 сигнал). Далее уточнения наличия жидкостного компонента возможно применение бесконтрастной МР-урографии, а для дифференциации жировой составляющей от кровоизлияния использование последовательности в режиме подавления сигнала от жировой ткани. Для выявления нарушений кровотока в почечной вене и НПВ обусловленных опухолевым тромбом, наряду с МР-флебографией рекомендуется использование быстрых градиентных эхо-последовательностей со «светлым» сигналом от кровотока. Эффект притока на этих последовательностях максимальный в поперечной плоскости. Иногда возможны артефакты потока, и в этих случаях возможно применение кардиосинхронизации, поскольку при наличии тромба имеет место стойкий дефект наполнения в течение всего сердечного цикла. Все схемы визуализации опухоли почки должны включать динамическую многосрезовую последовательность в режиме Т1.
4. Считаем целесообразным для диагностики, стадирования и определения тактики лечения включение МРТ в комплексное урологическое обследование больных с подозрением на рак мочевого пузыря и предстательной железы.
5. При раке мочевого пузыря выполнение МРТ показано в первую очередь для оценки процесса в стадиях Т2-Т4. Дифференциальная диагностика Т1 и Т2 стадий методом МРТ не всегда возможна. Рекомендуется применение МРТ для исключения рецидива после резекции в случае отсутствия опухоли (или неопределенных результатах) цистоскопии.
6. Для оценки степени инвазии опухоли в мышечный слой при раке мочевого пузыря исследование рекомендуется выполнение Т2-взвешенных быстрых спин-эхо последовательностей в трех ортогональных проекциях. Получение изображений в трех плоскостях обычно гарантирует, что, по меньшей мере, одна проекция позволит оптимально оценить взаиморасположение опухоли и подлежащего детрузора. Для этой же цели, а также оценки степени экстравезикальной инвазии и состояния лимфатических узлов необходимым является проведение контрастного динамического исследования с использованием трехмерных Т1-взвешенных импульсных последовательностей с подавлением сигнала от жировой ткани.
7. При подозрении на рак предстательной железы считаем необходимым применение МРТ для выявления заболевания (в том числе при отрицательных данных ТРУЗИ и биопсии), уточнения зон для прицельной биопсии, стадирования процесса и отбора пациентов для различных методов лечения. Кроме этого, метод показан для наблюдения в динамике после радикальной простатэктомии, на фоне лучевой (в том числе брахитерапии), химиотерапии, гормональной терапии.
8. Оптимизированный протокол импульсных последовательностей, который показан не только для выявления неопластического процесса, но и для адекватной оценки железы в целом как минимум включает в себя Т2-ввзешенные изображения в трех проекциях и Т1-взвешенные изображения в поперечной плоскости. При необходимости доконтрастный протокол может быть расширен за счет поперечных Т2-взвешенных изображений с подавлением сигнала от жировой ткани и фронтальных Т1-взвешенных изображений. Необходимым рекомендуемым компонентом данного протокола на завершающем этапе обследования является динамическое контрастное исследование и комплексный анализ пре — и постконтрастных томограмм.
Список основных научных работ, опубликованных по теме диссертации.
1. Магнитно-резонансная томография в диагностике опухоли почки. //В сборнике материалов I республиканского съезда урологов Узбекистана, Ташкент, 1992, C.182. Авторы: Клычева C. Ш.,
2. Magnetic resonance imaging renal cysts and tumors. //In book of abstracts of XI Annual Scientific Meeting of European Society of Magnetic Resonance in Medicine, Berlin, 1992, P. 323. Авторы: Ternovoj S. K., Belichenko O. I., Sharia M. A.
3. Клиническое применение МР-томографии почек при их кистозных поражениях, опухолях и гидронефротической трансформации у больных артериальной гиперотнией. //Автореф. дисс… канд. мед. наук. М., 1994, 26С. Автор:
4. Клиническое применение МР — томографии с парамагнитным контрастным средством «МАГНЕВИСТ» у больных с почечными кистами, опухолями и гидронефротической трансформацией. //Вестник рентгенологии и радиологии, 1994, №1, C.26-30. Авторы: , ,
5. Clinical using of magnetic resonance imaging in patients with renal cysts and tumors. //In book of abstracts «The European society for Magnetic Resonance in Medicine and Biology», XI Annual Scientific Meeting, Vienna, 1994, P. 371. Авторы: Sharia M. A., Belichenko O. I., Mikailov D. V., Abramova N. N.
6. Clinical possibilities of MRI with paramagnetic contrast medium Magnevist in patients with renal, tumors and hydronephrosis. //In book of abstracts «The Eureopean society for Magnetic Resonance in Medicine and Biology», XI Annual Scientific Meeting, Vienna, 1994, P. 370. Авторы: Belichenko O. I., Ternovoj S. K., Sharia M. A.
7. Магнитно-резонансная томография с повышенным контрастированием у больных с объемными поражениями почек и надпочечников (препарат Магневист). //Визуализация в клинике, 1994, №5, C.39-46. Авторы: , ,
8. МР-томография при гидронефротической трансформации, кистозных поражениях и опухолях почек у больных артериальной гипертонией. //Терапевтический архив, 1995, №4, C. 21-26. Авторы: , Беличенко О. И
9. MRI of renal tumors, cysts and hydronephrosis in patients with arterial hypertension. //In book of abstracts of 13th International Congress of Nephrology, Madrid, 1995, P. 325. Авторы: Belichenko O. I., Sharia M. A., Mikhailov D. V.
10. Computed tomography of renal cysts, stones and hydronephrotic transformations in patients with arterial hypertension. //In book of abstracts of 13th International Congress of Nephrology, Madrid, 1995, P. 326. Авторы: Sharia M. A., Mikhailov D. V.
11. Магнитно-резонансная томография почек и магнитно-резонансная ангиография почечных артерий в диагностике реноваскулярной гипертонии. //В сборнике материалов научно-практической конференции «Магнитно-резонансная томография в клинической практике» Санкт-Петербург, 1996, C.76-78. Авторы: , Абрамова И. В).
12. Магнитно-резонансная томография с применением парамагнитных контрастных средств у больных с опухолями почек и надпочечников. //В сборнике материалов научно-практической конференции «Магнитно-резонансная томография в клинической практике» Санкт-Петербург, 1996, C.79-80. Авторы: Михайлов О. И.,
13. MR-angiography of renal arteries and MR-imaging of kidneys in patients with renovascular hypertension. //In book of abstracts of 13th Annual meeting European Society for Magnetic Resonance in Medicine and Biology, Prague, 1996, P.221. Авторы: Sharia M. A., Belichenko O., Abramova N., Sergienko I.
14. Объемные поражения почек. //В сборнике «Клиническое применение магнитно-резонансной томографии с контрастным усилением (Опыт использования парамагнитного средства «Магневист»»), Москва, «Видар», 1996, С.88-95. Авторы: , ,
15. Магнитно-резонансные томо — и ангиография в оценке состояния почечных артерий и почек у больных реноваскулярной гипертонией. //Медицинская радиология и радиационная безопасность, №2, 1997, C.42-47. Авторы: , , ,
16. Магнитно-резонансная томография с контрастным усилением при опухолях почек и надпочечников. //Медицинская визуализация, 1997, №1, C.21-26. Авторы: , ,
17. MRI with paramagnetic contrast medium in patients with renal and adrenal tumors. //In book of abstracts of 14th Annual Meeting European Society for Magnetic Resonance in Medicine and Biology, Brusseles, 1997, P. 237. Авторы: Belichenko O., Sharia M., Mikhailov D., Kiseleva O.
18. Магнитно-резонансная томография и ангиография в оценке состояний почек и почечных артерий у больных артериальной гипертонией. //Вестник рентгенологии и радиологии, 1998, №4, C.50-59. Авторы: , ,
19. Функциональная магнитно-резонансная томография почек. //Медицинская визуализация, 1998, №2, С.56-59. Авторы: , ,
20. Магнитно-резонансная томография при объемных образованиях почек. //Медицинская визуализация, 1998, №3, C.12-17. Автор:
21. Функциональная магнитно-резонансная томография у здоровых лиц. //В книге материалов научно-практической конференции по лучевой диагностике. Санкт-Петербург, 1998, С.45-48. Авторы: , , Ходарева Е. Н,
22. MRI in patients with renal developmental anomalies and arterial hypertension. //Book of abstracts of 9th European Meeting on Hypertension, Milan, 1999, P.212. Авторы: Belichenko O., Sharia M., Kiseleva. O.
23. МР-томография при объемных образованиях почек. Актуальные проблемы хирургии. //Сборник трудов ММСУ им. , 2000, С.35-39. Автор:
24. МР-томография в диагностике патологии мочевого пузыря (случай из практики). //Медицинский бизнес, 2000, №4, , С.21-22. Автор:
25. Магнитно-резонансная томография в диагностике и стадировании рака мочевого пузыря //Урология, 2000, №1, С.43-45. Авторы: , , ,
26. Магнитно-резонансная томография почек у больных артериальной гипертонией. //М.: Издательский дом “Русский врач”, 2000, 196С. Авторы: , ,
27. The using of MRI in dynamic control in p-ts with renal cysts, tumors and hydronephrotic transformation and arterial hypertension. //In book of abstracts of 10th European Meeting on Hypertension, Milan, 2001, P.254. Авторы: Sharia M. A., Belichenko O., Mikhailov D., Abramova N., Mazaev A.
28. Prostatic cysts: diagnosis with magnetic resonance imaging. //In book of abstracts «The European society for Magnetic Resonance in Medicine and Biology» of 19th Annual Meeting, Cannes,, 2002, P.266. Авторы: Sharia M. A., Zaitseva E. V., Ternovoy K. S., Belichenko O. I., Mazaev A. A.
29. Диагностика кист предстательной железы методом магнитно-резонансной томографии. //Визуализация в клинике, 2002, №20, C.32-35. Авторы: , ,
30. Возможности магнитно-резонансной томографии в диагностике псевдокапсулы почки. //Визуализация в клинике, 2003, №4, C. 71-76. Авторы: , , , , , , ,
31. МРТ в диагностике кист предстательной железы. //В книге материалы Невского радиологического форума, Санкт-Петербург, 2003, C.227-228. Автор:
32. Магнитно-резонансная томография в диагностике опухолей почки. //В книге «Магнитно-резонансная томография в урологии», 2005, С. 30-62. Авторы: , , ,
33. Магнитно-резонансная томография в диагностике рака предстательной железы. //В книге «Магнитно-резонансная томография в урологии», 2005, С. 160-189. Авторы: , , ,
34. Методы томографии в диагностике опухоли почки. //Здравоохранение и медицинские технологии, 2007, №2, C.34-38. Автор:
35. Magnetic resonance imaging in patients with renal tumors and arterial hypertension. //In book of abstracts of 18 Scientific Meeting of the European Society of Hypertension and the 22 Scientific Meeting of the International Society of Hypertension, Berlin, 2008, P.284. Авторы: Sharia M. A, Ansheles A., Belichenko O. I.).
36. Экскреторная урография. //Глава в руководстве по амбулаторно-поликлинической инструментальной диагностике. Под ред. , 2008, C.400-413. Авторы: ,
37. Магнитно-резонансная и мультиспиральная компьютерная томография в комплексной диагностике опухолей почек. //Труды научно-практической конференции Центрального Федерального округа РФ, 2008, С.79-85. Автор:
источник