Киста у новорожденного – часто встречающееся доброкачественное образование. Оно представляет собой полость в органе, наполненную жидкостью. К концу беременности подобное явление у плода обычно рассасывается без постороннего вмешательства. Причины появления кист разные. Чаще всего кисты становятся результатом того, что у новорожденных ещё не установился обмен веществ.
Симптомы кисты новорожденных зависят от разновидности опухоли. Имеет значение её локализация, размер и сопутствующие осложнения. Новообразования различаются по злокачественности, наличию нагноения и воспалительных процессов. У кисты новорожденных бывают следующие симптомы:
Расстройство координации движений и запоздалость реакций.
Снижение чувствительности конечностей, вплоть до полной её утери (на некоторый период времени отнимается ручка, ножка).
Нарушение и ухудшение зрения.
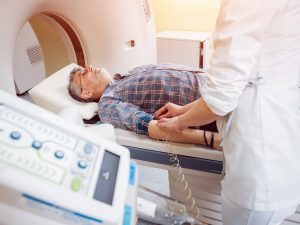
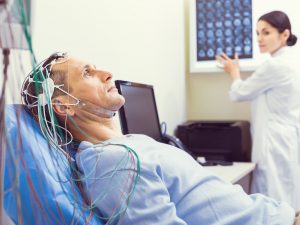
Киста у младенца выявляется с помощью ультразвукового исследования. Впервые такой метод диагностики применяется сразу после рождения. В процессе лечения ребенка нужно водить на УЗИ каждый месяц. Это даст возможность вести наблюдение за изменениями образования.
Киста головного мозга у новорожденных – это несвойственный нормальному организму пузырь в органе, заполненный жидкостью. Головной мозг новорожденного иногда поражается одной или даже несколькими кистами. Их наличие диагностируется ещё до рождения. В большинстве случаев (90% из 100) такая киста исчезает самостоятельно. Сложнее лечить образования, которые диагностируются после рождения. Это – свидетельство такого негативного фактора, как инфекция во время беременности или непосредственно при родах.
К лечению надо приступать немедленно. Принято считать, что киста пройдет самостоятельно, но это всего лишь вероятность. Нужно свести риск к минимуму и устранить источник возможных сильных головных болей и нарушений развития мозга. Обычно родителям предлагают сразу приступить к лечению, и от него не стоит отказываться. Особо опасны кисты, которые достигают больших размеров. В таких случаях их положение может меняться, а близлежащие ткани из-за этого сдавливаются, и головной мозг начинает страдать от механического воздействия.
Нельзя допускать опасности прогрессирования болезни. Это может привести к инсульту, который называют геморрагическим. Оперативность в диагностике и лечении – залог будущего здоровья малыша.
Субэпендимальная киста у новорожденного обычно свидетельствует о внутриутробном инфицировании. Опасность кисты определяется по её разновидности. Если диагностирована субэпендимальная киста у новорожденных, её рассматривают как патологию. Она обычно возникает из-за недостатка кислорода или в результате незначительного кровоизлиянии в отдел головного мозга, который называется желудочек. Если имело место кислородное голодание, ткани начинают отмирать. Их заменяет полость, которая наполняется жидкостью – киста.
В большинстве случаев, такие кисты у младенцев исчезают самостоятельно. На это требуется некоторое время. Опасности для мозга ребенка и его развития они не представляют. Если установлено наличие субэпендимальной кисты, немедленно начинается наблюдение ребенка, регулярно проводятся УЗИ и отслеживается процесс его развития. Это помогает предотвратить возможные осложнения.
При росте кисты одновременно увеличивается давление жидкости в ней. Нельзя допускать сдавливания тканей. Это может привести к деформациям головного мозга, в частности, из-за изменения положения образования. В результате самочувствие ребенка ухудшается до критического уровня.
Кисты сосудистых сплетений у новорожденного – легко излечимое часто встречающееся заболевание. Именно сосудистые сплетения в первую очередь образуются в голове человеческого эмбриона. Их обнаруживают уже на шестой неделе беременности, когда наблюдают за плодом с помощью УЗИ. С участием сосудистых сплетений производится особая мозговая жидкость – ликвор. Она служит основой для правильного развития клеток будущего спинного и головного мозга.
Чем опасна подобная киста? Сложнейшее по природе сосудистое сплетение образуется у будущего ребенка в количестве двух штук. Их наличие говорят о том, что мозг развивается нормально. В сосудистых сплетениях нет нервных клеток. Но именно в них образуется жидкость, питающая нервные клетки на начальных этапах развития эмбриона.
У подобного вида кисты есть свои особенности. Капли мозговой жидкости попадают в своеобразную ловушку, размещаясь в сосудистом сплетении. В результате появляются сосудистые кисты. В этих полостях заключен ликвор. Кисты образуются в правом и левом сосудистом сплетении, их легко обнаружить ультразвуком. Бывают и двусторонние образования. Появление такого образования свидетельствуют о том, что беременность проходит с нарушениями, но это ещё не значит, что ребенок родится больным.
Киста яичника у новорожденных возникает при определенных сопутствующих факторах. С разрушением экологии и по некоторым другим причинам, например, из-за инфекций или вредных привычек матери, у девочек сразу после рождения могут появиться нежелательные образования. Медицинская статистика подтверждает: подобных случаев становится все больше. Кисты во внутренних половых органах девочек появляются даже в очень раннем возрасте, а иногда и у плодов. Такие кисты нетрудно выявить во время планового УЗИ. По статистике они образуются не ранее, чем на 24 неделе беременности.
Почему у новорожденных девочек появляется киста яичника? Очень важна наследственность. Это один из самых существенных факторов, влияющих на появление новообразований на яичниках. Иногда причины бывают другими, но все они связаны со здоровьем матери:
источник
ведущий врач-невролог, врач высшей врачебной квалификационной категории
Перивентрикулярная киста у новорожденного свидетельствует о перенесенной гипоксии во время беременности. Мелкие кисты до4-х мм рассасываются сами , их лечить не нужно. Более крупные- дают в клинике нарушение сна ,провышенную возбудимость, нарушение тонуса , асиметрию тонуса. Лечат последствия этой кисты , А киста будет постепенно уменьшаться, в зависимости от ее размеров — будут и ее проявления .
Добрый день!
ребенку 3.5 года (не разговаривает, точнее говорит очень мало и в основном на своем) сделали КТ головного мозга:
В задних отделах перивентрикулярных областей и суправентрикулярных слева визуализируются группы мелких очагов ликворной плотности, округлой формы,с относительно четкими контурами, размером до 2-4 мм в d.
Заключение КТ- признаки ликворокистозных изменений взадних отделах перивентрикулярных областей и суправентрикулярных областей слева.
Подскажите пожалуйста, что нам теперь делать, ( врач невролог у которого мы были, успокоил, сказал что ни чего страшного нет, но я все равно беспокоюсь). Могут ли эти кисты со временен рассосаться? Может вы что то по советуете?
Заранее большое спасибо.
Пожалуйста, помогите нам разобраться в нашей проблеме! Нашей дочке 6 месяцев. В 1 месяц делали УЗИ головного мозга, нашли две кисты 3 и 4 мм с права и с лева соответственно. Прокололи уколы Кортексин , проделали массаж. Жалоб на ребенка не было. Развивается в соответствии с возрастом, хорошо набирает вес, спит спокойно, особо не капризничает. Был небольшой тонус, но после массажа все прошло. Сейчас становится на четвереньки, пытается ползать, но пока не сидит. В 6 месяцев пошли на повторное УЗИ. В заключении про кисты ничего не написали, но написано структурные изменения — гиперэхогенные включения по ходу сосудистой стенки. Примечание: Перивентрикулярно по латеральной поверхности в области тела желудочка участок значительной повышенной эхогенности с акустической тенью шириной 2,5 мм размером 10*3,6*6 мм. Заключение: УЗ признаки очаговых изменений перивентрикулярно справа ( участок глаза?). Мы очень испугались такого заключения, но невролог сказал, что внешне девочка абсолютно здорова и посоветовала нам переделать УЗИ в другом месте. Мы УЗИ переделаем, но волнения все равно остались, подскажите, что значит такой диагноз и чего нам ждать? Заранее большое спасибо за ответ!
Здравствуйте! Помогите пожалуйста расшифровать нейросонографию. У нас двойняшки: сын и дочь. Родились на 32 неделе. Нам сейчас 4 месяца. Прошли НСГ, назначили только массаж и лфк. Я очень переживаю за своих детей. Если вам не сложно, будьте добры помогите нам в консультации. Достаточно нам этого лечения и нет ли опасности для здоровья наших ребятишек? НСГ сына: Визуализация: удовлетворительная Структуры головного мозга расположены правильно и развиты соответственно возрасту. Субарахноидальное пространство (N до 3 мм) слева до 5,3 мм, справа до 3,8 мм. Межполушарная щель: (N до 5 мм) 4,4 мм. Перивентрикулярная область не изменена. Боковые желудочки (мм): передний рог (N до 4 мм) слева 5, справа 3,5 затылочный рог слева N. справа N. Третий желудочек (N до 3 мм) не расширен. Сосудистые сплетения: симметричны Справа: контуры ровные, эхогенность обычная, эхоструктура в верхних отделах визуализируется жидкостное включение d 3,2 мм. Слева: контуры ровные, эхогенность обычная, эхоструктура не изменена. Вещество головного мозга и базальные ганглии: структурных изменений нет. Структуры задней черепной ямки: без особенностей. IR=0,57 (N 0.55-0.75) Заключение: Эхографическая картина умеренной дилатации субарахноидального пространства слева, переднего рога левого бокового желудочка, кисты в проекции сосудистого сплетения правого бокового желудочка. Показатели мозгового кровотока в пределах нормы. НСГ дочери: Визуализация: удовлетворительная Структуры головного мозга расположены правильно и развиты соответственно возрасту. Субарахноидальное пространство (N до 3 мм) 4мм. Межполушарная щель: (N до 5 мм) делатирована до 7,3 мм. Перивентрикулярная область не изменена. Боковые желудочки (мм): передний рог (N до 4 мм) слева 6,5, справа 6,2 затылочный рог слева 17. справа 17. Третий желудочек (N до 3 мм) не расширен. Сосудистые сплетения: симметричны Справа: контуры ровные, эхогенность обычная, эхоструктура не изменена. Слева: контуры ровные, эхогенность обычная, эхоструктура не изменена. Вещество головного мозга и базальные ганглии: структурных изменений нет. Структуры задней черепной ямки: без особенностей. IR=0,62 (N 0.55-0.75) Заключение: Эхографическая картина умеренной дилатации ликворной системы головного мозга. Показатели мозгового кровотока в пределах нормы.
источник
1. Причины и факторы риска 2. Патогенез 3. Клиническая картина 4. Терапевтические мероприятия
Осложненные роды могут стать причиной травматизма у новорожденных детей. Одной из травм является гипоксико-ишемическое поражение вещества, которое располагается вдоль наружно-верхних отделов боковых желудочков головного мозга. Главным повреждающим фактором является кислородное голодание, хотя в некоторых случаях существуют и другие причины. Таким образом, при наличии мелкоочаговых инфарктов вещества ставится диагноз «перивентрикулярная лейкомаляция» (ПВЛ).
Изменения головного мозга проявляются кистами и полостями, которые формируются в течение примерно одного месяца. Именно поэтому в конце первого месяца жизни для всех новорожденных детей должна быть проведена нейросонография (НСГ).
Поражение носит необратимый характер. Это значит, что лечение, которое применяется после постановки этого диагноза, не может помочь избавиться от патологии.
У недоношенных новорожденных детей часто могут возникать другие поражения головного мозга. которые необходимо дифференцировать от ПВЛ. К некоторым из них относятся церебральная лейкомаляция, телэнцефальный глиоз, псевдокисты, мультикистозная энцефаломаляция, субкортикальная
лейкомаляция и т. д.
Возможность появления этой патологии повышается у недоношенных детей: при этом чем меньше вес при рождении, тем вероятнее развитие патологического процесса. К другим факторам риска относят пол ребенка: мальчикам диагностируют это заболевание чаще, чем девочкам.
Помимо гипоксии мозга на появление очагов ПВЛ может влиять избыточное количество углекислого газа (гиперкапния) в крови, а также кислородное отравление (гипероксия), которое иногда возникает при искусственной вентиляции легких во время реанимационных мероприятий. Опасной является ситуация резкой смены гипоксии гипероксией, что может случиться без контроля содержания и соотношения кислорода и углекислоты в крови во время ИВЛ. Кроме того, усугублять положение может развившаяся инфекция.
Отмечено также, что риск появления ПВЛ повышается, в зависимости от времени года: чаще всего она диагностируется у тех детей, последние два – три месяца которых приходятся на зиму или раннюю весну. Специалисты связывают это с влиянием метеорологических перепадов, которые влияют на беременность. Также может играть роль гиповитаминоз.
В результате названных причин возникает некроз белого вещества головного мозга, после чего к патологическому процессу добавляется дегенерация астроцитов (звездчатых нейроглиальных клеток с отростками), разрастание микроглии (специфических глиальных клеток ЦНС) и скопление липидосодержащих макрофагов в некротизированных тканях. После этого начинается фагоцитоз поврежденных участков – примерно через 5–7 дней, а через неделю происходит формирование кист (это занимает две недели, а иногда – больше). На завершающих стадиях возникают глиозные рубцы или псевдокисты. В некротизированных областях появляются вторичные геморрагические инфаркты. В течение 2–4 месяцев происходит атрофия ткани.
ПВЛ развивается в первые часы, но также может возникнуть и позднее – вплоть до 10 дней после рождения. Лейкомаляция также может поражать внутриутробно – если течение беременности отличается патологическим характером (гестоз, обострение хронического пиелонефрита, гепатита, фетоплацентарная недостаточность).
Уже в роддоме у детей отмечается синдром угнетения центральной нервной системы. Он выражается снижением:
- тонуса мышц;
- специфических рефлексов;
- двигательной активности;
Примерно у четверти новорожденных младенцев присутствует судороги. Почти половина детей страдает от синдрома гипервозбудимости. У некоторых младенцев могут отмечаться стволовые симптомы (нарушения сердечно-сосудистой, дыхательной деятельности). В некоторых случаях какие-либо аномалии в периоде новорожденности могут отсутствовать, а в отдельных вариантах ПВЛ приводит к летальному исходу, независимо от лечения.
Для этого патологического процесса характерно присутствие стадии «мнимого благополучия», которая может длиться 3–9 месяцев, после чего развиваются признаки церебральной недостаточности. Это проявляется нарушением сознания, глотательных рефлексов, дыхания, повышением артериального давления.
Перивентрикулярная лейкомаляция становится почти в 90% случаев причиной детского церебрального паралича (ДЦП), в 60% — сходящегося косоглазия.
Степень тяжести церебральных расстройств зависит от многочисленности и площади лейкомаляционных полостей. Однако в тех случаях, когда очаги распределены тонко вокруг желудочков, прогноз имеет более благоприятный характер.
Процент практически здоровых младенцев с ПВЛ составляет примерно 4%. Последствия поражения для них могут быть незначительны.
Изменения головного мозга носят необратимый характер – по этой причине радикальное лечение, позволяющее избавиться от патологии, не существует. Терапия направлена на устранение негативных симптомов и улучшение мозговых процессов. Стандартно используются ноотропы, корректоры мозгового кровообращения, а также препараты, позволяющие справляться с двигательными нарушениями.
Поскольку ПВЛ в большинстве случаев встречается у недоношенных новорожденных детей, главной мерой профилактики патологии является продление срока беременности, предупреждение преждевременных родов.
Частота осложнений после получения кровоизлияний может снижаться, если адекватно использовать в лечении препараты сурфаканта, уменьшающего проявление дыхательных нарушений. Кроме того, оснащение реанимации новорожденных современной аппаратурой для проведения автономной искусственной вентиляции легких снижает возможность тяжелого последствия для детей.
Поддерживающее лечение ребенка с данным диагнозом должно происходить в течение всего периода детства.
Итак, перивентрикулярная лейкомаляция – это тяжелое поражение головного мозга, которое встречается у новорожденных (преимущественно, недоношенных) детей вследствие тяжелых родов, осложненной беременности. Заболевание следует отличать от других патологий (среди которых псевдокисты, церебральная лейкомаляция, телэнцефальный глиоз и т. д.), по той причине, что лечение этих болезней может отличаться друг от друга.
С этим заболеванием вам нужно обратиться:
к неврологу, неонатологу
Перивентрикулярная лейкомаляция (ПВЛ) — это повреждение белого вещества вдоль боковых отделов желудочков мозга (инфаркт, некроз ткани), причина которого гипоксия и ишемия. У недоношенных детей повреждение возникает из-за незрелости мозга.
Под термином лейкомаляция подразумевают ишемическое размягчение белого вещества мозга в перивентрикулярных зонах, прилегающих преимущественно к наружной поверхности боковых желудочков. Процесс может затрагивать лобную, теменную, височную и затылочную области или ограничиваться локальным очагом. Конечным исходом ишемического поражения этих зон обычно является образование кист, от единичных до множественных, и от мелких до крупных, местами сливающихся.
Область, окружающая наружные углы боковых желудочков, включает в себя нисходящие двигательные пути. В непосредственной близости от желудочков расположены нервные волокна, иннервирующие нижние конечности, более латерально проходят нервные подокна, ответственные за иннервацию мышц рук, поэтому спастический процесс чаще развивается в ногах, чем в руках.
ПВЛ может вызвать нарушения развития моторики и когнитивные нарушения. ПВЛ возникает внутриутробно, во время или после рождения. Это серьезное заболевание, в результате которого риск инвалидности достигает до 93%.
Частота проявления у недоношенных детей весом менее 1500 грамм 12%, в последние годы 2-5%.
Нейросонографическая картина перивентрикулярной лейкомаляции предусматривает 4 степени повреждения белого вещества мозга.
I степень — преходящее повышение эхоплотности перивентрикулярных зон, больше 7 дней.
II степень — повышение перивентрикулярной эхоплотности, мелкие локальные кисты, расположенные вблизи боковых желудочков.
III степень — повышенная перивентрикулярная эхоплотность, обширное перивентрикулярное кистозное поражение.
IV степень — повышенная эхоплотность, распространяющаяся в белое вещество, в сочетании с кистами белого вещества.
Кроме того, выраженные перивентрикулярные лейкомаляции сопровождаются атрофией белого вещества мозга со вторичным расширением и деформацией тел боковых желудочков.
В клинической картине на ранней стадии перивентрикулярной лейкомаляции можно выделить три варианта:
— стертая форма, ничем не отличающаяся от обычных проявлений энцефалопатии, и выявление на этом фоне кист при УЗИ головного мозга оказывается весьма неожиданным;
— среди неврологических симптомов доминирует выраженная и длительная мышечная гипотония конечностей;
— неврологический статус с первых дней указывает на тяжелое поражение головное мозга.
Основной причиной перивентрикулярной лейкомаляции является хроническая внутриутробная гипоксия плода или острая интранатальная асфиксия, а предрасполагающим фактором — недостаточное кровоснабжение перивентрикулярных областей, так как эти отделы мозга являются «водоразделом» между мозговыми артериями и «питаются» их конечными ветками. Соответственно они легче подвергаются ишемии.
— недостаточное развитие артериальных кровеносных сосудов белого вещества мозга
— колебания кровяного давления, как повышение так и понижение (у глубоко
недоношенных авторегуляция кровоснабжения мозга недостаточно развита)
— недостаток кислорода в момент рождения
— ранняя острая дыхательная недостаточность (РДС)
— низкое содержание углекислого газа в крови
— сепсис, некротизирующий энтероколит (НЭК), хорионамнионит во время беременности матери
Ультразвуковое исследование головного мозга: в первые недели жизни наблюдается вокруг желудочков из-за уплотнения мозговой ткани т.н ишемический некроз. Через 2 недели, когда некротическая ткань восстанавливается, можно увидеть маленькие кисты, заполненные мозговой жидкостью. Это называется цистической дегенерацией.
Более точную информацию и прогноз можно получить с помощью магнитно-резонансной томографии (MRT) и ЭЭГ.
Ультразвуковая диагностика такого заболевания доступна далеко не каждому аппарату, часто в наших больницах стоят морально устаревшие аппараты УЗИ, не позволяющие проводить исследование на достаточно хорошем уровне. Качественное обследование возможно только если используется современное медицинское оборудование.
Диагностическим тестом перивентрикулярной лейкомаляции на УЗИ является наличие кист в перивентрикулярных областях или значительное повышение эхогенности в этих зонах, сохраняющееся до 7-12-го дня жизни. У недоношенных детей перивентрикулярные кисты при нейросонографическом исследовании обычно выявляются в возрасте 2-3 нед, однако встречается и более раннее их проявление, на 5—7-й день жизни. Это может случиться при остро возникшей ишемии на фоне отслойки плаценты, сопровождающееся выраженным кровотечением или как проявление внутриутробной инфекции с поражением ЦНС.
Риск инвалидности высокий, зависит от объема атрофии белого вещества и повреждения ткани мозга
Маленькие кисты могут быть причиной развития ДЦП и задержки умственного развития в детском возрасте. Позднее они могут проявиться в младенческом или младшем возрасте.
Радикальных методов лечения не существует. Важно предупреждение развития ПВЛ. Современная терапия позволяет в какой–то мере компенсировать возникшие нарушения. Сегодня интенсивное лечение недоношенных детей более «мягкое», происходит в условиях мониторинга. В результате риск развития серьезных заболеваний снижен.
НЕВОЗМОЖНО ИДТИ К БОГУ, ПЕРЕШАГНУВ ЧЕРЕЗ ЧЕЛОВЕКА
16.01. Новорожденные Перивентрикулярная киста поражает мозг новорожденного ребенка. Довольно часто по этой причине у ребенка могут случиться параличи. Болезнь проявляется крайне тяжелыми последствиями: небольшими участками некроза в перивентикулярных областях белого вещества головного мозга. Специалисты относят данную разновидность кисты к гипоксически-ишемической энцефалопатии. Проводить лечение кисты нужно только при помощи комплексов самых разных типов лечения. Данное заболевание можно отнести к тем, которые вылечить очень трудно и не всегда получается. В основе лечения находится прием самых разных медикаментов, а также хирургическое вмешательство. Очень трудно вылечить перивентрикулярную кисту самостоятельно.
Появиться киста данного типа может по нескольким причинам:
- процессы, которые были вызваны различными патологиями;
- аномалии в развитии плода и отклонения от нормы;
- инфекционные болезни разной степени тяжести;
- различный осложнения во время беременности.
Как правило, в большинстве случаев возникновение кисты происходит в перинатальном периоде.
При возникновении кисты семенного канатика к новорожденного ребенка у него появляется некоторое количество жидкости в данной области, а именно в семенном канатике. Все условия для ее образования создаются в области незаращенного вагинального отростка брюшины. Киста семенного канатика может напоминать водянку оболочек яичек. Происхождение этих болезней одинаковое, точно так же, как и лечение. Данный тип кисты может очень быстро увеличиваться и разрастаться. В таком случае это уже остро возникшая киста. Если же не будет должного лечения и при этом вовремя, то скорее всего киста семенного канатика превратится в паховую грыжу.
В некоторых случаях киста может соединяться с некоторыми органами брюшной полости. Если образование имеет такой характер, то тогда ее величина будет полностью зависеть от времени суток, ведь жидкость будет перетекать из брюшной полости в кисту и обратно. Это есть предрасположения к образования паховой грыжи или же пахово-мошоночной грыжи. В некоторых случаях это может произойти из-за того, что закупорилась полость с внутренней стороны прядью сальника, а иногда и из-за воспалительного процесса.
В большинстве случае лечение происходит при помощи хирургического вмешательства. Как правило, у детей до года практически всегда киста яичка исчезает самостоятельно. Такие дети, которые страдают кистой семенного канатика постоянно находятся под тщательным наблюдением хирурга. Наблюдает врач ребенка примерно до двух лет. Проводить операцию можно только в том случае, если ребенок достиг возраста, как минимум, 1,5 года.
Как правило данное заболевание поражает хориоидальное сплетение, которое находится в головном мозгу. Среди самых веских причин ее появления можно назвать инфекцию, которая находится в организме, перенесенная тяжелая травма, которая была получена или во время беременности, или же непосредственно во время родов. Хориоидальную кисту можно удалить только одним путем: при помощи хирургического вмешательства. Шанс, что киста исчезнет сама по себе — очень небольшой и не превышает примерно 45% всех известных случаев.
Понять, что у ребенка есть хориоидальная киста можно очень легко по ярко выраженных симптомах. У ребенка начинаются очень сильные судорожные реакции или подергивания. В некоторых случаях ребенок может быть постоянно сонным, а в других постоянно плакать и быть беспокойным. При этом организм малыша не может полноценно формироваться и развиваться. Начинает ухудшаться координация движений. После того, как будет проведена операция и киста будет удаленная еще на протяжении некоторого времени ребенку нужно будет проходить медикаментозную терапию.
источник
Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Среди неврологической патологии у новорожденных значительное место занимают расстройства мозговой гемодинамики в виде геморрагических и ишемических изменений, которые по частоте и локализации зависят от выраженности морфофункциональной незрелости центральной нервной системы и несовершенства механизмов ауторегуляции мозгового кровотока. Геморрагические и ишемические поражения головного мозга можно наблюдать в разных комбинациях.
Из всех геморрагически-ишемических поражений головного мозга наиболее распространенными сосудистыми поражениями, достоверно определяемыми при нейросонографии, являются периинтравентрикулярные кровоизлияния, перивентрикулярная и субкортикальная лейкомаляции. Они представляют серьезную проблему в неонатологии, поскольку являются одной из главных причин летальных исходов и психоневрологических нарушений у новорожденных, особенно недоношенных детей. Хотя мозг недоношенных новорожденных более устойчив к действию гипоксии, цереброваскулярные повреждения у них встречаются значительно чаще за счет большей уязвимости сосудистой системы, имеющей анатомо-физиологические особенности в разные сроки гестационного возраста.
Нарушения мозгового кровообращения у новорожденных детей.
- Пери-интравентрикулярные
кровоизлияния - Субарахноидальное кровоизлияние:
- субдуральное кровоизлияние
- внутримозговое (очаговое)
кровоизлияние - кровоизлияние в зрительный бугор
- кровоизлияние в сосудистое
сплетение бокового желудочка - кровоизлияние в мозжечок
- перивентрикулярная лейкомаляция
- субкортикальная лейкомаляция
- парасагиттальный некроз
- поражение зрительных бугров и базальных ганглиев
- инфаркты головного мозга
- очаговые ишемические поражения области ствола и мозжечка
Известно, что кортикальные и субкортикальные отделы мозга с 24 до 36-37 недель внутриутробного развития хорошо кровоснабжаются лепто-менингеальной эмбриональной сосудистой сетью, что и предохраняет эти структуры от повреждений у преждевременно рожденных детей. Набольший дефицит кровоснабжения испытывает перивентрикулярная зона (белое вещество мозга, лежащее выше боковых желудочков на 4-5 см), состоящая из нисходящих кортикальных путей. Глубокие слои перивентрикулярного белого вещества являются зоной смежного кровоснабжения между гередней, средней и задней мозговыми артериями. Сосудистые анастомозы в эти сроки гестации слабо развиты, и поэтому нарушение тока крови по глубоким артериям у маловесных новорожденных вызывает снижение перфузии мозговой ткани — перивентрикулярную ишемию и развитие перивентрикулярной лейкомаляции.
Основным источником перивентрикулярных кровоизлияний (ПВК) является герминальный матрикс (ГМ), функционирующий в мозге с эмбрионального периода. Максимально эта структура представлена у плодов в 12-16 недель гестации. Усиленно развиваясь до 6-го месяца внутриутробной жизни, она в дальнейшем претерпевает инволюцию и к 32-й неделе гестации практически перестает существовать. Герминальный матрикс расположен ниже и латеральнее эпендимы, выстилающей дно бокового желудочка, и находится непосредственно над головкой и телом хвостатого ядра. Герминальный матрикс — важнейшая структура мозга, поставляющая нейрональный и глиальный строительный материал для коры и подкорковых ганглиев в процессе раннего онтогенеза. Эта структура кровоснабжается в основном из бассейна передней мозговой артерии, однако ее незрелые сосуды с широкими просветами не имеют базальной мембраны и мышечных волокон. В этой зоне мало поддерживающей стромы, повышена фибрилолитическая активность. Эти факторы способствуют повышенной ранимости сосудов герминального матрикса, особенно у детей с экстремально низкой массой тела. В основе перивентрикулярных кровоизлияний лежит срыв ауторегуляторных возможностей мозгового кровотока, т. е. способности поддерживать постоянство кровенаполнения мозга независимо от колебаний системного артериального давления. Перивентрикулярные кровоизлияния могут быть изолированными (субэпендимальными), распространяться в желудочки (внутрижелудочковые) с вовлечением перивентрикулярной паренхимы (перивентрикулярные) головного мозга за счет развития вторичного геморрагического инфаркта в перивентрикулярной области.
В основу классификации положены степень распространенности кровоизлияния и реакция (расширение) желудочковой системы. В своей работе мы используем классификацию L. Papille et al, которая подразумевает четыре степени кровоизлияния:
- I степень — изолированное субэпендимальное кровоизлияние (субэпендимальная гематома),
- II степень — распространение субэпендимального кровоизлияния в полость бокового желудочка, без его расширения в остром периоде,
- III степень — массивное внутрижелудочковое кровоизлияние с расширением боковых желудочков,
- IV степень — сочетание внутрижелудочкового кровоизлияния и геморрагического перивентрикулярного инфаркта.
По нашему мнению, она наиболее точно отражает локализацию и степень распространения кровоизлияния, учитывает изменение размеров желудочков, является наиболее простой и удобной для практического применения.
При динамическом ультразвуковом наблюдении за новорожденными высокого риска отмечено, что подавляющее большинство перивентрикулярных кровоизлияний возникают и развивается на первой неделе жизни, преимущественно в возрасте от 24 до 72 часов после рождения. У маловесных детей в 15% случаев кровоизлияния возникают в более поздние сроки, после второй недели жизни. Если перивентрикулярное кровоизлияние возникает позже, оно почти всегда имеет доброкачественное течение и возможность осложнений при этом невелика. Отмечают случаи внутриутробной диагностики перивентрикулярных кровоизлияний.
Эхографическая характеристика перивентрикулярных кровоизлияний
ПВК I степени (субэпендимальное кровоизлияние). Субэпендимальную гематому визуализируют в виде гиперэхогенного округлого образования с четкими контурами в области головки хвостатого ядра, каудо-таламической вырезки или межжелудочкового отверстия. Увеличения размеров бокового желудочка при этом кровоизлиянии не отмечают. Изменение формы бокового желудочка на стороне кровоизлияния возможно при гематоме больших размеров.
ПВК II степени. Наряду с гиперэхогенными участками в области головки хвостатого ядра или межжелудочкового отверстия, в полости еще нерасширенного бокового желудочка, нередко с обеих сторон, определяют дополнительные гиперэхогенные структуры, которые связаны с сосудистыми сплетениями и деформируют их. При этом отмечают исчезновение каудо-таламической вырезки за счет дополнительных эхосигналов от сгустка крови.
Наличие расширенных, асимметричных, с неровными контурами глыбчатых сосудистых сплетений, позволяет диагностировать ПВК II степени.
ПВК III степени. Гиперэхогенные структуры (сгустки крови) наблюдают в расширенных боковых желудочках, в 85% случаев они могут быть с двух сторон. В наиболее тяжелых случаях образуются сгустки, которые повторяют форму желудочков мозга (тампонада). В III и IV желудочках сгустки выявляют значительно реже.
ПВК IV степени. Тромб, образовавшийся в боковом желудочке при ПВК III степени, может явиться причиной нарушения венозного оттока через ветви терминальной вены, расположенной перивентрикулярно. Это приводит к венозному инфаркту, что и является основным фактором в развитии перивентрикулярных поражений. Это кровоизлияние характеризуется наличием внутрижелудочкового сгустка крови, расширения желудочков и геморрагического венозного инфаркта в перивентрикулярной зоне, представленного гиперэхогенным участком с четкими контурами. Последний может быть расположен над передним рогом, телом или около заднего рога бокового желудочка. ПВК IV степени в 96-98% случаев одностороннее. В 15-23% наблюдений отмечают нарастание кровоизлияния от субэпендимального до паренхиматозного в течение первой недели жизни.
При динамическом сканировании (ежедневно на первой неделе жизни, далее 1 раз в неделю после 7 дня жизни) ПВК I степени сохраняется до двух-трех месяцев жизни, меняясь по структуре и эхогенности и уменьшаясь в размерах. В 52% гематома бесследно исчезает, или на ее месте, в 48% случаев, в течение 2-4 недель, образуется субэпендимальная псевдокиста (СК), особенностью которой является отсутствие субэпендимальной выстилки. Как правило, субэпендимальная псевдокиста редуцируется к 6-9 месяцам жизни.
Рассасывание внутрижелудочковых сгустков крови после ПВК II и особенно III степени происходит постепенно, чаще в течение 5-6 недель. В области паренхиматозного кровоизлияния при ПВК IV степени в 75-82% случаев на 24-36 сутки жизни образуется порэнцефалическая псевдокиста, связанная с полостью бокового желудочка. Наиболее характерным осложнением ПВК III-IV степени является расширение боковых желудочков, выраженность и частота которого определяется тяжестью перенесенного патологического процесса. Субкомпенсированная дилатация развивается в течение 1-3 недель и наблюдается у 48% детей с ПВК III степени. Обычно к моменту выписки ребенка из стационара можно сказать, было ли расширение желудочков транзиторным, персистирующим или прогрессирующим с развитием внутренней гидроцефалии. О полной или частичной окклюзии судят по расширению вышележащих отделов ликворной системы.
Перивентрикулярная лейкомаляция (ПВЛ) — ишемический инфаркт белого вещества головного мозга вокруг наружных углов боковых желудочков. До недавнего времени диагноз ПВЛ являлся заключением только патоморфологов, поскольку клинической симптоматики, указывающей на поражение перивентрикулярной области у детей раннего возраста, не существует. Патоморфологически при ПВЛ обнаруживают мелкие участки размягченного вещества мозга кпереди от передних рогов, вблизи латеральных углов боковых желудочков и латеральнее задних рогов. В одних случаях через несколько недель после ишемического инсульта происходит кальцификация и глиоз, оставляющие «перивентрикулярный шрам», в других образуются единичные или множественные полости (псевдокисты), которые со временем могут спадаться и ведут к вторичному расширению желудочков и субарахноидального пространства. В 25% случаев ПВЛ сочетается с очаговыми кровоизлияниями. В 25% наблюдений имеют место вторичные кровоизлияния в область некротизированной ткани с образованием геморрагических инфарктов, а иногда и ПВК.
На эхограмме в коронарной и парасагиттальной плоскостях острая (начальная) фаза ПВЛ характеризуется значительным повышением эхогенности перивентрикулярных зон с обеих сторон, более выраженным в области тел и задних рогов боковых желудочков. Реже отмечают повышение эхогенности над передними рогами. Нередко пораженный участок изоэхогенен с сосудистым сплетением и отделен от бокового желудочка только полоской ликвора. ПВЛ носит симметричный, т. е. всегда двухсторонний характер. Ультразвуковой диагноз на этой стадии сложен, так как повышение эхогенности может быть обусловлено особенностями васкуляризации и неполной миелинизацией перивентрикулярных зон у недоношенных новорожденных. Наиболее вероятно развитие ПВЛ, если при повторном исследовании через 10-14 дней сохраняется выраженная эхогенность в перивентрикулярных областях. В дифференциальной диагностике острой фазы ПВЛ и нормального ореола повышенной эхогенности помогает спектральная допплерография.
Поздней эхографической стадией ПВЛ является кистозная дегенерация, развивающаяся на месте высокой эхогенности. Кисты не имеют эпителиальной выстилки, возможно их слияние и образование более крупных полостей. При этом часто наблюдают минимальное и/или умеренное расширение желудочковой системы, преимущественно боковых желудочков за счет передних рогов и тел. Далее, в течение 6-8 недель, кисты спадаются, замещаются рубцовой тканью и вызывают вторичную атрофию вещества головного мозга. При атрофии боковые желудочки не теряют свои обычные очертания, но становятся более округлыми в области передних рогов и тел. При этом не отмечают эхографических признаков окклюзии ликворных путей.
Субкортикальная лейкомаляция (СКЛ) возникает вследствие нарушения кровоснабжения подкорковых структур лептоменингеальными сосудами в последнем триместре беременности. На эхограммах в начальных стадиях наблюдают отек мозгового вещества, который характеризуется диффузным повышением эхогенности тканей головного мозга и снижением (отсутствием) пульсации мозговых сосудов. В дальнейшем, как правило в течение двух недель, на фоне отека развиваются очаги усиления эхогенности без четких контуров. К концу месяца в веществе головного мозга формируются множественные, мелкие, паренхиматозные кисты. При этом незначительно расширяется желудочковая система и нередко субарахноидальное пространство.
Достаточно просто выявить дилатацию желудочков и асимметрию при ультразвуковом исследовании. При наличии сомнений необходимо проведение повторного исследования через какой-то промежуток времени. Одной из наиболее частых причин дилатации является врожденный стеноз сильвиева водопровода.
Агенезия мозолистого тела является другой частой врожденной аномалией развития, при которой развивается гидроцефалия. Это вызывает значительное смещение боковых желудочков и переднее смещение III желудочка.
- Субэпендимальное кровоизлияние визуализируется в виде одного или нескольких гиперэхогенных участков сразу ниже боковых желудочков и лучше выявляется в поперечных срезах, в области передних рогов. Подтвердите диагноз при сагиттальном сканировании: кровоизлияние может быть двусторонним. Это первая степень кровоизлияния.
- Внутрижелудочковое кровоизлияние в нерасширенные желудочки. Появляются дополнительные эхоструктуры на фоне анэхогенных желудочков (так же, как и от гиперэхогенных сосудистых сплетений), соответствующие сгусткам крови в желудочках. Если признаков желудочковой дилатации нет, то это вторая степень кровоизлияния.
- Внутрижелудочковое кровоизлияние в расширенные желудочки. Когда имеется внутрижелудочковое кровоизлияние в расширенные желудочки, то это III степень кровоизлияния.
- Внутрижелудочковое кровотечение, сопровождающееся кровоизлиянием в вещество мозга визуализируется в виде участков повышенной эхогенности в структуре мозга. Это IV степень кровоизлияния, наиболее выраженная.
- Осложнения кровоизлияний. При I и II степенях кровь обычно реабсорбируется в течение первой недели жизни, но более серьезные кровоизлияния (III и IV степени) могут вызвать постгеморрагическую гидроцефалию, а также давать рассасывание ткани с формированием кист полушарий головного мозга. При этом может иметь место задержка развития с неврологической симптоматикой.
Патология мозга новорожденных
- Некроз ткани мозга, определяющийся в виде гипоэхогенной, с нечетким контуром зоны, расположенной латеральнее боковых желудочков (перивентрикулярная лейкомаляция).
- Отек мозга может привести к облитерации желудочков и борозд мозга. Мозг при этом более эхогенен, чем в норме.
- Мозговые инфекции могут давать изменение эхогенности, в том числе и наличие точечных гиперэхогенных структур за счет кальцификации.
источник
В наши дни каждый третий ребёнок рождается с наличием объёмного образования в головном мозге. В 99% случаев – это киста, в 12% — перивентрикулярная. Заболевание представляет серьёзную проблему, так как приводит к массивной гибели нервных клеток и нарушению целого ряда мозговых функций.
Перивентрикулярная киста – это полостное образование в околожелудочковых областях белового вещества головного мозга. Патология выявляется у 12% новорожденных, которым проводилось нейросонографическое исследование.
С морфологической точки зрения – это мелкоочаговая зона коагуляционного некроза, возникшая после инфаркта белого вещества. Наиболее часто поражаются начальные отделы задних рогов боковых желудочков. Обычно образования заполнены жидкостным содержимым.
Основная причина, при которой появляется перивентрикулярная киста у новорожденного, — это гипоксически-ишемическое поражение головного мозга. Данное состояние диагностируется у каждого третьего ребёнка и является следствием следующих причин:
- артериальная гипотония;
- длительный период апноэ после рождения;
- нарушение кровотока в системе «мать-плацента-плод»;
- массивные кровотечения во время беременности;
- злоупотребление привычными интоксикациями (курение, употребление алкогольных напитков);
- обвитие пуповины вокруг шеи;
- ДВС-синдром у матери;
- пороки сердечно-сосудистой системы плода.
Так же способствуют формированию такие состояния, как недоношенность I-II степени, преждевременные роды и задержка роста и развития плода. В процессе формирования образования сменяют друг друга следующие стадии:
Лейкомаляция обычно развивается в течение нескольких часов после рождения, однако может наблюдаться и во время беременности. Крайне редко возможно отсроченное формирование – через 10 и более дней после появления на свет.
Систематика основана на морфологических изменениях в веществе головного мозга. После произведения 15 фронтальных срезов мозга по данным КТ или МРТ оценивается наличие патологических очагов и устанавливается степень тяжести:
- лёгкая степень – 1-4 среза;
- средняя степень – 5-8 срезов;
- тяжёлая степень – 9-13 срезов.
Перивентрикулярная киста головного мозга – самая опасная разновидность лейкомаляции. Сразу после рождения у детей наблюдаются признаки угнетения центральных отделов нервной системы:
- снижение тонуса скелетной мускулатуры;
- ослабление рефлексов;
- замедление двигательной активности.
У 25% новорожденных появляются судорожные припадки. Редко может наблюдаться стволовая симптоматика (угнетение сердечно-сосудистого и дыхательного центров) и летальный исход в течение нескольких часов после рождения.
Самый грозный симптом – развитие параличей, которые появляются не сразу, а после периода «мнимого благополучия», продолжительность которого составляет до 9 месяцев. Часто возникают гемипараличи и гемипарезы на стороне, противоположной патологическому процессу.
Могут быть эпизоды угнетения сознания, нарушение глотательных рефлексов, лабильность артериального давления и сходящееся косоглазие. До 90% случаев детского церебрального паралича обусловлены данной патологией.
Единственным и наиболее информативным методом раннего выявления патологии является нейросонография (ультразвуковое исследование головного мозга), с помощью которого можно не только найти очаг, но и выявить наличие инфекционно-воспалительных осложнений.
В трудных случаях для дифференциальной диагностики с другими отклонениями (новообразования, внутримозговые кровоизлияния, мультикистозная энцефаломаляция и т.п.) могут применяться рентгенографическое исследование, КТ, МРТ.
Терапия заболевания представляет большие трудности. У маленьких детей крайне трудно отследить те или иные симптомы, следовательно, неизвестно какой метод лечения нужно выбрать.
Консервативных методов не существует. Терапия может быть направлена только на купирование клинических проявлений. С этой целью используются:
- ноотропы – стимулируют умственную деятельность, память и мышление;
- препараты, нормализующие кровообращение;
- антигипоксанты.
Часто данная патология встречается у недоношенных детей. Следовательно, основной метод профилактики – пролонгирование сроков беременности до нормативных путём проведения мероприятий, направленных на предотвращение преждевременных родов.
При наличии дыхательных нарушений после рождения показано применение препаратов сурфактанта, ИВЛ. Подобные мероприятия снижают частоту развития осложнений и способствуют ограничению кистозных образований.
Если полостное образование приводит к параличам или неврологической симптоматике, то показано хирургическое лечение. Существует 2 основных метода:
- Радикальный. Киста удаляется посредством вскрытия полости черепа. Метод крайне опасен и реализуется только при угрозе жизни ребёнку.
- Паллиативный. Сущность оперативного вмешательства заключается в удалении жидкостного содержимого кисты. Манипуляции проводятся с использованием шунта или эндоскопа.
Перечень нежелательных явлений крайне широк, среди них можно выделить следующие:
- Инфекционно-воспалительные патологии. Возникают при инфицировании или при нарушении техники проведения операций.
- Угнетение дыхательного и сосудистого центров продолговатого мозга с развитием остановки дыхания и сердца.
- Полное нарушение проводимости с развитием параличей.
- Гидроцефалический синдром. Причина – повышение внутричерепного давления, вызванное значительным объёмом кисты.
Течение благоприятное при своевременном выявлении проведении адекватной терапии. Кисты, размером до 4 мм рассасываются самостоятельно в течение нескольких недель после рождения.
Основной метод профилактики – это предотвращение преждевременных родов и гипоксически-ишемического поражения головного мозга путём тщательного мониторинга состояния плода и общего состояния беременной.
Таким образом, перивентрикулярная киста – серьёзная проблема современной неонаталогии и педиатрии, которая приводит к инвалидизации большого числа детей. Врачам и руководителям здравоохранения необходимо чаще использовать и совершенствовать методы, направленные на ранее выявление патологии и назначение своевременного адекватного лечения.
источник
У каждого двадцать пятого человека на планете формируется ликворная киста головного мозга. Мужской пол более подвержен возникновению образований, женский – менее. Возраст человека при этом не играет абсолютно никакой роли.
Многих людей подобный диагноз приводит в сильный ужас. Они заранее готовятся к самому худшему, впадают в депрессию. Однако сильно ли страшна ликворная киста головного мозга и что это такое вообще?
Чтобы лучше понять особенности аномалии, стоит разобраться в причинах ее возникновения, возможных осложнениях и способах лечения.
В результате различных нарушений в организме человека могут появляться полости с жидкостью внутри. Ликворная киста является одним из таких образований. Она находится в головном мозге человека и может быть разных видов.
Внутри такую кисту заполняет ликвор. Это спинно-мозговая жидкость.
При нормальной циркуляции ликвором обеспечивается регулирование:
- оптимального для организма уровня внутричерепного давления;
- водно-электролитного гомеостаза;
- обмена, происходящего между кровью и мозгом.
Главная функция ликвора — это защита. Жидкость окружает головной мозг и оберегает его от различных повреждений.
Нормальная циркуляция ликвора представляет собой налаженную систему. Она включает несколько этапов:
- Образование жидкости в мозге.
- Ее движение вдоль желудочков.
- Попадание в субарахноидальное пространство спинного и головного мозга.
- Реабсорбацию ликвора в кровь.
При образовании в мозге кисты жидкость попадает туда во время своей циркуляции. Однако из-за плотной оболочки образования отток ликвора из него затрудняется. Так, в пустой полости постепенно накапливается жидкость.
Причин возникновения ликворных кист существует несколько. Это:
- воздействие негативных факторов на мозг в период внутриутробного развития плода, вызывающее дефекты в формирующихся у зародыша тканях;
- последствия менингита и энцефалита, приведшие к образованию спаек, мешающих ликворному оттоку;
- травмы;
- осложнения инфекционных болезней.
Клиническая картина, сопутствующая развитию аномалии, зависит от размеров ликворной кисты, ее локализации и особенностей циркуляции жидкости. Очень часто развитие образования какое-то время протекает скрытно. В этом случае обнаружение кисты происходит случайно, при диагностике другого заболевания.
У малышей первые проявления могут начаться через годы после появления на свет. Основными признаками ликворной кисты у детей являются:
- большой череп;
- боли в голове;
- умственная и физическая отсталость.
У младенцев могут замечаться: выбухающий родничок, расходящиеся швы черепа, закатывание глаз.
У взрослых беспокойные симптомы часто начинаются после травмы головы, инсульта, инфекционной болезни. Они проявляются неспецифическим образом:
- зрительными, слуховыми нарушениями;
- разбалансированностью движений;
- головокружениями, рвотой, тошнотой;
- головными болями;
- расстройствами психики;
- возникновением судорог;
- онемениями, покалываниями различных участков тела.
При обнаружении одного или нескольких подобных симптомов необходимо немедленно обратиться к врачу для проведения диагностики.
Классификация ликворных кист происходит по нескольким критериям:
- локализации (арахноидальная – на поверхности мозга, церебральная – внутри серого вещества);
- расположению (лакунарная, пинеальная, ретроцеребеллярная);
- этиологии (первичная – врожденная, вторичная – приобретенная).
Правильное определение вида образования важно для понимания возможных последствий аномалии и определения методов ее лечения. Основных видов кист всего два. Каждый из них имеет свои особенности.
- Арахноидальная ликворная киста головного мозга. Что это такое: полое новообразование доброкачественного характера. Локализуется в области паутинных оболочек головного мозга. Первичная арахноидальная киста появляется у плода как результат приема матерью во время беременности медикаментозных средств, попадания зародыша под действие радиации, воздействия на него токсических факторов. Вторичная возникает из-за перенесенных заболеваний, ушибов, операций, спровоцировавших повреждения мозговых оболочек. Появление и развитие этого типа кисты в большинстве случаев происходит бессимптомно. Только у двадцати процентов заболевших клинические признаки проявляются.
- Церебральная ликворная киста головного мозга. Что это такое: доброкачественное новообразование, которое располагается в самой толще головного мозга на месте погибших нейронов. Возникает на фоне кислородного голодания, инсультов, инфекционных заболеваний, сотрясений, трепанации черепа.
При отсутствии адекватного лечения каждый вид новообразования может нанести непоправимый вред здоровью человека.
Отсутствие клинической картины, характерной для наличия опасных ликворных кист, свидетельствует о малых размерах новообразования. В этом случае его наличия можно не бояться. Немедленного лечения оно не требует.
При обнаружении ликворной кисты на начальной стадии развития медики ограничиваются лишь наблюдением за ней. Если новообразование не растет и не вызывает неприятных симптомов, трогать его не нужно.
Опасными являются те ликворные кисты, которые постепенно увеличиваются. Достигнув определенного размера, они начинают сдавливать соседние ткани и вызывать дегенерацию мозговых клеток.
Если адекватная медицинская помощь человеком вовремя не получена, то развитие церебральной и арахноидальной ликворных кист головного мозга может вызвать:
- развитие гидроцефалии у детей;
- поражение органов слуха и зрения;
- мозговые воспаления;
- двигательные нарушения;
- парализацию;
- судороги;
- разрыв полости;
- смерть.
Чтобы избежать губительных последствий развития ликворной кисты головного мозга, нужно правильно ее лечить. Для этого специалист должен поставить верный диагноз. Лучше всего проходить обследование там, где квалификация врачей будет бесспорной – в центре нейрохирургии.
Основными методами диагностики ликворных кист головного мозга являются: магнитно-резонансная и компьютерная томографии. В качестве дополнительных исследований проводятся:
- биопсия;
- электрокардиография;
- анализы крови;
- допплерография.
Если наличие ликворной кисты головного мозга подтверждается, то врач принимает решение о целесообразности лечения аномалии. В случае его необходимости выбирается метод борьбы с патологией.
Вариант лечения ликворной кисты головного мозга зависит от интенсивности негативных проявлений аномалии, ее роста и наличия (либо отсутствия) некроза прилегающих тканей.
При диагностировании небольшого образования, требующего медикаментозной терапии, могут назначаться препараты, с различным действием:
- рассасывающим;
- ноотропным;
- ускоряющим снабжение клеток мозга кровью;
- стабилизирующим давление;
- понижающим уровень холестерина;
- антиоксидантным.
Такие лекарственные средства помогают кисте не только остановиться в росте, но и полностью исчезнуть. Однако следует помнить, что подобный исход лечения возможен только под контролем врача. Специалист должен выбрать препараты, назначить схему их приема и дозировки. Заниматься бесконтрольным приемом лекарств запрещено.
Параллельно с медикаментозными препаратами врач может назначить и прием народных средств. Большой популярностью пользуются чаи из сборов лекарственных трав:
- ромашки;
- малины;
- брусники;
- цикория;
- шиповника;
- календулы;
- череды;
- девясила;
- шикши;
- кукурузных рылец.
Главными задачами приема лечебных напитков является улучшение мозгового кровоснабжения и недопущение образования новых спаек. Каждый сбор нужно пить от трех до четырех месяцев. После этого следует заваривать чай из лекарственных трав в другом сочетании.
При борьбе с ликворными кистами часто применяется рецепт лечения болиголовом пятнистым. Он считается самым действенным средством народной медицины при подобной проблеме.
- Настойка готовится из оливкового масла и семян лекарственного растения. Они перемешиваются и хранятся в темном месте три недели. Средство необходимо капать в ноздри по 2 капли трижды в день.
- Терапию можно проводить еще одним способом: настойку пьют по определенной схеме. Начинают с одной капли, добавляя каждый день – по нарастающей. Когда доходят до сорока – идут на убыль. Такой курс лечения болиголовом длится семьдесят девять дней.
Не стоит забывать, что лекарственные травы не являются совершенно безопасными для организма. Во время их приема важно соблюдать определенную схему и дозировки. Самостоятельно выбирать средства народной медицины и лечиться ими по своему усмотрению нельзя.
Консервативная терапия не поможет, если у пациента наблюдаются:
- быстрое увеличение кисты;
- мозговые кровоизлияния;
- развитие гидроцефалии;
- некроз соседних тканей.
В подобных случаях требуется экстренное оперативное вмешательство. Это может быть:
- трепанация;
- эндоскопия;
- шунтирование;
- дренирование.
Для избегания нанесения вреда здоровью необходимые манипуляции должны быть выполнены врачом высокого класса. Поэтому процедуру рекомендуется проходить в центре нейрохирургии.
Следует помнить, что развитие ликворной кисты мозга – это аномальное состояние, требующее постоянного медицинского наблюдения. Если лечение необходимо, то правильно выбранный метод сыграет решающую роль в выздоровлении пациента. Именно поэтому при первых симптомах патологии нужно немедленно проходить диагностику, а после – полностью следовать рекомендациям специалиста.
источник
Клиника, диагностика, прогноз, осложнения перивентрикулярной лейкомаляции
Таким образом, основные клинические симптомы ПЛ в раннем периоде — это: 1) снижение тонуса нижних конечностей, 2) возрастание тонуса в шейных разгибателях, 3) приступы апноэ и брадикардии, 4) гипервозбудимость, 5) псевдобульбарный паралич с бледностью конечностей и 6) судороги.
При электроэнцефалографическом (ЭЭГ) исследовании в начальной стадии у многих детей обнаруживается пароксизмальная активность и депрессия ЭЭГ. Данные ЭЭГ используются для прогноза последствий ПЛ. В то же время специфичность проявлений ПЛ на ЭЭГ низкая (в том числе на амплитудной интегрированной ЭЭГ).
Наибольшее распространение в диагностике ПЛ получило нейросонографическое исследование (НСГ), которое выполняют через большой родничок в 2-х плоскостях — коронарной и сагиттальной. Смена угла наклона датчика позволяет оценить структуру головного мозга в различных его отделах и выявить различные повреждения. ПЛ относят к группе ишемических поражений перивентрикулярных областей боковых желудочков мозга. На месте ранее выявляемых очагов уплотнения в последующем образуются эхосвободные кистозные образования. Такие изменения называют «кистозной ПЛ». Средний срок образования кист составляет 19 дней с момента рождения. Наиболее выраженные эхографические проявления ПЛ наблюдались на 3—5 дни жизни, причем повышенная эхоген- ность стойко сохранялась до 10 дня, а в последующем формировались единичные или множественные кисты перивентрикулярных областей мозга (Валид М. А. и соавт., 2005). При НСГ-исследовании глубоко недоношенных детей (менее 1500 г) ПЛ обнаруживалась у 31,9 % детей. Авторы обнаруживали в зависимости от стадии процесса следующие изменения: участки повышенной зхоплотности, кисты (локализованные и распространенные, вентрикуломегалию и церебральную атрофию
Имеется классификация степеней тяжести ПЛ, основанная на данных нейросонографии (см. выше). Особую трудность представляет диагностика ПЛ в острой фазе, поскольку ореол повышенной перивентрнкулярной эхоплотности в норме присутствует у недоношенных новорожденных. Эти изменения могут исчезать в течение 2—3 недель после рождения и свидетельствовать о каких-либо нарушениях кровообращения в перивентрикулярных областях мозга.
Оценивая результаты нейросонографического исследования (НСГ). следует иметь в виду, что, во-первых, повышенная эхоплот- ность — не синоним ПЛ, что это могут быть очаги умеренного отека мозга, телэнцефалической лейкоэнцефалопатии, астроглиоза, перивентрикулярного геморрагического инфаркта, энцефалита и других патологических процессов. Тем более что в 85 % случаев ПЛ 1-й степени тяжести наблюдается полное выздоровление, что сомнительно при понимании ПЛ как процесса с обязательными некрозами мозговой ткани. Абсолютно справедливо замечание А. Б. Пальчика и Н. П. Шабалова (2000),что «исследователь видит зоны повышенной или пониженной эхогенности, а не «отек», «ишемию», «кровоизлияние», «сгусток», «кальцификат», «лейкомаляцию» и т. д.; на основании данных нейросонографии он может лишь предположить о причинах и сути измененной эхогенности». Во-вторых, сомнительно относить все случаи 4-й степени ПЛ с распространенными поражениями бе-лого вещества полуовальных центров к истинной ПЛ. Такие поражения более характерны для мультикистозной энцефаломаляции или так называемой «комплексной ПЛ», а не ПЛ с характерными именно перивентрикулярными очагами. Полагаю, что требуется усовершенствование нейросонографической классификации ПЛ. Нейросонография позволила сделать прорыв в диагностику ПЛ, популяризировать данное поражение как одно из наиболее изученных. Вместе с тем необходимо комплексное изучение других пора жений головного мозга, чтобы не заниматься гипердиагностикой ПЛ и не относить любые поражения в белом веществе больших полушарий к ПЛ.
При так называемой «некистозной» форме ПЛ НСГ-исследование может быть отрицательным в 50—70 % случаев, поэтому целесообразно проведение неоднократных исследований (динамическое сканирование). Это повышает диагностическую информативность НСГ при ПЛ.
Особенно много заблуждений возникает при оценке «кист» и «псевдокист» белого вещества мозга, которые специалисты УЗИ не дифференцируют между собой. Поэтому обнаруженные кисты у новорожденных первых дней жизни ошибочно относят к ПЛ, возникшей антенатально. ПЛ — это в основном постнатальный процесс, а в первые дни жизни могут обнаруживаться псевдокисты, представляющие собой порок развития головного мозга, а не истинные кисты. Псевдокисты не имеют никакого отношения к ПЛ, хотя могут сочетаться с ПЛ.
В своих исследованиях я обнаружил высокую частоту поражений зрительной лучистости и рекомендовал для диагностики ПЛ «более тщательное исследование функции зрения». Отрадно, что такие исследования в настоящее время появились. Выявлено, что у детей с ПЛ в 100 % случаев наблюдаются офтальмологические осложнения. У 80,3 % детей с ПЛ обнаруживается синдром расширенной экскавации диска зрительного нерва, свидетельствующий о транссинаптической нейрональной дегенерации и ретроградной дегенерации аксонов. Поскольку очаги ПЛ в основном двусторонние, постольку в подавляющем большинстве случаев (93,4 %) обнаруживаются билатеральные поражения диска зрительного нерва. Выявлялись и другие офтальмологические нарушения: деформация диска зрительного нерва, его атрофия, гипоплазия и др. Следует отметить, что распшрения экскавации зрительного нерва могут обнаруживаться и при других патологических процессах головного мозга, если они затрагивают зрительную лучистость и стриарную кору. Ранняя диагностика офтальмологической патологии у новорожденных с ПЛ позволяет назначить своевременное лечение, избежать значительной зрительной депривации и назначить более эффективную функциональную реабилитацию.
Для диагностики и прогноза формирования ПЛ в настоящее время рекомендуют исследование в сыворотке крови мозгового нейротрофического фактора (BDNF) и специфического белка астроцитарной глии S-100. Повышение концентрации S-100 с высокой достоверностью позволяет прогнозировать развитие тяжелых структурных повреждений мозга, особенно при сочетании ПЛ с ВЖК, когда наблюдалось превышение показателей нормы в 10—12 раз. У новорожденных с ПЛ уровень сывороточной концентрации BDNF низкий.
Прогноз ПЛ. По моим и литературным данным, при ПЛ поражаются прежде всего кортико-спинальный тракт, зрительная и слуховая лучистости. Следствием ПЛ являются 1) ДЦП (чаще спастическая диплегия, при тяжелых поражениях квадриплегия), 2) задержка психомоторного развития, и 3) нарушения зрения (нарушения фиксации, нистагм, страбизм и др.). Могут нарушаться функции слуха. По данным О. Н. Малиновской и соавт. (2005), исходом ПЛ являются: 1) выздоровление (19,5 %), 2) детский церебральный паралич (ДЦП) (80,5 %), 3) судорожный синдром и эпилепсия (37,5 %) и 4) задержка психоречевого развития (66 %). Все дети с задержкой развития страдали ДЦП, причем чем значительнее двигательные нарушения, тем грубее нарушения психоречевого развития. У всех детей с 3 и 4 степенями тяжести по данным
НСГ развивался ДЦП. Такой исход как выздоровление может вызвать возражения, так как самое минимальное повреждение головного мозга при ПЛ сопровождается разрушением нервных волокон, их ретроградной дегенерацией, астроглиозом и др. Надо полагать, что не все случаи ПЛ по данным НСГ-исследования представляют случаи истинной ПЛ. В то же время такие последствия, как эпилепсия, вероятно, связаны с поражениями корковых структур и су- бикулюма гиппокампа, которые весьма чувствительны к гипоксии. Надо дифференцировать между собой последствия ПЛ и последствия других сопутствующих поражений головного мозга, что представляет трудную задачу.
По данным J. Volpe (2003), 10 % выживших глубоко недоношенных детей (массой до 1500 г) с ПЛ страдают ДЦП, а 50 % в дальнейшем имеют психомоторные нарушения.
При ДЦП по данным НСГ определяют 5 основных типов нарушений: ПЛ (33,1 %), постгеморрагическую порэнцефалию, аномалии развития, кортикальную и субкортикальную атрофию, повреждения базальных ганглиев (Гайнетдинова Д. Д., 2001). ПЛ и ДЦП — это разные нозологические единицы. По моим данным, после перенесенной ПЛ формируются кисты в белом веществе мозга с характерным преобладанием в определенных отделах мозга (см. топографию), в той или иной степени атрофируется белое вещество, а при тяжелой степени поражения гипоплазируются мозолистое тело, кора больших полушарий и расширяются боковые желудочки (возникает вентрикуломегалия).
Считают, что ДЦП формируется у всех детей с ПЛ, не удерживающих голову к 6 мес. скорригированного возраста. Причем от степени тяжести ПЛ зависит прогноз неврологических нарушений. При ПЛ 1 степени все дети самостоятельно передвигались, при ПЛ 2-й степени передвигались самостоятельно или с поддержкой 80 % детей, а при 3-й степени — только 15 % детей передвигались самостоятельно, а 45 % больных не передвигались и не могли сидеть самостоятельно.
Для профилактики ПЛ рекомендуется антенатальная диагностика хориоамнионитов с последующим введением матери на 24-31 неделях беременности бетаметазона, положительно влияющего на защитную реакцию плода при воспалении. Важно предупреждать преждевременные роды, не употреблять наркотики (кокаин), диагностировать внутриутробные инфекции, предупреждать пролонгированную гипокарбию при искусственной вентиляции легких и т. д.
Многие исследовали указывают на роль фактора некроза опухоли (ФНО) в развитии ПЛ (вызывает артериальную гипотензию, усиливает интраваскулярную коагуляцию, способствует гибели олигодендроцитов и т. д.). В то же время кортикостероиды блокируют продукцию ФНО астроцитами и снижают его активность, что позволяет считать обоснованным их применение при лечении и профилактике ПЛ. Однако имеются данные, что раннее введение дексаметазона у недоношенных детей при СДР коррелирует с развитием ПЛ. При ранней терапии дексаметазоном в первые три дня жизни возрастает частота неврологических осложнений и ДЦП. Поэтому рекомендуется использовать этот препарат после 2-й недели жизни или применять альтернативные препараты (будесонид, пулимикорт) и ингаляционные стероиды (флутиказон, беклометазон).
У детей, находящихся на ИВЛ, очень важно контролировать газы крови, поскольку доказано, что гипероксия, гиперкапния и ацидоз являются факторами риска развития ПЛ. Терапевтические мероприятия при ПЛ во многом сходны с мерами при лечении «гипоксически-ишемической энцефалопатии». Это введение антиоксидантов, ингибиторов образования кислородных радикалов, блокаторов кальциевых каналов и антагонистов кальция и т. д. Целесообразно применение и давно известной кранио-церебральной гипотермии (охлаждение головки), способствующей замедлению обменных процессов в головном мозге и снижающей риск ишемиче- ских его поражений.
В терапии ПЛ важно использовать препараты, улучшающие мозговое кровообращение (винпоцетин, стугерон, ницерголин) и ноотропы (пирацетам). При респираторном дистресс-синдроме целесообразно назначение препаратов сурфактанта, уменьшающих тяжесть дыхательных расстройств и уменьшающих потребность в ИВЛ, а тем самым снижающих риск возникновения новых очагов ПЛ. В терапии ДЦП, возникших вследствие ПЛ, рекомендуется использование церебролизина (Гайнетдинова Д Д., 2001), обладающего антикласто- генной и антиоксидантной активностью. Все разработки по лечению церебральной ишемии и гипоксически-ишемической энцефалопатии 3-й степени целесообразно применять и при лечении ПЛ.
источник