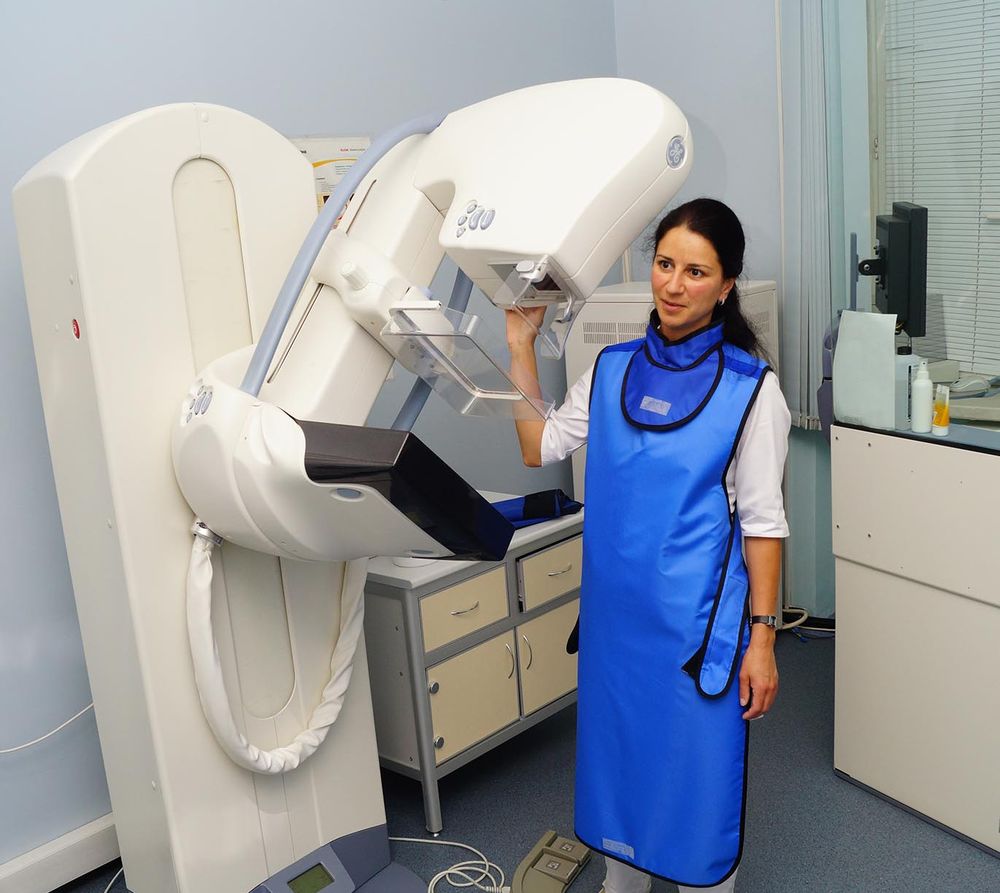
Деление на стадии — выражение, используемое для описания различных исследований, обычно производимых после того, как поставлен диагноз далеко развившегося рака, чтобы определить, локализована ли еще болезнь или уже распространилась на другие области тела. Например, операция по извлечению нескольких подмышечных лимфоузлов производится для определения стадии рака.
Когда речь идет о раке молочной железы, деление на стадии производится для определения стадии рака. Основная цель врача в этой ситуации состоит в том, чтобы удалить рак пока он еще остается в пределах груди (если в другой груди обнаруживается еще одна опухоль, это обычно «новый первичный рак», а не метастаз первого). Если уже известно, что рак присутствует в других частях тела, удаление молочной железы имеет разве что ограниченное значение, если только она не болезненна, инфицирована или изъязвлена. Необходимость установления стадии, если выявлен запущенный рак — еще одна причина для отделения диагноза от лечения: чтобы не оперировать больше, чем необходимо.
В большинстве случаев подозрительные симптомы вызваны доброкачественными образованиями. Но одна- две из каждых десяти биопсий влечет диагноз рака. После этого от образца потребуется информация для принятия решения о немедленном первичномлечении или, если необходимо, последующем вспомогательномлечении, дополняющем главное, — об операции. Информация поступает от «маркеров», или прогностических индикаторов риска возврата первичного рака, который был удален. Следует знать о «маркерах» до диагностической биопсии, даже если она покажет, что уплотнение является раковой опухолью.
Один из важнейших лабораторных анализов — это анализ на рецептор эстрогена (РЭ). Определение числа рецепторов женского гормона эстрогена в клетках опухоли — это косвенный способ определения, зависит ли раковая опухоль от этого гормона при своем росте. При этом обычно определяется и другой показатель — рецептор прогестерона (РП).
Если большинство клеток содержит много рецепторов, опухоль называется РЭ-богатой, или РЭ-позитивной. Опухоль, клетки которой содержат мало рецепторов — РЭ-бедна, или РЭ-негативна. Все раковые опухоли молочной железы содержат некоторое число клеток с рецепторами эстрогена, и вопрос состоит в том, как много рецепторов эстрогена содержится в заданном объеме клеточного материала. Если присутствуют также рецепторы прогестерона, их количество важно для предсказания реакции организма на гормональную терапию.
Определения рецепторов эстрогена и прогестерона стали рядовыми анализами. Один из них, доля S-фазы, может принести пользу в предсказании агрессивности рака. Этот показатель в буквальном смысле означает долю клеток, которые находятся в «синтетической» стадии процесса деления на дочерние клетки. Высокая доля S-фазы указывает, что клетки активно делятся, опухоль быстро растет.
Другой показатель — плоидия, которая описывает, насколько раковыми являются клетки опухоли по сравнению со здоровыми клетками молочной железы. Изучая это, специалисты могут оценить, насколько раковые клетки отклонились от нормальных клеток молочной железы и, соответственно, насколько агрессивной может быть опухоль.
Доля S-фазы и плоидия, наряду с состоянием подмышечных узлов, размером опухоли, гистологическим типом, содержанием рецепторов эстрогена и прогестерона, могут вносить свой вклад в картину маркеров, которая помогает онкологам рекомендовать при необходимости вспомогательную терапию или другое лечение после первичной операции.
Амплификация онкогена, определение наличия онкогена HER-2 — это пример другого исследования, проводимого для определения числа экземпляров определенного аномального гена в клетке опухоли. Этот метод активно используется, данные, накопленные о нем и о других новых маркерах, достаточно убедительны для того, чтобы рекомендовать эти анализы как стандартные.
Если поставлен диагноз рака молочной железы, в первую очередь лечению должна подвергаться грудь, где обнаружена опухоль. Следующая задача — определить, надо ли и, если надо, как лечить весь организм в целом, если есть сильное подозрение, что рак мог распространиться за пределы молочной железы.
Операция, независимо от того, следует ли за ней радиотерапия, является первичным местным лечением. Мероприятия вспомогательной терапии проводятся в дополнение к первичной терапии, чтобы уничтожить раковые клетки, оставшиеся в молочной железе или в отдаленных областях тела женщины. Такова цель химиотерапии и гормональной терапии.
Принятие решений начинается с того, может ли грудь быть сохранена или же безопаснее удалить всю ткань молочной железы путем мастэктомии. Затем, если ее решено сохранить, делать ли в дальнейшем облучение. Следующая проблема: нужна ли вспомогательная терапия и какая будет наиболее эффективна. Рекомендации, даваемые хирургом, базируются на том, что дали многие годы исследований вариантов лечения, применявшихся тысячами врачей в тщательно контролируемых клинических испытаниях.
Первичное лечение будет заключаться либо в том или ином варианте мастэктомии (удаления молочной железы), либо в частичной операции по удалению только опухоли (иссечение уплотнения). После иссечения уплотнения обычно применяется облучение сохраненной груди высокой дозой ионизирующего излучения.
Раковые клетки могут развиться либо из клеток, выстилающих протоки (рак протока) или в дольках (рак долек).
Карцинома протока in situ (DCIS). Эти раковые клетки развиваются из ткани протоков и остаются в протоках. Этот тип рака, ранее считавшийся редким, по современным оценкам составляет от 15 до 25% всех вновь диагностируемых случаев рака молочной железы. Если рак обнаружен на этой стадии, шансы на излечение очень высоки.
Карцинома долек in situ. По существующим оценкам только у 30-50% женщин с этим типом рака в течение ближайших 10 лет развивается истинный инвазивный рак молочной железы.
Этот рак способен метастазировать и распространяться по всему телу. Лечение такое же, как при инвазивном раке протока.
Сорокапроцентная частота рецидива местного рака свидетельствует в пользу утверждения о том, что рак молочной железы — мультицентричное заболевание. Другими словами, женщины, у которых возникла в груди одна опухоль, с высокой вероятностью имеют и другие очаги рака. Когда проводится сохраняющая грудь операция, вероятность рецидива является поводом для немедленного завершающего лечения радиацией, чтобы искоренить остающиеся в груди очаги рака.
Химиотерапия использует цитотоксичные (убивающие клетки) препараты, обычно в определённых сочетаниях.
Гормональная терапия может помочь женщинам, у которых рост раковой опухоли зависит от концентрации эстрогенов.
Пластическая операция, создающая искусственную выпуклость груди в случае, если настоящая грудь удалена после хирургического лечения рака, называется «восстановительной маммопластикой». Также разработаны специальные импланты, которые привели к тому, что искусственная грудь стала ближе к настоящей по форме и упругости.
источник
«Результаты УЗИ молочных желез выявили образование, подозрительное на онкологию», «результаты маммографии не позволяют однозначно исключить наличие злокачественного образования», «биопсия показала наличие раковых изменений в молочной железе и требуется расширенное обследование». Это лишь немногие из самых страшных слов, которые женщина может услышать от своего врача.
Молочные железы состоят из трех основных типов тканей — жировой, соединительной и железистой. Раком молочной железы (РМЖ) называют злокачественные опухоли, развивающиеся именно из клеток железистой ткани. Вопреки расхожему мнению, РМЖ заболевают как женщины, так и мужчины, однако у женщин он встречается примерно в 100 раз чаще.
Рак груди развивается так же, как и любая другая злокачественная опухоль в организме. Одна или несколько клеток железистой ткани в результате произошедшей в них мутации начинают аномально быстро делиться. Из них образуется опухоль, способная прорастать в соседние ткани и создавать вторичные опухолевые очаги — метастазы.
Мутации, которые приводят к РМЖ, бывают наследственными и приобретенными.
Распространенными наследственными генетическими причинами рака молочной железы становятся мутации в генах BRCA1 и BRCA2. Носительницы мутации BRCA1 имеют риск заболеть раком молочной железы 55–65%, а носительницы BRCA2 — 45%. Такие генетические дефекты передаются по наследству от родителей детям, они становятся причиной рака молочной железы примерно в 15% случаев.
Намного чаще опухоль возникает из-за приобретенных мутаций: они возникают в клетках молочной железы и не передаются по наследству. Например, в 20% случаев увеличено количество копий гена, кодирующего HER2 — белок-рецептор, который находится на поверхности клеток и стимулирует их размножение.
«Молекулярно-генетический портрет» опухоли имеет важное значение при выборе оптимального лечения.
Чаще всего опухоли молочных желёз развиваются из клеток молочных протоков — в этом случае врачи говорят о протоковом раке молочной железы или протоковой карциноме. Довольно часто злокачественные опухоли вырастают из клеток долек молочной железы, этот тип рака называют инвазивной лобулярной карциномой (инвазивный рак молочной железы). Стоит отметить, что рост опухоли возможен и из других клеток железистой ткани.
К сожалению, полной информации о причинах возникновения рака молочной железы у ученых пока нет. Существует список факторов риска, влияющих на вероятность появления опухоли, однако у некоторых болезнь диагностируют при отсутствии этих факторов, другие же остаются здоровыми при наличии сразу многих из них. Тем не менее, ученые все же связывают развитие рака груди с определенными обстоятельствами, наиболее часто предваряющими его появление. К ним относятся:
- Возраст. Большинство случаев РМЖ приходятся на женщин в возрасте 55 лет и старше.
- Наследственность. Если РМЖ диагностирован у кого-то из близких родственников, риск повышается вдвое.
- Рак молочной железы в анамнезе.
- Повышенная плотность ткани молочной железы по результатам маммографии.
- Некоторые доброкачественные новообразования в молочной железе.
- Раннее начало менструаций — до 12 лет.
- Поздняя менопауза — после 55 лет.
- Отсутствие детей или поздние (после 35 лет) первые роды.
- Воздействие радиации, например, в ходе лучевой терапии, проводимой для лечения другого типа рака.
- Курение и злоупотребление алкоголем. Если женщина ежедневно потребляет 28–42 г этилового спирта, ее риски повышаются на 20%.
- Лишний вес и низкая физическая активность.
- Использование гормональных препаратов: оральные контрацептивы, заместительная гормональная терапия в постменопаузе.
- Травмы молочных желез.
- Сахарный диабет.
- Работа по графику с ночными сменами.
Довольно часто на ранних стадиях рак молочной железы протекает бессимптомно. Но в ряде случаев признаки, указывающие на наличие заболевания, все же есть, и их можно заметить.
В первую очередь, к симптомам, которые должны насторожить, относят уплотнения в молочных железах, рядом с ними или в подмышечной впадине. В 9 случаях из 10 уплотнения бывают доброкачественными, однако установить это наверняка можно только на осмотре у маммолога.
К симптомам рака молочной железы относят:
- Отвердение кожи
- Участок втяжения кожи
- Эрозия кожи
- Покраснение кожи
- Выделения из соска
- Деформация молочной железы по типу ряби
- Припухлость кожи
- Увеличенные в размерах вены
- Втяжение соска
- Нарушение симметрии молочных желез
- Симптом лимонной корки
- Пальпируемый узел внутри молочной железы.
При появлении указанных симптомов, а также любых других изменений в молочных железах (например, необычных или болезненных ощущений) нужно немедленно проконсультироваться с маммологом.
В Европейской клинике ведёт консультативный приём и выполняет операции известный российский хирург-маммолог, доктор медицинских наук Сергей Михайлович Портной (автор более 300 печатных работ, член правления Российского общества онкомаммологов, автор трех патентов на изобретения).
Сергей Михайлович выполняет весь объем оперативных вмешательств на молочной железе, включая органосохраняющие и реконструктивные пластические операции.
Самостоятельно проверять грудь на наличие узелков или каких-либо других изменений стоит раз в месяц, по окончании менструации. Домашнюю диагностику удобнее всего проводить, принимая ванну или находясь под душем. О любых изменениях, которые удалось обнаружить, стоит как можно быстрее рассказать врачу.
Порядок проведения самообследования молочных желез:
- Разденьтесь выше пояса и встаньте перед зеркалом.
- Поднимите руки вверх и заведите их за голову. Внимательно осмотрите грудь. Повернитесь правым, левым боком.
- Ощупайте молочные железы в положении стоя сложенными указательным, средним и безымянным пальцем. Начинайте с верхней наружной части груди и двигайтесь по часовой стрелке.
- Сожмите сосок двумя пальцами. Проверьте, выделяется ли из него что-нибудь.
- Снова ощупайте молочные железы — теперь в положении лежа.
70% случаев рака молочной железы выявляются пациентами самостоятельно в результате самообследования груди.
О роли биопсии в диагностике рака молочной железы рассказывает врач Европейской клиники Портной С.М.:
Для подтверждения или исключения диагноза в первую очередь проводится мануальное обследование груди. Затем, при наличии подозрений или в качестве скрининговой процедуры, может быть назначена маммография, рентгенологическое исследование молочных желез. Как правило, женщинам до 35 лет ее выполнение не рекомендуется, в молодости ткань молочных желез особенно чувствительна к радиоактивному облучению.
Ультразвуковое исследование (УЗИ) молочных желез позволяет оценить структуру их ткани и отличить, например, опухоль от кисты, наполненной жидкостью.
Если результаты маммографии или УЗИ указывают на наличие новообразований в молочной железе, врач, как правило, назначает биопсию, лабораторное исследование образца тканей из молочной железы. Биопсия позволяет выяснить, является ли опухоль злокачественной, а также определить ее тип и стадию. Кроме того, исследование биопсийного материала дает ответ на вопрос, является ли опухоль гормонозависимой, что также влияет на схему лечения.
При необходимости могут использоваться и другие диагностические методы, например, магнитно-резонансная томография (МРТ).
После постановки диагноза основной задачей лечащего врача является определение стадии онкологического заболевания, то есть размера опухоли, ее расположения, наличия метастазов и агрессивности. От этих факторов зависит прогноз лечения и подбор оптимальных методов терапии. Как правило, для уточнения стадии проводятся анализы крови, маммография другой молочной железы, сканирование костей, а также компьютерная или позитронно-эмиссионная томография. В некоторых случаях определить стадию опухоли можно только при проведении операции.
Стратегия лечения рака молочной железы зависит от многих факторов — типа рака, стадии, чувствительности клеток опухоли к гормонам, а также общего состояния здоровья пациентки.
Основной метод лечения рака груди — хирургическая операция. Если болезнь удалось диагностировать на ранней стадии, хирург может выполнить лампэктомию, удаление тканей опухоли и небольшой части окружающей ее здоровой ткани. При более крупных опухолях молочная железа удаляется целиком (такая операция называется мастэктомией), равно как и ближайшие к ней лимфатические узлы. Если по оценке врача риск развития рака во второй молочной железе достаточно высок, пациентке может быть рекомендовано удаление обеих молочных желез сразу.
Чтобы разобраться, распространились ли раковые клетки в лимфатические узлы, и определиться с объемом хирургического вмешательства, может быть проведена сентинель-биопсия, или биопсия сторожевого лимфоузла. Во время операции в опухоль вводят радиофармпрепарат или флуоресцентный краситель — это помогает визуализировать лимфоузел, который первым принимает лимфу от ткани молочной железы. Его удаляют и проводят гистологическое исследование. Если в сторожевом лимфоузле не обнаруживают опухолевых клеток, можно ограничиться удалением очага в молочной железе. В противном случае показано иссечение регионарных лимфоузлов.
Лучевую терапию (то есть воздействие на опухоль ионизирующим излучением) при раке молочной железы, как правило, используют после проведения хирургической операции. Терапия проводится с целью уничтожения раковых клеток, которые могли остаться в организме.
Химиотерапия, то есть использование препаратов, убивающих раковые клетки, может проводиться после операции по удалению опухоли, как и лучевая терапия. В некоторых случаях химиотерапию проводят до оперативного лечения для того, чтобы уменьшить размер слишком крупной для удаления опухоли.
В Европейской клинике для лечения рака молочной железы применяются наиболее современные, оригинальные европейские и американские химиопрепараты. У нас есть возможность составить «молекулярный отпечаток» опухоли, подобрать на основании его анализа наиболее эффективные и безопасные комбинации лекарств.
Для лечения рака молочной железы, чувствительного к гормонам, используют гормональную терапию — к ней относится несколько разных методов, останавливающих выработку гормонов в организме или блокирующих их поступление к опухоли. Гормональная терапия позволяет снизить вероятность рецидива опухоли, а также, в случае выявления неоперабельной опухоли, помогает контролировать ее рост.
Для лечения рака молочной железы применяют также таргетную терапию — препараты, поступающие непосредственно к тканям опухоли и минимально воздействующие на здоровые клетки организма. Таргетную терапию используют либо отдельно, либо в комбинации с другими методами лечения — в зависимости от того, какая схема лучше всего подойдет пациенту.
Если рак молочной железы диагностирован на ранних стадиях (0-I), пятилетняя выживаемость приближается к 100%. То есть, можно сказать, что удается вылечить практически всех женщин. Далее, в зависимости от стадии, прогноз относительно пятилетней выживаемости ухудшается:
- На II стадии — 93%.
- На III стадии — 72%.
- На IV стадии — 22%.
Совокупность имеющихся в арсенале онкологов методов лечения рака молочной железы позволяет в большинстве случаев добиться ремиссии заболевания или, как минимум, продлить жизнь с сохранением ее качества. Однако следует помнить, что эффективность лечения в целом напрямую зависит от того, было ли лечение начато своевременно, то есть на ранних стадиях заболевания.
Максимальная эффективность противоопухолевого лечения достигается только в том случае, если оно проводится в соответствии с международными протоколами, при этом учитываются индивидуальные особенности каждого пациента. Именно так назначают лечение онкологи Европейской клиники.
источник
С онкологическим заболеванием груди, как правило, связано множество вымышленных фактов. Именно поэтому стоит разобраться в симптомах, потенциальных рисках и других факторах.

Правда: Около 70% женщин с установленным диагнозом не имеют никаких идентифицируемых факторов риска заболевания. Однако, если хотя бы у одного родственника I степени (родителя, сестры или ребенка) был рак молочной железы, то риск повышается примерно в 2 раза.

Правда: Многие считают, что такие бюстгальтеры пережимают лимфатическую систему груди, вызывая накопление токсинов, а также вызывают рак. На самом деле, ни тип бюстгальтера, ни плотность белья или любой другой одежды не имеют никакого отношения к раку груди.

Правда: Около 80% образований и уплотнений в груди связаны с доброкачественными (нераковыми) изменениями, кистами и другими факторами. Но врачи настоятельно рекомендуют обращать внимание на любые изменения, ведь раннее диагностирование, как правило, способствует позитивному исходу. Врач может порекомендовать провести маммограмму, ультразвук или биопсию для определения типа образования.

Правда: Современные исследования полностью опровергают утверждения о том, что оперативное вмешательство вызывает или способствует распространению рака молочной железы. Непосредственно во время операции врач может обнаружить, что ткани поражены больше, чем считалось ранее. Тем не менее исследования на животных показали, что после операции иногда происходит временный рост метастаз, чего не было обнаружено у людей.

Правда: Согласно исследованиям, женщины с имплантатами в груди не причисляются автоматически к группе риска. Однако им для более полного изучения ткани груди, кроме стандартной маммограммы, требуется дополнительное рентгеновское исследование.

Правда: Если быть точным, то риск увеличивается по мере взросления. Вероятность получить такой диагноз в 30 лет составляет 1:233, а к моменту достижения 85 лет этот показатель вырастает до 1:8.

Правда: Американское онкологическое общество не подтверждает этот слух, но признает, что необходимы дополнительные изучения. Ранее исследователи наткнулись на следы парабенов в образцах опухолей рака. Парабены, используемые в составе некоторых антиперспирантов, обладают слабыми эстрогеноподобными свойствами. Однако это исследование не установило наличие прямой причинно-следственной связи между этими явлениями, так же как и не позволило с точностью идентифицировать источник парабенов в опухолях.

Правда: Между размером груди и риском развития рака связи также нет. Возможно, дело в том, что очень большую грудь сложнее исследовать, проводить маммографию или МРТ. Однако все женщины, независимо от размера груди или других физиологических особенностей, должны проходить скрининги и осмотры.

Правда: Обнаруженное уплотнение под кожей может указывать на рак груди (или одно из доброкачественных состояний молочной железы), но необходимо быть настороже и к другим видам изменений. К последним относятся: припухлость, раздражение кожи или сыпь, боль в груди или сосках, втягивание соска внутрь, покраснение, шероховатость или утолщение сосков или кожи груди, а также любые выделения, кроме грудного молока.
Рак молочной железы может распространяться на лимфатические узлы подмышек и вызывать распухание в этом месте до того, как опухоль в груди станет достаточно большой и ощутимой. С другой стороны, маммограмма может определить наличие заболевания, протекающего без каких-либо симптомов.

Правда: К сожалению, эта болезнь развивается иногда даже после полного удаления молочной железы. Это может случиться, например, на месте рубца. Шанс, хоть и небольшой, но существует. Тем не менее мастэктомия в качестве превентивной меры снижает риск развития рака на 90%.

Правда: Оба анамнеза одинаково важны для адекватной оценки рисков. В любом случае стоит рассматривать ситуацию с женской половиной семьи, так как именно она более уязвима к раку молочной железы. Но другие виды рака у мужчин-родственников также следует брать во внимание для более точного определения вероятности развития болезни.

Правда: Нет объективных причин считать такое утверждение верным. Более того, по результатам некоторых исследований стало известно, что кофеин может даже фактически снизить риск.

Правда: Для снижения риска можно сделать многое, например, похудеть, если присутствует избыточный вес, регулярно заниматься физической активностью, снизить или исключить употребление алкоголя и курение, проводить регулярное самообследование и клиническую диагностику, маммограмму и МРТ, участвовать в клинических испытаниях и т.д. Кроме того, некоторые предпочитают проводить профилактическую мастэктомию.

Правда: Раньше действительно считалось, что женщины с такими изменениями в груди больше подвержены риску развития рака, но на самом деле это не так. Для обследования им только нужно проводить маммограмму вместе с ультразвуком.

Правда: Уровень излучения, используемого при маммограмме, настолько мал, что связанные с ним риски являются просто ничтожными по сравнению с преимуществами, полученными в результате теста. Обследование может обнаружить уплотнения задолго до того, как их можно будет нащупать или заметить другим образом. Американское онкологическое общество рекомендует женщинам в возрасте от 40 лет и старше делать скрининг-маммограмму раз в 1-2 года.

Правда: Убедительных доказательств этого утверждения на сегодняшний день не существует. Проведенное в 2004 году исследование не выявило увеличения распространения рака среди пациентов, перенесших пункционную биопсию по сравнению с теми, у кого не было этой процедуры.

Правда: От этого заболевания в США умирают примерно 40 000 женщин в год. Однако ежегодная смертность от инсульта составляет 96 000 человек, от рака легких – 71 000 человек, а хронические заболевания дыхательных путей убивают около 67 000 человек.

Правда: Несмотря на ее важную роль для скрининга и диагностики рака груди, маммограмма не обнаруживает 10-20% случаев заболевания. Вот почему клинические обследования и самообследования груди являются важными элементами процесса скрининга.

Правда: Крупное исследование 2007 года, финансируемое Национальным институтом рака, не выявило закономерного повышения риска развития рака груди из-за использования выпрямителей волос. Среди участников исследования были афро-американские женщины, использовавшие устройства минимум 7 раз в год на протяжении 20 лет или дольше.

Правда: Показатели позитивного исхода примерно равны для тех, кто прошел через мастэктомию, и тех, кто выбрал вариант с частичным удалением молочной железы и послеоперационной лучевой терапией. Но в случаях, связанных с обширной карциномой молочной железы, наличием мутаций гена BRCA или особенно крупных опухолей, лампэктомия не может считаться подходящим вариантом лечения.

Правда: Все в точности наоборот – из-за наличия этого фактора риск развития онкологии значительно повышается, особенно в период менопаузы.

Правда: Принимая во внимание связь эстрогена с раком груди, ученые допускали такую вероятность. Однако в ходе исследований они не получили подтверждения, но эта проблема все же требует дополнительного изучения.

Правда: В 2003 году было проведено исследование с целью выяснить причины широкой распространенности рака груди в некоторых районах Нью-Йорка. Ученым не удалось обнаружить связь между болезнью и электромагнитными полями от ЛЭП. Более раннее исследование, проведенное в районе Сиэтла, дало аналогичный вывод. Тем не менее исследование потенциальных факторов экологического риска продолжается.

Правда: Ввиду того, что абортивное вмешательство нарушает гормональные циклы во время беременности, а рак груди связан с уровнями гормонов, многочисленные исследователи долгое время изучали причинную связь, но не нашли убедительных доказательств ее подтверждения.

Правда: Увы, нет. Конечно, вполне возможно определить некоторые факторы риска (семейный анамнез и наследственные мутации гена), а также скорректировать образ жизни (сократить или прекратить употребления алкоголя и никотина, снизить вес, заниматься физической активностью и проводить регулярные скрининги). Однако примерно 70% женщин с диагнозом «рак молочной железы» не имеют идентифицируемых факторов риска, а это означает, что заболевание развивается по необъяснимым на данный момент причинам.
источник
По распространенности рак молочной железы (РМЖ) занимает первое место среди онкологических заболеваний. Он поражает ежегодно 1 млн. 600 тыс. женщин в мире и свыше 66 тыс. в Российской Федерации.
В ближайшие 20 лет во всех странах прогнозируется почти двукратное увеличение заболеваемости женщин раком груди, что объясняется увеличением продолжительности жизни и улучшением методов диагностики.
За последние годы, благодаря более раннему выявлению опухолей, смертность от рака груди у женщин снижается. В развитых странах, где применяется маммографический скрининг населения, этот показатель снизился на 30–50%.
Рак молочной железы – это не единообразное заболевание. При лечении клиницисты учитывают принадлежность опухоли к конкретному подтипу. Генетическое тестирование и иммуногистохимический метод, позволяют надежно определить биологические подтипы РМЖ. Эти подтипы сами по себе включают многие факторы риска и предсказывающие признаки, что позволяет выбрать наиболее эффективную терапию для больного.
Доказанное с помощью молекулярно-генетического анализа и иммуногистохимического исследования патогенетическое разнообразие РМЖ позволяет индивидуализировать лечение.
Увеличение выживаемости при раке молочной железы связано не только с широкомасштабным внедрением маммографического скрининга, но и адекватным использованием системных видов лечения.
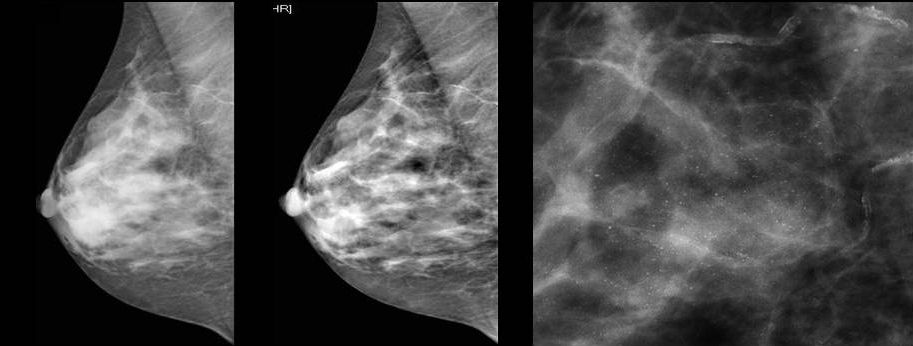
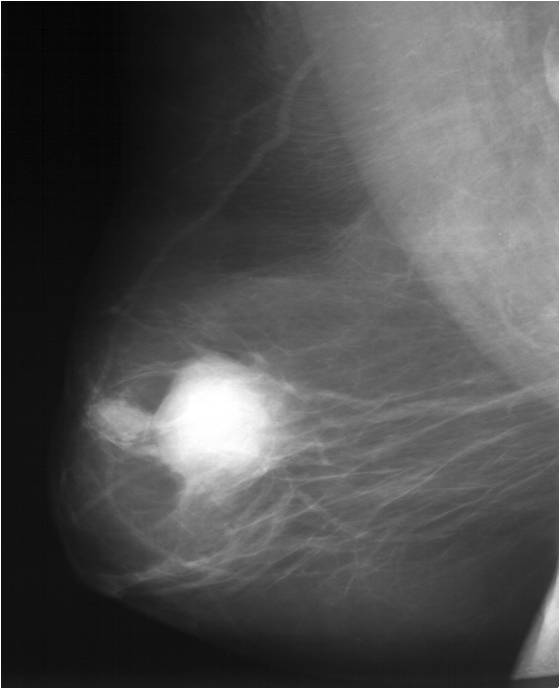
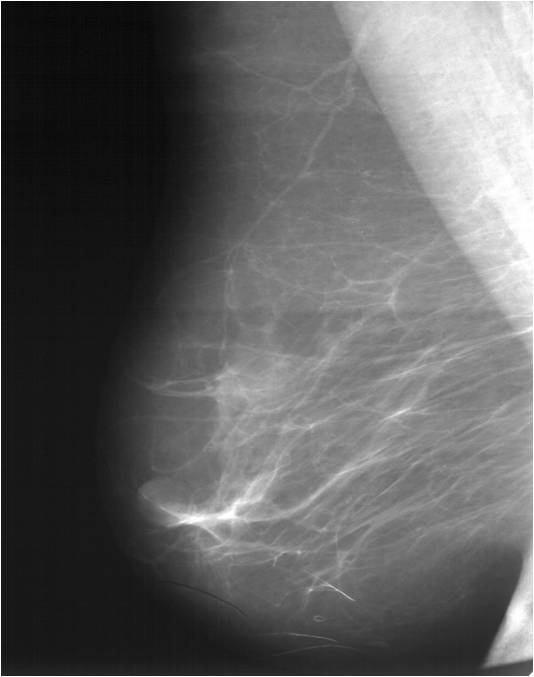
Для выявления злокачественных опухолей молочной железы существует определенный алгоритм диагностики, и его первичный элемент — маммографический скрининг. Чувствительность этого метода диагностики для опухолей от 2 мм до 5 мм составляет около 85%. Маммографическое исследование выполняют в двух проекциях.
Молодым женщинам с плотным строением молочной железы необходимо включение в программу наблюдения методов УЗИ и МРТ.
Поскольку традиционный маммографический скрининг у женщин до 40 лет малоэффективен, для скрининга может понадобиться альтернативная методика — МРТ. Современная контрастная магнитно-резонансная томография — высокочувствительный метод диагностики заболеваний молочной железы.
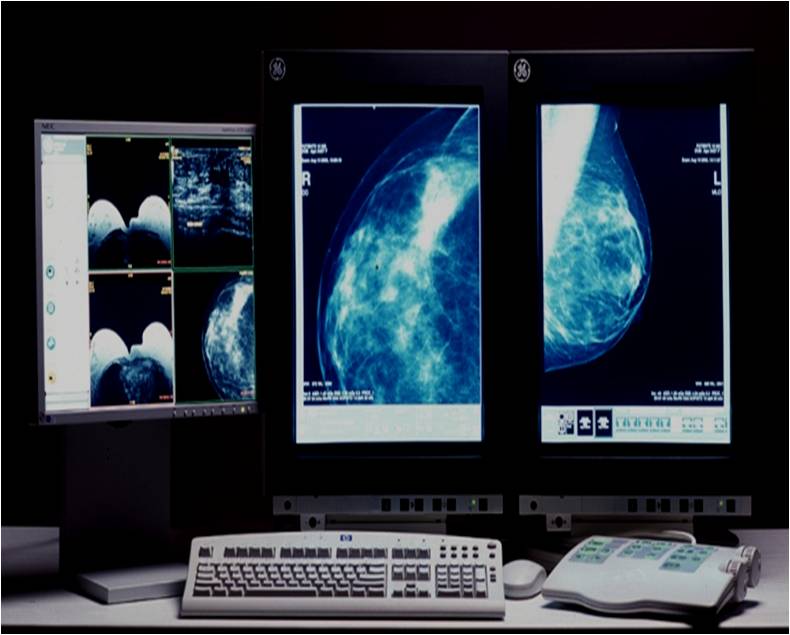
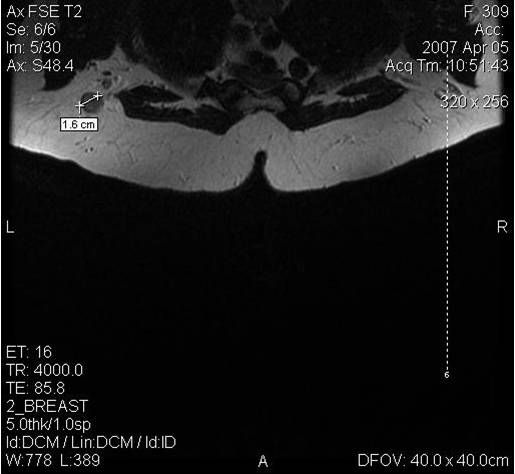
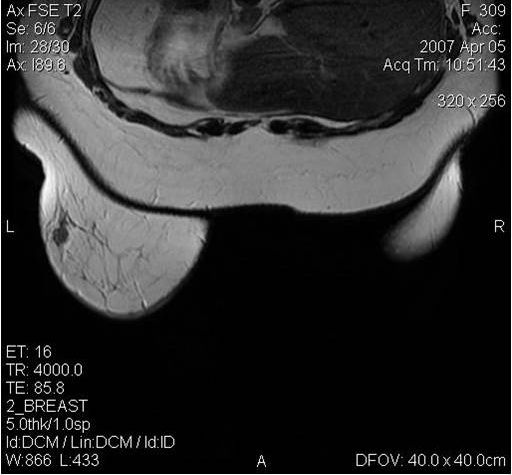
МРТ-диагностика рака молочной железы
У женщин с мутациями BRCA1 или BRCA2 при проведении МРТ возможно диагностировать рак молочной железы на самых ранних стадиях.
При ряде показаний женщинам назначается биопсия молочной железы под контролем УЗИ. Это исследование позволяет прицельно брать биологический материал для гистологического исследования, определения уровня экспрессии стероидных гормонов и статуса Her-2.
Известно множество факторов, повышающих риск возникновения рака молочной железы. На некоторые из них повлиять невозможно:
- семейная история по РМЖ,
- раннее менархе (начало месячных),
- позднее наступление менопаузы.
В то же время существуют и модифицируемые факторы, такие как:
- избыточный вес в постменопаузе,
- использование заместительной гормонотерапии,
- потребление алкоголя,
- курение
Стратегические шаги, направленные на снижение риска возникновения РМЖ включают контроль веса и борьбу с ожирением, регулярную физическую активность, уменьшение потребления алкоголя.
Большинство факторов риска рака молочной железы связано с действием гормонов на ткань молочной железы (раннее менархе, позднее наступление менопаузы, ожирение, применение гормональных препаратов). Считается, что именно женские половые гормоны, стимулируют процессы клеточного роста и повышают риски повреждения ДНК, что может привести к развитию злокачественного новообразования.
Только 5–10% случаев рака молочной железы обусловлены унаследованными мутантными генами BRCA. Но при этом, среди носителей мутаций риск возникновения заболевания может достигать 80%.
Чем младше возраст выявления первичного заболевания рака груди, тем выше вероятность заболеть контралатеральным раком, т.е. противоположной молочной железы.
Семейная история с наличием заболеваний раком молочной железы у кровных родственников, даже без ассоциации с мутациями BRCA, также повышает риск возникновения РМЖ.
Ожирение
Различными исследованиями доказано существование связи между заболеваемостью первичным РМЖ в постменопаузе и ожирением. Есть подтверждение связи между избыточным весом и низкой выживаемостью при всевозможных видах РМЖ.
Алкоголь
Алкоголь — также установленный фактор риска возникновения первичного РМЖ. Достоверность его отрицательного воздействия на пациентов, перенесших рак молочной железы, убедительна, так как он влияет на увеличение количества циркулирующих эстрогенов.
Только врач может оценить значимость различных симптомов. Однако каждой женщине необходимо знать, при каких симптомах надо обращаться к маммологу:
- «Образование», уплотнения, узел, инфильтрат, опухоль, «шарик» — что-то подобные этому вы обнаружили. Это еще не повод решить, что у вас РМЖ, но повод показаться специалисту.
- Деформация контура молочной железы, ареолы или соска (втяжение кожи или наоборот выбухание)
- Втяжение соска; особенно, если появилось недавно
- Выделение крови из соска
- Отек кожи всей молочной железы или ее локального участка
- Появление раздражения, мокнутые «ранки», язвочки, корочки на соске или ареоле
- Изъязвления (длительные, без видимой причины) на коже груди
- Дискомфорт в подмышечной области и обнаружение лимфоузлов ( «шариков» ) в подмышечной области
- Изменение цвета кожи молочной железы — покраснение, повышение температуры кожи в этой области.
Все эти симптомы могут быть проявлениями различных заболеваний (их насчитывается несколько десятков), возможно, не злокачественной природы. Однако, это может решить только специалист по заболеваниям молочной железы.
Признаки и симптомы рака молочной железы
0 стадия
Это стадия, когда не выявлена первичная опухоль, или она не может быть оценена, а также в случае неинвазивного рака молочной железы (что означает опухоль не выходит за границы своего появления, так называемый рак in situ).
1 стадия
Раковые клетки в этой стадии инвазируют или прорастают в соседние ткани. Опухолевый узел не более 2 см, лимфоузлы при этой стадии не поражены.
2 стадия
В этой стадии опухолевый узел превышает 2см и может достигать до 5см. При этой стадии могут быть поражены лимфоузлы, но поражение лимфоузлов носит одиночный характер, они не спаяны друг с другом и находятся на той же стороне, что и опухоль. В случае поражения лимфоузлов размер опухоли может быть и менее 2см.
3 стадия
Инвазивный рак, более 5 см или с явным и значительным поражением лимфатических узлов. При этом лимфоузлы могут быть спаяны между собой.
4 стадия
На этой стадии опухоль прорастает в кожу груди, грудную стенку либо во внутренние грудные лимфатические узлы. Она может быть любых размеров.
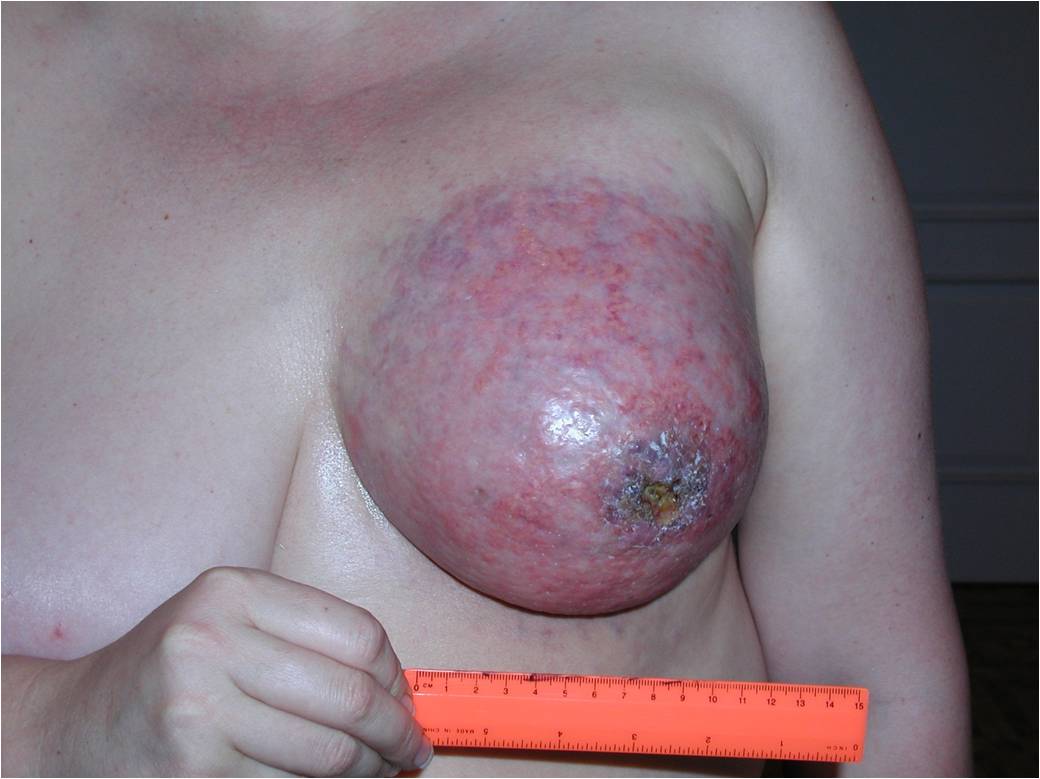
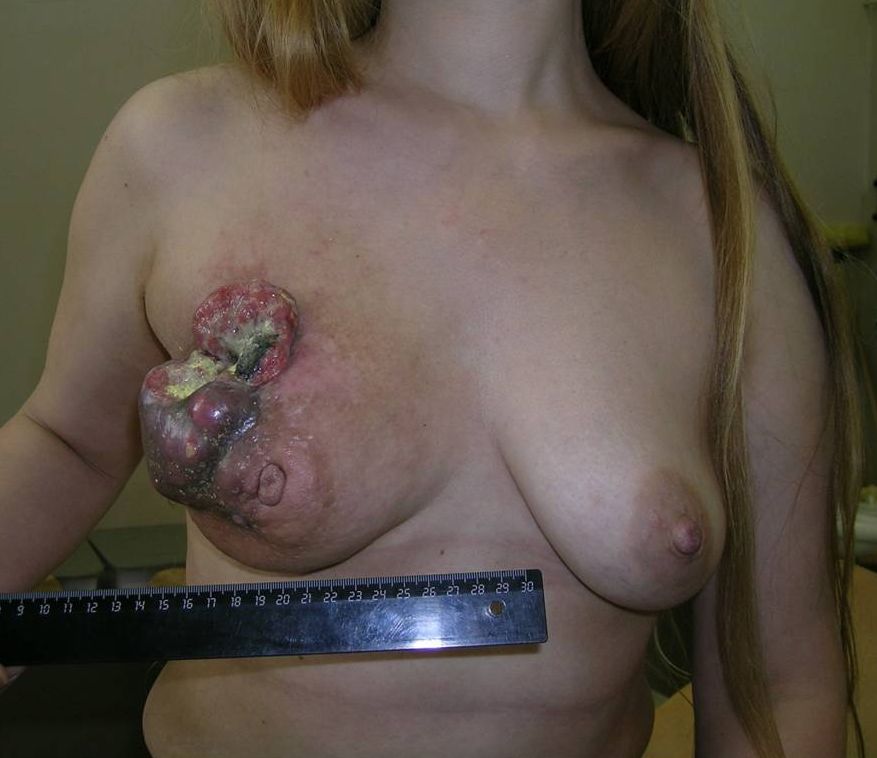
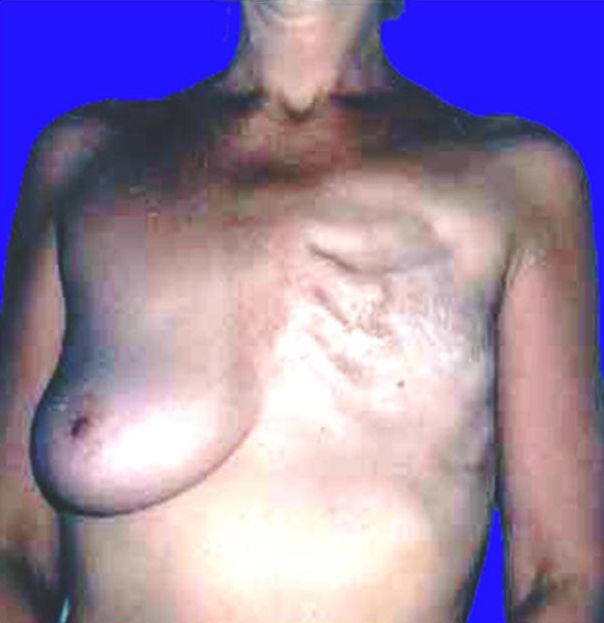
К 4 стадии рака молочной железы относится воспалительный рак, он встречается до 10 % всех случаев. Симптомы воспалительной формы рака груди это покраснение кожных покровов, железа становится теплой, отмечается увеличение и/или уплотнение части либо всей молочной железы. Кожа приобретает вид апельсиновой корки. Эту форму рака надо дифференцировать с воспалением молочной железы – маститом.
Также при 4 стадии опухоль может распространяться за пределы грудной клетки, в подмышечную область, внутренние грудные лимфатические узлы. Возможны метастазы в надключичные лимфатические узлы, а также в легкие, печень, кости или головной мозг.
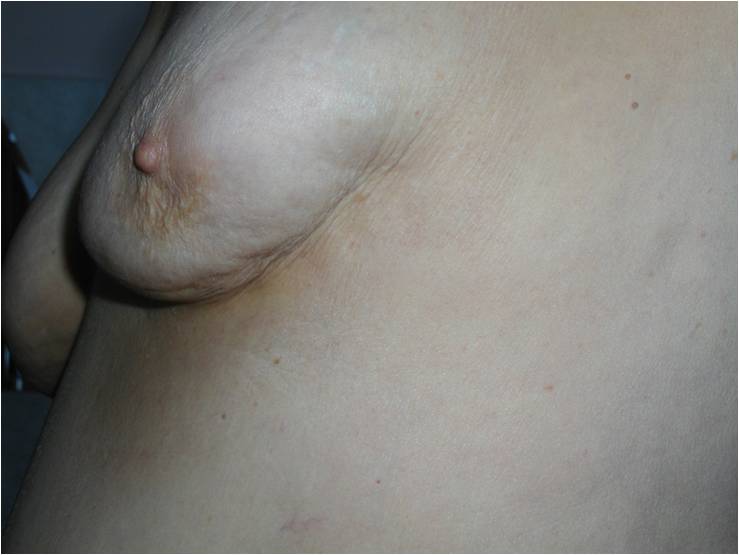
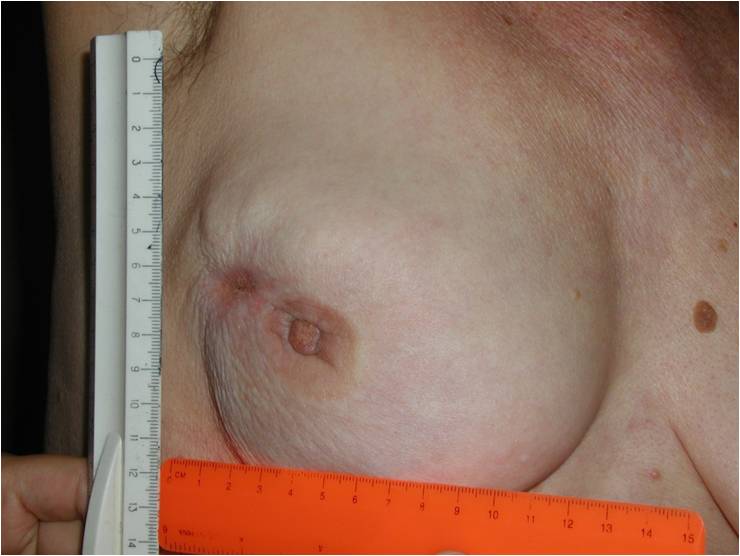
Как выглядит рак груди в разных стадиях:
Хирургическая операция — основной метод лечения при опухолях груди, и от качества его проведения во многом зависит исход заболевания. По данным некоторых штатов Индии, в которых по религиозным мотивам не проводится хирургическое лечение, показатели заболеваемости практически равняются показателям смертности. Обычно смертность от РМЖ в два — четыре раза уступает заболеваемости.
Однако, после хирургического лечения чаще всего следует лучевое. Местное лечение без послеоперационной лучевой терапии часто приводит к локально-регионарным рецидивам заболевания. Дело в том, что после завершения хирургической операции невозможно исключить существования скрытых отдаленных метастазов. Даже у больных с опухолями менее 1 см в диаметре в 10% случаев возможен рецидив заболевания.
Локализация отдаленных метастазов при РМЖ
Сейчас во всем мире наблюдается тенденция к сокращению объема хирургического вмешательства без потери эффективности. Хирургическое и лучевое лечение РМЖ развивается и совершенствуется в направлении органосохранения.
Благодаря внедрению маммографического скрининга, резко возросло число больных с ранней стадией заболевания, когда лимфоузлы не поражены метастазами. В этом случае «классическое» удаление всех уровней лимфоузлов было бы избыточной калечащей процедурой. На помощь хирургам пришел метод биопсии сигнальных (сторожевых) лимфатических узлов.
Поскольку, метастазы в подмышечных лимфоузлах появляются последовательно от первого ко второму, затем к третьему уровню, то достаточно определить наличие метастазов именно в первом лимфоузле. Его назвали «сигнальным»: если сигнальный лимфатический узел не содержит метастазов, то другие лимфоузлы также не метастатические.
Благодаря этому органосохраняющему методу, тысячи пациенток избежали избыточной полной хирургической диссекции, удаление раковой опухоли не привело к удалению груди.
Последние результаты клинических испытаний, в том числе и при участии НИИ онкологии им. Н.Н. Петрова, подтвердили безопасность отказа от полной подмышечной диссекции. Биопсия сигнальных (сторожевых) лимфатических узлов постепенно вытесняет подмышечную диссекцию как стандартную процедуру стадирования РМЖ.
Концепция биопсии сигнальных лимфатических узлов приобретает все большее признание и введена для многих локализаций опухолей в стандарты хирургического лечения Европейской Организацией по Изучению и Лечению Рака (EORTC).
Химиотерапия, наряду с хирургическим вмешательством, является одним из основных методов терапии рака. Послеоперационная химиотерапия улучшает результаты хирургического лечения, как и прогноз заболевания.
Ранее решение о назначении химиотерапии основывалось на двух факторах:
- стадия заболевания
- состояние регионарных лимфоузлов.
Благодаря многочисленным исследованиям ученых изменяются представления о биологии рака молочной железы, и выбор режимов химиотерапии значительно расширяется. И сегодня химиотерапевтическое лечение назначают даже при отсутствии метастазов в лимфоузлах, если небольшие по размеру опухоли обладают агрессивными биологическими характеристиками.
Люминальный А рак
При люминальном А раке избегают назначать проведение химиотерапии, особенно при негативных лимфоузлах, и применяют одну эндокринотерапию.
Люминальный В рак
Люминальные В опухоли характеризуются высокой агрессивностью. В этом случае чаще всего будет назначена химиотерапия, а выбор лечения основывается на оценке риска развития рецидива.
HER2-позитивный рак молочной железы
Лечение HER2-позитивного рака молочной железы основано на применении стандартных схем химиотерапии – трастузумаб и ХТ, основанная на антрациклинах и таксанах. Однако, только небольшой процент пациентов выигрывает от лечения, но все подвержены связанной с этим токсичностью.
Трижды негативный РМЖ
Трижды негативный рак молочной железы обычно ассоциируется с плохим прогнозом. Из-за редкой встречаемости особых типов РМЖ нет достаточных данных о роли адъювантной химиотерапии.
Химиотерапия при РМЖ у очень молодых женщин
Рак молочной железы в молодом возрасте обычно протекает агрессивно, часто встречаются гормонорезистеные и HER2-позитивные опухоли с иными свойствами, чем у более пожилых женщин. Для таких пациенток, моложе 35 лет, адъювантная полихимиотерапия почти всегда является необходимым методом лечения.
Химиотерапия пожилых пациенток
У пожилых пациенток (старше 65 лет) при решении вопроса о назначении адъювантной химиотерапии обязательно учитываются общее состояние организма и наличие сопутствующих хронических заболеваний.
В идеале пожилые пациенты должны подвергаться гериатрической оценке для определения их «пригодности» к адъювантому лечению. Потенциальный эффект лечения должен быть сбалансирован с теми рисками для организма, которые несет химиотерапия. Врач определяет наиболее эффективный и при этом наиболее безопасный специфический режим, основываясь на подтипе опухоли и индивидуальных характеристиках пациента.
Гормонотерапия
Молодые женщины с гормоноположительным раком молочной железы сохраняют риск рецидива заболевания на протяжении по крайней мере 15 лет после первичного заболевания. Онкологи должны определить, кто из пациентов нуждается в долгосрочной адъювантной терапии тамоксифеном или ингибиторами ароматазы.
Неоадъюватная (предоперационная) терапия
Неоадъюватная терапия занимает ведущую роль в лечении женщин с неоперабельным раком молочной железы, а также имеет важное значение при операбельных опухолях, когда выполняются органосохраняющие операции.
Эффект неоадъювантного лечения ДО (слева) и ПОСЛЕ (справа)
Лучевое лечение после проведенного хирургического вмешательства играет важную роль в терапии рака молочной железы и прогнозе заболевания. В НМИЦ онкологии им. Н.Н. Петрова было проведено исследование роли лучевой терапии после органосохраняющих операций (секторальная резекция с аксиллярной лимфоаденэктомией) у пациенток с минимальным РМЖ.
Анализ десятилетней безрецидивной выживаемости доказал более высокую эффективность лечения в группе больных, где применялась послеоперационная лучевая терапия.
Использование лекарственных препаратов для снижения риска заболевания называется химиопрофилактикой. На сегодняшний день одобренными препаратами для профилактики рака молочной железы являются тамоксифен и ралоксифен.
Тамоксифен может использоваться как пременопаузальными, так и постменопаузальными женщинами. Прием тамоксифена приводит к снижению риска РМЖ на 38% на более чем 10 летний период. Наиболее распространенными нежелательными явлениями на фоне приема препарата являются приливы.
В настоящее время клинические исследования изучают роль другого класса препаратов – ингибиторов ароматазы для оценки эффектов снижения риска РМЖ, которые сегодня используются только для лечения РМЖ. Предварительные результаты оказываются многообещающими. Ингибиторы ароматазы действуют только у женщин с нефункционирующими яичниками.
Профилактические хирургические операции по удалению молочных желез проводятся только в одном случае – если женщина является носителем мутаций в генах BRCA1 и BRCA2, известных как «синдром Анджелины Джоли». Мировой практикой доказано, что при удалении ткани обеих молочных желез риски РМЖ снижаются более чем на 90%. Такие операции выполняются в клиниках США и Израиля. В Европе подход к этому вопросу более консервативный.
В НМИЦ онкологии им. Н.Н. Петрова при проведении хирургического лечения женщинам с мутациями BRCA1 предлагается профилактическое удаление и реконструкция молочной железы.
Рак молочной железы (РМЖ) является самым распространенным онкологическим заболеванием среди женщин во всем мире и, в том числе, в России.
Благодаря многочисленным публикациям в прессе, обсуждениям проблемы на телевидении и радио многие женщины знают о существовании опухолей молочной железы. Однако значительная часть женщин не осведомлена об основных фактах, касающихся этого заболевания: как часто и почему оно возникает, каковы ранние признаки и симптомы опухоли, какие методы лечения применяются и насколько они эффективны.
По механизму возникновения РМЖ делится на 3 группы:
– Случайный (спорадический рак около 65% всех опухолей), ведущая роль в этиологии которого отводится длительному и/или интенсивному воздействию эстрогенов.
– Семейный рак (около 25% опухолей) – при наличии рака молочной железы у матерей, сестер и дочерей риск заболевания повышается в 9 раз.
– Генетический рак (около 10% всех опухолей), который характеризуется аутосомно-доминантным типом наследования, ранним возрастом возникновения, вертикальной передачей как с материнской, так и с отцовской стороны. В основе лежат мутации генов BRCA 1/2, p53, pTEN, CHEK 2 и др.
Факторы риска возникновения РМЖ можно условно разделить на две большие группы – основные и второстепенные. К основным факторам риска следует отнести: генетический фактор: мутации генов BRCA-1/2, p53, pTEN, CHEK 2 обусловливают более ранее начало заболевания, а также риск возникновения рака второй железы у этих больных (до 46%); семейный анамнез (рак молочной железы у близких родственников); состояние репродуктивной сферы: риск увеличен на 40%, если первая беременность и роды были после 30 лет, при наличии в анамнезе большого количества абортов, особенно до первых родов, отсутствие лактации; фиброзно-кистозная болезнь (мастопатия), особенно с атипической пролиферацией эпителия (протоковой и дольковой). На фиброзно-кистозной болезни следует остановиться чуть более подробно, так как в наши дни мастопатией страдают до 80% женщин репродуктивного возраста. Риск возникновения рака молочной железы на фоне фиброзно-кистозной болезни возрастает в 3-5 раз, а при пролиферативных формах – в 25-30 раз. На амбулаторном приеме онколога до 50% пациенток составляют больные с фиброзно-кистозной болезнью.
Факторы риска возникновения фиброзно-кистозной болезни во многом сходны с таковыми при РМЖ. К ним относятся: гиперпластические процессы гениталий (генитальный эндометриоз, миома матки, гиперплазия эндометрия); факторы репродуктивного характера (количество беременностей, родов, абортов, возраст при беременности и родах, длительность лактации, время появления менархе и наступления менопаузы и др.); гинекологическая патология (хронические воспалительные заболевания, синдром поликистозных яичников); эндокринные формы бесплодия; ятрогенная гиперэстрогенемия (прием дифазных контрацептивов, заместительная гормонотерапия, ЭКО); заболевания печени; эндокринная патология (гипотиреоз, сахарный диабет, ожирение, аденома гипофиза, заболевания надпочечников и др); психотравмирующие ситуации; генетическая предрасположенность.
К второстепенным факторам риска возникновения и развития РМЖ относятся: оваривально-менструальный статус (раннее менархе и поздняя менопауза увеличивают риск в 2,5 раза); гормональные факторы (риск увеличивается при многократных попытках экстракорпорального оплодотворения, при подготовке к которому женщина получает большие дозы эстрогенов; онкопатология генитальной сферы (рак яичников или эндометрия) увеличивают риск более, чем в 2 раза; ионизирующее излучение в дозе более 10 Гр. увеличивает риск в 3 раза; алкоголь в дозе 50 мл., ежедневно увеличивает риск в 1.4-1.7 раза; употребление пищи с высоким содержанием жирных кислот; ожирение в постменопаузе.
Женщины, находящиеся в группе риска (в соответствии с наличием вышеуказанных факторов) должны находиться под динамическим наблюдением врачей, начиная с 20-летнего возраста. Ежегодное УЗИ молочных желез показано всем женщинам, начиная с 20 лет, маммография показана женщинам группы риска в возрасте до 40 лет один раз в два-три года, а начиная с 40 лет – ежегодно. В случае наличия у близких родственников, особенно по женской линии, онкологической патологии и, в особенности, рака молочной железы, женщине следует обратиться в кабинет медицинской генетики для определения возможного наличия у неё мутаций онкогенов BRCA 1/2, p53, pTEN, CHEK 2 и др
Различают несколько клинических форм РМЖ: узловую, диффузную (отечно-инфильтративную, рожистоподобную, маститоподобную и панцирную), а также рак Педжета соска.
Узловые формы рака встречаются наиболее часто — в 75-80% случаев. Клиническим проявлением этой формы является наличие узлового образования в ткани молочной железы. Наиболее часто поражается верхне-наружный квадрант (до 50%). С сожалением следует констатировать, что приблизительно в 80% случаев женщины выявляют изменения в молочной железе сами.
Клиническая картина узловой формы РМЖ чрезвычайно многообразна и в первую очередь зависит от стадии заболевания. Условно симптомы РМЖ можно разделить на характерные для ранних стадий и клинические признаки, характерные для поздних форм рака.
К клиническим симптомам ранних форм рака относятся следующие:
- наличие опухолевого узла в ткани молочной железы;
- плотная консистенция опухоли (опухоль может быть деревянистой или даже каменистой плотности);
- ограниченная подвижность либо полное её отсутствие; как правило, безболезненность опухоли, наличие симптома «умбиликации» — втяжение кожи над опухолью, определяемое при сдвигании кожи;
- наличие одиночного плотного подвижного лимфатического узла в подмышечной области на стороне опухоли, либо нескольких аналогичных лимфоузлов, не спаянных между собой;
- возможны кровянистые выделения из соска, которые встречаются лишь при внутрипротоковом раке и внутрипротоковой папилломе.
К симптомам, характерным для более распространенных форм опухоли относятся:
- заметная на глаз деформация кожи молочной железы над определяемой опухолью (особенно при осмотре с поднятыми вверх руками);
- выраженный симптом «умбиликации» (втяжения) кожи над опухолью;
- явления лимфостаза – симптом «лимонной корки» над опухолью или за её пределами;
- прорастание кожи опухолью и/или изъязвление опухоли;
- выраженное утолщение соска и складки ареолы (симптом Краузе);
- втяжение и фиксация соска;
- деформация молочной железы, уменьшение или увеличение её размеров, подтягивание её вверх, фиксация к грудной стенке;
- множественные плотные малоподвижные или неподвижные лимфатические узлы в подмышечной области на стороне опухоли, иногда сливающиеся в конгломераты;
- плотные надключичные лимфатические узлы на стороне поражения.
Диффузные формы встречаются большей часть у женщин более молодого возраста и отличаются высокой агрессивностью и злокачественностью. Они характеризуются диффузным уплотнением всей ткани молочной железы, обусловленным опухолевой инфильтрацией; увеличением её размеров; гиперемией кожи молочной железы и местной гипертермией (при маститоподобных и рожистоподобных формах возможна общая температурная реакция); выраженным симптомом «лимонной корки» по всей поверхности молочной железы; резким утолщением соска и складки ареолы; втяжением и прочной фиксацией соска; в подавляющем большинстве случаев имеются пораженные подмышечные лимфатические узлы. В ряде случаев дифференциальный диагноз диффузных форм РМЖ весьма затруднителен, особенно с маститом и рожистым воспалением кожи. Различают первичные диффузные формы рака, когда опухолевый узел в железе не определяется, и вторичные – с наличием опухоли, чаще больших размеров, при которых отек и инфильтрация ткани железы и кожи обусловлены блоком отводящей лимфосистемы за счет массивного поражения регионарных лимфатических коллекторов.
Рак Педжета встречается в 3-5% всех случаев РМЖ. Начинается с появления сухих или мокнущих корок в области соска, покраснения и утолщения соска. Процесс может распространяться на ареолу. Клиническая картина на этой стадии может приводить к диагностическим ошибкам, когда устанавливается диагноз экземы соска и проводится длительное, но безуспешное лечение. Постепенно сосок уплощается, может возникнуть изъязвление, процесс распространяется на кожу молочной железы за пределы ареолы. Одновременно процесс может распространяться по крупным млечным протокам вглубь молочной железы, с формированием в её ткани опухолевого узла. Позже появляются метастазы в регионарных лимфатических узлах.
Категория T (tumor) – первичная опухоль
Т0 – первичная опухоль не определяется
Tis – carcinoma in situ – прединвазивный рак
Т1 — опухоль до 2 см. в наибольшем измерении
Т2 – опухоль до 5 см. в наибольшем измерении
Т3 – опухоль более 5 см. в наибольшем измерении
Т4 – опухоль любого размера с прямым распространением на грудную стенку и/или кожу.
Категория N (nodus) – регионарные лимфатические узлы.
N0 – нет признаков поражения метастазами регионарных лимфатических узлов
N1 – метастазы в 1 – 3 подмышечных и/или во внутригрудных лифмоузлах на стороне поражения.
N2 – метастазы в 4 – 9 подмышечных и/или во внутригрудных лимфоузлах на стороне поражения, либо метастазы в спаянных между собой лимфоузлах.
N3 – метастазы в 10 и более подмышечных и/или внутригрудных или в надключичных лимфоузлах на стороне поражения.
Категория М (metastases) – отдаленные метастазы. Могут поражать любой орган и ткань организма, но наиболее излюбленной локализацией отдаленных метастазов при раке молочной железы являются кости, легкие, печень, плевра. Менее часто встречаются метастазы в головной мозг, кожу, яичники, контрлатеральные лимфоузлы.
М0 – нет признаков отдаленных метстазов
М1 – имеются отдаленные метастазы.
Группировка по стадиям в соответствии с отечественной классификацией и системой TNM представлена в таблице.
В случае одновременного развития двух и более опухолей в пределах одной молочной железы (мультицентрический рост) стадирование производится по размерам наибольшего узла. Синхронное возникновение опухолей в обеих молочных железах классифицируется по каждой из них.
Если вы привыкли откладывать визиты к врачу на самый последний случай, следует начать с малого – самообследования. Маммологи рекомендуют проводить его регулярно раз в месяц, в первую фазу овариально-менструального цикла. Женщинам в периоде менопаузы нужно выбрать для этого определенный день месяца. Перед началом осмотра и ощупывания молочных желез нужно исключить наличие выделений – кровянистых или серозных – на внутренней стороне белья. Подобные следы, как и такие изменения кожного покрова молочной железы, как локальная морщинистость, сухость, покраснение, втяжения, изменение контура железы и подкожного сосудистого рисунка, наличие ранее отсутствовавших уплотнений, могут быть сигналом о сбое в организме и являются поводом для консультации со специалистом. Кроме того, насторожить должны появление образования в подмышечной области, боль в этой зоне, втяжение соска, отек ткани железы и вызванный этим эффект «лимонной корки».
На приеме у специалиста необходимо сообщить о семейной наследственности – если кто-то из родственников, особенно по женской линии, перенес онкологическое заболевание. Генетическая отягощенность сегодня выявляется просто и точно: для этого достаточно определить, является ли женщина носителями мутировавших генов BRCA 1 и/или 2, p53, pTEN, CHEK 2 и др.
Осмотр и пальпация молочных желез проводится в вертикальном и горизонтальном положении пациентки, причем исследовать необходимо не только молочные железы, но и все зоны регионарного метастазирования.
Далее пациентка направляется на маммографию. Рентгеновская маммография показана всем женщинам старше 40 лет, но может выполняться и в более раннем возрасте при сомнительной или подозрительной ультразвуковой картине. Маммография может показать изменения в молочных железах за 1.5 – 2 года до появления клинических проявлений опухолевого процесса. При наличии кровянистых выделений из соска широко используется метод дуктографии, при котором в сецернирующий проток вводится тупоконечная игла, через которую вводится контрастное вещество с последующим выполнением рентгенологического исследования.
К преимуществам рентгеновской маммографии относятся: высокая чувствительность, что дает возможность выявлять 85-90% случаев рака молочной железы; возможность выявлять микрокальцинаты до 0,5мм; возможность выявления опухоли задолго до того, как она будет определяться пальпацией. Ультразвуковое исследование – УЗИ – основано на получении изображения при помощи высокочастотных звуковых колебаний и позволяет четко определять кисты, крупные образования в ткани молочных желез и состояние регионарных лимфатических узлов. УЗИ показано всем пациенткам, независимо от возраста.
Преимуществами ультразвуковой томографии являются его безопасность и неинвазивость, отсутствие рентгеновского облучения. Изображение получается сразу, не требуя проявления пленки или цифровой обработки сигнала при цифровой маммографии. Метод позволяет дифференцировать кисты и солидные опухоли и может использоваться при биопсии опухоли.
К его недостаткам можно отнести следующие: УЗИ не обладает такой детальностью, как рентгеновская маммография; не позволяет выявлять микрокальцинаты. Кроме того, заключение УЗИ во многом носит субъективный характер, а надежность его результата целиком зависит от опыта и квалификации врача.
Следует отметить, что рентгеновская маммография и ультразвуковое исследование – это два взаимодополняющих метода исследования, позволяющие объективизировать картину изменений в молочных железах.
Магнитно-резонансная томография в настоящее время, по мнению ряда авторов, является наиболее информативным методом исследования молочных желез. Её действие основано на воздействии магнитным полем на определенный орган или участок органа. Сигнал, отражаемый при этом, преобразуется компьютером в цифровое изображение ткани.
Однако, достоверно подтвердить или опровергнуть диагноз злокачественного новообразования молочных желез возможно только при морфологическом исследовании клеточного или тканевого состава опухоли. К методам морфологической диагностики относятся цитологическое и гистологическое исследование. В последние годы широко используется иммуногистохимическое исследование опухолевой ткани для определения молекулярно-биологического типа рака молочной железы.
Тонкоигольная биопсия. Показаниями к ней служат: все сомнительные очаги в ткани молочной железы размерами > 0.5 см.; кисты размерами более 2 см, особенно при наличии внутрикистозных папиллярных разрастаний; кисты размерами менее 2 см. при сомнительной УЗ картине. При необходимости тонкоигольная пункция выполняется под контролем УЗИ или маммографии. Также обязательному цитологическому исследованию подлежат выделения из соска, особенно кровянистые.
К преимуществам тонкоигольной биопсии относятся: она занимает мало времени, не требует наложения швов, не оставляет рубцов, не требует анестезии. Однако цитологический метод является менее информативным по сравнению с гистологическим ввиду того, что для исследования забираются клетки, а не ткань опухоли, что не позволяет определить морфологический вид опухоли, степень злокачественности и другие важные параметры, характеризующие опухоль.
CORE-биопсия (пистолетная биопсия, трепанобиопсия) – является более совершенным и информативным методом морфологической диагностики рака молочной железы. К преимуществам CORE-биопсии можно отнести быстроту её выполнения, практическое отсутствие дискомфорта. Не требует хирургического разреза, наложения швов и обычно не оставляет рубца, позволяет взять образец большего объема по сравнению с тонкоигольной аспирацией, что обеспечивает более высокую точность диагноза. В случае подтверждения диагноза рак молочной железы возможно сразу определить степень злокачественности опухоли, рецепторный статус, экспрессия гена HER2/neu, степень протиферативной активности опухоли Ki-67. Высокая точность метода позволяет не проводить хирургическую биопсию, если опухоль доброкачественная. К недостаткам метода можно отнести необходимость местной анестезии, может потребоваться несколько введений иглы, возможно появление гематомы и/или болезненности в течение нескольких дней.
В последние годы все большее распространение получает метод стереотаксической вакуумной биопсии на установке «Маммотест-Маммовижн-Маммотом». Установка обеспечивает такую же точность диагностики, как хирургическая биопсия, но при значительно меньших затратах; отсутствие необходимости применения общей анестезии; безопасность, эффективность и быстроту работы; максимальный доступ к молочной железе; максимально безопасные и комфортные условия для пациента. При доброкачественных опухолях позволяет удалить все образование целиком без последующего хирургического вмешательства. К недостаткам метода следует отнести необходимость местной анестезии, возможное появление гематомы и болезненности в течение нескольких дней и высокая стоимость исследования, которая может не покрываться страховкой.
И, наконец, финальным методом получения материала для морфологической диагностики является хирургическая биопсия – иссечение опухоли или секторальная резекция молочной железы. Требует срочного (интраоперационного) гистологического исследования удаленного материала. Хирургическая биопсия позволяет получить ткань опухоли или всю опухоль целиком, а также крупный образец нормальной ткани для сравнительного анализа, что позволяет определить взаимодействие опухоли с окружающими тканями. В случае подтверждения диагноза рака необходимо расширение объема хирургического вмешательства до радикальной операции. Хирургическая биопсия оставляет после себя рубец, требуется наложение швов, увеличивается время заживления раны после хирургического вмешательства, повышается вероятность инфекционных осложнений и образования гематом по сравнению с пункционной биопсией, возможно изменение внешнего вида молочной железы.
Лечение РМЖ является весьма сложной проблемой, однако, в последние годы с внедрением новых химиопрепаратов, методик лучевой терапии, таргетного лечения достигнуты значительные успехи в этом разделе клинической онкологии.
При РМЖ в комплексе лечебных мероприятий используется практически весь арсенал основных противоопухолевый воздействий: хирургический метод, лучевая терапия, лекарственное лечение – химиотерапия, гормонотерапия, таргетная терапия.
Выбор метода лечения каждой больной планируется с учетом основных прогностических факторов: клинических – возраста, состояния овариально-менструальной функции, степени распространенности опухолевого процесса (у первичных больных – стадии заболевания), размера и локализации первичной опухоли; и морфологических – гистологический и имууногистохимический вариант опухоли, количество пораженных метастазами регионарных лимфатических узлов, степень злокачественности опухоли, рецепторного статуса опухоли, экспрессия гена HER2/neu, степень протиферативной активности опухоли Ki-67.
Лечение можно разделить на два компонента: локальное воздействие – хирургическое вмешательство и лучевая терапия (пред- и послеоперационная) и системное – химиотерапия, гормонотерапия, таргетная терапия.
Хирургическое лечение. Операциями выбора при раке молочной железы являются радикальная мастэктомия в различных модификациях, радикальная резекция (секторальная резекция с подмышечной лимфодиссекцией), лампэктомия, туморэктомия. Широко распространенные в последние годы органосохраняющие операции не показаны при больших размерах опухоли в молочной железе небольшого размера. Осложнениями хирургического лечения при раке молочной железы являются: вторичный лимфостаз верхней конечности, связанный с удалением основных путей лимфооттока при аксиллярной лимфодиссекции, нарушения чувствительности кожи, связанные с пересечением межреберно-плечевых нервов, дефицит тканей передней грудной стенки, повышенная потливость, рубцовые изменения кожи.
Косметические дефекты после радикальных операций, приводящие к значительной психо-эмоциональной травме у оперированных женщин, в настоящее время устраняются путем все более широкого выполнения одномоментных либо отсроченных реконструктивно-пластических операций. Дефект тканей замещается либо собственными тканями организма (аутопластика) или другимгим способом пластики является аллопластика – установка силиконовых эндопротезов или экспандеров.
Лучевая терапия. Основной её целью является девитализация низкодифференцированных опухолевых клеток, подавление роста метастазов в лимфатических узлах и кровеносных и лимфатических сосудах. В качестве самостоятельного метода предоперационной терапии в настоящее время лучевая терапия практически не используется. Проведение послеоперационной лучевой терапии показано после органосохраняющих операций, у пациенток после мастэктомии со стадией T4N2-3. К осложнениям лучевой терапии относятся постлучевая эритема и отек, постлучевой фиброз, лимфостаз. Менее часто встречается лучевой пульмонит и лучевой миокардит.
Химиотерапия применяется для профилактики и лечения метастазирования, а также в качестве неоадъювантного воздействия для перевода опухоли в операбельное состояние при первично-неоперабельных опухолях. Рак молочной железы – опухоль, чувствительная к большинству современных противоопухолевых препаратов. Эффективность отдельных препаратов составляет от 20 до 75%. Для усиления противоопухолевого эффекта используются комбинации цитостатиков. Наибольшей противоопухолевой активностью при раке молочной железы обладают таксаны и антрациклины.
Основные принципы химиотерапии: подбор препарата с учетом спектра его действия; выбор оптимальной дозы, режима и способа введения; учет факторов, требующих коррекции дозы во избежание тяжелых осложнений химиотерапии. Токсичность химиотерапии объясняется повреждающим действием химиопрепаратов не только на опухолевые клетки, но и на здоровые клетки кишечного эпителия, кроветворения, волосяные фолликулы и т.д. Интервалы в 3-4 недели между введением химиопрепаратов обеспечивает полную регенерацию поврежденных нормальных тканей.
В зависимости от времени проведения химиотерапия делится на неоадъювантную, проводимую перед операцией с целью уменьшить опухолевую массу, перевести опухоль в операбельное состояние для возможного выполнения органосохраняющий операции, и адъювантную, которая проводится после операции с целью подавления возможно существующих микрометастазов рака в органах и тканях организма.
Гормональное лечение. Рак молочной железы является гормонозависимой и гормоночувствительной опухолью. У 50-70% больных опухоль содержит специфические белки, называемые рецепторами стероидных гормонов – эстрогенов и прогестерона. У этих больных гормонотерапия дает выраженный эффект. В настоящее время используются два вида гормональных препаратов: антиэстрогены (тамоксифен и его аналоги), блокирующие гормональные рецепторы, и ингибиторы ароматазы, используемые у женщин в менопаузе и препятствующие образованию эстрогенов за счет превращения андрогенов в эстрогены (аримидекс, летрозол, аромазин и др.).
Таргетная терапия используется у больных, опухоли которых экспрессируют специфический белок, регулирующий рост опухоли — HER2/neu. Этот белок встречается у 20-30% больных. Таргетный препарат герцептин (трастузумаб) блокирует этот рецептор. Препарат не действует на опухолевые клетки без данного рецептора. Таргетная терапия обладает цитостатическим, а не цитотоксическим действием, она меньше угнетает кроветворение, но чаще вызывают сыпи, кардиотоксичность, утомляемость, диарею.
Таким образом, можно констатировать: возможности диагностики и лечения рака молочной железы значительно расширились за последнее десятилетие, выбор оптимальной лечебной тактики при РМЖ строится с учетом биологических характеристик опухоли, распространенности процесса и индивидуальных особенностей больных. В этих условиях особое значение приобретает своевременное обращение больных за медицинской помощью, ранняя диагностика и использование всех современных методов лечения. Усовершенствование терапевтических подходов, наряду с улучшением ранней диагностики, нашло свое отражение на популяционном уровне в виде снижения смертности от РМЖ в ряде стран, в том числе и в России. Повышение онкологической настороженности женщин, наличие полноценной информации о заболевании, современных возможностях диагностики и лечения рака молочной железы, своевременное обращение к врачу при первых признаках болезни, позволяют быть уверенными в том, диагноз рак молочной железы перестал быть приговором.
источник