Удаление груди — нередко болезненный вопрос для женщины с раком молочной железы. Однако избавляться от пораженного органа целиком нужно далеко не всегда. Иногда грудь можно сохранить, убрав только опухоль. Не всегда нужно удалять и подмышечные лимфоузлы. Даже если вам показано удаление молочной железы, у вас есть возможность бесплатно и единовременно сделать реконструкцию — установить имплантаты по квоте.
Вместе с врачами-онкологами, резидентами Высшей школы онкологии Александром Петрачковым и Анной Ким мы сделали подробный разбор темы.
Какие общие факторы учитываются врачом при назначении операции при раке молочной железы?
Онкологическая хирургия молочной железы делится на два вида:
1. удаление всего органа (органоуносящая операция);
2. удаление только части органа (органосохраняющая операция).
Мастэктомия — это удаление молочной железы целиком. Единых показаний для ее удаления нет. Однако обычно мастэктомию проводят, если есть:
— внутрипротоковая карцинома, которая занимает почти всю железу;
— несколько очагов. Грубо говоря, вырезать несколько кусков ткани нецелесообразно;
— желание пациентки (в том числе при совмещении с реконструкцией молочной железы);
«Мастэктомия перестает быть «плохой» операцией, потому что теперь ее можно делать с одномоментной реконструкцией. Реконструкция — восстановление молочной железы с помощью протеза (имплантата). Отсроченную реконструкцию делают по желанию пациентки, когда мастэктомия была некоторое время назад»
— кровотечения при распадающейся опухоли;
Важно: Удаление опухоли или всей железы при метастатическом раке груди нецелесообразно! Это возможно только при наличии осложнений со стороны первичной опухоли.
«Не стоит забывать, что сейчас разрабатываются методы генетического исследования женщин с генетической мутацией. Им требуется удаление молочной железы целиком, потому что у них даже в оставшейся железе может возникнуть рак. Однако вопрос остается дискутабельным в профессиональных сообщества. Сейчас идут исследования, которые говорят, что это только опция, есть вариант гормональной профилактики тамоксифеном у женщин-носительниц гена BRCA1»
Да. Чем ниже стадия, тем более щадящие варианты мастэктомии могут быть. Например, возможно полное сохранение всей кожи и соска, а вместо удаленной железы ставится имплантат.
При необходимости реконструкция проводится в несколько этапов — ставится временный имплантат, расширяется и заполняется водой. Затем он растягивает кожу, создавая объем для новой молочной железы. После этого хирург меняет протез на постоянный с силиконом.
Когда действительно нужно удалять подмышечные лимфоузлы (проводить лимфодиссекцию)?
Это дискуссионный вопрос. Сейчас считается, что необходимо удалять только клинически позитивные узлы или когда сигнальные лимфоузлы не обнаруживаются. Удаление лимфоузлов действительно снижает количество рецидивов, но качество жизни пациентки может сильно снизиться.
Раньше полная подмышечная лимфодиссекция была популярной операцией, когда онкология была более радикальной. Сейчас от этого подхода уходят. Многие зарубежные исследователи считают удаление лимфоузлов стадирующей операцией. Она нужна, чтобы понять, насколько распространилось заболевание, и выбрать тактику лечения. Сейчас ее должны делать в следующих случаях:
— при пораженных сигнальных лимфоузлах,
— при выраженных клинических показаниях, когда до начала лечения есть пораженные лимфоузлы и они не исчезают после химиотерапии.
Объем вмешательства зависит от возраста пациентки?
«Вообще я о таких прецедентах слышал. Но есть правила, как обязан себя вести онколог — он должен обсуждать все возможные варианты с пациенткой. Органосохраняющая операция и мастэктомия обладают схожей эффективностью. Выбирать, что ей будут делать, будет только пациентка. Если мы видим небольшую опухоль, то мы предлагаем оба варианта.
Женщины бывают разные. Они хотят разных вещей и по-разному относятся к своему организму, телу. Кто-то очень боится рака и настроена еще до визита к врачу все удалить, не всегда врач может переубедить.
Такие прецеденты должны уйти в прошлое, потому что сам пациент должен решать, что ему больше нужно, если врач не видит препятствий со стороны своих возможностей и онкологических познаний»
Можно ли пойти в частную клинику, чтобы восстановить грудь после мастэктомии?
«Частные клиники общего профиля также занимаются реконструкцией после удаления железы. Однако клиники эстетической медицины специализированно занимаются эстетической хирургией — подтяжкой и увеличением молочных желез. Эстетикой с точки зрения реконструкции занимаются в основном в государственных крупных центрах. Эти операции входят в раздел государственного финансирования. Можно получить операцию по квотам, государство их оплатит»
Какие могут быть протезы (имплантаты)?
Чаще всего имплантаты производятся в Америке. Сейчас стали появляться протезы из Кореи, Мексики, Германии и других стран. Какой имплантат достанется пациентке — зависит от того, что разыграно в тендере. Протезы пока не подвергаются импортозамещению. Они все схожего хорошего качества, стерилизованы и запечатаны. По факту разницы между ними нет — такие же используют в частных клиниках пластической хирургии.
Какие могут быть осложнения при протезировании (установке имплантатов)?
лимфорея (когда комится жидкость после имплантации). Необходимо пунктировать или дренировать;
протрузии имплантатов (когда имплантат продавливает кожу на месте шва). От этого никто не застрахован, но наибольшие риски есть у пациенток после лучевой терапии — кожа истончается, нарушается ее кровоснабжение и риск осложнений увеличивается.
липосакция, когда забирается собственная жировая ткань в шприцы и потом она пересаживается;
использование лоскута из жировой ткани с сосудами.
Это разные по принципу операции и разные по результату, потому что лоскут позволяет сделать единомоментно полный объем молочной железы. Что же про липофилинг, то это, как правило, не больше 100-200 мл за один сеанс, а это редко когда позволяет полностью восстановить ткань молочной железы.
Органосохраняющие операции предполагают просто удаление опухоли из органа. Формат выполнения зависит от того, насколько большая зона удаляется и насколько женщина хочет косметически восстановить железу. Можно ограничиться только удалением опухоли:
без пластики (с незначительной деформацией, не влияющей на качество жизни);
с пластикой лоскутами, восполняющими форму и объем (со спины, живота);
с онкопластикой — маскировкой операции под обычную пластическую операцию с помощью перемещения тканей. Это нужно тем, кто хочет неплохой косметический результат (если есть возможность сделать органосохранную операцию).
Операции с использованием лоскутов
Если врач предлагает лоскутные пластики, то это тоже может быть исполнено в двух вариантах :
если удалена кожа, то мы берем лоскут с других частей тела с кожей;
если кожа не удалена, то мы можем взять только жир и эта операция часто эстетически выигрышная. Однако она технически сложная: занимает порой 7-8 часов, имеет немало осложнений и мало кто владеет навыками таких операций сейчас.
Показания для органосохраняющей операции:
— ранние стадии — T1-T2 (в зависимости от вида новообразования), в том числе после предоперационной химиотерапии.
Фактически, органосохраняющую операцию можно выполнить и при большой опухоли (больше 5 см), просто от органа ничего не останется. Поэтому при больших опухолях мастэктомия целесообразнее.
Примечание: после органосохраняющей операции женщине всегда показан курс (или несколько) лучевой терапии. Теоретически, можно сделать органосохраняющую операцию и на 3-4 стадии, но это необходимо обсудить с врачом. Все зависит от того, какая опухоль у пациентки.
«Когда размер опухоли 5 см и больше — в любом случае уйдет большая часть железы и называть операцию органосохраняющей будет уже неразумно. Почему назначается химиотерапия до операции? Одна из причин — возможность прооперировать органосохранно. Чем меньше размер опухоли, тем меньший объем ткани нужно удалять и тем легче проходит операция. При органосохраняющих операциях можно сделать онкопластику — замаскировать операцию по резекции железы под пластическую операцию. Это будет выглядеть как подтяжка, хотя на самом деле у женщины удалили злокачественную опухоль»
Что лучше с эстетической точки зрения — мастэктомия с реконструкцией или органосохраняющая операция?
Радикальная резекция не всегда обеспечивает лучший косметический результат по сравнению с мастэктомией. Лучевая терапия нужна всегда, после нее может много эстетических нюансов:
— излишняя пигментация кожи,
— деформация кожи от лучевого ожога.
К сожалению, все эти эффекты могут помешать эстетическому результату. Но это не отменяет то, что лучевая терапия всегда нужна после органосохранных операций.
Как различаются подходы к операциям при раке молочной железы в крупных городах и регионах?
«Регионы и крупные города уже подтягиваются к Москве и Питеру. А столица и Петербург оперируют на том же уровне, что и западные коллеги. Сейчас общая тенденция – уменьшать объем операций, не делать сверхрадикальных вмешательств, то есть с удалением мышцы. Если говорить о том, что происходит вне областных центров, то там до сих пор встречаются сверхрадикальные операции. Нужно понимать, что необходимость удаления всей опухоли — это столп всей онкохирургии»
Как понять, что мне могут сделать органосохраняющую операцию или реконструкцию имплантатами?
Обязательно сначала спросите врача: «Могу ли я сохранить грудь? Если нет, какие есть варианты реконструкции?»
Задача врача — обеспечить полной информацией. Он также должен обеспечить безопасность вмешательства — как онкологического, так и эстетического. Пациентка приходит к своему онкологу, зная о своей стадии, желании удалить новообразование, страхах. Если она живет далеко и для нее будет проблематично наблюдаться после реконструкции, ей также нужно сказать об этом врачу. Если вы не уверены в своем враче, напишите другим врачам и уточните все.
Если человек не разбирается в своем диагнозе, может быть есть список вопросов, который стоит задать врачу?
— На какой стадии заболевание?
— Насколько это злокачественная опухоль, требует ли это дополнительного лечения?
— Перечислите симптомы: боли, втянутый сосок, гусиная кожа, покраснение и другие поражения кожи.
Все это может послужить критерием к вмешательству и стоит все это задавать своему врачу. Также стоит уточнить, возможна ли реконструкция.
Врачи вообще заинтересованы в органосохраняющих операциях и реконструкциях, а не только в мастэктомии?
Сохранить грудь — это технически даже проще, чем удалить полностью молочную железу. Однако пока не все и не везде могут делать реконструкции. Обычно происходит так, потому что немногие могут этому обучиться. Такое бывает из-за дорогого обучения, у кого-то больница не может обеспечить оборудованием, в том числе протезами.
источник
Удаление опухоли обычно выполняется по поводу фиброаденомы. Кожный разрез делается либо над самой опухолью, либо по краю ареолы (околососковый кружок), либо по субмаммарной складке (складка под молочной железой). Два последних варианта более эстетичны. Обычно, через год рубец от такого разреза довольно трудно найти. Производится удаление самой опухоли, при этом не повреждаются протоки молочной железы (и не возникает проблем для последующего кормления грудью), не возникает деформации железы, не возникает дефицита объёма железы. Ушивается «ямка» в месте расположения опухоли, накладывается внутрикожный шов.
Хирургическое лечение рака молочной железы, несомненно, является основным методом комплексного лечения. Его эффективность существенно возрастает при сочетании с химиотерапией, гормональной терапией и лучевой терапией.
Одним из основных принципов лечения рака молочной железы в Европейской клинике является проведение в основном органосохраняющих операций, так и операций полного удаления молочной железы (мастэктомия), с учетом индивидуальных показаний.
Суть органосохраняющей операции при раке молочной железы заключается в удалении только очага опухоли молочной железы с небольшим количеством окружающей здоровой ткани (лампэктомия и квадрантектомия). После такой операции обычно следует курс лучевой терапии на область оставшихся тканей молочной железы и регионарных зон.
Важно знать, что при инвазивном раке обе эти операции сочетаются с обязательным удалением подмышечных лимфатических узлов — лимфаденэктомией. При неинвазивных формах рака в настоящее время полного трехуровнего удаления лимфоузлов не производится, поскольку это резко ухудшает качество жизни пациенток — развивается отёк верхней конечности (лимфедема), нарушения подвижности в плечевом суставе, а также хронические боли.
Поэтому в Европейской клинике в рамках первого комплексного обследования в обязательном порядке проводится биопсия «сторожевого» лимфоузла. Суть данной методики состоит в определения поражённости раком подмышечного лимфатического узла. Такая методика дает возможность проводить органосохраняющее лечение и сохранять подмышечные лимфоузлы, если они не поражены метастазами. Это, безусловно, положительно сказывается на качестве дальнейшей жизни пациентки. Наличие раковых клеток в «сторожевом» лимфоузле свидетельствует о высоком риске обнаружения этих клеток в отдаленных органах и тканях организма, то есть о риске развития метастазов. В этом случае выполняются МР-томография и сцинтиграфия. Мы в обязательном порядке проводим гистологическое и иммуногистохимическое исследования операционного материала (удаленных тканей молочной железы и лимфоузлов).
Такую операцию делают при узловой мастопатии (сборный диагноз, включающий и ситуации с уплотнением в молочной железе неизвестной природы). Кожный разрез производят либо над уплотнением, либо по краю ареолы, либо по субмаммарной складке. Удаляется уплотнение, образовавшийся дефект ткани железы ушивается, накладывается внутрикожный шов.
Особая техника секторальной резекции применяется при внутрипротоковой папилломе (обычно это маленькая опухоль, расположенная в протоке и проявляющаяся выделениями из соска). В проток вводится красящее вещество. Кожный разрез делается по краю ареолы, за соском находят прокрашенный проток, в этом месте его пересекают, выделяют к периферии от соска с тем, чтобы была удалена папиллома. Ушивается ткань железы и кожа внутрикожным швом.
В Европейской клинике ведёт консультативный приём и выполняет операции известный российский хирург-маммолог, доктор медицинских наук Сергей Михайлович Портной (автор более 300 печатных работ, член правления Российского общества онкомаммологов, автор трех патентов на изобретения).
Сергей Михайлович выполняет весь объем оперативных вмешательств на молочной железе, включая органосохраняющие и реконструктивные пластические операции.
Применяется при внутрипротоковой папилломе, когда её не удаётся локализовать, при множественных внутрипротоковых папилломах, располагающихся в центральных отделах протоков. Операция приемлема в тех случаях, когда не предвидится кормление грудью. После кожного разреза, выполненного по краю ареолы, за соском пересекают все протоки. Ткань железы с центральными отделами протоков выделяют на 2–3 см и удаляют. Дефект ткани железы ушивается, накладывается внутрикожный шов.
Используется при аденоме соска, — редкой доброкачественной опухоли или как диагностический этап для морфологической диагностики рака Педжета. Клиновидно резецируется сосок, накладываются узловые швы тонким шовным материалом. Часть протоков при этом пересекаются, что может осложнить последующую лактацию.
Мастэктомия — удаление молочной железы (без лимфатических узлов). Выполняется при неинвазивных формах рака (протоковый рак in situ, дольковый рак in situ), синдроме наследственного рака молочной железы, как профилактическая операция. Если не планируется одновременное воссоздание молочной железы, на груди остаётся тонкий линейный рубец. В тех случаях, когда операция сочетается с одномоментной реконструкцией молочной железы, мастэктомия производится в технике кожесохраняющей мастэктомии (удаляется сосково-ареолярный комплекс, вся остальная кожа железы сохраняется) или подкожной мастэктомии (сохраняется вся кожа железы). После таких операций остаётся «кожаный мешочек», который должен заполнить пластический хирург. Эстетический результат таких операций обычно очень хороший.
Радикальная мастэктомия, то есть операция, включающая удаление молочной железы с грудными мышцами и жировой клетчаткой 1–3 уровней, стала выполняться William Stewart Halsted с 1882 г. в Больнице Джона Хопкинса (John Hopkins Hospital, Baltimore, Maryland, USA). Первое описание операции, произведённой 13 больным, относится к 1891 г., это описание было частью статьи, посвященной заживлению ран (W. S. Halsted «The treatment of wounds with especial reference to the value of the blood clot in the management of dead spaces». John Hopkins Hospital Rep., 1890–1891. 2:255.). Удаление жировой клетчатки обусловлено нахождением здесь лимфатических узлов, которые нередко были поражены метастазами рака и представляли собой множественные плотные узлы различного размера. Анатомическое деление клетчатки производится относительно малой грудной мышцы: клетчатка кнаружи от малой грудной мышцы — это клетчатка 1 уровня, кпереди и кзади от малой грудной мышцы — 2 уровня, кнутри от малой грудной мышцы — 3 уровня. Удаление мышц объяснялось тем, что при запущенных формах болезни (которых было большинство) были поражены метастатическим процессом лимфатические сосуды, проходящие сквозь, мышцы и фасции, покрывающие мышцы.
К недостаткам операции относится деформация грудной стенки. В настоящее время показаниями к радикальной мастэктомии по W. S. Halsted являются прорастание первичной опухолью большой грудной мышцы и поражение лимфатических узлов Роттера, а также выполнение паллиативных операций.
D. H. Patey и W. H. Dysonв 1948 г. предложили модифицированную методику радикальной мастэктомии, отличающуюся от операции W. S. Halsted сохранением большой грудной мышцы. В блок удаляемых тканей включается молочная железа, малая грудная мышца и лимфатические узлы 1–3 уровней. Операция в большинстве случаев не уступает по эффективности операции Холстеда, её преимуществом является меньшая травматичность и меньшая деформация грудной стенки. В то же время, не всё просто с остающейся большой грудной мышцей. При удалении малой грудной мышцы неизбежно пересекается 1–2 мелких нервных веточек (латеральный пекторальный нерв и ветвь медиального пекторального нерва), иннервирующих наружную часть большой грудной мышцы. Впоследствии, конечно, это приводит к атрофии наружной части большой грудной мышцы.
Модификация радикальной мастэктомии по J.L Madden предполагает сохранение обеих грудных мышц и удаление клетчатки I и II уровней.
Является вариантом модифицированной радикальной мастэктомии, разработанным в ФГБУ РОНЦ им. Н. Н. Блохина РАМН. Подразумевает удаление молочной железы, удаление клетчатки I–III уровней без удаления малой грудной мышцы в отличие от операции Patey & Dyson. Преимуществом операции является полное удаление клетчатки и сохранение мышц, и их иннервации.
Все предыдущие операции, выполняющиеся при раке, носили название «радикальная». Тем самым подразумевалось, что болезнь удаляется с мельчайшими «корнями» и не должна вернуться, операция была направлена на предотвращение развития метастазов. В других случаях, когда опухоль уже дала метастазы или когда местное распространение болезни столь велико, что наиболее вероятно после операции последует развитие метастазов, операция не может претендовать на название радикальной. В таких случаях она может выполняться с паллиативной целью, то есть с целью устранить непосредственные неприятности, связанные с наличием опухоли, — распад опухоли, кровотечение; либо с целью уменьшения объёма опухолевой ткани и создания условий для более эффективного лекарственного лечения.
В нашей клинике выполняется широкая панель онкологических операций, включающих одновременную реконструкцию молочной железы. Возникает вопрос: это безопасно? Не провоцирует ли дополнительная операция быстрое развитие метастазов?
Для ответа на эти вопросы нами были проанализированы сведения о 503 больных РМЖ I — III стадий, получавших лечение в ФГБУ РОНЦ им. Н. Н. Блохина РАМН в 1992—2002 гг. В основную группу вошли 124 больные, средний возраст 41,5 года (24–67). Женщины были оперированы в объеме радикальной мастэктомии с сохранением грудных мышц в сочетании с первичной реконструкцией молочной железы: экспандером (n=14) или кожно-жировым лоскутом на широчайшей мышце спины с использованием эндопротеза (n=18), или поперечным ректоабдоминальным лоскутом на мышечной ножке (n=92). Контрольную группу составили 379 больных, средний возраст 40,1 года (26–79). 145 больным выполнены органосохраняющие операции, 234 — радикальная мастэктомия с сохранением грудных мышц. Группы были сопоставимы по основным факторам, оказывающим влияние на прогноз (стадия, возраст, проводимое лечение). Лекарственное и лучевое лечение проводились по общим принципам. Медиана длительности прослеженности 63,7 (20,4–140,5) месяца.
Частота местных рецидивов составила:
- в молочной железе после органосохраняющих операций — 4,1%;
- после модифицированной радикальной мастэктомии — 1,7%;
- после модифицированной радикальной мастэктомии с первичной реконструкцией — 1,6% (p>0,05).
За весь срок наблюдений рецидив болезни (то есть не только местно, а в любых органах и тканях) наблюдался в 18,6±3,5% в группе с реконструкцией молочной железы (у 23 больных) и в 18,2±2,0% в контрольной группе (у 69 больных, p>0,05). Кривые безрецидивной выживаемости и общей выживаемости в сравниваемых группах статистически не различаются.
По данным многофакторного анализа факт выполнения первичной реконструкции молочной железы не влияет на развитие рецидива болезни. Анализ факторов, влияющих на рецидив болезни, показывает преобладающее влияние таких известных факторов, как критерии T, N, возраст, проведение химиотерапии. Факт проведения первичной реконструкции не оказывал статистически значимого влияния на процесс рецидивирования опухоли. Таким образом, первичная реконструкция молочной железы может безопасно выполняться больным РМЖ.
Однако, чем больше объем операций, тем вероятнее осложнения их заживления, особенно у пациенток при сопутствующем сахарном диабете, ожирении и длительном курении. У них длительное заживление раны может отсрочить проведение адъювантной лучевой терапии, химиотерапии. Поэтому для больных с планируемой адъювантной химиотерапией или лучевой терапией, имеющих перечисленные факторы, ухудшающие заживление раны, предпочтительнее отказаться от первичной реконструкции.
История развития органосохраняющих операций при раке молочной железы относительно коротка. Такие операции стали возможны благодаря сочетанию трёх основных факторов: 1) более раннему выявлению болезни; 2) осознанию того, что расширение объёма операции при ранних формах рака не приводит к улучшению выживаемости больных; 3) применению лучевого воздействия на сохранённую молочную железу как мощного средства снижения вероятности местного рецидива.
G.Crile Jr. в 1975 г. представил10-летние результаты рандомизированного исследования, сравнивающего органосохраняющую операцию частичную мастэктомию (partial mastectomy) с тотальной мастэктомией. В группах сравнения было по 42 больных первично операбельным раком. Смертность от рака за 10 лет составила 34% и 38% соответственно.
Минимальное по объёму удаляемой ткани молочной железы хирургическое вмешательство — лампэктомия (lump — глыба, кусок, комок), было разработано в ходе исследований Национального проекта дополнения операций на молочной железе и кишечнике (США, NSABBP).
В исследование входили больные с величиной опухоли не более 4 см. Сравнивались группы больных с разными видами лечения: лампэктомией (1-я группа), лампэктомией с лучевой терапией (2-я группа), модифицированной радикальной мастэктомией (3-я группа).
При 12-летнем наблюдении местный рецидив в молочной железе развился у больных 1-й группы в 35%, 2-й группы — в 10%. Достоверные различия общей выживаемости и выживаемости без отдалённых метастазов между сравниваемыми группами отсутствовали. Общий вывод о равной эффективности органосохраняющего лечения и радикальной мастэктомии подтвержден и при 20-летнем наблюдении. Частота местного рецидива после лампэктомии составила 39,2%, после лампэктомии с облучением — 14,3%.
Обретя собственный опыт в выполнении лампэктомии, мы пришли к необходимости её модифицировать. Модификация касается двух моментов: опухоль удаляется обязательно с запасом здоровых тканей вокруг неё, обязательно производится ушивание ткани железы. Для опухолей небольшого размера (до 1–2 см) лампэктомия остаётся лучшей операцией: нетравматичной и элегантной.
При больших размерах опухоли или при её центральной локализации для сохранения формы железы возникает необходимость в привлечении дополнительных усилий по перемещению тканей, и / или вмешательства на контралатеральной железе для сохранения симметрии, то есть необходимость в выполнении онкопластических резекций.
Термин «онкопластическая резекция» общепринят в мировой литературе, подразумевает под собой выполнение резекции молочной железы по поводу рака с использованием методов пластической хирургии для восстановления формы железы, возможно также совмещение с одновременным оперативным вмешательством на противоположной железе для восстановления симметрии.
Одна из первых операций, которую можно отнести к онкопластическим резекциям (термин «онкопластическая резекция» был предложен позже), это реконструкция молочной железы по A.Grisotti — наиболее успешный метод восстановления формы железы после удаления её центрального отдела. После резекции центрального отдела железы вместе с соском и ареолой от медиального края образовавшейся раны вертикально вниз производится кожный разрез, который затем продляется латерально по субмаммарной складке. Ниже раневого дефекта часть кожи деэпидермизируется, оставляется островок кожи, соответствующей по размерам ареоле. В проекции вертикальной части кожного разреза ткань железы рассекается на всю толщу до субмаммарного пространства, мобилизуется весь нижне-наружный квадрант железы. Мобилизованная ткань железы ротируется, её часть, располагающаяся под кожным островком, перемещается в центральный отдел и подшивается. В последующем может быть выполнен татуаж вновь созданной «ареолы» и пластика соска.
В России период выполнения онкопластических резекций стартовал с начала 90-х годов, когда была предложена операция, использующая технику редукционной пластики перевернутого «Т». Операция выполнялась при нижних локализациях опухоли, обязательной была редукционная пластика противоположной железы.
В настоящее время вариантов онкопластических резекций очень много, можно сказать, что их столько, сколько пациенток. Техника и ход операции диктуется онкологической ситуацией, формой молочных желёз, особенностями состояния тканей, излюбленными приёмами хирурга.
Органосохраняющие операции не являются автоматически адекватным видом лечения. Необходимо тщательное обследование пациенток, которым планируется такая операция. Лучше сделать мастэктомию, чем несоответствующую онкологическим критериям органосохраняющую операцию.
«Чистота» краёв резекции — главный показатель адекватности органосохраняющей операции. Органосохраняющая операция признается радикальным вариантом местного лечения только в сочетании с лучевой терапией.
Хирургия — наиболее радикальный метод лечения онкологических заболеваний. Но, даже если опухоль полностью удалена, и врач констатировал ремиссию, в будущем сохраняется риск рецидива. Каждая женщина, успешно прошедшая лечение, должна находиться под наблюдением у врача.
Посещать маммолога придется раз в несколько месяцев. Со временем врач будет приглашать на осмотры все реже, спустя 5 лет — примерно раз в год (если в течение этого времени не возникало рецидивов). Спустя 6–12 месяцев после хирургического вмешательства врач назначит маммографию, затем ее нужно будет проходить ежегодно. По отдельным показаниям назначают регулярные осмотры гинеколога, определение плотности костей и другие исследования.
Средняя продолжительность жизни после операции по удалению рака молочной железы оценивается по показателю пятилетней выживаемости. Он обозначает процент пациентов, которые остаются живы в течение пяти лет с того момента, когда был установлен диагноз. Пятилетняя выживаемость при раке молочной железы в первую очередь зависит от стадии, на которой начато лечение:
- I стадия — практически 100%.
- II стадия — 93%.
- III стадия — 72%.
- IV стадия — 22%.
Помимо стадии, играют роль и такие факторы, как возраст, общее состояние здоровья женщины, тип опухоли, образ жизни. Специальных рекомендаций, которые помогли бы существенно улучшить прогноз выживаемости после операции по поводу рака молочной железы, не существует. Нужно в целом вести здоровый образ жизни: правильно питаться, поддерживать физическую активность, следить за массой тела, избегать курения и алкоголя.
После лечения организм восстанавливается, поэтому он должен получать достаточное количество белка. В ближайшее время после операции не стоит переживать о лишних калориях, даже если у вас есть избыточная масса тела. Сейчас важно восстановиться. Сбросить вес можно потом.
Некоторые вещества, которые содержатся в растительных продуктах, помогают укрепить здоровье и снизить риск рецидива:
- Фитоэстрогены, которые содержатся в сое, согласно результатам некоторых исследований, помогают снизить риск рецидива эстроген-позитивного рака. В ходе других исследований не было обнаружено такого эффекта.
- Антиоксиданты содержатся во многих фруктах и овощах, особенно много их в брокколи, чернике, моркови, манго. Они помогают защитить клетки от повреждения.
- Ликопин — один из антиоксидантов, который придает красный цвет томатам и розовый — грейпфруту.
- Бета—каротин придает оранжевый цвет моркови, абрикосам. Есть некоторые данные в пользу того, что он помогает предотвращать рак.
Стоит ли принимать биологически активные добавки? Диетологи считают, что рацион, богатый разнообразными свежими продуктами, намного лучше, чем БАДы.
источник
Молочная железа у женщин находится на уровне III-VI ребер между парастернальной и передней подмышечной линиями. Поверхностная фасция груди образует капсулу для молочной железы, фасция сращена с ключицей и способствует фиксации железы (подвешивающая связка молочной железы). От фасциальной капсулы вглубь железы отходят радиально расположенные перегородки, которые окружают отдельные дольки (от 15 до 20) и располагаются по ходу выводных протоков. Соединительно-тканная строма железы связана с поверхностной фасцией и кожей, и этим объясняется появление при раке молочной железы участков втяжения кожи над опухолью (симптом «площадки»).
Величина молочной железы и форма определяются ее функциональным состоянием, количеством жировой клетчатки и зависит: от возраста, типа телосложения, предшествующих родов и кормлений. Молочную железу принято делить на четыре квадранта: верхне-наружный, нижне-наружный, верхне-внутренний и нижне-внутренний. Разница строения квадрантов заключается в количестве железистых элементов: их больше всего в верхне-наружном квадранте, затем они убывают от верхне-внутреннего к нижне-наружному, меньше всего их в нижне-внутреннем квадранте. Это отражается на частоте развития опухолей в отдельных квадрантах.
Кровоснабжение молочной железы осуществляется из трех источников: из латеральной грудной артерии, из межреберных артерий и из внутренней грудной артерии. Глубокие вены железы сопровождают артерии, а поверхностные вены образуют подкожную сеть, связанную с подмышечной веной. Иннервируют молочную железу и покрывающую ее кожу ветви межреберных, надключичных и передних грудных нервов.
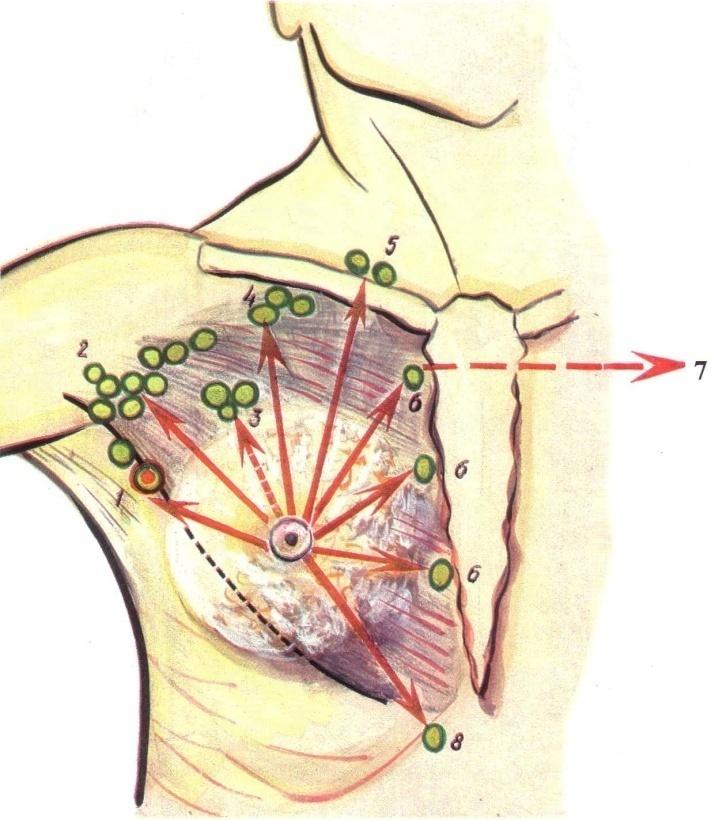
Рис. 62. Пути оттока лимфы от молочной железы (основные группы лимфатических узлов). 1 – лимфатический узел Зоргиуса; 2 – подмышечные лимфатические узлы; 3 – межгрудные лимфатические узлы; 4 – подключичные лимфатические узлы; 5 – надключичные лимфатические узлы; 6 – парастернальные лимфатические узлы; 7 – контрлатеральные лимфатические узлы подмышечной полости; 8 – надчревные лимфатические узлы;
Лимфатические сосуды молочной железы хорошо развиты и представлены поверхностными и глубокими. По лимфатическим сосудам чаще, чем по кровеносным сосудам, распространяются метастазы при раке молочной железы и инфекция при гнойном воспалительном процессе в ней. Поэтому важно иметь представление о строении лимфатических сосудов молочной железы, направлении лимфооттока, топографии регионарных лимфатических узлов, связях с соседними лимфатическими бассейнами. Отток лимфы от молочной железы происходит в различные группы лимфатических узлов (рис. 62). Самым главным и определяющим путем оттока лимфы является подмышечный путь, в этом направлении дренируется около 4/5 лимфы, оттекающей от молочной железы. В подмышечные лимфатические узлы, расположенные по ходу подмышечной вены, отводится лимфа преимущественно от латерального отдела молочной железы. От медиального отдела молочной железы лимфа оттекает по сосудам в парастернальные лимфатические узлы по ходу внутренней грудной артерии и вены. От верхнего отдела молочной железы отток лимфы происходит в подключичные и надключичные лимфатические узлы; от нижнего отдела железы — в лимфатические узлы предбрюшинной клетчатки.
Увеличение регионарных лимфатических узлов сравнительно рано появляется у большинства больных раком молочной железы. Оценка состояния лимфатических узлов, наряду с определением локализации опухоли, является обязательным диагностическим приемом, позволяющим получить представление об операбельности опухоли.
В области молочной железы имеются несколько слоев клетчатки: подкожная; между листками поверхностной фасции (внутри капсулы молочной железы); ретромаммарная (между задним листком капсулы железы и собственной фасцией).
Наиболее часто ткани молочной железы воспаляются при кормлении грудью — возникает абсцесс, причиной которого является повторное механическое раздражение, повышение давления в молочных ходах, а при повреждении кожи в области соска возникают «входные ворота» для инфекции. Вдоль соединительно-тканных перегородок и выводных протоков инфекция проникает вглубь и вызывает воспаление молочной железы (мастит). В зависимости от локализации выделяют следующие формы мастита: субареолярный, антемаммарный (подкожный), интрамаммарный (паренхиматозный и интерстициальный), ретромаммарная флегмона.
При гнойном мастите наиболее радикальным способом лечения является вскрытие гнойной полости, поскольку происходит быстрое распространение инфекции на соседние дольки с их разрушением. При субареолярном мастите проводится параареолярный разрез. При антемаммарном и интрамаммарном маститах разрезы производят в радиарном направлении, чтобы не повредить выводные протоки и не разрушить соединительно-тканные перегородки, отграничивающие интактные дольки. Разрез должен обеспечивать хороший отток гноя, поэтому длина разреза должна превышать вдвое глубину раны. Для лучшего оттока гнойного отделяемого делают дополнительный разрез (контрапертуру). Необходимо тщательно произвести ревизию раны. Если радиальные соединительно-тканные перегородки целы, то их обязательно сохраняют; если они расплавлены гноем, то нужно соединить между собой гнойные полости. Полость абсцесса дренируют резиновой или полихлорвиниловой трубкой.
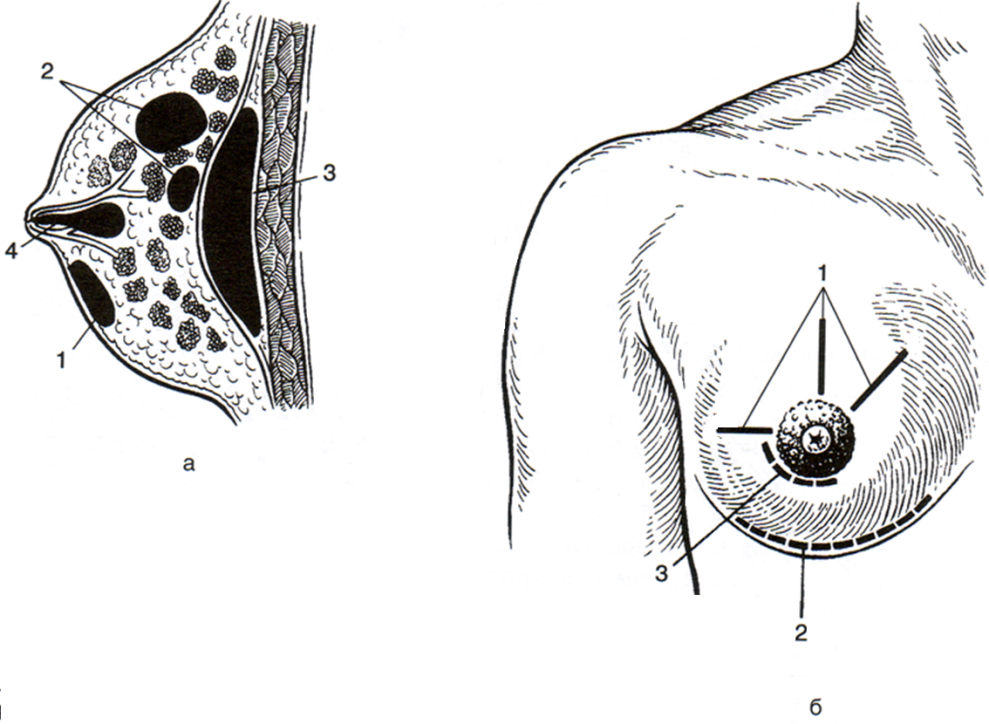
Существенным недостатком радиарных разрезов являются грубые послеоперационные рубцы на коже молочной железы, что приводит не только к неудовлетворительным косметическим результатам, но иногда и к функциональным нарушениям. В связи с этим заслуживает внимания субмаммарный дугообразный разрез Барденгейера (1903) по переходной складке под молочной железой. Из этого разреза отслаивают заднюю поверхность железы от грудной фасции, благодаря этому становится возможным вскрыть абсцесс с его задней поверхности. При этом рассечение ткани молочной железы производят также в радиарном направлении. Поскольку кожа передней поверхности молочной железы при этом не повреждается, а рубец после заживления раны практически незаметен, использование указанного доступа имеет определенные преимущества, особенно при глубоких интрамаммарных абсцессах и ретромаммарных флегмонах (рис. 63).
Операции при доброкачественных опухолях молочной железы заключаются в частичном ее удалении — секторальная резекция молочной железы. Разрез производится в виде удлиненного эллипса над пальпируемым уплотнением. Производят иссечение в виде клина одной или нескольких долек в пределах здоровых тканей.
Рак молочной железы является наиболее частым опухолевым заболеванием. При раке молочной железы прогноз зависит от двух факторов: гистологической картины опухоли и стадии заболевания (по системе TNM). Прогноз может быть улучшен только операцией, произведенной в начальной стадии заболевания. Маммография является важнейшим специальным методом ранней диагностики. Данные этой методики настолько серьезны, что при положительных результатах маммографического исследования рекомендуется производить операцию, даже если у пациентки отсутствуют жалобы и опухоль не пальпируется.
В настоящее время лечение рака молочной железы является комплексным, включающим оперативные, лучевые и химиотерапевтические методы. Однако хирургическое вмешательство — главный, а иногда и решающий этап лечения первичного очага и метастазов в регионарные лимфатические узлы. Техника современной операции при раке молочной железы основывается на трех основных принципах (Раков, 1960): радикальность, соблюдение правил абластики и проведение антибластических мероприятий. Соблюдение этих принципов обеспечивает успех оперативного вмешательства. Принцип соблюдения правил абластики – «анатомическая футлярность хирургического вмешательства» заключается в удалении единым блоком молочной железы вместе с опухолью, с большой и малой грудными мышцами в пределах грудино-ключичной фасции. Принцип соблюдения антибластических мероприятий направлен на уничтожение опухолевых клеток в ране (электрохирургическая методика оперирования; однократное использование кровоостанавливающих зажимов, салфеток, шариков; предоперационная лучевая терапия). Принцип радикализма – удаление опухоли и доступных лимфатических узлов.
Рис. 63. Виды гнойных маститов (а) и применяемые разрезы (б), а: 1 – субареолярный абсцесс; 2 – интрамаммарный абсцесс; 3 – ретромаммарная флегмона; 4 – галактофорит. б: 1 – радиарные разрезы; 2 – субмаммарный разрез по Барденгейеру; 3 – параареолярный разрез.
Радикальная мастэктомия по Холстеду-Майеру (1884), выполняемая при раке молочной железы, с поражением подмышечных лимфатических узлов состоит из четырех этапов: доступ, удаление опухоли молочной железы в пределах здоровых тканей, удаление регионарных лимфатических узлов, ушивание раны. Ее суть заключается в удалении единым блоком всей молочной железы с большой и малой грудными мышцами, а также жировой клетчаткой и лимфатическими узлами подмышечной полости в пределах анатомических футляров.
При обнаружении метастазов не только в подмышечных, но и в парастернальных лимфатических узлах производится расширенная радикальная мастэктомия (по Урбану-Холдину). При этой операции вначале выполняют радикальную мастэктомию по Холстеду без отсечения большой грудной мышцы. После этого резецируют участки ребер (II-V)на протяжении 3-4см от грудино-реберных сочленений. Производят мобилизацию клетчатки и удаление лимфатических узлов вдоль внутренней грудной артерии. Однако большинство авторов придерживается мнения, что при проникновении опухоли в средостение скальпель не сможет обеспечить радикальности.
Радикальная, а тем более расширенная, мастэктомия является технически сложной и весьма травматичной операцией. В послеоперационном периоде возможны нарушения функции верхней конечности (удаление большой грудной мышцы), лимфостаз, нарушение венозного оттока и др.
Использование комбинированных способов лечения (лучевая и химиотерапия) позволяет в ряде случаев применять при раке молочной железы более щадящие операции. Их применение возможно только на ранних стадиях заболевания, при отсутствии прорастания опухоли и метастазирования в регионарные лимфатические узлы. К числу таких щадящих операций относится мастэктомия с сохранением большой грудной мышцы (по Пейти). Преимущества этой операции: меньшая травматичность по сравнению с операцией Холстеда, сохранение большой грудной мышцы и движений верхней конечности в полном объеме. Недостатком является возможность транспекторального метастазирования, так как лимфатические сосуды и узлы в большой грудной мышце не удаляются.
источник
Рак молочной железы одна из наиболее распространенных опухолей у женщин.
Рост злокачественной опухоли молочной железы сопровождается диффузным прорастанием соседних тканей раковой опухолью с изъязвлением кожи или вовлечением в процесс глубжележащих слоев, собственной фасции, мышц, ребер. Инфильтративный рост опухоли приводит к проникновению раковых клеток в лимфатическое русло и попаданию их в лимфатические узлы, вначале – в регионарные, затем – в отдаленные. Поэтому важно знать топографию лимфатических сосудов молочной железы и направления лимфооттока.
Самым главным и определяющим путем оттока лимфы и распространения опухолевых клеток является подмышечный путь. Отток лимфы от молочной железы и распространение опухолевых клеток в лимфатические узлы подмышечной впадины происходит по трем направлениям:
1) через передние грудные лимфатические узлы (так называемые узлы Зоргиуса и Бартельса), расположенные по наружному краю большой грудной мышцы на уровне второго – третьего ребра, или соответственно на третьем и четвертом зубцах передней зубчатой мышцы.
2) интрапекторально – через лимфатические узлы Роттера, расположенные между большой и малой грудными мышцами,
3) транспекторально – по лимфатическим сосудам, пронизывающим толщу большой и малой грудных мышц через узлы, расположенные внутри мышц, между их волокнами
В подмышечные лимфатические узлы, количество которых колеблется от 10 до 75, отводится лимфа преимущественно от латерального отдела молочной железы.
От медиального отдела молочной железы лимфа оттекает по сосудам, которые через первое-пятое межреберья проникают в глубину и впадают в окологрудинные (парастернальные) лимфатические узлы, расположенные по ходу внутренней грудной артерии и вены.
От верхнего отдела молочной железы отток лимфы происходит в подключичные и надключичные лимфатические узлы Наконец, от нижнего отдела железы лимфа оттекает в лимфатические узлы и сосуды предбрюшинной клетчатки, а также в поддиафрагмальные узлы.
Увеличение регионарных лимфатических узлов сравнительно рано появляется у большинства больных раком молочной железы. Оценка состояния лимфатических узлов, наряду с определением величины и локализации опухоли, является обязательным диагностическим приемом, позволяющим получить представление об операбельности опухоли.
В настоящее время лечение рака молочной железы является комплексным, включающим оперативные, лучевые и химиотерапевтические методы. Однако хирургическое вмешательство – главный, а иногда и решающий этап лечения первичного очага и метастазов в региональные лимфатические узлы. Техника современных операций при раке молочной железы основывается на трех основных принципах:
Соблюдение правил абластики: удаление всего органа одним блоком без обнажения очага и пересечение лимфатических и кровеносных сосудов далеко за пределами органа.
Соблюдение антибластических мероприятий: уничтожение в ране опухолевых клеток (предоперационная лучевая терапия, использование при операции электроножа, лазерного скальпеля, однократное использование кровоостанавливающих зажимов и т.д.).
Соблюдение принципа радикализма, связанного с абластикой и антибластикой, что в первую очередь обусловлено удалением лимфатических коллекторов в пределах анатомической зоны и фасциальных футляров.
Различают следующие виды оперативных вмешательств при раке молочной железы:
1) радикальная мастэктомия: удаление единым блоком молочной железы большой и малой грудных мышц, подмышечной, подлопаточной и подключичной клетчатки вместе с лимфатическими узлами;
2) расширенная радикальная мастэктомия: дополнительно удаляются парастернальные лимфатические узлы, расположенные по ходу внутренней грудной артерии;
3) мастэктомия с сохранением большой грудной мышцы: предложена с целью профилактики развития постмастэктомического синдрома, в основе которого лежит нарушение оттока лимфы и венозной крови от верхней конечности по причине вовлечения в рубцовый процесс подмышечной вены;
4) резекция молочной железы (расширенная секторальная резекция, квадрантэктомия). Эта операция заключается в удалении сектора молочной железы в одном блоке с лимфатическими узлами подключично-подмыщечпой зоны. Она возможна при ограниченных узловых формах опухолей, локализующихся в верхне-наружном квадранте молочной железы. Операция заключается в иссечении из ткани молочной железы сектора, включающего опухолевый узел и неизмененную ткань железы на расстоянии 3-5 см от края опухоли в каждую сторону. При этом иссечение сектора (квадранта) выполняют с учетом расположения междольковых фасциальных перегородок, соблюдая принципы футлярности. Вместе с резецированным сектором выделяют подлопаточно-подключично-подмышечный блок клетчатки и лимфатических узлов, сохраняя большую и малую грудные мышцы. Выделенную клетчатку с подключичными и подмышечными лимфоузлами удаляют единым блоком с сектором молочной железы. При локализации опухоли в медиальных и центральных отделах железы выполнение таких операций не оправдано как вследствие технических сложностей, так и в связи с преимущественным метастазированием таких опухолей в парастернальные лимфатические узлы.
Пластические операции на молочной железе. Показаниями для выполнения пластических операций на молочной железе является микромастия, аллазия молочных желез, состояние после мастэктомии. Различают следующие способы пластики молочной железы:
аутопластику с использованием кожно-фасциально-мышечного лоскута на сосудистой ножке, сформированного в основном из широчайшей мышцы спины или свободная пластика (с наложением микрохирургических сосудистых анастомозов) кожно-фасциально-мышечными лоскутами взятыми в паховой или ягодичной областях.
протезирование с применением полимерных протезов, заполненных силиконовым гелем. Протезы помещают в ретромаммарное клетчаточное пространство.
Ранения груди. В мирное время повреждения грудной клетки являются причиной смертных случаев в 25 % транспортных катастроф.
Ранения органов груди возникают не только при прямом воздействии огнестрельного или холодного оружия: нередко органы повреждаются отломками ребер или грудины.
Все ранения груди делятся на две группы:
1) непроникающие – без повреждения внутригрудной фасции;
2) проникающие – с повреждением внутригрудной фасции и париетальной плевры в тех местах, где она прилежит к этой фасции.
Проникающие ранения груди, как правило, относятся к числу тяжелых, летальность при этом виде повреждений груди достигает 40 %.
Основные причины гибели раненых – это травматический (плевропульмональный) шок, кровотечение (кровопотеря) и инфекции. При этом смерть от шока и кровотечения наступает, как правило, в первые часы (иногда дни) после ранения. Инфекция проявляет себя в более поздние сроки, осложняя течение раневого процесса.
Пневмоторакс. При проникающих ранениях груди (как правило) и при закрытых травмах груди (в случае повреждения ткани легкого или бронхиального дерева) развивается пневмоторакс.
Под пневмотораксом понимают скопление воздуха в плевральной полости. Попадание воздуха в плевральную полость может происходить двумя путями:
1) через отверстие в грудной стенке при проникающем ранении, сопровождающемся повреждением париетальной плевры (наружный пневмоторакс);
2) через поврежденный бронх или легочную ткань (внутренний пневмоторакс).
Поступление воздуха в плевральную полость при ее «разгерметизации» обусловлено отрицательным давлением в ней. Пневмоторакс обычно сопровождается развитием плевропульмонального шока, гемотораксом и ателектазом легкого.
Различают три вида пневмоторакса: закрытый, открытый, клапанный.
Закрытый пневмоторакс характеризуется однократным попаданием воздуха в плевральную полость в момент ранения. Это приводит к ателектазу легкого на поврежденной стороне. В результате спадения стенок раневого канала, имеющего небольшие размеры, отверстие в париетальной плевре закрывается, что приводит к разобщению полости плевры с атмосферой. Закрытый пневмоторакс может также возникнуть при закрытых незначительных повреждениях легочной ткани.
При отсутствии кровотечения (гемоторакса) раненые с закрытым пневмотораксом, как правило, не требуют хирургического вмешательства: воздух через 7-12 дней рассасывается, легкое расправляется.
При наличии большого объема воздуха в полости плевры, особенно при пневмогемотораксе, показано удаление крови и воздуха путем плевральной пункции.
Более опасными являются пневмоторакс открытый и клапанный.
При открытом пневмотораксе наблюдается циркуляция воздуха в пневральной полости.
Открытый пневмоторакс возникает чаще при зияющей ране грудной стенки. При этом образуется свободное сообщение между плевральной полостью и атмосферным воздухом. Значительно реже открытый внутренний пневмоторакс развивается при повреждении главного бронха или трахеи. При открытом пневмотораксе, как правило, развивается плевропульмональный шок.
Первая помощь при открытом пневмотораксе, обусловленном повреждением грудной стенки, заключается в наложении на рану асептической, окклюзионной повязки из индивидуального пакета, липкого пластыря, марлевой повязки, смоченной водой или пропитанной маслом. Наконец, можно просто закрыть рукой рану.
Хирургическое лечение открытого пневмоторакса заключается в срочном оперативном закрытии раны грудной стенки и дренировании плевральной полости, целью которых является полное расправление легкого. Операция начинается с первичной хирургической обработки раны грудной стенки, которую выполняют экономно, иссекая лишь явно нежизнеспособные ткани. При отсутствии признаков продолжающегося внутреннего кровотечения торакотомию не производят и приступают к хирургическому закрытию дефекта грудной стенки.
Способы хирургического закрытия дефекта грудной стенки и герметизации плевральной полости можно разделить на две группы:
ушивание раны плевро-мышечными швами;
пластическое закрытие раны с использованием мышечных лоскутов (из большой грудной мышцы, диафрагмы) или синтетических материалов.
Клапанный пневмоторакс может быть наружным (при повреждении грудной стенки) и внутренним (при разрыве легкого или бронха). При этом виде пневмоторакса формируется свободный клапан, который пропускает воздух только в плевральную полость, в результате чего быстро наступает ателектаз легкого и происходит смещение органов средостения.
Врачебная помощь при клапанном пневмотораксе состоит в пункции плевральной полости толстой иглой во II-IV межреберном промежутке по среднеключичной линии. Таким образом клапанный пневмоторакс переводят в открытый, тем самым резко снижается внутриплевральное давление. Хирургическая помощь при этом виде пневмоторакса зависит от конкретной ситуации и может заключатся:
в дренировании плевральной полости и активной аспирации при помощи водоструйного насоса;
в выполнении торакотомии (вскрытии грудной полости) и ушивании раны легкого или бронха.
Наиболее распространенной хирургической манипуляцией, которая применяется для лечения эксудативных плевритов гемо- и пневмоторакса является пункция полости плевры. При выполнении этой процедуры необходимо соблюдать следующие правила:
пункцию проводят в VI-VII межреберье по задней подмышечной и лопаточной линии, по верхнему краю ребра (при пневмотораксе пункцию проводят во II-IV межреберье по среднеключичной линии);
выпот удаляют медленно, порционно (по 10-15-20 мл) и не более 1 л за один прием.
При неосторожных движениях иглой и неправильном выборе точки вкола иглы могут быть такие осложнения:
ранение межреберных сосудов и нервов;
повреждение легкого, диафрагмы, печени, селезенки и др. органов.
При быстрой эвакуации содержимого полости плевры может развиться коллаптоидное состояние.
Для лечения хронических эмлием плевры, кавернозного туберкулеза иногда применяют операцию – торакопластику.
Принцип операции заключается в иссечении части ребер и создании податливого участка грудной стенки для приведения в соприкосновение пристеночной и висцеральной плевры с целью ликвидации остаточных полостей и сдавлении легкого.
Различают следующие виды торакопластики: интраплевральную (со вскрытием полости плевры) и экстраплевральную; полную (резекция всех ребер) и частичную.
При травмах, ранениях, туберкулезных кавернах, кистах и злокачественных опухолях легких выполняют различные по объему оперативные вмешательства, направленные на удаление патологического очага:
пульмонэктомия – удаление всего легкого;
лобэктомия – удаление доли легкого;
сегментэктомия – удаление сегмента легкого;
клиновидная резекция легкого – выполняется при огнестрельных, ножевых ранениях легкого
Повреждения перикарда и сердца при проникающих ранениях груди – явление довольно частое (14 %). Клиническая картина и особенности хирургической тактики связаны с локализацией, размером и глубиной раны сердца. Повреждения сердца подразделяют на две группы:
1) непроникающие – без повреждения эндокарда,
2) проникающие – с повреждением эпикарда.
В свою очередь, среди непроникающих ранений выделяют.
а) изолированные ранения миокарда,
б) ранения коронарных сосудов,
в) сочетанные ранения миокарда и коронарных сосудов.
Проникающие ранения сердца также подразделяются на две подгруппы
а) изолированные повреждения стенок желудочков и предсердий,
б) повреждения, сочетанные с ранением глубоких структур (клапанов сердца, перегородок)
При осмотре раненого следует иметь в виду, что возможность ранения сердца тем больше, чем ближе входное отверстие к его проекции па переднюю стенку груди. Кровотечение при ранениях сердца часто бывает внутриплевральным. Из наружной раны кровь обычно вытекает непрерывной или пульсирующей тонкой струйкой, при гемопневмотораксе рана грудной стенки покрывается кровавой пеной. Нередко наблюдается также кровотечение в полость перикарда, что может привести к тампонаде сердца. При скоплении крови в полости перикарда сдавливаются правое предсердие и тонкостенные полые вены. Затем происходит нарушение функции желудочков сердца вследствие механического их сдавления. Острая тампонада сердца проявляется триадой Бека (падение артериального давления, резкое повышение центрального венозного давления и ослабление сердечных тонов).
Одним из способов диагностики кровоизлияния в полость перикарда и оказания экстренной помощи при угрожающей тампонаде является пункция.
Пункция выполняется толстой иглой.
При способе Марфана прокол делают под мечевидным отростком строго по средней линии, продвигая иглу снизу вверх на глубину 4 см, а затем отклоняют ее конец кзади.
По Ларрею иглу вкалывают в угол между прикреплением левого седьмого реберного хряща и основанием мечевидного отростка на глубину 1,5-2 см, а затем отклоняют ее кверху параллельно грудной стенке.
Успех лечения при ранении сердца определяют три фактора: срок доставки пострадавшего в лечебное учреждение, быстрота оперативного вмешательства и эффективность интенсивной терапии. Справедливо утверждение, что если пострадавший с ранением сердца доживает до поступления в операционную, то его жизнь должна быть спасена.
Хирургический доступ при ранении сердца должен быть простым, малотравматичным и обеспечивать возможность ревизии всех органов грудной полости. Для обнажения сердца вполне допустимо расширение раны грудной стенки, что обеспечивает быстрейший подход к месту повреждения сердца (принцип «прогрессивного расширения раневого канала»).
Широко используется боковая торакотомия по четвертому или пятому межреберью: от левого края грудины до задней подмышечной линии без пересечения реберных хрящей. После вскрытия грудной полости широко рассекается перикард продольным разрезом впереди от диафрагмального нерва.
При ревизии сердца необходимо наряду с передней осмотреть и его заднюю поверхность, поскольку ранения могут быть сквозными. Осмотр надо производить, подводя ладонь левой руки под верхушку сердца и слегка «вывихивая» его в рану. Первый палец хирурга при этом прикрывает рану передней стенки для временного прекращения кровотечения. Осматривая сердце, необходимо помнить, что оно плохо переносит изменения положения, особенно повороты по оси, которые могут вызвать остановку сердца вследствие перегиба сосудов.
Для ушивания раны сердца пользуются круглыми (лучше атравматическими) иглами. В качестве шовного материала используют синтетические нити. Шов стенок желудочков сердца должен захватывать всю толщу миокарда, но нити не должны проникать в полость сердца, во избежание образования тромбов. При небольших ранах сердца накладывают узловые швы, при ранах значительных размеров пользуются матрацными швами. Ушивая рану желудочка, вкол иглы делают так, чтобы вторым движением иглы захватить сразу же другой край раны. Швы затягивают осторожно, чтобы не вызвать прорезывания тканей.
Фаза работы сердца при наложении швов практического значения не имеет.
При ушивании раны сердца необходимо соблюдать исключительную осторожность в отношении собственных сосудов сердца. Перевязка венечных артерий недопустима. При повреждении венечных артерий для восстановления кровотока следует попытаться наложить сосудистый шов.
Перикард ушивают редкими одиночными швами.
Одной из распространенных операций, которая в настоящее время применяется для лечения ишемической болезни сердца является аорто-коронарное шунтирование. Принцип операции заключается в создании обходного кровотока посредством соединения аорты и коронарных сосудов с помощью аутовенозного трансплантата или сосудистого протеза. Ряд хирургов для улучшения коронарного кровотока используют маммарно-венечный анастомоз (анастомоз между сосудами миокарда и внутренней грудной артерией) или имплантацию внутренней грудной артерии в миокард. В последнее время для ликвидации стенозов коронарных артерий применяется баллонная ангиопластика и имплантация сосудистых стентов.
При рубцовых (ожоговых) и опухолевых стенозах пищевода (после его резекции) выполняют пластику этого органа.
Различают следующие виды пластики пищевода:
тонкокишечная – за счет формирования трансплантата на сосудистой ножке из тощей кишки;
толстокишечная – в качестве трансплантата может использоваться поперечная, восходящая и нисходящая ободочная кишка.
желудочная – пластику дистальных отделов пищевода можно проводить с использованием трансплантата, сформированного из большой кривизны желудка.
В зависимости от расположения трансплантата выделяют:
подкожную (предгрудинную) пластику пищевода;
загрудинную – трансплантат располагается в переднем средостении.
Расположение трансплантата в ортотопическую позицию, т.е. в заднем средостении используют крайне редко из-за больших технических трудностей. В последнее время, в связи с развитием микрохирургической техники, разработана свободная пластика пищевода, когда кровоснабжение тонко- или толстокишечного трансплантата пищевода происходит за счет формирования микрососудистых анастомозов между сосудами кишки и межреберными артериями или ветвями внутренней грудной артерии.
источник