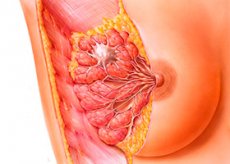
В современном мире рак молочной железы – это наиболее часто встречающееся онкологическое заболевание среди женщин. Риск заболеть раком молочной железы резко повышается после 50 лет. Всемирная Организация Здравоохранения (ВОЗ) сообщает неутешительную статистику: в мире ежегодно регистрируется почти 1 млн. новых случаев рака молочной железы. Также стоит отметить, что рак грудной железы может встречаться и среди мужчин, но составляет менее 1 % от общего числа больных.
- Генетические факторы. Существуют доказательства наследственной предрасположенности к развитию опухолей молочной железы. Женщины, у которых в семье по материнской линии были больные раком молочной железы, имеют больший риск заболеть.
Влияние гормонов. Молочная железа состоит из гормонозависимых тканей. Экспериментально развитие рака молочной железы было вызвано у животных, путем введения им эстрогенов (женских половых гормонов). Также возникновение злокачественных опухолей молочных желез у подопытных животных достигалось в результате нарушения функции яичников при облучении и односторонней кастрации.
Ионизирующая радиация. Риск возникновения рака молочной железы повышен у женщин, часто подвергавшихся рентгенологическим исследованиям (например, многократное проведение рентген-исследований при туберкулезе).
- Женский пол;
- Раннее начало менструаций (до 12 лет);
- Позднее наступление менопаузы (после 55 лет);
- Поздние первые роды (после 30 лет) и нерожавшие женщины;
- Возраст старше 50 лет;
- Атипическая гиперплазия ткани молочной железы;
- Наличие семейного рака молочной железы (особенно рака у родственников первой линии);
- Мутации генов BRCA-1, BRCA-2;
- Ожирение;
- Наличие рака половых органов, в том числе вылеченного (рак яичников, рак шейки матки, рак тела матки);
Рак молочной железы имеет свою гистологическую классификацию. Это — классификация по типу опухолевой ткани.
Гистологические типы опухолей молочной железы делятся на:
1. Неинфильтрирующие:
- Внутрипротоковый рак in situ
- Дольковый рак in situ
2. Инфильтрирующие:
- Инфильтрирующий протоковый рак
- Инфильтрирующий протоковый рак с преобладанием внутрипротокового компонента
- Инфильтрирующий дольковый рак
- Слизистый (медуллярный) рак
- Папиллярный рак
- Тубулярный рак
- Аденокистозный рак
- Секреторный рак
- Апокринный рак
- Рак с метаплазией:
— плоскоклеточного типа;
— веретеноклеточного типа;
— хондроидного и остеоидного типа;
— смешанного типа.
3. Болезнь Педжета (рак соска);
4. Саркома;
5. Лимфома (первичная);
6. Метастазыопухолей других органов.
Более подробно про гистологические виды опухолей молочных желез вы можете прочитать в соответствующем разделе.
Рак молочной железы 0 стадия (рак in situ):
0 стадия рака молочной железы подразумевает размеры опухолевого узла до 1 см и отсутствие метастазов в региональных лимфатических узлах и отдаленных органах. Прогноз при стадии рака молочной железы очень благоприятный. Лечение проводится, в основном, хирургическое. На данной стадии рака молочной железы возможно полное излечение пациентки.
Рак молочной железы 1 стадии:
Рак молочной железы 1 стадии означает, что опухолевый узел имеет размеры менее 2 см с отсутствием метастазов в ближайших лимфатических узлах. На 1 стадии рак молочной железы протекает бессимптомно, поэтому его трудно обнаружить самостоятельно. Именно поэтому женщинам следует ежегодно проходить маммографию или УЗИ молочных желез с последующей консультацией маммолога. Рак молочной железы 1 стадии хорошо поддается лечению и также имеет благоприятный прогноз.
Рак молочной железы 2 стадии:
Рак молочной железы на 2 стадии считается самым распространенным. При раке молочной железы 2 стадии размер опухоли варьируется от 2 до 5 см. Также, выявляются метастазы в подмышечных и надключичных лимфатических узлах. При раке молочной железы 2 стадии у пациентки появляются такие симптомы и признаки как: наличие пальпируемого образования в молочной железе, асимметрия молочных желез, дискомфорт в молочной железе.
Лечение рака молочной железы 2 стадии состоит из комбинации нескольких видов противоопухолевой терапии. Обычно, первым этапом лечения является операция. После неё, при наличии показаний назначается послеоперационная (адъювантная) химиотерапия, лучевая терапия и гормональная терапия. В некоторых случаях перед операцией проводят предоперационную химиотерапию для того, чтобы максимально уменьшить размер опухолевого узла.
Продолжительность жизни при раке молочной железы 2 стадии зависит от множества факторов и правильности проведенного лечения. Пятилетняя выживаемость пациенток с раком молочной железы 2 стадии составляет 88%. В целом, при раке молочной железы на 2 стадии прогноз благоприятный.
Рак молочной железы 3 стадии:
3 стадия рака молочной железы устанавливается, если размер опухолевого узла больше 5 см. При таких размерах опухоль уже распространяется на кожу молочной железы, подрастает к грудным мышцам. Также наблюдается поражение ближайших лимфатических узлов.
Лечение рака молочной железы 3 стадии комбинированное, и включает в себя различные виды лечения. Сюда входят такие методы, как химиотерапия, лучевая терапия, оперативное вмешательство. При раке груди 3 стадии, чаще всего, лечение начинают с предоперационной (неоадъювантной) химиотерапии, которая позволяет уменьшить опухолевый узел и убрать метастазы в лимфатических узлах, что дает возможность выполнить хирургическое удаление молочной железы.
При правильно проведенном лечении, прогноз при раке груди 3 стадии оптимистичный. Рак молочной железы 3 стадии не излечим, но благодаря правильно проведенному лечению, ремиссия заболевания может длиться годами.
Рак молочной железы 4 стадии:
Рак груди 4 стадии считается самой запущенной ситуацией. При раке молочной железы 4 стадии наблюдаются большие размеры опухолевого узла с врастанием в окружающие ткани, поражены лимфатические узлы, и есть отдаленные метастазы в различные органы. При 4 стадии рака молочной железы, чаще всего, метастазы поражают легкие, печень, головной мозг и кости.
Инфильтративно-отечная форма рака молочной железы автоматически считается 4-й стадией рака из-за своих морфологических особенностей. Прогноз при раке молочной железы 4 стадии, к сожалению, неблагоприятный. Средняя пятилетняя выживаемость составляет 41%.
При раке молочной железы 4 стадии редко применяют хирургическое лечение из-за наличия метастазов в отдаленные органы. Основным методом лечения метастатического рака груди являются химиотерапия, таргетная терапия и гормональная терапия. Операции при раке груди 4 стадии выполняют только в целях санации, если наблюдается распад опухоли. Но наука не стоит на месте, и современные схемы лечения метастатического рака молочной железы, которые применяются, в том числе в нашей стране, позволяют значительно продлевать жизнь пациенткам, сохраняя при этом, хорошее качество жизни.
Существуют узловая и диффузная формы рака молочной железы.
Узловая форма рака молочной железы. Представлена локальным ростом в виде узла. При пальпации (прощупывании) обнаруживается округлое, плотное, бугристое образование с нечеткими контурами, нередко с ограниченной подвижностью, при этом пальпация данного образования чаще безболезненна. Если данная опухоль располагается под соском, то можно наблюдать его отклонение в сторону, фиксацию (симптом площадки), складки ареолы (симптом Краузе) или втяжение (симптом умбиликации). При прогрессировании заболевания может присоединяться симптом «лимонной корки» — лимфатический отек кожи, прилегающей к новообразованию. Увеличение или уплотнение подмышечных лимфатических узлов также должно вызвать настороженность.
К диффузным формам рака молочной железы относятся: отечная форма, панцирный рак, маститоподобный рак, рожистоподобный рак, болезнь Педжета, скрытая форма рака.
- Инфильтративно-отечная форма рака молочной железы имеет быстрое течение, так в начале заболевания наблюдается увеличение объема и отечность молочной железы, покраснение (гиперемия) кожи и наличие «лимонной корки», местное повышение температуры.
- Панцирный рак молочной железы – это своеобразная диффузно-инфильтрирующая форма. Злокачественный процесс распространяется по лимфатическим сосудам молочной железы на стенку грудной полости, в подмышечную впадину, руку, что сопровождается местной инфильтрацией, которая как панцирь, сковывает движения и дыхание больной.
Маститоподобная форма рака молочной железы. Данная форма характеризуется отсутствием четких контуров. Кожа, прилегающая к новообразованию, покрыта розовыми пятнами (раковый лимфангит) или гиперемирована. В толще тканей прощупывается инфильтрат без признаков размягчения. Подвижность железы снижена. Данная патология может сопровождаться повышением температуры тела.
Рожистоподобный рак молочной железы. Эта форма характеризуется выраженным покраснением кожи с неровными языкообразными краями, которое внешне напоминает рожистое воспаление. Гиперемия может распространяться за пределы молочной железы на грудную стенку. Чаще рожистоподобный рак имеет острое течение с высокой (до 40°С) температурой тела. Данная форма рака молочной железы имеет агрессивное течение, быстро метастазирует в лимфатические узлы и другие органы.
Рак Педжета. Процесс начинается с уплотнения и покраснения соска и ареолы. Внешне мокнущая поверхность, появляющаяся после слущивания сухих корочек, напоминает экзему. Одновременно опухоль распространяется и в глубину железы, поражает подмышечные лимфоузлы.
- Скрытый рак молочной железы. Часто данную форму путают с подмышечным лимфаденитом, так как в самой железе опухоль не определяется, а лимфоузлы уже поражены метастазами и увеличены.
- Самообследование молочных желез необходимо проводить в хорошо освещенном помещении с опущенными, а затем поднятыми руками. Обращать внимание нужно на наличие асимметрии, деформации контура, отёк или гиперемию кожи молочной железы, расширение подкожной венозной сети, деформацию ареолы, изменение положения соска. Оптимальное время для самообследования или визита к маммологу — это с 7-го по 14-й дни цикла.
- Ультразвуковое исследование. Чувствительность данного метода в диагностике заболеваний молочной железы составляет 98,4%, а специфичность — 59%. Его преимущества: возможность использования у молодых женщин, отсутствие вредного влияния на организм. Однако УЗИ не может служить методом скрининга рака, поскольку не выявляет микрокальцинаты (отложения солей кальция) и перестройку структуры ткани железы, характерных для рака in situ (рак на месте). При наличии патологических образований оценивают края и форму, акустический эффект позади образования, внутреннюю эхоструктуру, эхогенность, эффект компрессии, отношение высоты образования к ширине. Необходимо также обследовать регионарные лимфатические узлы.
- Маммография. Рентгенологическое исследование на специально разработанных аппаратах — основной метод ранней диагностики рака молочной железы. Для повышения качества изображения и снижения лучевой нагрузки используют усиливающие экраны, компрессию железы. Стандартно выполняют снимки каждой железы в двух проекциях — вертикальной и косой (45°).
В интерпретации маммограммы учитывают:
— асимметрию плотности и васкуляризации (кровоснабжения) симметричных участков желёз;
— нарушения строения железы;
— наличие опухолевидных образований: локализация, размер, плотность, форма, контуры; — наличие микрокальцинатов;
— структуру и степень развития железистой ткани с учётом возраста и гормонального статуса;
— состояние кожи, соска;
— наличие патологически изменённых лимфатических узлов.
Рентгеноконтрастное исследование протоков молочной железы (дуктография) чрезвычайно важно в дифференциальной диагностике внутрипротоковых папиллом и рака молочной железы, а также позволяет уточнить локализацию поражённого участка.
- Компьютерная томография и магнитно-резонансная томография — вспомогательные методы в диагностике опухолей молочной железы, но они чрезвычайно важны в диагностике распространённых процессов, когда необходимо найти первичную опухоль при скрытом раке, оценить состояние внутригрудных лимфатических узлов или исключить распространение метастазов в легкие, печень, скелет.
- Тонкоигольная аспирационная биопсия — наиболее простой способ получения материала для цитологического исследования в амбулаторных условиях, не требует анестезии.
- Трепан-биопсия. Использование специальной иглы позволяет получить необходимое количество ткани для гистологического изучения характера патологического процесса, включая дифференциальную диагностику инвазивного рака и поражений in situ, степень дифференцировки опухоли, наличие в ней рецепторов эстрогенов, прогестеронов. Этот метод также применяют амбулаторно, однако он уже требует местной анестезии. При непальпируемых опухолях, микрокальцинатах введение иглы проводят под контролем УЗИ или маммографии (стереотаксическая биопсия).
Пример: трепан-биопсия молочной железы
- Биопсия. Хирургическую или эксцизионную биопсию следует выполнять при подозрении на рак молочной железы, если при тонкоигольной аспирапионной биопсии и трепан-биопсии не удалось подтвердить (исключить) злокачественное новообразование. В таких случаях чаше требуется госпитализация больной, как правило, общая анестезия, срочное гистологическое исследование удалённого препарата и при необходимости расширение объёма операции вплоть до мастэктомии (удаления молочной железы). Возможное расширение объёма операции при раке требуется обсудить с больной и получить её письменное согласие до выполнения биопсии.
- Цитологическое исследование пунктата позволяет верифицировать рак молочной железы путём выявления злокачественных элементов рака или диагностировать доброкачественные изменения, определяя степень пролиферации и дисплазии эпителиальных клеток железы. Цитологическое исследование выделений из соска обязательно при наличии кровянистых или обильных серозных выделений из протока.
- Гистологическое и гистохимическое исследование. Кроме ответа на вопрос о наличии злокачественной опухоли и её характеристиках, при неопухолевых заболеваниях гистологическое исследование даёт подробную характеристику о состоянии ткани молочной железы и риске развития рака.
- Определение опухолевых маркеров. Онкомаркеры — специфические вещества, которые обнаруживаются в крови больных раком. При раке молочной железы определяют маркеры: РЭА, СА 15-3, СА-27, СА-29.
1. Первичная профилактика рака молочной железы во многом связана с экологическими и социальными аспектами. Это — нормализация семейной жизни, детородной функции, грудное вскармливание.
2. Вторичная профилактика заключается в выявлении и лечении нарушений эндокринной системы, патологии женских половых органов, нарушений функции печени, где в норме инактивируются эстрогены. Для женщин с высоким риском рака молочной железы (наличие кровных родственников с данным заболеванием, выявление мутаций BRCA1, BRCA2) к числу профилактических мероприятий относят: назначение антиэстрогенов, овариэктомия и даже профилактическая двусторонняя мастэктомия с протезированием молочных желёз.
3. Скрининг рака молочной железы. Под скринингом подразумевают регулярное профилактическое обследование лиц с повышенным риском рака молочной железы. Отсутствие факторов риска не может исключить возможность развития злокачественного новообразования. Цель скрининга — выявление опухоли на ранних стадиях.
Единственный метод ранней диагностики — маммография. При неблагоприятном семейном анамнезе в отношении рака молочной железы маммографию рекомендуют проводить ежегодно с возраста 35 лет. Всем остальным женщинам маммографию проводят ежегодно с 50 лет. Это относится к женщинам, не имеющим патологических изменений на маммограммах (поданным предыдущих обследований).
4. Профилактические осмотры маммолога. На начальном этапе программа скрининга рака молочной железы профилактический клинический осмотр имеет большее значение, чем внедрение маммографии, поскольку может использоваться независимо от места проживания пациентки, не требует финансовых затрат, позволяет выявлять патологические изменения размером от 1 см и своевременно направлять женщин для углублённого обследования в специализированные центры. Клинический осмотр должен проводить каждый врач при первичном осмотре пациентки. Врач должен обратить внимание пациентки на методику обследования, порекомендовать провести самообследование дома в этот же день, чтобы запомнить нормальное строение молочных желёз.
5. Самообследование молочной железы. Это — простой, не требующий затрат и специального оборудования метод диагностики патологических состояний молочной железы. Более 80% случаев опухоли в молочной железе женщины обнаруживают самостоятельно. Лучший способ освоения методики самообследования — обучение женщин медицинским работником во время клинического осмотра (женщина может проводить самообследование по любой методике, главное, чтобы она делала его регулярно и каждый раз одним и тем же способом).
Про симптомы и признаки, а также про методы лечения рака молочной железы читайте в отдельных страницах данного подраздела.
источник
Под отёчно-инфильтративной формой рака молочной железы (РМЖ) понимают варианты болезни, сопровождающиеся отёком и/или гиперемией кожи молочной железы. Для истинной или первичной отечно-инфильтративной формы (ОИФ) РМЖ характерно диффузное распространение опухоли по тканям молочной железы, отсутствие выявляемого первичного опухолевого узла и плохой прогноз. Сходный прогноз наблюдается и при вторичной ОИФ, то есть узловой форме РМЖ, сопровождающейся вторичным отёком кожи.
ОИФ РМЖ отличается от локализованного рака не только степенью распространённости опухоли; при этом варианте возрастает частота опухолей с неблагоприятным прогнозом и снижается частота относительно благоприятных прогностических факторов. Так, частота редких морфологических форм рака с относительно доброкачественным течением (слизистый, папиллярный, тубулярный и медуллярный) при раннем РМЖ (T1-2N0M0) составляет 11,4%, а при местно-распространенном, включая и ОИФ, – 2,6% (2p=0,0001). Доля анеуплоидных многоклоновых (по индексу плоидности ДНК) опухолей при узловой форме РМЖ составляет 6%, а при ОИФ – 20% (2p=0,0013); частота поражения лимфатических узлов – 39% и 87% (2p=0,0000); частота рецепторонегативных опухолей по рецепторам эстрогенов – 43% и 55% (2p=0,0058), по рецепторам прогестерона – 49% и 65% (2p=0,0006) соответственно (1).
Судьба больных, не получавших по разным причинам системную адъювантную терапию, описывается кривыми, представленными на рис. 1 и 2 (данные РОНЦ им. Н.Н. Блохина РАМН). При наличии отёка кожи 5-летняя безрецидивная выживаемость (БРВ) равна 23%, общая выживаемость (ОВ) — 30%, 10-летние БРВ и ОВ равны 0%. Драматические и чрезвычайно выразительные результаты свидетельствуют о том, что с появлением отёка и/или гиперемии кожи молочной железы РМЖ становится системной болезнью на 100% и его лечение невозможно без системной терапии
Лечение ОИФ РМЖ складывается из предоперационного (индукционного) лечения, местного лечения (операция или ЛТ, или сочетание ЛТ с операцией) и адъювантной терапии.
Предоперационная (индукционная) химиотерапия
Трудно переоценить значение эффективности предоперационной химиотерапии (ХТ): прогрессирование на фоне ХТ означает начало конца, эффективная ХТ даёт шансы на радикальное излечение.
Схемы CMF, VCMFP. Истинная ОИФ РМЖ не является исходно резистентной к лечению. Так, например, проведение ХТ по схеме VCMFP в сочетании с эндокринной терапией (ЭТ) позволило в 84% случаев добиться эффекта различной степени выраженности и выполнить больным радикальную операцию (2). Дальнейшее течение болезни, в большинстве случаев, оказывается обескураживающим. Несмотря на проведение профилактической ХТ по схеме CMF и профилактической ЭТ, уже на первом году наблюдений рецидивы и метастазы развиваются в 50% случаев, 3-летняя БРВ составляет 24%, 5-летняя – 19% (3). Таким образом, второй особенностью ОИФ РМЖ является быстро манифестирующаяся лекарственная устойчивость; ответом на это должно быть последовательное проведение нескольких линий системной терапии.
Схемы, включающие антрациклины (FAC, FEC, AC, EC), применяются наиболее часто, значительно реже антрациклины назначаются в виде монохимиотерапии. Поддержка кроветворения гранулоцитарным (Г-КСФ) или гранулоцитарно-макрофагальным (ГМ-КСФ) колониестимулирующими факторами позволяет увеличить интенсивность дозы препаратов, что может привести к повышению эффективности ХТ.
U. Coskun и соавт. (4) описывают свой опыт проведения предоперационной ХТ у 91 больной местно-распространенным РМЖ (30 больная – IIIa стадия, 61 больная – IIIb стадия). ХТ по схеме FAC или AC была эффективна в 91%, по схеме FEC или EC – в 82%, по схеме CMF – в 60 % случаев (p 0.05). Полученные данные могут свидетельствовать о перспективности дальнейшего изучения эффективности высокодозной ХТ в качестве адъювантного лечения местно-распространенного РМЖ (14).
Лучевая терапия. Относительно сроков проведения лучевой терапии в лечении местно-распространенного РМЖ существуют различные мнения. Согласно новой концепции, лучевую терапию проводят после операции и завершения адъювантной ХТ (39,40,36;). Schwartzberg L. и соавт., (9), L.E. Morrell и соавт. (20), M. Colozza и соавт. (19) проводят лучевую терапию после операции перед адъювантной ХТ; а V.F. Semiglazov и O.M. Golubeva (32), J. Yau и соавт. (41) – перед операцией. Наконец, некоторые авторы предпочитают проводить лучевую терапию одновременно с предоперационной ХТ (30,12,42).
По нашим данным лучевая терапия в прогностически неблагоприятных случаях (первичная ОИФ, вторичная ОИФ с отёком кожи, занимающим более 50% поверхности молочной железы) должна проводиться в полной дозе. Так, частота местных и регионарных рецидивов после лучевой терапии в дозе 40 Гр составила 43% (3/7), после лучевой терапии в дозе 60-70 Гр — 5% (2/39), р
источник
Отечный рак молочной железы,
особенности клинического течения, проблемы диагностики и лечения
Чхиквадзе Т.В., ФГУ «РНЦРР Росмедтехнологий»,
Онкологический клинический диспансер №1
Департамента здравоохранения г. Москвы.
Обзор посвящен проблемам диагностики и лечения отечной формы рака молочной железы, которая отличается высокой злокачественностью, ранним и быстрым лимфогенным и гематогенным метастазированием, неудовлетворительными отдаленными результатами. Приведены современные данные результатов исследований по выяснению биологических особенностей этой формы опухоли, клинического проявления и эффективности различных методов лечения.
Отёчный рак молочной железы (ОРМЖ), относится к диффузным формам опухоли и встречается у 1-5% больных раком молочной железы (РМЖ) (221, 110, 79, 112, 225, 255, 153). По данным различных авторов ОРМЖ является одной из наиболее злокачественных форм опухоли, имеет неблагоприятный прогноз — общая 5-летняя выживаемость в среднем не превышает 12-50% (254, 155, 172, 130, 110, 127, 220).
Различают первичную отёчную форму (синонимы – истинно отёчный, маститоподобный, инфламаторный или воспалительный рак, раковый мастит, панцирный рожистоподобный рак, кожный лимфатический канцероматоз, инфильтративно-отёчный рак и т.д.) и вторичную отечную форму рака молочной железы. По международной классификации злокачественных опухолей TNM (6-е издание, 2002г) первичный ОРМЖ обозначается как T4d, и вторичный — как T4b. Термин «воспалительная форма РМЖ — inflammatory breast cancer (IBC)» чаще применяется в англоязычной литературе и относится к первичному отечному РМЖ. Вторичная форма ОРМЖ встречается чаще – у 25% пациенток, и в отличие от первичной формы, представляет собой местно распространенный узловой рак молочной железы, осложненный лимфогенным метастазированием, блоком оттока лимфы и присоединившимся отеком молочной железы (21, 117).
Первое описание ОРМЖ было сделано Charles Bell в Англии в 1807 году. Он указал на крайне неблагоприятный прогноз при появлении диффузных изменений молочной железы, багровой окраски кожи над опухолью и болезненности молочной железы, рекомендовал не откладывать надолго выполнение операции (91). Однако на протяжении многих последующих лет эта форма рака молочной железы не рассматривалась как отдельная форма опухоли и рассматривалась в группе больных с местно распространенным раком молочной железы. Тактика лечения по отношения ОРМЖ в различные периоды менялась в зависимости от развития и совершенствования тех или иных методов лечения – хирургического, лучевого или лекарственного.
В начале 20 века, в 1909 году, A. Leitch указал на необходимость наличия 2 главных диагностических признаков ОРМЖ: диффузной отёчности молочной железы в виде гипертрофии и «лимонной корки», сочетание которых он считал патогномоничным симптомом «острого рака» (167). Термин «острый рак» он ввел для обозначения быстро растущих и диссеминирующих опухолей молочной железы, которые имеют фульминантное течение, и могут приводить к быстрому фатальному исходу, особенно у молодых пациенток. Он указывал на необходимость вовремя распознавать и максимально быстро и широко оперировать, описал макро- и микроскопическую картину данной формы рака молочной железы, изучил причину появления «лимонной корки» — наличие изменений в дерме, связанных с блоком лимфатических сосудов и возникновением лимфостаза.
В настоящее время связи с ростом заболеваемости раком молочной железы в целом и с ростом заболеваемости ОРМЖ в частности изучение особенностей клинического течения и разработка оптимальных методов лечения ОРМЖ является одной из актуальных проблем клинической онкологии. Национальный института рака США в 1998г представил, а в 2005г дополнил анализ данных 3636 пациентов ОРМЖ с 1988г по 2000г. Было отмечено удвоение частоты заболеваемости ОРМЖ к 1992 году по сравнению с 1975г с 0,3 до 0,7, а к 1997-99гг – до 2,5 на 100 тыс. женского населения. Общая заболеваемость ОРМЖ среди белого населения по данным анализа составила 2,2, а среди пациенток негроидной расы – 3,1 на 100 тыс. женского населения (153, 110, 170). Большинство (58%) больных были моложе 50 лет и среди них преобладали пациентки негроидной расы (225, 255). В нашей стране в статистических отчетах ОРМЖ не выделяется как отдельная форма РМЖ.
ОРМЖ характеризуется быстрым клиническим течением, уже в начале заболевания проявляется увеличением объема и отечностью молочной железы, гиперемией кожи и наличием «лимонной корки», местным повышением температуры, диффузным уплотнением ткани железы. При первичном ОРМЖ нет четко отграниченного, определяемого пальпаторно и на маммограмме опухолевого узла. При вторичной форме, наряду с вышеуказанными симптомами, в железе определяется опухолевый узел. После появления отека молочной железы течение болезни, в том числе и характер метастазирования, становится таким же агрессивным, как и при первичном ОРМЖ.
В клинике Gustave-Roussy была разработана и в дальнейшем имела клиническое применение система стадирования отёка под названием «Poussee Evolutive» (PEV), основанная на симптомах воспаления и опухолевой инвазии молочной железы (213):
- PEV 0 – опухоль без увеличения в объеме молочной железы или признаков воспаления;
- PEV 1 – с заметным увеличением объема за последние 2 месяца, но без признаков отёка;
- PEV 2 – с воспалением и отеком меньшим, чем 50% поверхности молочной железы;
- PEV 3 – с воспалением и отеком большим, чем 50% поверхности молочной железы.
Следует отметить, что на момент установления диагноза около 1/3 пациентов ОРМЖ имеют опухоль с отечно-воспалительными симптомами вовлечения всей молочной железы — PEV3, тогда как 2/3 – локализованное (менее 50%) поражение молочной железы — PEV2. Вовлечение всей молочной железы (PEV3) является плохим прогностическим фактором (169).
Для ОРМЖ характерно и раннее метастазирование в регионарные лимфатические узлы, которое может отмечаться у 95%, при этом поражение надключичных лимфатических узлов (N3) в среднем отмечается у 30-40% больных (75, 86, 121, 138, 255, 251).
Для больных ОРМЖ не характерно наличие какой-либо определенной гистологической формы опухоли. Опухоль молочной железы может быть представлена инфильтрирующим протоковым, дольковым, медуллярным, слизистым или другой гистологической формой рака. Однако большая часть больных ОРМЖ имеют высокую степень злокачественности опухоли (по Nottingham классификации (137,144)) в отличие от других форм РМЖ (159, 132, 255).
Многие исследователи при ОРМЖ в опухоли отмечают преобладание пролиферирующих лимфатических эндотелиальных клеток, в отличие от узловых форм РМЖ, особенно на периферии опухоли. При ОРМЖ средняя площадь, занимаемая лимфатическими сосудами опухоли, также больше, что указывает на склонность к более высокому гематогенному и лимфогенному метастазированию (244, 245).
источник
Способ относится к медицине, точнее к онкологии, и может найти применение при лечении местнораспространенного рака молочной железы. Способ заключается в проведении системной и регионарной химиотерапии с эмболизацией артерии, питающей опухоль, и последующем выполнении лучевой терапии непосредственно после химиоэмболизации, причем такое химиолучевое лечение проводят на фоне введения больному преднизолона. Лучевую терапию осуществляют в режиме среднего фракционирования дозы по 3 Гр 5 раз в неделю до суммарной дозы 45 Гр на основание молочной железы и до 33-36 Гр на зоны регионарного лимфооттока, что эквивалентно суммарной дозе 60 Гр на основание железы и 44-48 Гр на зоны регионарно лимфооттока при обычном фракционировании. После проведения такого курса лечения далее для поддержания полученного эффекта осуществляют традиционную химиотерапии. Способ позволяет повысить эффективность лечения, снизить токсичность химиопрепаратов. 1 з.п. ф-лы.
Изобретение относится к медицине, точнее к онкологии, и может найти применение при лечении местнораспространенного рака молочной железы.
Рак молочной железы (РМЖ) занимает первое место в структуре заболеваемости и смертности от злокачественных новообразований среди женщин. Специальное значение этой формы рака настолько велико, что исследования по проблеме РМЖ занимают одно из ведущих мест в современной онкологической науке. В связи с этим каждое исследование с достижением положительных результатов лечения этой патологии заслуживает серьезного внимания специалистов.
Особое место в лечении РМЖ занимает так называемый инфильтративно-отечный рак, составляющий 1-3% всех форм первичного рака. Он относится к диффузно-инфильтрирующим формам его, характеризующимся распространением опухолевого процесса на все структуры МЖ, включая кожу и подкожно-жировую клетчатку.
В последние годы рядом исследователей доказано, что опухоли МЖ, обладающие инфильтративной формой роста, отличаются высокой степенью злокачественности, проявляющейся быстрым ростом опухоли, бурным метастазированием и значительным ухудшением отдаленных результатов. Такой рак поздно диагностируется и выявляется, как правило, тогда, когда уже имеет место распространенное поражение МЖ. Чаще всего инфильтративно-отечная форма РМЖ встречается у молодых женщин, нередко в период беременности и лактации. Выявить опухолевый узел в ткани железы часто бывает трудно. Пальпируется инфильтрат без четких контуров, занимающий большую часть железы. Отек обусловлен блокадой лимфатических путей самой железы метастатическими эмболами или их сдавлением опухолевым инфильтратом.
Традиционная схема лечения больных первичным инфильтративно-отечным РМЖ, как и других видов местнораспространенного рака, состоит в проведении индукционной терапии FAC (5-фторурацил, адриабластин, циклофосфан), в случае объективного эффекта — мастэктомия (или лучевая терапия) и лучевая терапия (после операции) и адъювантная химиотерапия.
Индукционная терапия FAC проводится, как правило, 1 раз в недели) в течение 4-х недель на курс и включает 4 таких курса.
Лучевая терапия осуществляется 25-ю фракциями по 2 Гр до суммарной очаговой дозы (СОД) 50 Гр. Повышение дозы до 65-75 Гр показано при возрасте больных менее 40 лет, наличии перитуморальных внутрилимфатических эмболов или при разрезе через опухоль, а также в случаях внутрипротокового рака с инфильтративным компонентом [EUROCANCER, Paris, 26-29 avr. 1994/ Pathol.Biol. — 1994-42, N.10-956-957]. Операция показана только в тех случаях, когда под влиянием лучевой и химиотерапии отек и инфильтрация кожи МЖ исчезают, что обычно наблюдается не ранее, чем через 6-8 недель после окончания лечения. В случае неоперабельности — только консервативное химиолучевое лечение [Hortobagyi G.N., Cancer, 1990, 66/6, Suppl.1387-91].
И все же несмотря на такое комплексное лечение 5-летняя выживаемость больных не превышает 5%, число местных рецидивов составляет 50-80% и практически 90% больных погибает в первые 2 года [Hortobagyi G.N. et al.Diseases of the Breast Lippincott-Raven, Philadelphia New York, 1996, 585-601].
Одним из методов лечения инфильтративно-отечного РМЖ является проведение регионарных инфузий [Баженова А. П. и др. Рак молочной железы, Медицина, 1985, с. 47] . Прогноз у таких больных, как отмечает автор книги, неблагоприятный.
Известно применение высокодозной лекарственной терапии в сочетании с пересадкой костного мозга либо стволовых клеток периферической крови в качестве индукционной терапии в предоперационном периоде или в комбинации с лучевой терапией в послеоперационном периоде в качестве консолидирующего лечения. Однако в литературе имеется лишь одно рандомизированное исследование с продолжительностью наблюдения в 37 месяцев [Antman К.Н., Dose-intensive therapy in breast canctr Baltimore. Williams a/Wilkms, 1992, 701]. По мнению ряда авторов, этот лечебный подход может увеличить безрецидивную выживаемость, но не влияет на результаты лечения при диссеминированном процессе.
Таким образом, как видно из приведенных исследований по лечению инфильтративно-отечного РМЖ, эта проблема онкологии остается нерешенной — ни в одном из них не удалось увеличить выживаемость больных, а также снизить число местных рецидивов.
Наиболее близким к предлагаемому является способ лечения инфильтративно-отечного РМЖ посредством комбинированной терапии [Санчакова А.В., Вопр. онкол., т.XVIII, N 4, 1972, c.6-10], взятый нами в качестве прототипа.
Способ заключается в том, что трем группам больных (всего 207 человек) инфильтративно-отечной формой РМЖ проводилось 3 схемы лечения: больным I группы (73 чел.) проводили оперативное удаление первичного очага и затем лучевое лечение, больным II группы (74 чел.) — оперативное, лучевое и гормональное лечение, больным III группы (60 чел.) — оперативное, лучевое, гормональное и химиотерапевтическое лечение. Лучевая терапия во всех группах больных проводилась в одинаковых условиях: облучение первичного очага с 2-3 полей, очаговая доза — 50-60-70 Гр, регионарных областей — с 3-4 полей, очаговая доза — 25-30 Гр. Гормональное лечение применялось в зависимости от состояния репродуктивной функции: в репродуктивном периоде и в тех случаях, когда менопауза не превышала 5 лет, производилась овариоэктомия с последующей андрогенотерапией: тестостерон-пропионат по 100 мг 3 раза в неделю внутримышечно. В группе больных, у которых менопауза превышала 5 лет, применялась терапия эстрогенами: синэстрол по 60-80 мг внутримышечно ежедневно в сочетании с глюкокортикоидами (преднизолон по 10-15 мг ежедневно). Оперативное удаление первичной опухоли и ее регионарных метастазов проводилось там, где операция технически была выполнима. Химиотерапия осуществлялась курсами. В качестве химиопрепаратов использовались тиоТэф по 200-300 мг и циклофосфан по 4-5 г на курс лечения.
При анализе результатов лечения учитывалось число выживших в сроки 3 и 5 лет по отношению к общему числу прослеженных больных, а также время появления и число первых рецидивов и отдаленных метастазов. Автор (Санчакова А.В.) пришла к выводу, что, во-первых, современное лечение должно быть комплексным, во-вторых, наиболее перспективным компонентом комплексного лечения является химиотерапия. Она позволяет, хотя и незначительно, но все же снизить процент отдаленных метастазов при высокозлокачественных формах РМЖ. В то же время автор отмечает, что несмотря на то, что комплексное лечение позволяет в определенном проценте случаев добиться стойких местных результатов, оно не избавляет больных от появления отдаленных метастазов, число которых в анализируемом ею методе составляло 76,7+5,0%. Причем, как свидетельствует анализ результатов лечения, добавление гормонотерапевтического компонента в схему лечения существенно не изменяет результаты. Наблюдается даже тенденция к некоторому снижению выживаемости и увеличению числа рецидивов и метастазов. Другим серьезным недостатком способа является высокая общая токсичность химиотерапевтического компонента при системном введении его.
Технической задачей настоящего изобретения, учитывая вышеприведенные данные о сложности лечения инфильтративно-отечного РМЖ, явилась разработка способа, обладающего более низкой общей токсичностью и превышающего эффективность известных методов.
Эта задача решена тем, что при химиолучевом лечении инфильтративно-отечного РМЖ химиотерапию осуществляют сначала в виде 2-недельной системной, затем — регионарной с химиоэмболизацией молочной железы, а лучевую терапию проводят непосредственно после регионарной в режиме среднего фракционирования дозы ежедневно по 3 Гр до суммарной очаговой дозы 45 Гр на основание молочной железы и до 33-36 Гр на зоны регионарного лимфооттока, причем химиолучевое лечение осуществляют на фоне введения преднизолона по 20-30 мг перорально или парэнтерально, а затем проводят традиционное химиотерапевтическое лечение.
Целесообразно химиотерапевтическое лечение проводить в виде 6 курсов циклофосфана, метотрексата и 5-фторурацила, причем первые 3 курса — через 6-8 недель каждый по 3-4 недели, последующие — по 2 недели каждые 3 месяца.
Предварительное проведение 2-х-недельного курса химиотерапии по схеме CMF (циклофосфан, метотрексат, 5-фторурацил) позволяет несколько уменьшить опухолевую массу в молочной железе, частично снять интоксикацию и воздействовать на опухолевые клетки, находящиеся в крови и попадающие с нею в другие органы.
Регионарная химиотерапия, выполняемая чрезбедренным доступом с введением катетера во внутреннюю грудную артерию, питающую опухоль, обеспечивает создание высокой концентрации химиопрепаратов в зоне опухоли. Поскольку внутриартериальная инфузия химиопрепаратов за счет попадания их в другие артерии может вызывать некроз кожи передней брюшной стенки [Douglas H.A. et al., J. of Vascular and Interventional Radiology, March-April 1995, 6: 249-251], предлагаемое нами введение 5-фторурацила и метотрексата в 5 мл липоидола за счет химиоэмболизации (маслом) предотвращает дальнейшее прохождение их и, тем самым, снижает до минимума побочные явления внутриартериальной химиотерапии.
Проведение лучевой терапии непосредственно после регионарной химиотерапии, т.е. на фоне действия на опухоль химиопрепаратов, значительно усиливает противоопухолевый эффект. Это особенно важно ввиду радиорезистентности инфильтративно-отечных форм РМЖ.
Введение больной во время всего курса химиолучевого лечения преднизолона делает возможным такое последовательное лечение, предупреждая возможность лейкопении во время проведения лучевой терапии. Именно возникновение лейкопении вынуждает онкологов проводить лучевое лечение не ранее чем через 2-3 недели после химиотерапии, что снижает эффект лечения. Наблюдаемая нами у некоторых больных уже после окончания курса лучевой терапии (при отмене преднизолона по окончании ее) лейкопения во время проведения им последующих курсов традиционной химиотерапии купировалась введением нейпогена без перерыва курса лечения. При необходимости одновременно с нейпогеном дополнительно вводили в течение нескольких дней преднизолон.
Введение преднизолона, кроме того, дает возможность проводить лучевую терапию в режиме среднего фракционирования дозы по 3 Гр 5 раз в неделю до суммарной очаговой дозы (СОД) 45 Гр на основание молочной железы, эквивалентной режиму обычного фракционирования по 2 Гр 5 раз в неделю до СОД 60 Гр, и по 3 Гр до СОД 33-36 Гр на зоны регионарного лимфооттока, эквивалентной СОД 44-48 Гр обычного фракционирования.
Введение преднизолона целесообразно проводить в первой половине дня после еды по 30 мг внутримышечно в будние дни и по 20 мг перорально в выходные, а в те дни, когда осуществляется внутривенное введение химиопрепаратов, вводить его одновременно с ними внутривенно.
Проведение после химиолучевого лечения традиционной химиотерапии в виде рекомендуемых нами 6 курсов CMF, как показали многолетние клинические наблюдения за больными с местнораспространенным раком, способствует продлению и улучшению качества жизни этого тяжелого контингента больных.
Сущность способа поясняется примером.
Больная Г., 1956 г.р., поступила в клинику ЦНИРРИ 26.04.2000 г. с диагнозом: рак правой молочной железы Т4ВNXМX — инфильтративно-отечная форма.
Из анамнеза: больна около 2-х месяцев, когда случайно заметила образование в правой молочной железе, которое за последнее время значительно увеличилось в размерах и появился отек. Обследовалась в поликлинике по месту жительства, от предложенной операции отказалась.
При поступлении в ЦНИРРИ: Состояние удовлетворительное. Местно — на фоне фиброаденоматоза обеих молочных желез в правой — на границе верхних квадрантов плотное, неоднородное, без четких контуров образование более 5 см и диаметре. Кожа правой молочной железы отечна, подмышечные лимфатические узлы отчетливо не определялись.
На маммограмме: в правой половине груди в центральном верхнем отделе узел 4,5х5,0х5.7 см с признаками злокачественного роста и лимфангоитом, достигающим кожи и грудной стенки и инфильтрирующий кожу на всем протяжении. В левой молочной железе — фиброаденоматоз.
Ультразвуковое исследование (УЗИ) от 26.04.2000 показало умеренно выраженные явления фиброза в левой молочной железе, в правой на границе верхних квадрантов определялось гипоэхогенное неправильной формы образование 4,5х4,7х5,4 см с признаками инфильтративного роста. Кожа отечная.
Гистологически: при трипанбиопсии опухоли — Б 135925-926 — инфильтрирующий тубулярный рак.
На рентгенограмме органов грудной клетки — в легких без очаговых и инфильтративных изменений. УЗИ органов брюшной полости — без патологических изменений.
Остеосцинтиграфия — без гиперфиксации радиофармпрепарата ( 99 Tc).
Клинический анализ крови от 26.04.2000 г.: Нв-126 г/л, Эр.- 4,15х10 12 /л, Л-5,0х10 9 /л, СОЭ-5 мм/ч, п-3, с-65, э-1, б-1, м-9, л-21.
Биохимические показатели крови — не изменены.
27.04.2000 г. начата полихимиотерапия по схеме CMF: 27.04 и 4.05.2000 г. вводили внутривенно капельно по 1 г 5-фторурацила и 40 мг метотрексата и по 1 г циклофосфана внутримышечно на одно введение. Одновременно внутривенно вместе с химиопрепаратами больной ввели 30 мг преднизолона.
Состояние больной удовлетворительное, отек в молочной железе немного уменьшился.
15.05.2000 г в ангиографическом кабинете была проведена регионарная химиотерапия правой молочной железы: под местной анестезией 1% раствором новокаина (20 мл) произведена катетеризация правой бедренной артерии, катетер установлен в правой внутренней грудной артерии и через него введено: 1 г 5-фторурацила за 15 минут, затем через микрокатетр — 50 мг метотрексата в 5 мл линоидола и для предупреждения воспаления — 80 мг гентамицина. Одновременно внутримышечно введен 1 г циклофосфана. Ангиографическая процедура заняла 1 час без побочных явлений. Больную перевели в палату. Через час у нее началась рвота — ее купировали внутривенным введением 5 мл (5 мг) новобана на 10 мл 0,9% раствора хлористого натрия. Вечером у больной появилась гиперемия кожи правой молочной железы, поднялась температура до 38,5 o . Больной ввели литическую смесь (4 мл 50% раствора анальгина и 1 мл 1% раствора димедрола).
Утром 16.05.2000 г больной стало легче, и ей начали лучевую терапию, продолжая в первой половине дня ежедневные инъекции преднизолона по 30 мг внутримышечно по будним дням и по 20 мг перорально в выходные дни.
Лучевую терапию выполняли в режиме среднего фракционирования дозы: на основание правой молочной железы с 2-х тангенциальных встречных полей по 3 Гр в день 5 раз в неделю до СОД 45 Гр, эквивалентной режиму обычного фракционирования по 2 Гр 5 раз в неделю до СОД 60 Гр (парастернальная зона включалась одновременно с молочной железой), и на зоны регионарного лимфооттока справа фигурным полем (надподключично-подмышечно) по 3 Гр в день 5 раз в неделю до СОД 33-36 Гр, эквивалентных обычному фракционированию до 44-48 Гр. Лучевая терапия проводилась под динамическим контролем периферической крови. По окончании курса дозу преднизолона каждые 2 дня снижали на 5-10 мг до полной его отмены.
Лучевое лечение больная перенесла удовлетворительно, без перерыва. За время лечения отек спал, границы опухолевого образования стали четче. Было принято решение перевести ее на последующее традиционное химиотерапевтическое лечение.
7.06.2000 г начат курс полихимиотерапии по схеме CMF: 7.06, 14.06, 21.06 и 27.06.2000 больной внутривенно капельно вводили по 1 г 5-фторурацила и 40 мг метотрексата и внутримышечно по 1 г циклофосфана на введение. Возникающая тошнота купировалась внутривенным введением 5 мг новобана на 10 мл 0,9% раствора хлористого натрия. На появление лейкопении 29.06 и 3.07.2000 г вводили подкожно по 300 мкг нейпогена и внутримышечно 30 мг преднизолона, а также 2 раза в день в течение 7 дней вводили внутримышечно по 1 г цефазолина. Курс химиотерапии не прерывали.
Состояние больной удовлетворительное, опухоль заметно уменьшилась, сосок не втянут, кожа молочной железы не утолщена.
На маммограммах правой молочной железы: на границе верхних квадрантов определялся бугристый опухолевый узел размером 2,0х2,1х1,5 см (вдвое меньше по сравнению с последним исследованием).
УЗИ: в верхне-внутреннем квадранте правой железы гипоэхогенное неоднородное бугристое образование размером 15х11х12 мм.
5.07.2000 г больная выписана из клиники в удовлетворительном состоянии под наблюдение онколога по месту жительства с очередной явкой в институт через 8 недель.
6.09.2000 г повторная госпитализация в клинику.
Состояние больной удовлетворительное. Местно — кожа правой молочной железы без отека и инфильтрации, на границе верхних квадрантов ограниченноподвижное уплотнение, не спаянное с кожей и грудной стенкой, около 3 см. Регионарные лимфатические узлы не определялись. Кожа не изменена.
На маммограммах от 8.09.2000 г опухолевый узел в глубине правой молочной железы уменьшился почти вдвое.
Клинико-рентгенологическое, ультразвуковое, сцинтиграфическое исследования — патологии не выявили. Клинический и биохимический анализы крови — в пределах нормы.
С 12.09.2000 г (12.09, 19.09, 26.09 и 3.10.2000 проведен курс полихимиотерапии по схеме CMF аналогичный первому курсу, который больная перенесла удовлетворительно (без лейкопении).
Аналогичный курс химиотерапии проведен больной в ноябре-декабре 2000 г.
Результаты последнего обследования больной 25.12.2000 г: кожа правой молочной железы не изменена, отека нет, опухолевый узел в глубине на границе верхних квадрантов около 2 см, лимфатические узлы в подмышечных и подключичных областях не определяются. Левая молочная железа — в норме. На маммограммах, по сравнению с предыдущими данными от 8.09.2000 г, опухолевй узел уменьшился еще на 1/3, нарастает фиброз. Клинико-рентгенологическое исследование органов и систем организма патологических изменений не обнаружило. Больная находится в ремиссии. Очередной курс химиотерапии планируется провести ей в апреле 2001 г.
Предлагаемым способом проведено лечение 6 больных. Срок наблюдения за ними составляет к настоящему времени от 10 месяцев до 1,5 лет. Все они находятся в удовлетворительном состоянии, что позволяет надеяться на длительную ремиссию.
Предлагаемый способ, на наш взгляд, может стать методом выбора при лечении инфильтративно-отечного РМЖ. Способ является достаточно эффективным ввиду массивного воздействия на опухоль одновременно химио- и лучевого факторов и несмотря на это он удовлетворительно переносится больными.
Способ разработан в клинике ЦНИРРИ и прошел клиническую апробацию у 10 больных с положительным результатом.
1. Способ лечения инфильтративно-отечного рака молочной железы посредством химиолучевой терапии, отличающийся тем, что химиотерапию по схеме СМF сначала осуществляют в виде 2-недельной системной, затем — регионарной с химиоэмболизацией молочной железы, а лучевую терапию проводят после регионарной в режиме среднего фракционирования дозы ежедневно по 3 Гр до суммарной очаговой дозы 45 Гр на основание молочной железы и до 33-36 Гр на зоны регионарного лимфооттока, причем химиолучевое лечение осуществляют на фоне введения больному преднизолона по 20-30 мг ежедневно перорально или парэнтерально, а затем проводят курс химиотерапии по схеме СМF аналогичный первому.
2. Способ по п.1, отличающийся тем, что проводят 6 курсов циклофосфана, метотрексата и 5-фторурацила, причем первые 3 курса проводят по 3-4 недели каждый через 6-8 недель, последующие — по 2 недели каждые 3 мес.
источник
Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Эффективность лечения, продолжительность жизни и её полноценность во многом зависят от гистологической структуры опухолевого образования – то есть, от формы рака молочной железы. Характеристика ракового очага является вторым фактором успешного прогноза заболевания после степени запущенности процесса и его первичности.
Клинические симптомы рака могут отличаться или быть одинаковыми, однако от формы рака напрямую зависит дальнейшее развитие болезни и её исход.

Отечная форма рака грудной железы – это одна из разновидностей диффузной опухоли, которая отмечается в 2-5% случаев всех раковых опухолей молочных желез. Отечная форма отличается неблагоприятным прогнозом: выжить на протяжении пяти лет удается лишь 15-50% больных.
Выделяют первичный и вторичный вариант отечной формы. Для заболевания характерно стремительное клиническое развитие, когда уже на начальных этапах наблюдается значительное увеличение размеров и отечность пораженной железы, покраснение кожных покровов и типичная «лимонная корка». Местно повышается температура, грудь уплотняется. В первичном варианте патологии отсутствует четкий пальпируемый раковый узел, который ярко выражен при вторичном течении.
После того как в железе начинается отечная стадия, рак принимает агрессивный характер и стремительно развивается, отдавая массовые метастазы.
Отечная форма может проявляться при разных гистологических видах опухолей:
- при инфильтрующем протоковом раке;
- при дольковом раке;
- при медуллярном раке;
- при слизистом раке и пр.
Часто в такой опухоли наблюдаются преимущественно пролиферирующие лимфатические эндотелиальные клетки.

Инфильтративная форма рака молочной железы имеет и другое название – инвазивная. Данная форма имеет несколько типов:
- инфильтративная форма протокового рака (очаг распространяется с молочных протоков в жировую ткань);
- инфильтративная форма долькового рака (опухоль берет свое начало с дольковых железистых участков);
- прединфильтративная форма протокового рака (процесс способен трансформироваться в инвазивную форму при неадекватном лечении).
В чем заключаются особенности инфильтративной формы?
Инфильтрация распространяется на значительную часть грудной железы, при этом четкие границы процесса проследить нельзя. Зачастую о патологии говорит увеличение одной из желез, мраморный окрас кожи на ней, присутствие характерной «лимонной корочки».
Как и в предыдущем варианте, существует разделение на первичную и вторичную подкатегорию: без опухолевого узла, и с пальпируемым четким уплотнением.
Основными признаками инфильтративной формы являются:
- неправильная форма железы, её увеличение в размерах;
- втяжение соска или ближайшей к нему кожи;
- появление спаянного с тканями неподвижного узла (ограниченного уплотнения) до 10 см в диаметре.
Первичная инфильтративная форма чаще встречается у пациенток после 40-летнего возраста, а вторичная может быть обнаружена вне зависимости от возрастной категории.
Отечно-инфильтративная форма представляет собой сочетание двух предыдущих форм. Истинная, или первичная злокачественная патология заключается в диффузном распространении ракового процесса в тканях железы, а вторичная – в появлении четко-пальпируемого узлового образования, сопровождающегося отечностью кожных покровов.
Отечно-инфильтративная форма рака молочной железы может отличаться от локальной опухоли не только масштабом поражения, но и крайне негативным прогнозом. Особенно это касается первичного типа опухоли, так как такой рак обычно выявляется на поздних стадиях, когда процесс уже выходит за пределы молочной железы.
В большинстве случаев отечно-инфильтративная форма рака диагностируется у пациенток в молодом возрасте, иногда даже во время беременности или грудного кормления. При осмотре прощупывается уплотнение, не имеющее четких границ, и распространяющееся на значительный участок железы. Отечность тканей при этом выражена, что объясняется ущемлением лимфатических сосудов небольшими метастазами или непосредственно самой опухолью.
Узловая форма раковой опухоли встречается чаще других форм. Для неё характерно формирование в железе уплотнения в виде узла разных размеров. Чаще всего поражаются верхне-наружные квадранты груди.
Типичные признаки данной формы обычно следующие:
- появление прощупываемого плотного узелка в тканях органа, без явных границ, с ограничением подвижности;
- выявление необъяснимой морщинистости кожи, либо слишком гладкая кожа (по типу площадки), либо втянутость кожных покровов над пораженным участком;
- прощупывание уплотненных лимфатических узлов в подмышечной зоне со стороны пораженной груди.
Реже первым признаком злокачественного процесса могут стать выделения из млечных протоков.
С нарастанием злокачественного процесса клиническая картина расширяется:
- появляется «лимонная корка» признак диффузной отечности;
- изменяется околососковая область, сосок становится плоским;
- железа визуально деформируется;
- увеличиваются и уплотняются лимфоузлы в области подмышек;
- распространяются метастазы, появляется соответствующая пораженным органам симптоматика.
Рожистоподобный рак – это наиболее агрессивная форма рака молочной железы, которая отличается стремительным распространением, молниеносным течением и непредсказуемостью. Такая опухоль имеет особую склонность к рецидивам, быстро и массово распространяет метастазы, вне зависимости от используемых методов лечения.
Рожистоподобная форма раковой опухоли проявляется следующими клиническими признаками:
- резко возникающее покраснение кожных покровов на молочной железе;
- возможное распространение покраснения за пределами пораженной железы;
- покраснение напоминает рожистое воспаление (отсюда и термин рожистоподобной формы) – пятно с «рваными» зубчатовидными границами;
- иногда резко повышается температура тела.
Зачастую такой рак действительно ошибочно принимают за рожистый воспалительный процесс и назначают неправильное лечение с применением физиотерапии и противовоспалительных препаратов. В таких случаях теряется драгоценное время, и состояние пациента стабильно ухудшается. Поэтому очень важно правильно проводить дифференциальную диагностику заболевания.
Второе название рожистоподобного рака – воспалительная форма рака молочной железы. Это достаточно редкий вид раковой опухоли, доля которого составляет не более 3% от всех злокачественных заболеваний молочных желез. Обычно его обнаруживают только после проведения маммографии или ультразвукового исследования.
Что представляет собой маститоподобная форма рака молочной железы? И здесь название говорит само за себя: такая раковая опухоль обладает всеми признаками мастита, и часто ошибочно принимается за воспалительный процесс.
Клиническая картина маститоподобного рака следующая:
- пораженная молочная железа заметно увеличивается;
- при прощупывании ощущается плотность (натянутость) тканей;
- кожные покровы на месте поражения становятся выраженно красными;
- местная температура повышается;
- присоединяется инфекция, что ещё больше напоминает признаки мастита.
Общая температура тела также повышается: налицо все признаки воспалительного процесса и интоксикации организма.
Далее отечность железы распространяется на верхнюю конечность и околоключичную зону. При отсутствии адекватной терапии могут появляться изъязвления на коже.
Если через 2 недели после лечения обычного мастита не наблюдается положительной динамики, то можно заподозрить маститоподобный рак: для дифференциации рекомендуется провести дополнительные методы диагностики, такие как рентген, УЗИ, гистологическое исследование.
Диффузная форма рака может включать в себя как отечную форму, так и воспалительную рожистоподобную и маститоподобную формы. Сущность заболевания определена в его названии – от латинского «diffusum, diffundo» (распределенный, расплывчатый, не имеющий четких границ). Такая опухоль прорастает в виде разлитого инфильтрата, который поражает железистый орган по всем направлениям – то есть, не имеет четкой направленности процесса.
Уплотненный или эластично-плотный инфильтрат зачастую охватывает несколько секторов, либо значительную часть грудной железы. Вследствие возникновения механического препятствия в виде опухоли нарушается естественный отток лимфы, что приводит к увеличению и значительной деформации органа. В близлежащих зонах скопления лимфоузлов наблюдается распространение метастазов.
Диффузная форма протекает остро, с быстрым метастазированием.
Как вы уже убедились, различные формы рака молочной железы могут иметь разные клинические проявления. При этом течение заболевания во многом зависит от гормонального фона в организме. Например, в молодом возрасте, и особенно во время беременности и грудного кормления рак развивается быстро, со скорым метастазированием. А в пожилом возрасте опухоль способна существовать на протяжении нескольких лет, не распространяясь в другие органы.

источник