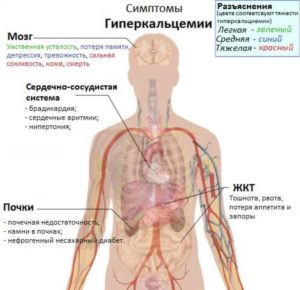
Если диагностированы метастазы в костях при раке молочной железы сколько живут зависит от адекватного и своевременного лечения. Появление метастазов в костях считается очень опасным осложнением распространения рака. Чаще всего, при появлении метастазов, врачи говорят о 4 стадии рака. Они отмечают, что, если болезнь активно развивается и метастазы поразили костную ткань, то продолжительность жизни пациента составляет всего пару месяцев.
Появление метастазов в костной ткани негативно сказывается на общем здоровье пациента.
Медики отмечают, что метастазы образуются у больного при развитии рака:
Важно отметить, что метастазы могут появиться и при развитии рака иных органов: ребер, позвоночника, черепа, бедра, плеча и в костях тазового дна.
Их образование связано со способностью человеческого организма постоянно костеобразовываться. Этот процесс возникает под влиянием двух групп клеток:
- Остеокласт. Они регулируют процесс разрушения и поглощения костных клеток.
- Остеобласт. Они осуществляют выработку новой костной ткани.
В том случае, если здоровье пациента находится на нормальном уровне, то данный процесс осуществляется 1 раз в 10 лет. Если же данный процесс нарушен, то происходит аномальная выработка данных клеток.
Медики разделяют два вида рака в зависимости от поражения клеток:
- Остеолитический рак заключается в поражение остеокласт. Благодаря этому осуществляется истончение костной ткани, человек часто ломает конечности.
- Остеобластический рак заключается в нарушении структуры остеобластов. Благодаря этому происходит увеличение костной ткани, образование наростов и иных новообразований.
Медики отмечают, что на ранних стадиях рак не проявляется никакими симптомами. В результате этого его трудно выявить. При переходе болезни в более тяжелую стадию пациента могут беспокоить следующие симптомы:
- сильная головная боль;
- появление болевых ощущений в конечностях. Обычно это связано с оказанием чрезмерного давления на нервные окончания;
- резкое увеличение внутрикостного давления и нарушение двигательной активности;
- частые переломы конечностей. Это связано с чрезмерным истончением костной ткани;
- появление опухоли или уплотнения в проблемной области.
- увеличение количества кальция в крови. Это является очень опасным для человека, так как кальций оказывает негативное воздействие на работу сердечной системы и вызывает развитие почечной недостаточности;
- появление поражений в нервной системе, оказание чрезмерного давления на спинной мозг и нервные корешки. В запущенных случаях они ведут к развитию паралича.
- интоксикация организма. Обычно об этом свидетельствует появление апатии, депрессии, вялости, хронической усталости, слабости, тошноты, потери аппетита.
Важно отметить, что развитие в организме метастазов может выявить только специалист. Для этого им могут быть применены дополнительные методы исследования:
- использование рентгенографии. Является очень информативным методом, но не позволяет выявить рак на ранней стадии.
- применение компьютерной томографии. С ее помощью специалист может выявить степень развития рака, а также изучить внутренние ткани на наличие в них повреждений.
- использование МРТ диагностики. Она позволяется выявить масштаб метастазированной области и дать наиболее полную картину болезни.
- применение сцинтиграфии. С ее помощью можно выявить степень накопления раковыми клетками специальных лучей. Также данный метод позволяет наиболее точно определить зону появления метастазов.
Помимо этого, пациенту будет назначена сдача биохимического анализа крови и биопсия.
Важно отметить, что метод лечения зависит от степени развития болезни и особенностей самого пациента.
Медики отмечают, что в настоящее время разработано несколько методик избавления от метастазов. К ним следует отнести:
- Использование химиотерапии . Внедрение специальных препаратов оказывает негативное воздействие на процесс распространения раковых клеток. Медики отмечают, что данный способ имеет огромное количество различных побочных эффектов.
- Применение лучевой терапии. Она основана на оказании воздействия на раковые клетки с помощью специальных рентгеновских лучей. Многие пациенты отмечают, что данный способ является одним из самых действенных при избавлении от раковой опухоли. Недостатком данной терапии является длительный период реабилитации больного.
- Проведение медикаментозной терапии. Обычно, если метастазы поразили кости, то применяются такие препараты как биосфосфаты. Они помогают быстрее восстановить костную ткань.
Для достижения большого эффекта медиками проводиться комплексная терапия. Помимо этого, больному назначается прием обезболивающих средств и иммунномодуляторов.
Важно отметить, что при поражении метастазами костей специалисты дают не очень положительный прогноз на выживаемость. Обычно такие метастазы свидетельствуют о переходе болезни в тяжелую стадию.
Таким образом, при раке молочной железы с метастазами в кости обычно пациенты живут от 3 месяцев до 1 года. В некоторых случаях отмечается, что пациенты могут жить около 2 лет.
В данном случае выживаемость зависит от следующих факторов:
- от того, какие лечебные мероприятия проводились в первое время при лечении начальной стадии рака;
- от конечной степени развития болезни;
- от особенностей течения заболевания и способности организма противостоять болезни.
Таким образом, метастазы, особенно в костях, являются очень опасным осложнением грудной онкологии, но чем ранее пациенту был поставлен диагноз и проведено грамотное лечение, тем выше шанс на продолжение жизни у пациента и быстрое избавление от болезни.
источник
Рак молочной железы широко распространен по всему миру. Ежегодно огромное число женщин (до полутора миллионов) пополняет ряды заболевших. Причины болезни до сих пор остаются предметом споров ученых. Высокая смертность является следствием того, что начальные стадии почти всегда протекают бессимптомно. Имея некоторые присущие болезни признаки, женщины обычно не придают им значения, относя их к обычному недомоганию от усталости. Некоторые из них регулярно проводят самообследование груди. И только медицинские осмотры или случайности помогают выявить патологию. Хотя по статистике за последние 10 лет число пациенток с диагнозом рак молочной железы I-II стадии, динамично возрастает.
В определенное время некоторые клетки молочной железы по необъяснимым причинам начинают мутировать. Если женщина здорова и у нее сильный иммунитет, он быстро уничтожает изменившиеся клетки. Но ослабленная иммунная система с ними бороться не в силах. Они молниеносно растут и делятся. Это процесс образования первичного злокачественного образования. Если сразу не проводилось лечение, то от этой опухоли отрываются клетки и начинают «путешествие» по организму. Этот процесс называется метастазированием. Когда метастазы рака молочной железы достигают отдаленных органов, это уже рак IV стадии, который характеризуется выходом опухоли за пределы груди и области подмышек и появлением в других структурах.
Различают два пути распространения метастазов. Если раковые клетки попали в лимфоток, они обнаруживаются в регионарных лимфатических узлах, расположенные вблизи первичной опухоли. Это подмышечные, передние грудные, подключичные и надключичные, окологрудинные лимфоузлы. Этот путь распространения называется лимфогенным.
Когда атипичные клетки оторвавшись от основной опухоли попадают в кровеносное русло, они «оседают» во внутренних органах, костной системе и головном мозге. Такой путь называют гематогенным.
Метастазы при раке молочной железы вызывают характерные клинические симптомы:
- в костях – вызывают значительные боли в позвоночнике и конечностях даже в покое, повышенная хрупкость вызывает частые переломы;
- в головном и спинном мозге – общее недомогание, головокружения и головные боли, тошнота, резкая смена настроения и изменения в поведении;
- в легких – частые респираторные заболевания, постоянный сухой или продуктивный кашель, затрудненный вдох, одышка;
- в печени – женщина ослаблена, тошнота и рвота, снижается аппетит, она худеет, появляются желтуха, боли в правой стороне живота, вздутие. При исследовании функций печени – резкое повышение количества билирубина, показателей печеночных трансаминаз. Вздутие живота обусловлено асцитом (скоплением жидкости в брюшной полости). При этом состоянии врачом выполняется лапароцентез (прокол передней брюшной стенки) с целью удаления жидкости из брюшной полости.
Под кожей прощупываются плотные безболезненные уплотнения – это признак поражения лимфоузлов. Если это произошло в паху или в подмышечной впадине, то на стороне поражения конечность может отекать.
Куда метастазирует рак молочной железы, связано со свойствами первичного очага и частотой поражения органа. Например, гормонозависимые опухоли чаще всего выявляются в легких и костях. HER2-положительные раки (с избытком HER2-рецепторов на поверхности клеток, которые вынуждают их бесконтрольно делиться) – в печени и головном мозге.
Метастазы могут быть солитарными (одиночными) или множественными, что встречается гораздо чаще. Опухоль может метастазировать сразу в несколько органов, или в одном из них образует колонии злокачественных клеток.
Рак молочной железы 4 стадии с метастазами в легкие чаще всего диагностируется при прохождении пациенткой рентгенографии грудной клетки. Для более полной картины выявления метастазов применяется сцинтиграфия скелета с введением радиоактивных изотопов, и получают двухмерное изображение путем определения излучения, которое исходит от них. Но этот метод в России пока применяется только в крупных медицинских учреждениях. Чаще применяют полное сканирование всего тела и МРТ.
Определить поражение печени помогают анализы крови, ультразвук и КТ; головного мозга – КТ и МРТ. Для выявления мелких очагов применяется гибридный метод визуализации – ПЭТ-КТ (позитронно-эмиссионная и компьютерная томография).
При поражении легких и печени проводится биопсия.
Как только прозвучит диагноз «метастатический рак молочной железы», каждая женщина начинает паниковать, боясь близкого исхода болезни. Её волнует, сколько осталось жить. Говорить конкретно и однозначно об этом невозможно, ведь все зависит от совокупности многих факторов. И у каждой своя неповторимая история. Но одно можно утверждать с точностью, что ранее выявление злокачественной опухоли гарантирует пациентке длительную жизнь. Именно по этой причине важно с вниманием относиться к своему здоровью, ведь за вас этого никто не сделает.
В медицине принято рассматривать 5-летнюю выживаемость при такой патологии. Это означает количество пациентов в процентах, у которых обнаружено заболевание и переживших пятилетний рубеж.
Пациенты с 0 и I стадиями, прошедшие адекватное лечение, выживают 100%. При размере опухоли 2 см и появлении ее в подмышечных лимфоузлах, а также с размером опухоли до 5 см без метастазов – это II стадия, и живут более 5 лет 93% женщин. На III стадии, когда метастазы затрагивают подмышечные и загрудинные лимфоузлы, цифра уменьшается до 72%. Рак молочной железы IV стадии показывает выживаемость не более 22%. Но даже в таком периоде есть благоприятные факторы для продления жизни:
- выявлено, что опухоль гормонозависима;
- нет метастазов в важных органах;
- новообразование хорошо отвечает на воздействие гормональной и химиотерапии.
Лечение рака груди с метастазами и раннего периода заболевания существенно отличаются между собой. Если в начале болезни врачи часто применяют довольно агрессивный курс лечения, имея целью полное избавление от рака, то при метастазах они стараются максимально контролировать опухоль. При этом подбирается метод с наименьшей токсичностью.
Лучевую терапию эффективно используют для «укрощения» метастазов в мозге. Но если есть возможность удалить очаг без ущерба для женщины, то производится операция. Это может быть сделано в случае одиночного метастаза или для улучшения качества жизни.
Гормональное лечение. Если опухоль признана гормонозависимой, то такие препараты, как Тамоксифен и Аримидекс способны эффективно контролировать опухоль, а иногда даже лучше, чем многие цитостатики. К тому же они менее токсичны, чем химиопрепараты.
Лечение моноклональными антителами. У 25% женщин диагностируют HER2 позитивный рак молочной железы, имеющий избыток HER2-рецепторов в клетках. Существует два вида тестов на этот белок: иммуногистохимия и флуоресцентная гибридизация in situ (FISH). Материал для тестов забирается во время хирургического вмешательства или биопсии. Этот вид опухоли признан самым агрессивным. Для его лечения применяют специальные препараты: Герцептин, Лапатиниб, Кадсила и новейший препарат Бейодайм, позволяющие улучшить состояние пациентки и продлить жизнь.
При HER2-отрицательном раке, который выявляется у 75% пациентов, Герцептин не применяется, поскольку в таком случае он показывает низкую эффективность.
Химиотерапия. При раке молочной железы с метастазами часто применяется метод химиотерапии.
В настоящее время лучшим считается цитостатик Кселода, действующий избирательно только на клетки опухоли. Здоровые клетки при этом получают минимальное воздействие.
Поддерживающая терапия позволяет уменьшить интенсивность мучительных симптомов и продлить сроки ремиссии заболевания. Новое поколение препаратов, называемое бисфосфонаты, очень эффективно уменьшают боли в костях и их разрушение (Аредиа, Зомета).
Правильно подобранное лечение – залог длительности жизни пациентов с последней стадией рака. Оно помогает улучшить качество жизни и добиться длительной ремиссии.
источник
Появление mts (метастазов) в костях обусловлено распространением раковых клеток по кровеносным сосудам из первично пораженного органа в костные ткани, развиваясь в злокачественные опухоли. Чаще всего раковые клетки мигрируют из первично пораженных щитовидной, предстательной и молочной желез, легких, почек, а также при Саркомах, лимфомах и лимфоме Ходжкина. Реже встречаются метастазы из шейки матки, яичников, ЖКТ и мягких тканей и очень редко из других органов. Наиболее частую локализацию имеют метастазы в кости с обильным кровоснабжением: кости таза, рук, ног, грудной клетки, позвоночник, череп, костный мозг и в ребрах. Не редко метастазы обнаруживаются в тазобедренном суставе, плечевом и коленном суставах. При раке груди у женщин, при раке щитовидной железы, почек и легких метастазы могут пойти в мечевидный отросток, тело и рукоятку грудины, а также в подвздошную кость, ребра, тазовые, тазобедренные кости и кости плеча.
Опухоли нарушают работу остеобластов и остеокластов — больших многоядерных клеток, ответственных за регуляцию строения и разрушения костных тканей в процессе клеточного обновления.
Хирургическое вмешательство, патологические переломы и прочие осложнения метастазирования могут вызвать хилостаз (застой лимфы), что приводит к отекам. Метастазы в костях могут причинять сильные боли, например, при меланоме позвоночника или опухоли седалищной кости, которая может сдавливать нерв.
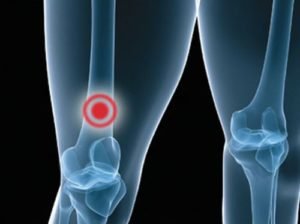
Основные симптомы вызывают гиперкальциемия, патологические переломы и спинномозговая компрессия. Также отмечается повышенная температура из-за активного метаболического процесса и ускоренного деления клеток.
У трети пациентов метастазы в костях вызывают гиперкальциемию. Кальций, входящий в состав костей, при эрозии кости высвобождается и попадает в кровь. Гиперкальциемия вызывает ряд симптомов:
Нервная система:
- Нестабильность психики;
- Заторможенность;
- Депрессия;
- Расстройство умственной деятельности.
Сердечно-сосудистая система:
- Понижение давления;
- Аритмия.
- Отсутствие аппетита;
- Тошнота;
- Рвота;
- Язвенные образования.
Мочевыделительная система:
- Увеличенное образование мочи;
- Почечная недостаточность;
- Интоксикация.
Пораженный метастазами участок кости становится хрупким из-за сбоя в работе остеобластов и остеокластов, что приводит к патологическим переломам. Патологические переломы появляются, если повреждено более половины внешнего костного слоя. Перелом может спровоцировать несильный удар или же очевидная причина может вовсе отсутствовать. От метастатических поражений чаще всего страдают бедренные кости, грудной и поясничный отдел позвоночника.
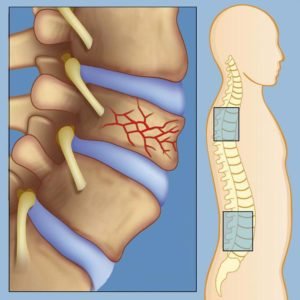
Если компрессии способствовало постепенное увеличение опухоли, то признаки сдавливания спинного мозга бывают долго не замечены, в отличие от случая, когда к компрессии приводит сдвинувшийся обломок позвонка.
Остеобласты и остеокласты — основные клетки, участвующие в нормальном обновлении костных тканей. При метастазах в костях нарушается аллостаз (способность организма реагировать на нетипичные изменения и осуществлять гомеостаз – саморегуляцию), из-за чего клетки начинают работать с патологическим уклоном, организм не справляется с регуляцией клеточных процессов и в костях возникает субтотальное поражение.
Остеобласты — это строительные клетки скелета, которые заполняют собой пустые участки, производят межклеточное вещество (матрикс) и превращаются в клетки костной ткани (остеоциты). Если из-за метастазов в костях происходит сбой работы остеобластов, то в костях образовываются остеосклеротические очаги (иначе склеротические, т. е. уплотнения) — такие нарушения называются остеобластическими или бластическими, а образование уплотнений остеобластическим процессом.
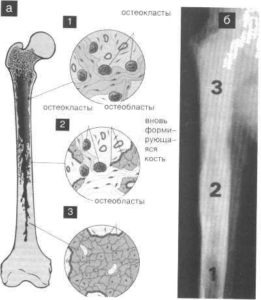
Редко встречаются метастазы в костях, приведшие к одному единственному типу повреждения и проявление повреждений чаще всего смешанного типа, с признаками как уплотнения тканей на отдельных участках, так и разрушения.
Чтобы проверить наличие метастазов, существует ряд процедур для диагностики на разных стадиях развития заболевания:
- Сцинтиграфия — обследование путем ввода радиоактивных изотопов для получения двумерного изображения, где проявляются пораженные участки, которые выглядят как белые пятна. Помогает узнать о присутствии метастазов на раннем этапе их развития;
- Рентгенография — позволяет выявить характер поражения, заметный только на поздних стадиях;
- Компьютерная или магниторезонансная томография дают трехмерное изображение скелета;
- Биохимическое исследование крови для проверки уровня кальция в плазме крови и диагностики гиперкальциемии;
- Биопсия — позволяет точно определить злокачественность новообразований и поставить окончательный диагноз.
Лечение назначается врачом-онкологом на основании данных анализа крови, локализации первичных и вторичных раковых образований, стадии разрушения и разновидности поражения костей (остеобластические и остеолитические лечатся по-разному). Основное направление лечения заключается в устранении тяжелых осложнений для улучшения качества жизни пациента. Если болят позвоночник и кости, то прибегают к обезболиванию. Как лечить метастазы онколог определяет после всех необходимых диагностических процедур.
Оперативное вмешательство производится в случае, если пошли тяжелые осложнения, такие как перелом, спинномозговая компрессия, потеря подвижности конечностей или паралич. Оперативным путем удаляются опухолевидные образования. Если необходимо восстановить структуру костей, устанавливаются поддерживающие штифты и пластины. Операцию показано делать при благоприятной картине заболевания и хорошем общем состоянии пациента. В иной ситуации рекомендуется для поддержки костей использовать приспособления для фиксации.
Для проведения операции остеосинтеза (сращения костей посредством сплавов металла) рекомендуется использовать титан, чтобы избежать металлоза – окисления металла и проникновения его частиц в мышечную ткань. При сильной деформации кости после удаления опухоли в некоторых клиниках пластический хирург проводит пластическую операцию на кость или эндопротезирование суставов.
Химиотерапия и лучевая терапия назначаются для уничтожения раковых клеток, предупреждения дальнейшего развития метастазов. Курс химии и облучения подготавливает пациента к операции и поддерживает после нее. Лучевой терапией называется просвечивание ионизирующим излучением, которое разрушает раковые клетки, либо введение препаратов стронций-89 или самарий-153. Постлучевые осложнения требуют реабилитации по окончанию курса.
* Только при условии получения данных о заболевании пациента, представитель клиники сможет рассчитать точную смету на лечение.
К бисфосфонатным препаратам относят:
Бисфосфанаты, содержащие азот:
- Алендронат;
- Памидронат;
- Ибандронат.
Бисфосфанаты, не содержащие азот:
- Тидронат;
- Клодронат;
Лекарства, содержащие азотистые соединения, обладают большим терапевтическим эффектом, нежели бисфосфонаты без азота.
Повышение иммунитета применяется в целях распознавания и борьбы с раковыми клетками. Препараты, повышающие иммунитет, увеличивают количество иммунных антител и повышают их способность распознать и убить раковые клетки.
Также в зависимости от локализации, опухоли в костях могут быть излечимы, поэтому среди пациентов с метастазами встречаются те, кто победил недуг. Вопрос о том, сколько осталось жить, ставится при уже необратимом процессе развития метастатических опухолей, когда разрушение костей непоправимо.
- Рак легких — полгода.
- Рак простаты — от 1 до 3 лет.
- Рак груди — от полутора до двух лет.
- Рак почек — 1 год.
- Рак кожи — полгода.
- Рак печени — от полугода до года.
- Рак предстательной железы — в случае гормонально зависимого заболевания — от 8 месяцев до полутора лет. В иных случаях — около 1 года.
- Миелома(опухоль и клеток плазмы в костном мозге) — от 2 до 3 лет.
- Рак щитовидной железы — 4 года;
Метастазы в кости менее опасны, чем метастазы в органы грудины и брюшной полости. Рекомендуется максимально понизить нагрузку на пораженные участки скелета, в зависимости от расположения метастазов использовать костыли, почаще лежать, носить поддерживающий корсет или головодержатель и не поднимать тяжести. Питание должно включать продукты, полезные для костей и общего иммунитета.
Можно ли вылечить метастазы в костях? Раннее обнаружение метастазов и строгое соблюдение назначенного врачом лечения и рекомендаций повышает шансы победить болезнь и спасти пациенту жизнь.
Анонимно. У подруги диагностировали сначала рмж, потом литические метастазы. Врач ей сказал, что с мтс живут долго, подруга ездит каждый месяц капать зомету и в целом чувствует себя хорошо.
Анонимно. Мне тоже врач сказал, что выживаемость при мтс в кости выше, чем если бы в органы. Было две химии, сейчас принимаю бисфосфонаты регулярно и продолжаю полноценно жить, поэтому не нужно отчаиваться.
Анонимно. Бабушка с метастазами 10 с половиной лет прожила, но боли были и несколько переломов, она активная, на месте не сидела. От болей принимала морфин.
источник
Метастазы в костях могут развиться абсолютно при любом злокачественном процессе, для некоторых раков это практически обязательная локализация, при других заболеваниях — редкость. В метастатическом рейтинге первое место по частоте встречаемости достанется метастазам в лёгкие, второе — печеночным очагам и третье — скелетным метастазам.
Метастазы в костях трудно лечатся и обещают боли, тем не менее, скелетные очаги менее прочих локализаций опухоли сокращают жизнь, но способны испортить её переломом или сдавлением спинного мозга.
По клинико-рентгенологическим признакам все костные очаги подразделяют на три группы:
- остеобластические — с преобладанием уплотнения сверх физиологической меры, но дополнительно наросшая опухолевая ткань не придаёт кости прочности и может сдавливать проходящие по соседству нервы;
- остеолитические — превалирует разрушение структуры и вероятность перелома увеличивается по мере разрастания рака;
- смешанные — сочетание двух видов и это ситуация встречается чаще всего.
Практически не случает такого, чтобы у пациента были исключительно остеолитические или только остебластические очаги, как правило, диагностируется сочетание с превалированием либо разреженной литической, либо избыточной бластической структуры.
Лидер среди всех злокачественных процессов, протекающих с метастатическим поражением скелета, миеломная болезнь — разрушение кости начинается в самом начале заболевания и в 100% клинических случаев отмечается множественная деструкция костной ткани.
При раке молочной и предстательной желёз у двух третей больных диагностируются скелетные метастазы, а патологоанатомические наблюдения выявляют вовлечение костей в злокачественный процесс практически у 90% пациентов. При раке молочной железы (РМЖ) превалируют смешанные и остеолитические варианты, при раке простаты — остеобластические.
Высокая частота метастазирования в кости отмечается при раке легкого, но при мелкоклеточном варианте — вдвое чаще и множественные костные дефекты, тогда как при немелкоклеточном — у 40% больных с тяготением к очагам единичным или солитарным, то есть единственному.
Каждый четвёртый, страдающий раком почки, имеет скелетные метастазы, при карциноме мочевого пузыря костные новообразования встречаются много реже.
При раке толстой кишки костное метастазирование выявляется у каждого восьмого больного, при раке желудка — не часто, поскольку раньше и обильнее рак поражает печень и брюшную полость. Рак кишечника тяготеет к мелкоочаговым и множественным вторичным образованиям.
При злокачественных процессах время появления метастазов в кости различается, тогда как скорость роста очага зависит исключительно от индивидуальных биологических характеристик опухолевой ткани, меняющихся под воздействием лечения и по мере раковой диссеминации.
При первичном обращении костные очаги при отсутствии других проявлений ракового процесса имеются едва ли у 20% пациентов, в подавляющем большинстве случаев опухолевое поражение костей признак диссеминации рака — распространения по системам или генерализации. При РМЖ, немелкоклеточной карциноме легких и раке толстой кишки именно так и происходит.
При раке предстательной железы нередко скелетная патология обнаруживается одновременно с опухолью простаты или в ближайшие сроки после диагностики неблагополучия в половой железе.
При карциноме почки часто сначала находят метастазы в костях и легочной ткани, а после обнаруживается первичная опухоль.
Локализация метастаза в кости определяется не нозологической принадлежностью первичной злокачественной опухоли, а функциональной нагрузкой и связанной с нею развитостью кровоснабжения. Множественные очаги в скелете более характерны для высоко агрессивного рака, единичные и тем более один метастаз свидетельствует в пользу благоприятного прогноза заболевания.
- Чаще всего вторичные отсевы рака возникают в обильно питаемых кровью губчатых костях — позвонках, причём преимущественно в испытывающих высокую нагрузку поясничных и грудных отделах позвоночника.
- Далее по частоте следуют метастазы в костях таза — почти половина всех случаев, типичные локализации — подвздошная и лонные кости.
- Вполовину реже отмечается метастазирование в костях черепа и нижней конечности, где превалирует поражение бедренной кости.
- Грудная клетка, преимущественно ребра и грудина, вовлекаются в злокачественный процесс практически в 30% случаев.
Вопреки сложившимся мифам, скелетное метастазирование часто протекает без выраженной боли и даже вовсе без симптомов. Остеобластические очаги реже сопровождаются болевыми ощущениями, нежели остеолитические.
Опасные проявления метастатического костного поражения:
- гиперкальциемия — значительное повышение концентрации кальция из-за разрушения костного матрикса приводит к тяжелейшему состоянию, требующему коррекции метаболизма фактически реанимационными мерами;
- перелом — для возникновения достаточно разрушения половины поперечника кости или позвонка, каждому одиннадцатому пациенту с патологическим переломом необходима срочная хирургическая помощь;
- синдром сдавления или компрессии спинного мозга осколками сломанного грудного или поясничного позвонка осложняется тяжелыми неврологическими нарушениями ниже зоны повреждения;
- нарушение двигательной активности вплоть до паралича возможно при сдавлении спинного мозга в шейном отделе остеобластическим очагом или повреждении отломками при литическом разрушении.
Осложнения метастазирования в кости фатально отражаются на состоянии пациента и активно мешают проведению адекватного лечения, что может сократить срок жизни при безусловном отсутствии качества.
Боль обусловлена тремя причинами:
- разрушением раковым конгломератом обильно иннервированной надкостницы;
- раздражением в надкостнице болевых рецепторов биологически активными продуктами жизнедеятельности раковых клеток;
- вовлечением в метастатический узел нервных окончаний мышц.
Невыносимая боль далеко не всегда связана со скелетным метастазированием, как правило, это следствие высокой агрессивности опухолевых клеток в терминальной стадии процесса, когда в крови огромна концентрация биологически активных веществ — цитокинов, которые буквально «жгут» нервные окончания даже не поражённых опухолью тканей.
При высокой степени злокачественности первичной опухоли болевой синдром отмечается чаще и более интенсивный. Наиболее наглядный пример, распространенные и постоянные боли в абсолютно целых костях при аденокарциноме легкого, операция с удалением пораженного легкого полностью излечивает боль.
Диагностика скелетных повреждений не сложная, но высокотехнологичная, начинают с изотопного обследования — остеосцинтиграфии, выявляющей минимальные раковые новообразования. Затем засвеченные изотопом «горячие очаги» подвергают рентгенографии или, что лучше, компьютерной томографии (КТ). ПЭТ — «королева» доказательств, к сожалению, дорогое исследование, поэтому для контроля эффективности терапии не очень подходит.
Для выявления очагов в скелете маркеры костной резорбции не подходят, в практической онкологии активного применения не нашли.
Анализы крови позволяют заподозрить опухолевое поражение костного мозга, что часто сопровождает метастазирование в грудину.
Можно ли вылечить метастазы в костях? Однозначно лечением можно продлить жизнь при хорошем самочувствии. С одной стороны, скелетные поражения — манифестация распространения рака по организму, с другой — признак относительно благоприятного прогноза заболевания при отсутствии опухоли в других тканях и висцеральных (внутренних) органах, что даёт годы жизни при стабилизации процесса.
На этапе костного метастазирования вопрос о радикальном лечении уже не стоит, но операция не исключается при благоприятной гистологической структуре и солитарном — единственном костном поражении. Так при раке легкого или почки с метастазом в плечевую кость или бедро можно выполнить одномоментное вмешательство с удалением больного органа и резекцией кости с протезированием, но после нескольких месяцев химиотерапии.
Химиотерапия — главный метод лечения костных поражений, лекарственная схема определяется первичной опухолью. При раке молочной и предстательной железы хорошие результаты демонстрирует гормональная терапия.
Дополнение химиотерапии локальным облучением позволяет повысить общий результат терапии, снять боль и уменьшить вероятность перелома. Так при поражении шейных позвонков лучевая терапия обязательна уже на первом этапе.
Операция необходима при угрозе сдавления (компрессии) спинного мозга поломанным позвонком, как правило, удаляется поражённая часть позвонка — ламинэктомия. При длительной — более полугода стабилизации в результате химиотерапии можно поставить вопрос об удалении поражённой кости конечности с заменой на протез, если больше нет других проявлений рака.
Использование бисфосфонатов при метастатическом поражении скелета стало стандартом адекватной терапии.
Человеческие кости постоянно обновляются: остекласты разрушают, а остеобласты наращивают ткани, в норме процессы уравновешены, в присутствии злокачественной опухоли остеокласты приобретают избыточную активность. Бисфосфонаты по своему строению схожи с костным матриксом, поэтому после введения в организм направляются в кости, где губительно действуют на активизированные раковыми продуктами остеокласты, параллельно снимая боль и оберегая от переломов.
Бисфосфонатами можно лечиться около двух лет, при утрате чувствительности к ним аналогичную роль выполняет моноклональное тело деносумаб. Демосумаб и бисфосфонаты относят к остеомодифицирующим агентам (ОМА).
Для назначения ОМА недостаточно выявления «горячих» очагов при остеосцинтиграфии, их применяют при доказанном рентгенологическими методами опухолевом поражении. Как каждое противоопухолевое средство эти препараты обладают токсичностью, в том числе могут привести к почечной недостаточности и некротическому разрушению челюсти.
Химиотерапия и ОМА — основные методы лечения скелетных поражений, но не единственные. Лечение костных метастазов должно быть комплексным, только комбинацией облучения и лекарств, с коррекцией метаболизма и присоединением паллиативной хирургии можно избавить от боли и вернуть пациенту активную жизнь.
Когда и что нужно и возможно в каждом конкретном клиническом случае онкологического заболевания знают специалисты нашей клиники. Узнайте больше, звоните:
источник
Метастазы в кость ─ это наиболее часто встречаемая локализация поражения при распространенном раке молочной железы (РМЖ). Нарушение скелетной анатомии и функциональности происходит за счет ростовых факторов опухолевых клеток. Ростовые факторы стимулируют активность остеокластов (многоядерные клетки огромных размеров, которые разрушают костную ткань). Частота костных метастазов при раке грудной железы достигает 65 – 75%.
Этапы метастазирования опухоли при прогрессировании заболевания:
- Прогрессирование первичной опухоли ─ раковые клетки взаимодействуют с микроокружением, образуются удаленные преметастатические ниши.
- Диссеминация (рассеивание и распространение) опухолевых клеток ─ раковые клетки мигрируют, агрессивно поражают ткани и выходят в кровяное русло.
- Оседание в костной ткани ─ случайное и беспорядочное их попадание и оседание в костной ткани, уклонение от иммунитета.
- Выживание раковой клетки ─ миграция атипичных клеток в специфичные ниши.
- Распространение опухоли и ангиогенез (образование новых кровеносных сосудов, питающих опухоль) ─ раковые клетки подчиняют клетки микроокружения и формируют собственную сосудистую систему.
- Прогрессия метастаза и прогрессирование заболевания в целом ─ опухоль становятся независимой от микроокружения.
Моделирование костной ткани осуществляется остеобластами и остеокластами (костные клетки). Опухоль стимулирует разрушение костной ткани остеокластами. Ростовые факторы усиливают развитие раковых клеток. Происходит дисбаланс физиологического процесса моделирования костей. Другие виды клеток, которые находятся в окружении, также могут влиять на развитие опухоли.
Ростовые факторы выделяются атипичными клетками. Они принимают участие и обуславливают все процессы образования опухоли:
- Факторы, образованные в костной ткани, стимулируют рост и миграцию опухоли.
- Факторы, образованные в самой опухоли, организовывают разрушение кости.
- Факторы, препятствующие образованию здоровой костной ткани.
- Факторы экспрессии молекул раковых клеток, которые способствуют обширному метастазированию.
Чаще поражаются «несущие» части скелета ─ бедренные и тазовые кости, позвоночник. Переломы приводят пациента к длительной инвалидности. Восстановление очень медленное. Продолжительный и устойчивый болевой синдром.
Важно! Угроза патологического перелома сохраняется даже в случае эффективной противоопухолевой терапии.
К клиническим проявлениям метастатической болезни относятся:
- деформация костей;
- гиперкальциемия ─ много кальция в крови;
- боль;
- нарушение опорной функции;
- патологические переломы;
- неврологические нарушения.
Рак молочной железы с метастазами в кости ─ это тяжелое состояние больных, сопровождаемое переломами. Дисфункциями систем и органов, вызванными гиперкальциемией фиксируется в 65% случаев.
Высокий кальций встречается в 7 – 15% случаев. Сопровождается такими симптомами, как сухость во рту, постоянная жажда, запоры, рвота, полиурия (увеличение суточной нормы выделяемой мочи). В тяжелых случаях наблюдается развитие острой почечной недостаточности, потеря сознания.
Сверхсильные боли ─ частое осложнение при распространенных опухолях (42 – 95% случаев). Причины болевого синдрома:
- Раковые клетки выделяют химические вещества, которые стимулируют болевые рецепторы.
- За счет увеличения опухолевой массы повышается внутрикостное давление.
- Растяжение надкостницы и микропереломы.
- Реактивное мышечное сокращение.
- Проникновение раковых клеток в нервные окончания.
- Сдавление нервов.
Боль бывает острая и хроническая. Острая или «прорывная» боль характеризуется внезапным приступом. Хроническая ─ постоянная, пульсирующая, изнуряющая, усиливается при прогрессировании.
Еще одно осложнение ─ это декомпрессия спинного мозга, встречается в 3% случаев.
Можно ли полностью излечить заболевание с метастазами?
Цель лечения ─ это подавление опухоли, предотвращение осложнений (компрессия тканей, переломы), восстановление утраченных функций, улучшение качества жизни.
Терапия РМЖ с метастазами в кость направлена на системное лечение основного заболевания. А также на замедление разрушения костной ткани и ускорение ее восстановления. По показаниям назначается:
- лучевая терапия;
- хирургическое вмешательство;
- ортопедическое лечение;
- наркотические препараты для снятия боли.
Бисфосфонаты являются стандартом лечения при РМЖ. Они останавливают развитие метастазов в кость, оказывают профилактическое и терапевтическое действие на остеопороз, который является следствием онкологического заболевания.
Применение бисфосфонатов значительно:
- увеличивает время до первого костного осложнения;
- снижает риск развития гиперкальциемии;
- уменьшает количество используемых наркотических анальгетиков;
- сокращение показаний к проведению лучевой терапии костей;
- улучшает результаты комплексного лечения и выживаемость.
Женская онкология имеет тенденцию к омоложению. Заболевание встречается у женщин в возрасте от 30 лет. Если есть метастазы в костях при раке молочной железы, вопрос, сколько живут, становится актуальным.
Насколько качественно будут жить пациенты, их активность и жизнедеятельность зависят от течения заболевания и адекватной терапии. Значительно затрудняют специфическое лечение и негативно влияют на выживаемость осложнения. Пятилетняя выживаемость отмечается у 20%. Медиана (усредненный показатель) составляет 24 месяца.
источник
Метастазы рака молочной железы в кость. Многие считают рак молочной железы заболеванием, поражающим только женщин. Однако в редких случаях он может развиваться и у мужчин.
Статья на конкурс «био/мол/текст»: Диагностирование рака молочной железы с метастазами в костях — это событие, которое меняет жизнь пациента. Как правило, такую патологию невозможно вылечить, но можно контролировать с помощью постоянного лечения. Что же происходит с костями при метастазировании? Какие методы терапии использует современная медицина?
Эта работа опубликована в номинации «Свободная тема» конкурса «био/мол/текст»-2018.
Генеральный спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.
Спонсором приза зрительских симпатий выступил медико-генетический центр Genotek.
В 1889 году британский врач Стивен Педжет описал концепцию «семена и почва». Согласно его теории, опухолевые клетки распространяются по организму не случайным образом, а требуют взаимодействия с микросредой органа-хозяина. Злокачественные клетки, или «семена», атакуют только подходящие для роста органы, то есть «почву». Таким образом, очаги роста опухоли в новых органах (метастазы) будут развиваться только тогда, когда определенные «семена» будут высажены на пригодную для них «почву».
Педжет обнаружил, что у женщин с раком молочной железы (РМЖ) метастазы развивались с гораздо большей вероятностью в костях, чем в любых других органах [1].
Наш обзор посвящен метастазам РМЖ в кость, изменениям, которые вызывают опухолевые клетки в кости, а также современной терапии таких метастазов.
Рак молочной железы — злокачественная опухоль железистой ткани молочной железы. Это наиболее распространенная злокачественная опухоль у женщин, а по числу заболевших среди мужского и женского населения она занимает второе место после рака легких. В 2018 году было зарегистрировано более двух миллионов новых случаев [6].
Рисунок 1. Очаги возникновения вторичной опухоли при РМЖ. Первоначально опухоль развивается в груди. Однако по мере роста опухоли раковые клетки отрываются и распространяются по соседним тканям или отправляются в отдаленные органы, такие как легкие. Однажды в другой ткани они могут образовать вторичную опухоль.
Современная медицина разработала эффективные способы лечения РМЖ 1–3 стадии, что значительно увеличило выживаемость пациентов [7]. Однако 9 из 10 смертей от РМЖ обусловлены нарушением функций различных органов, вызванным распространением раковых клеток по организму, то есть метастазированием. Как правило, РМЖ может распространяться на кости, головной мозг, легкие, печень и лимфатические узлы (рис. 1). Согласно статистическим исследованиям, самой частой областью метастазирования является кость [8]. Она — преобладающее место развития метастазов люминального и Her2-позитивного типов РМЖ, при этом существенно менее предпочитаемое метастазами трижды негативного типа РМЖ [9].
На ранних стадиях метастазы РМЖ в костях бессимптомны, в результате их трудно выявить. Однако всем пациентам с РМЖ раз в несколько месяцев проводят биохимический анализ крови и биопсию для обнаружения рецидива заболевания. Для диагностирования метастазов в кости необходимо пройти рентгенографию, компьютерную томографию, магнитно-резонансную томографию, сцинтиграфию [8].
Кость — это динамическая ткань, играющая центральную роль в поддержании гомеостаза всего организма. Основными элементами кости считаются остеобласты, которые участвуют в создании и минерализации кости, остеокласты, обеспечивающие разрушение (резорбцию) костной ткани, и остеоциты, поддерживающие структуру (рис. 2). Все эти клетки костной ткани ответственны за «строительные работы»: поглощение старых клеток кости и порождение новых. Они существуют в равновесии и регулируют работу друг друга, что помогает обеспечить гомеостаз кости. Сбалансированный цикл образования и разрушения костной ткани называют добродетельным циклом (от англ. virtuous cycle) ремоделирования костей [10].
Рисунок 2. Костные клетки. В костной ткани обнаружены четыре типа клеток. Недифференцированные остеогенные клетки могут развиться в остеобласты. Когда остеобласты попадают в кальцинированную матрицу, их структура и функции меняются, и они становятся остеоцитами. Остеокласты по внешнему виду отличаются от других клеток костной ткани.
Кость также содержит красные клетки костного мозга и эндотелиальные клетки, которые образуют капилляры сосудистой системы кости [11].
Все типы клеток разделяют один «дом», следовательно, они взаимодействуют между собой и регулируют функции друг друга. Однако сосудистая система кости направляет метастазирование раковых клеток в эту микросреду [12].
Одиночные клетки могут оторваться от исходной опухоли в груди и распространиться по организму двумя способами: гематогенным (по кровеносным сосудам) и лимфогенным (по лимфатическим сосудам). Лимфогенные метастазы поражают соседние и отдаленные лимфатические узлы, а гематогенные чаще появляются в костном мозге и костях (рис. 3). Более подробно об образовании гематогенных метастазов рассказывает статья «Обнаружены организаторы побега раковых клеток из первичного очага» [13].
Рисунок 3. Схематическое изображение распространения раковых клеток по кровеносной системе.
Как только клетки РМЖ достигают кости, они создают перекрестные помехи в слаженной работе костных клеток. Раковые клетки врываются в добродетельный цикл и приводят к дисбалансу в сторону резорбции кости. В результате возникает порочный цикл (от англ. vicious cycle).
При определенных условиях раковые клетки отделяются от опухоли и становятся мигрирующими. Они интравазируют в соседние кровеносные сосуды и распространяются по организму, в кровотоке клетки могут попасть в ловушку и экстравазировать. При их выходе в подходящую ткань начинается рост вторичной опухоли.
Даже на ранних этапах РМЖ опухолевые клетки могут мигрировать в костный мозг. Они могут бездействовать долгое время и вызвать рецидив спустя годы .
Процесс ремоделирования костной ткани состоит из пяти основных этапов: покоя, активации, резорбции, реверсии, формирования (рис. 4). В каждом этапе участвуют разные типы клеток кости [15].
Рисунок 4. Ремоделирование кости. Состоит из пяти фаз: 1) фаза покоя — остеоциты неподвижны; 2) фаза активации — дифференцировка остеокластов из преостеокластов; 3) фаза резорбции — разрушение кости остеокластами; 4) фаза реверсии — дифференцировка остеобластов; 5) фаза формирования — остеобласты создают и минерализуют кость.
Межклеточный матрикс на 85–90% состоит из коллагеновых волокон, которые обеспечивают структурную поддержку минерализации кости. Остальная часть — это протеогликаны, карбоксилированные белки, клеточные адгезивные белки и факторы роста.
Остеобласты образуются из мезенхимных стволовых клеток. Во время своей работы они выделяют в костный матрикс смесь факторов роста и белков, образуя специфическую микросреду. Затем они подвергаются запланированной клеточной гибели или дифференцируются в остеоциты (рис. 5).
Рисунок 5. Схема дифференцировки остеобластов, остеоцитов. Остеобласты начинают дифференцироваться из мезенхимных стволовых клеток в костном мозге.
Остеобласты выделяют факторы роста кости, включая трансформирующий фактор роста β (TGF-β), инсулиноподобные факторы роста (IGF), факторы роста фибробластов (FGF), интерлейкины, тромбоцитарный фактор роста (PDFG). Эти факторы остаются внутри костного матрикса и высвобождаются после деградации кости. Этот процесс обеспечивает обратную связь между формированием и резорбцией кости [11].
Остеокласты — фагоциты для кости — дифференцируются из линии моноцитов/макрофагов (рис. 6). Активированные остеокласты собираются на поверхности кости и присоединяются к ней через специальные рецепторы. Они подкисляют микроокружение на границе кость—остеокласт и секретируют ферменты, участвующие в деградации: протеазы, коллагеназу и щелочную фосфатазу.
Рисунок 6. Схема дифференцировки остеокластов. Остеокласты — гигантские многоядерные клетки, дифференцируются из гемопоэтических стволовых клеток линии моноцитов/макрофагов костном мозге.
Развитие зрелых остеокластов — это многоступенчатый процесс, который регулируется сложной системой цитокинов и взаимодействием внутри стромы кости. Соседние стромальные клетки и остеобласты продуцируют колониестимулирующий фактор макрофагов (M-CSF), который действует через рецептор колониестимулирующего фактора 1 (c-FMS) на многоядерных предшественниках, и активируют экспрессию рецептора RANK (рис. 7). Его лиганд, RANKL, так же, как M-CSF, синтезируется остеобластами и стромальными клетками в ответ на действие паратиреоидного гормона (PTH). RANKL — цитокин из семейства факторов некроза опухоли. Связываясь со своим рецептором, он активирует ряд важных факторов, которые регулируют экспрессию генов остеокластов. Это создает условия для финальной дифференцировки, слияния предшественников и функционирования возникших многоядерных остеокластов. Активированные остеокласты разрушают кость и высвобождают TGF-β и другие факторы роста кости, усиливающие пролиферацию остеобластов [11].
Рисунок 7. Модель нормального костного ремоделирования. Кость постоянно реконструируется. Этот процесс требует взаимодействия костеобразующих остеобластов и костеразрушающих остеокластов. Подробности в тексте.
Остеобласты продуцируют остеопротегерин (OPG) — цитокин из семейства факторов некроза опухоли. Он связывается с RANKL, ингибируя взаимодействие RANK—RANKL, и, следовательно, подавляет остеокластогенез и резорбцию кости. Взаимодействие RANK—RANKL—OPG помогает поддерживать добродетельный цикл.
Переключение между добродетельным и порочным циклами связано с деятельностью раковых клеток. Они нарушают баланс костного микроокружения несколькими способами: стимулируют рост и устраняют физический барьер, то есть минерализованную костную матрицу (рис. 8).
Рисунок 8. Порочный цикл костного метастаза РМЖ. В костях клетки РМЖ секретируют факторы (фиолетовые стрелки), которые нарушают дифференцировку и активность остеобластов, увеличивают продукцию RANKL, усиливая образование остеокластов. На остеокласты они влияют и непосредственно. Зрелые остеокласты разрушают в кость, тем самым высвобождая внедренные в костный матрикс факторы роста. Они, попадая в опухолевое микроокружение, способствуют росту опухоли (красная стрелка). Тот же эффект дают факторы, выделяемые остеобластами и остеоцитами (синяя стрелка).
Традиционно костные метастазы делят на две категории: остеолитические и остеобластные. Остеолитические поражения чаще всего встречаются при РМЖ и характеризуются чрезмерной активацией остеокластов. При этом доминирующий процесс в кости — разрушение. Остеобластные поражения чаще встречаются при раке предстательной железы и характеризуются чрезмерной активацией остеобластов.
Однако в последние годы стало ясно, что разделение костных метастазов на чисто остеолитические или остеобластные неправильно, так как примерно у 20% пациентов с метастазами в кости, возникающими из опухолей молочной железы, поражение смешанное [18].
В этом обзоре мы более подробно рассмотрим механизм остеолитического поражения костной ткани.
В резорбции костной ткани участвуют остеокласты, деятельность которых находится под контролем целого ряда клеток костного мозга. Опухолевым клеткам необходимо препятствовать такому контролю и продуцировать собственные факторы, регулирующие активность остеокластов. Ключевым участником является TGF-β, который активирует рост опухоли и подавляет иммунную систему. TGF-β индуцирует синтез белка, связанного с паратиреоидным гормоном (PTHrP), и интерлейкина 11, которые стимулируют активацию остеокластов. В случае с PTHrP это обусловлено его способностью связываться с рецептором РТН и изменять соотношение RANKL/OPG в пользу RANKL [16].
Опухолевые клетки также продуцируют факторы, ингибирующие дифференцировку остеобластов, а значит, подавляют формирование костей [19].
Таким образом, при метастазировании РМЖ опухолевые клетки усиливают резорбцию кости путем прямого секретирования RANKL, что приводит к высвобождению биоактивных молекул. Эти продукты деградации вовлечены в регуляцию добродетельного цикла и стимулируют рост опухоли в случае развития метастаза в кости. Например, кальций — это первый продукт, выделяющийся при разрушении костного матрикса. Опухолевые клетки экспрессируют на своей поверхности кальций-чувствительные рецепторы, которые реагируют на повышение уровня кальция и стимулируют рост опухоли [20].
При метастазах РМЖ костная ткань резорбируется преимущественно собственными нормальными клетками. Прямая деградация костной ткани опухолью встречается редко. Метастатические клетки РМЖ способны продуцировать коллагеназу и другие ферменты, разрушающие кость [21], [22].
Остеобласты проходят сложный многоступенчатый процесс дифференцировки. Все клетки на разных стадиях дифференцировки играют определенную роль в добродетельном/порочном циклах.
Первый этап дифференцировки представлен преостеобластами, которые находятся в стенках гаверсовых и фолькмановских каналов. Для незрелых остеобластов характерна высокая производительность RANKL. При костных метастазах они могут стимулировать остеолиз [20], [21]. Некоторые источники сообщают, что RANKL может стимулировать пролиферацию вторичной опухоли РМЖ в кости [23], [24].
В присутствии раковых клеток преостеобласты усиливают производство провоспалительных цитокинов, таких как интерлейкин-6, моноцитарный хемотаксический белок, фактор некроза опухоли α, макрофагальный воспалительный белок 2 и др. Эти молекулы помогают поддерживать опухолевые клетки и также являются остеокластогенными.
Зрелые остеобласты, в отличие от преостеобластов, расположены на поверхности эндотелия. Во время формирования кости они выделяют биологически активные вещества, которые проявляют свою функцию только после высвобождения из разрушающейся костной матрицы. Среди этих молекул есть факторы, которые стимулируют рост опухоли и неоангиогенез — формирование новых микрососудов для питания опухоли [11]. В конце концов остеобласты дифференцируются в остеоциты или подвергаются апоптозу .
Гибель остеобластов — это не случайное событие, а строго регулируемый процесс, необходимый для обеспечения определенного размера и архитектуры кости. Метастазирующая опухоль РМЖ способна вызывать апоптоз остеобластов, продуцируя индукторы апоптоза [11]. Однако влияние апоптотических остеобластов на добродетельный и порочный циклы описано плохо.
Опухолевые клетки также могут выделять вещества, активирующие остеобласты. В настоящее время факторы, ответственные за этот процесс, не совсем ясны. Основная роль отводится эндотелину-1 (ЕТ-1). Этот фактор секретируется клетками РМЖ и рака предстательной железы и стимулирует возникновение остеобластных метастазов. В результате может начаться процесс ненормального костеобразования [26]. Кости быстро растут, становятся утолщенными, жесткими, негибкими.
Последний этап дифференцировки остеобластов представлен остеоцитами. Они локализованы в костном матриксе, что делает их идеальными регуляторами ремоделирования кости. Однако это же преимущество становится недостатком при развитии костных метастазов, поскольку они способны подпитывать порочный цикл.
Остеоциты — важные продуценты RANKL. Также они могут контролировать метастатический рост, секретируя факторы, некоторые из которых активируют пролиферацию раковых клеток молочной железы [16].
Пациент с костными метастазами испытывает мучительную сильную боль, у него повышается риск переломов, качество жизни катастрофически снижается. Терапия метастазов РМЖ в кости включает в себя различные методы, которые могут влиять как на саму опухоль, так и на ее микроокружение [11].
Чаще всего метастатический РМЖ возникает через несколько месяцев или лет после завершения лечения раннего рака. Риск возникновения вторичной опухоли после лечения РМЖ варьирует от человека к человеку. Но это сильно зависит от характеристики раковых клеток, стадии первичной опухоли, способов лечения. Например, в течение 15 лет вторичная опухоль в кости возникает у примерно 30% пациентов с HER2-позитивным и у 15% — с трижды негативным РМЖ [9].
Наиболее агрессивной вторичной опухолью считается метастатический трижды негативный РМЖ. Он часто поражает пациенток молодого возраста. С таким типом метастазов продолжительность жизни пациентов может не превысить и 6 месяцев [27].
В настоящее время метастатический РМЖ нельзя излечить. Однако это не означает, что его нельзя лечить. Терапия метастазов РМЖ в кости направлена на увеличение продолжительности и качества жизни. Современные методы лечения в США позволяют продлить жизнь 35% таких пациентов по меньшей мере на пять лет, а некоторые пациенты могут прожить 10 и более лет после постановки диагноза [27].
До начала лечения врач объясняет, какие поправки нужно внести в диету и образ жизни пациента. Во-первых, необходимо принимать достаточное количество кальция и витамина D, во-вторых, регулярно выполнять физические упражнения. Соблюдение этих правил позволит пациенту сохранить кости крепкими и минимизировать проявления остеопороза [28].
Тактику лечения врач определяет индивидуально для каждого пациента в зависимости от:
- типа и локализации первичной опухоли;
- количества и расположения вторичных опухолей в кости;
- наличия метастазов в других органах;
- возраста и общего состояния больного;
- предыдущего лечения;
- побочных эффектов.
В лечении костных метастазов можно выделить два основных подхода:
- системную терапию, которая направлена на лечение первичной опухоли;
- местную терапию, которая должна облегчить боли пациентов и уничтожить вторичную опухоль [27].
Системная терапия включает в себя гормональную терапию, химиотерапию и таргетную терапию.
Гормональная, или эндокринная, терапия — основной способ лечения пациентов с метастатическим РМЖ, положительным по эстрогеновым/прогестероновым рецепторам. Такой способ лечения подразумевает, что лекарственный препарат блокирует действие эстрогена или прогестерона либо снижает их концентрацию в организме. Это может замедлить рост и деление опухолевых клеток.
Существуют различные факторы, позволяющие определить, какой вид гормональной терапии подходит пациенту. К ним относится эффективность и безопасность доступных видов лечения, предшествующая терапия (в том числе гормональная), но в первую очередь — нахождение пациентки в пременопаузе или постменопаузе. Для женщин в пременопаузе гормональная терапия начинается с подавления функции яичников, чтобы остановить производство гормонов. В постменопаузе яичники уже не функционируют, и эстроген производится в жировой ткани и надпочечниках; в этом случае используют ингибиторы ароматаз [27].
Если первый препарат гормональной терапии перестает работать, то назначают второй, и т.д. В какой-то момент — может, через несколько месяцев или лет — гормональная терапия перестает вызывать ответ, и тогда рекомендуют переключиться на химиотерапию.
Побочные эффекты эндокринной терапии зависят от вида лечения и могут включать в себя мышечные боли, чувство усталости, легкую тошноту. К серьезным побочным эффектам относят повышение риска инсульта, рак матки, потерю прочности костей [29].
Химиотерапия — это первый этап лечения метастазов РМЖ, если первичная опухоль HER2-положительная и не имеет рецепторов к эстрогену/прогестерону. К химиотерапии обращаются и когда гормональная терапия перестает действовать [27].
Химиотерапевтические препараты, например 5-фторурацил, капецитабин или метотрексат, попадая в кровоток, разносятся по всему организму, уничтожая любые быстрорастущие клетки, в том числе и здоровые.
На выбор вида химиотерапии влияют агрессивность и быстрота роста раковых клеток, предшествующие варианты химиотерапии, побочные эффекты и т.д. [28].
Как и при гормональной терапии, если первый препарат или комбинация препаратов перестали действовать, и опухоль начинает расти, переходят на второй, третий и т.д. препараты. С каждым таким переходом шансов на уменьшение размеров опухоли становится всё меньше.
Побочные эффекты зависят от вида лекарства. К наиболее частым относят усталость, анемию, выпадение волос, тошноту и рвоту, а к самым серьезным — поражения сердца, легких, почек, вероятность возникновения другого вида рака. Пациентам могут назначать лекарственные средства, которые предотвращают или уменьшают выраженность побочных эффектов. Например, некоторые химиотерапевтические препараты повреждают ДНК, и для ее репарации и снижения вероятности возникновения устойчивости к химиотерапии назначают поли(AДФ-рибоза)-полимеразы (PARP) [28].
Таргетная, или молекулярно-таргетная, терапия — активно развивающееся направление лечения рака. Она блокирует рост раковых клеток за счет вмешательства в конкретный молекулярный механизм канцерогенеза.
Таргетная терапия используется как системный подход для лечения костных метастазов РМЖ. Она применяется либо в виде монотерапии, либо в сочетании с гормональной или химиотерапией.
Для лечения положительных по эстрогеновым/прогестероновым рецепторам и HER2-негативных метастазов РМЖ используют ингибиторы киназ CDK4 и CDK6. Ингибиторы CDK4/6 предназначены для прерывания роста опухолевых клеток. FDA одобрило три препарата на их основе: рибоциклиб, палбоциклиб, абемациклиб. Первый из них в начале 2018 года одобрил и Минздрав России.
Для увеличения эффективности эндокринной терапии положительных по гормональным рецепторам и HER2-негативных метастатических опухолей используют ингибиторы mTOR [27].
Для лечения HER2-позитивного метастатического рака активно применяют ингибиторы тирозинкиназы, такие как лапатиниб [27].
Многие таргетные методы лечения относятся к иммунотерапии. Иммунотерапия — это новейший, действенный и перспективный метод лечения многих форм рака. В последнее время ее применяют и для лечения костных метастазов.
Есть два способа действия: усиление иммунной системы, чтобы организм сам боролся с раком, и использование белков, уничтожающих раковые клетки. Иммунотерапия рака предполагает введение в организм противоопухолевых биопрепаратов: цитокинов, моноклональных антител или опухолевых вакцин. Ее используют и в системном, и в местном лечении вторичных опухолей при РМЖ.
Иммунотерапия в качестве системного подхода применяется в лечении HER2-позитивного РМЖ. Опухолевые клетки этого типа выставляют на своей поверхности большое количество рецепторного белка HER2, который важен для их роста. И для лечения используют антитела, которые блокируют внутриклеточные сигналы синтеза этого белка или вмешиваются в его работу. К таким моноклональным антителам относятся трастузумаб и пертузумаб [27].
Побочные эффекты таргетной терапии зависят от вида лекарственного средства. Однако для всех них типичны тошнота, рвота, диарея и слабость. К серьезным побочным эффектам можно отнести снижение сердечной функции и заболевания печени, например гепатит [28].
Местную, костно-таргетную терапию в сочетании с системной рекомендуют всем пациентам с костными метастазами РМЖ. К ней относят использование бисфосфонатов и деноcумаба, лучевую терапию и хирургические вмешательства. Выбор между этими видами лечения зависит от размера метастазов, осложнений, предпочтений пациента.
Бисфосфонаты — это стандартная терапия, используемая для уменьшения боли в костях, снижения темпов метастазирования, предотвращения потери костной массы и значительного улучшения качества жизни пациентов.
Рисунок 9. Формула бисфосфоната
Бисфосфонаты представляют собой молекулы, состоящие из двух фосфонатных групп, соединенных атомом углерода (рис. 9). Такая химическая конфигурация позволяет им с высокой степенью сродства связываться с гидроксиапатитной составляющей кости. Дополнительные функциональные группы, присоединенные к центральному атому углерода, придают бисфофонатам различные фармакологические свойства [7].
Бисфосфонаты вводят в организм перорально или путем инфузий. Основной механизм их действия заключается в ингибировании резорбции кости, поскольку после эндоцитоза они стимулируют апоптоз остеокластов. Это разрывает порочный круг сигналов между остеокластами и раковыми клетками в кости [16].
Применение бисфосфонатов может сопровождаться гриппоподобными симптомами и гипокальциемией. Эти препараты обладают выраженной нефротоксичностью и противопоказаны при низком клиренсе креатинина. Их применение, в особенности золедроновой кислоты, повышает риск остеонекроза челюстей.
У пациентов с метастатическим РМЖ радиотерапию используют как способ облегчения боли и профилактики осложнений [33].
Машина фокусирует ионизирующее излучение на метастазах в кости. Облучение, длящееся всего несколько минут, уничтожает раковые клетки.
Побочные эффекты зависят от облучаемого места. К наиболее распространенным последствиям лучевой терапии относятся раздражение кожи и чрезмерная утомляемость [28].
Для радиотерапии могут использоваться и так называемые радиофармацевтические препараты. Обычно это радиоизотопы щелочно-земельных металлов (стронций-89, самарий-153). Их можно избирательно доставлять прямо к метастазу. Во-первых, они могут самостоятельно накапливаться в зонах повреждения кости (как «имитаторы» кальция). Во-вторых, радиоизотопы можно конъюгировать с лигандами, обеспечивающими их направленную доставку в кость [29], [34]. В области костных метастазов исходящее от препарата излучение «убивает» рак.
Препарат усиливает местный эффект лучевой терапии, облегчает боль, иногда сокращает потребность в дальнейшей радиационной терапии.
К основным недостаткам использования радиоизотопов относится уменьшение содержания в крови тромбоцитов и лейкоцитов [28].
Хирургическое вмешательство у пациентов с метастазами в кости проводится редко. Основное показание для него — патологический перелом [7]. С помощью хирургии также можно стабилизировать слабую кость путем вставки винтов, стержней и т.д.
Рисунок 10. Механизм действия деносумаба. Высокоаффинное связывание деносумаба с RANKL ингибирует созревание и активность остеокластов, предотвращая взаимодействие RANKL с рецептором RANK на зрелых и незрелых остеокластах.
Иммунотерапией при местном лечении костных метастазов РМЖ можно назвать применение деноcумаба.
Деноcумаб — человеческое моноклональное антитело (IgG2), которое специфично связывается с RANKL. В результате не образуется связи RANKL—RANK (рис. 10). Лечение денозумабом предотвращает производство остеокластов и, следовательно, останавливает резорбцию кости [7].
На фоне применения деносумаба часто развиваются суставные и мышечные боли, гипокальциемия, инфекционные заболевания [35].
Сейчас ведется разработка средств для лечения метастатического рака молочной железы, нацеленных на новые мишени. Мишенями могут стать катепсин К, TGF-β, PTHrP, хемокиновые рецепторы и т.д. [30], [34]. Эти молекулы играют важную роль в порочном цикле, следовательно, воздействие на них может остановить рост вторичной опухоли или разрушение кости. Перспективным препаратом остается и деносумаб. Показано, что он улучшает минеральную плотность костей [20]. Однако из-за сложности механизмов костного метастазирования возникает необходимость комбинирования лекарственных препаратов, нацеленных на разные мишени.
Следующая задача состоит в том, чтобы разработать для каждого пациента индивидуальное лечение, предсказывая возможный клинический исход. Геномное и протеомное профилирование имеет прогностический потенциал, коррелирующий с прогрессированием заболевания. Такое профилирование может прогнозировать и исход лечения тем или иным препаратом. В будущем подобные технологии помогут отбирать пациентов, находящихся в группе риска возникновения метастатического РМЖ, и исключать ненужное лечение [20], [21].
Таким образом, РМЖ с метастазами в костях — это уже не приговор. Но, к сожалению, лечение такого рака — сложный, выматывающий процесс. Разумеется, говорить о 100% излечении пока невозможно. Однако использование стандартных терапевтических методов совместно с новыми подходами способно продлить жизнь пациентам и улучшить их состояние, то есть игра всё же стόит свеч.
Важно запомнить, что рак — это не паразит, который колонизирует и разрушает здоровые ткани. Это «умная» группа клеток, которая взаимодействует с нормальными клетками хозяина и использует важные тканевые сигналы ради собственного благополучия.
источник