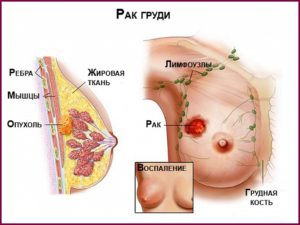
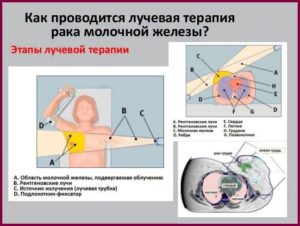
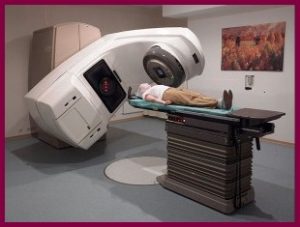
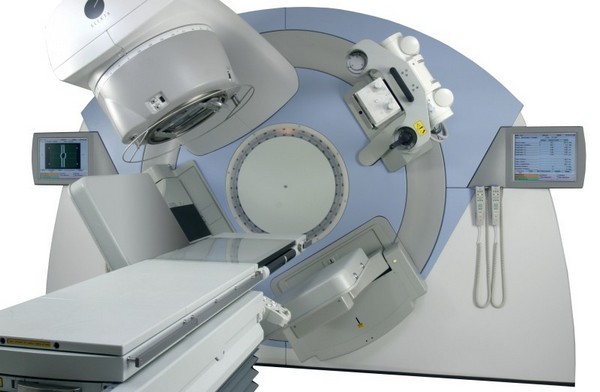
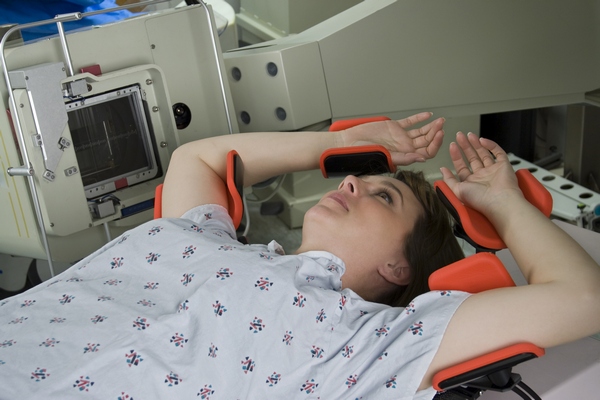
Здравствуйте дорогие читатели. Сегодня наша статья посвящена одному из методов, нацеленных на «добитие» раковых клеток после оперативного удаления основного их ядра. Итак, что такое лучевая терапия (ЛТ), и к каким результатам она приводит.
Лучевая терапия при раке молочной железы после операции используется для повышения выживаемости пациента, так как оставшиеся после «грубого» вмешательства скальпеля «отломки» опухоли подвергаются губительному воздействию корпускулярного или волнового излучения.
К корпускулярным типам относят:
- α и β — частицы;
- нейтронное;
- ионы углерода;
- протонное,
К волновому относят γ и рентген-излучение.
Метод предусматривает не разрушение опухолевых клеток, как думают многие, то есть некроз, что было бы очень печально для организма и привело бы его неминуемому отравлению, а инактивацию раковых клеток.
Инактивация в данном случае — это прекращение деления атипичной клетки, разрушение связей на уровне молекулы из-за:
- ионизации атомарной структуры ДНК;
- радиолиза воды в жидкой части патологической клетки.
Радиолиз означает, что вода в цитоплазме клетки формирует перекись и свободные радикалы, воздействующие на структуру ДНК.
Повреждает ли здоровые клетки такая терапия? Конечно. Облучение можно использовать потому, что оно наиболее действенно в отношении быстро делящихся и стремительно растущих клеток. Такими качествами обладают:
- раковые клетки;
- нормальные клетки красного костного мозга.
Направленное излучение сильнее повреждает раковые клетки, как активно растущие. Окружающие здоровые ткани тоже пострадают, но меньше. Во-первых, благодаря «прицельности» облучения здоровые ткани страдают в небольшом объеме. Во-вторых, даже подвергаясь той же дозе излучения, здоровые ткани (если это не костный мозг) повреждаются меньше, чем раковые клетки. Тем не менее им понадобиться некоторый период на восстановление.
Лучевая терапия в зависимости от времени ее проведения делится:
- на адъювальную (постоперационную);
- неадъювадьную (предоперационную) или индукционную.
Адъювадьное лечение нацелено на предотвращение рецидива болезни. Женщинам после органосохраняющей операции на молочных железах часто назначается ЛТ для предотвращения рецидива.
Неадъювальная терапия проводится до операции. Ее цель облегчить проведение процедуры для врача, снизить скорость роста опухоли на период подготовки к операции и повысить выживаемость пациента.
В лечении онкобольных применяют терапию:
- контактную (брахивальную);
- дистанционную;
- радионулкидную.
В первом случае облучается непосредственно опухоль. То есть источник излучения прикладывается к опухолевым тканям:
- интраоперативно;
- на поверхностную опухоль;
- в интерстициальную (закрытую тканями) опухоль в виде игл, шариков и т.п.
Метод щадящий, но на практике применяется редко. Дистанционное воздействие имеет больше побочных эффектов. Проводится сквозь здоровые ткани ради разрушения глубоко лежащих опухолей. Этот метод самый распространенный. Он универсальный и его можно использовать при разных новообразованиях.
В его рамках разрабатывается перспективная протонная терапия, позволяющая целенаправленно уничтожать именно рак на любой глубине. Вся доза выделяется в «теле» опухоли на последнем миллиметровом «рывке» пробега частиц. Окружающие ткани страдают минимально. Недостатком метода является его дороговизна (нужен дорогой циклотрон).
Последний метод предполагает введение радионудлида или составного фармпрепарата в сосуд или через рот. Радионуклид накапливается в опухолевых тканях и разрушает его.
ЛТ может быть элементом комплексного лечения и использоваться после химиотерапии или совместно с ней. Иногда такого курса достаточно, и можно избежать оперативного вмешательства.
Для лечения опухолей локализующихся вне молочной железы могут использоваться и другие методы ЛТ (РТМИ, РТВК, стереотаксическая радиохирургия).
В ЛТ входит предлучевой этап (выбор дозы, подготовка к облучению), лучевой и постлучевой. Лучевой этап после операции длится 14-21 день, при самостоятельном лучевом лечении курс пролонгируется до 4-6 недель.
Обычно сеансы проводят ежедневно пять дней подряд с интервалом в два дня ради восстановления тканей. Постлучевой этап начинается сразу после окончания процедур. Этот период требует щадящего режима, правильного питания и позитивного эмоционального настроя.
Лечение рака молочной железы обычно предполагает постоперационную ЛТ. Такое лечение должно уничтожить очажки неоплазии, оставшиеся после операции. Если у вас есть метастазы, цель ЛТ — уменьшение размера опухолевого очага и уменьшения боли при развитии рака.
Питание при ЛТ своеобразное:
- дробное;
- полноценное;
- высококалорийное;
- витаминизированное;
- с достаточным количеством минералов.
Пить нужно при лучевом лечении много, порядка 3 литров, включая соки, витаминные чаи, минеральную воду.
При ЛТ нельзя курить или принимать алкоголь. Вредные привычки при раке вообще противопоказаны. Также стоит убрать из своего рациона всевозможные сласти. Косметика и парфюмерия в период лечения могут полежать на полочке. Когда принимаете душ, не заливайте водой места облучения и не используйте мыло. Оно сушит кожу.
Если ткани в месте облучения зудят и краснеют, обратитесь к врачу. Не нужно самостоятельных мер (приложения холодных примочек или смазывания мазями). Носите одежду из натуральных тканей, свободного покроя, избегая трения облучаемых мест. Участки, подверженные облучению, нужно защищать от прямого солнечного света.
В процессе лечения, не пренебрегайте обычными рекомендациями для выздоравливающих: гуляйте, полноценно спите. Умеренная физическая активность вам только на пользу.
Последствия обработки ракового очага при ЛТ в основном связаны с одновременным повреждением здоровых тканей. Побочные эффекты могут быть:
К местным осложнениям относят явления, связанные с тем, что под «удар» попадает не только рак, но и здоровая ткань. К основным проявлениям относят:
- зуд;
- шелушение;
- гиперемию кожи;
- появление волдырей в зоне облучения, затем их изъязвления;
- усиление ломкости сосудов, кровоизлияния.
Системные осложнения развиваются, потому что опухолевые клетки погибают под воздействием излучения, продукты их распада попадают в системный кровоток, развиваются лучевые реакции:
- повышенная утомляемость и слабость;
- ЖКТ-расстройство (тошнота, рвота);
- ухудшение качества кожи и ее придатков (ломкость ногтей и выпадение волос);
- угнетается кроветворение и нарушение системы крови.
Кроме описанного разделения, специалисты делят последствия от ЛМ на лучевые:
Первые развиваются в течение первых 3 месяцев после лечения, вторые — после трехмесячного рубежа.
Реабилитация начинается сразу после окончания терапии. Первая консультация онколога проводится в промежутке с 1 по 3 месяц. Все последующие консультации проводятся раз в полугодие. Сроки реабилитации и специфические меры зависят от степени развития осложнений и интоксикации здоровых тканей.
В этот период важна диета (витамины, минералы и белки), здоровый сон и умеренная физическая активность. Обязателен контроль за состоянием тканей с помощью УЗИ и МРТ методов. Некоторые пациенты не ощущают серьезных последствий после ЛТ. Их беспокоит легкая слабость, которая быстро проходит при правильной диете и полноценном отдыхе. Реже развивается полноценная лучевая реакция.
На этом мы прощаемся с вами. Надеемся, наша статья помогла вам понять суть лучевого лечения при раке молочной железы. Читайте наши новые тексты и приглашайте друзей через социальные сети.
источник
При раке молочной железы химиотерапия после операции назначается для профилактики возврата болезни.
Всем нашим пациентам мы обеспечиваем возможность пройти химиотерапию у лучших специалистов Санкт-Петербурга.
Химиотерапию можно начинать через 2-3 недели после операции, но не ранее, чем через неделю после удаления дренажа (если после этого в зоне операции не копится лимфа). Если начать химиотерапию до заживления ран — процесс заживления затягивается. Перед началом химиотерапевтического лечения пациенту рекомендуется с календарём проследить даты последующих введений: чтобы они не совпадали со всенародными праздниками (новогодние и майские каникулы, прочее). Так как в эти дни государственные учреждения закрыты и сроки проведения последующих циклов химиотерапии могут сбиваться.
Обычно назначают 4-6 циклов химиотерапии в адьювантном режиме. Каждое повторное введение — это новый цикл химиотерапии. Иногда используют одинаковые препараты, иногда — разные. Назначение препаратов осуществляет химиотерапевт — в зависимости от свойств опухоли (ИГХ) и распространённости болезни (стадии).
Для эффективности химиотерапии важно проводить её ритмично: она эффективно действует только на делящуюся раковую клетку. Именно поэтому химиотерапию проводят через каждые 3 недели (21 день). Интервал между циклами необходимо строго соблюдать: те клетки, которые не делились при предыдущем введении препаратов будут чувствительны к лечению при очередном их введении.
Существуют и еженедельные схемы введения препаратов. Увеличение интервала между введениями на 1 день уменьшает эффективность химиотерапии на 5%.
Опухолевые клетки в родоначальной опухоли могли прорасти в её кровеносные или лимфатические сосуды и с током крови «улететь» в другие органы или ткани организма (до того, как опухоль была удалена при операции). Из-за своих малых размеров эти отдельные опухолевые клетки могли остаться невыявлеными при Ваших обследованиях до операции (рентгенография, КТ, МРТ, ПЭТ, УЗИ, ОСГ). По результатам гистологического и ИГХ исследований удалённой опухоли и лимфатических узлов можно предполагать о такой вероятности. Для того, чтобы уничтожить такие опухолевые клетки, или замедлить их рост — проводится химиотерапия и гормонотерапия.
Нередко организм не успевает восстановиться между курсами химиотерапии для очередного введения. В этом могут помочь препараты поддержки. Если администрация не обеспечила медиков данными препаратами, они вынуждены увеличивать сроки между циклами химиотерапии своим пациентам, что влияет на эффективность лечения, либо уменьшать дозы вводимых препаратов. Сказать пациентам что «лекарств нет» — значит спровоцировать жалобу на своего главного врача. За это увольняют.
В любом случае, не стоит боятся химиотерапии, опасаясь её токсичности и вреда: Ваш врач оценивает все риски и стремиться сделать так, чтобы Ваши шансы на выздоровление были максимальными (с учётом рисков токсичности от химиотерапии). Для уменьшения проявлений токсичности химиотерапии есть специальные препараты.
Для купирования тошноты и рвоты стандартом является Зофран (уколы, свечи, таблетки). Но он дорог, а потому пациентам в наших государственных учреждениях обычно назначают финансово-доступный Церукал и/или Эмесет. Эффективными препаратами являются Китрил и Навобан.
Некоторые наши пациенты отмечали уменьшение тошноты и кишечного дискомфорта при приёме ими препарата Энтеросгель.
Для купирования гематологической токсичности (падение лейкоцитов в контрольном анализе между циклами химиотерапии) используются стимуляторы лейкопоэза (стимулирует производство лейкоцитов: Neupogen, Филграстим, Neulasta, Неуластим, Лейкостим) и/или эритропоэза (стимулирует костный мозг к производству эритроцитов — необходимы при развитии анемии: Procrit, Эпоген, Аранесп).
- ВО, 2-я линия, д. 49, телефон 8 (812) 323-57-20
- 2-й Муринский пр-т, д. 39, телефон 8 (812) 448-63-62 и 8 (911) 958-55-61.
- ул.Гжатская, д.22, корп.4, телефон 8 (812) 386-386-5 и
- ул.Садовая, д.25, лит.А, телефон 8 (812) 401-61-33, сайт: www.dia-f.ru
Легально назначать Вам купленные самостоятельно лекарства врач не имеет права: это дискредитирует государственную систему закупок медикаментов.
Для контроля за показателями крови регулярно сдавайте анализы на 14 день после введения препаратов (максимальные проявления гематологической токсичности — для решения вопроса о целесообразности назначения вышеуказанных препаратов); а так же максимально приближенно к дате очередного введения (для решения вопроса о вашей готовности к очередному циклу химиотерапии).
Иногда пациентам для повышения уровня лейкоцитов в анализе назначают Преднизолон в таблетках. Преднизолон стимулирует выход лейкоцитов из ткани в кровоток, тем самым делает «нормальным» анализ не повышая общее количество лейкоцитов. Это явный признак того, что врач лимитирован в назначении пациенту необходимых стимуляторов лейкопоэза.
Информирование врачом пациентов об отсутствии чего-либо необходимого для их лечения провоцирует жалобы (со стороны тех, кто верует, что медикам предоставлено всё необходимое для лечения пациентов). Эти жалобы дискредитируют медицинских чиновников, неспособных организовать работу. Месть таких чиновников выливается на подчинённых. Именно поэтому в государственных учреждениях медики не могут открыто рекомендовать пациентам то, что им необходимо для правильного лечения. Если Вы сомневаетесь в правдивости написанного — смотрите ЗДЕСЬ.
Введение некоторых препаратов (Доксорубицин, Адриамицин, Адриабластин, Герцептин) сопровождается их кардиотоксичностью: они могут увеличить риск инфаркта или усугубления сердечной недостаточности. Поэтому перед назначением этих препаратов показано выполнение пациентам ЭХО-сердца. Далее это обследование должно выполняться перед каждым нечётным курсом химиотерапии (перед 3, 5, 7, 9 и т.д.). В ряде случаев (пациентам с сердечной патологией) вместо Доксорубицина назначают менее кардиотоксичный препарат Фарморубицин (Эпирубицин). Из-за низкой кардиотоксичности он может назначаться в большей дозе. С той же целью (облегчение переносимости) может быть применён Эндоксан вместо препарата Циклофосфан.
Cпециалист-кардиолог, которого мы рекомендуем нашим пациентам для лечения и поддержки сопутствующей сердечно-сосудистой патологии при получении ими химиотерапии (в Санкт-Петербурге): Загатина Анжела Валентиновна (работает в частной сети), её телефон: 8(921)329-70-87.
Пациентам до 45 лет перед химиотерапией и во время её проведения (или введениями герцептина) — перед каждым нечётным курсом — бесплатно и без направления (по полису ОМС и без него, благотворительно) делают эхокардиографию (ЭХО сердца) экспертного класса: определение ФВ в 2D и 3D режиме, GLS лж и пж на ультрасовременном оборудовании. Обращаться по адресу: м. Чернышевская, ул. Кирочная 41, СЗГМУ им. Мечникова. Обращаться по тел. 8-960-280-14-06, Ковалёва Надежда Николаевна (для согласования времени визита).
Мы делаем всё возможное, чтобы наши пациенты получили качественное лечение
при раке молочной железы.
Очень важно для пациента сразу правильно подобрать схему химиотерапевтического лечения, с учётом ЕГО стадии болезни, иммуногистохимических свойств именно ЕГО опухоли и исходного состояния здоровья. Выбор схемы химиотерапии во многих медицинских учреждениях обусловлен не этими факторами, а наличием лекарств: лечат тем — что есть, или тем, чем распорядилось лечить руководство, ориентируясь на срок годности имеющихся препаратов. Именно поэтому очень важно, чтобы лечение назначал химиотерапевт, не зависящий от указаний чиновников, а мотивированный только на оказание качественной помощи. Для этого мы рекомендуем проконсультироваться у нескольких химиотерапевтов учреждений с разной подчинённостью (городские, федеральные, частные) — если их назначения совпадут — значит Вам назначили то, что Вам действительно необходимо. Ещё есть вариант Ваших дополнительных частных консультаций с Вашим же врачом вне стен государственного учреждения.
Дополнительно о химиотерапии при раке молочной железы
можете прочитать ЗДЕСЬ.
В нашей стране назначение химиотерапии происходит по стандартам. Стандарты лечения рака молочной железы (для специалистов) Вы можете посмотреть ЗДЕСЬ. Для подбора химиотерапевтического лечения в развитых странах применяется система Adjuvantonline, тест Oncotype DX или MammaPrint. В отличии от развитых стран (в которых страховые компании оплачивают эти тесты) мы можем организовать указанные обследования нашим пациентам, но платно (около 4100 USD).
Недавно В Санкт-Петербурге появилась компания Genext, которая предлагает аналогичный анализ EndoPredict (Эндо-Предикт). Принцип анализа аналогичен Oncotype DX или MammaPrint. Тест выполняется в Мюнхене, стоит — 140 т. р.
Результаты всех этих тестов позволяют в 1/3 — 1/4 случаев отказаться от традиционно запланированной химиотерапии в пользу гормонотерапии и наоборот.
Герцептин и его аналоги (Пертузумаб, Бейодайм или Пертузумаб+Трастузумаб или Перьета и Герцептин, Бевацизумаб) не являются химиопрепаратами. Лечение ими называют ещё иммунотерапией или таргетным лечением. Это моноклональные антитела к фактору Her2/neu. Он показан только тем, у кого Her2/neu «+++» или «3+» или выявлена Fish-амплификация (Фиш)! Это препарат против эпидермального фактора роста опухоли: он нарушает рост и деление опухолевых клеток, когда они обусловлены активацией таких рецепторов на опухолевых клетках. Для пациентов с Her2/neu 0, 1+, или 2+ — Герцептин и его аналоги не нужны — они будут неэффективны. Пациентам с Her2/neu 2+ показан анализ опухоли на fish, так как 2+ это промежуточное значение — не понятно: есть или нет этот фактор.
Герцептин обладает кардиотоксичностью (требует контроля ЭХО-сердца перед каждым нечётным введением). Он может сочетаться с параллельным введением другихнекардиотоксичных химиопрепаратов (например, паклитаксел или доцетаксел), гормонотерапией (анастрозол), с лучевой терапией. Курс лечения герцептином составляет 1 год. Если Вам предложили его на 6-8 месяцев — значит закупки препарата в этом учреждении для всех нуждающихся не обеспечены. Его просто нет в нужных количествах. Если Вы не можете его докупить — рассмотрите вариант переезда в тот регион, где он есть на весь курс. Если кто-то сомневается в правдивости написанного — смотрите ЗДЕСЬ.
Существуют более новые препараты, чем Герцептин для данной группы пациентов, но они ещё более дорогие (см. выше в скобках).
Проводились исследования об эффективности химиотерапии на фоне назначения пациентам герцептина. Длительность наблюдения в исследовании составила 6 мес (за эффективностью химиотерапии!). Теперь наши медицинские чиновники, не обеспечив всех нуждающихся лекарством, ссылаясь на это исследование, подменяя понятия, рекомендуют проводить таргетное лечение герцептином до 6 мес.
Если Вам планируется длительное введение химиопрепаратов (таргетных препаратов), для сохранения своих периферических вен (на руках) рассмотрите вопрос установки специального порта для химиотерапии. Подробнее о порте для химиотерапии смотрите ЗДЕСЬ. Имейте в виду, что для введения лекарств в порт необходимы иглы со специальным углом заточки (чтобы не повредить порт). Чаще всего их тоже «на всех не хватает», и Вам, возможно, придётся покупать их самим.
В процессе химиотерапии нарушается процесс нормального деления клеток волос и ногтей. Это определяет их ломкость — волосы теряют свою гибкость и элластичность и обламываются на уровне кожи. После химиотерапии процесс нормального деления клеток волос восстановится, и волосы отрастут вновь. В Германии пациентам при назначении химиотерапии по страховке просто перечисляют 200 евро на приобретение парика. У нас об этом приходится заботиться самим пациентам. Как вариант, можно приобрести готовый парик из искусственных или натуральных волос, либо под Вашу причёску могут постричь парик-заготовку и покрасить в цвет Ваших волос — чтобы полностью имитировать Вашу причёску и максимально скрыть Ваши временные проблемы. В этом вопросе Вам помогут ЗДЕСЬ.
О профилактике выпадения волос при химиотерапии можно прочитать ЗДЕСЬ. Однако на практике — все указанные в ссылке способы — лишь растягивают процесс во времени. Они не показали ожидаемой эффективности и за рубежом рутинно не применяются.
Иногда химиотерапию проводят до операции — чтобы создать более удобные условия для хирурга: например у Вас большая опухоль, которая не позволяет выполнить операцию с сохранением груди, или в подмышке имеются крупные метастатические лимфоузлы — при химиотерапии они уменьшатся и может появится шанс выполнить операцию с сохранением молочной железы, а сам факт уменьшения опухоли докажет эффективность подобранного лечения. Если Вам предлагают химиотерапию до операции — значит это оптимально для Вашего лечения: эффективность такого подхода доказана. Принципиально не важно: получите Вы часть суммарной дозы препаратов до операции и часть после, получите Вы всю химиотерапию до операции или всю после неё — суммарно Вы получите одинаковую дозу лекарств.
Если химиотерапия проводится до операции, то каждые 2 цикла (перед нечётным) проводится оценка её эффективности: маммографический или КТ — контроль размера опухоли и лимфатических узлов. Ожидается, что они будут уменьшаться. Если они увеличиваются — значит подобранная схема лечения не работает: её нужно менять.
Если химиотерапию проводят для уменьшения размеров опухоли с перспективой выполнения операции по сохранению молочной железы — до её начала необходимо маркировать опухоль (обозначить её границы). Во время проведения химиотерапии опухоль может стать незаметной, и тогда определение границ удаления будет осуществляться по маркировке (её делает Ваш хирург).
Если Вам назначена химиотерапия до операции, очень важно пройти современные обследования лёгких, печени и костей (КТ грудной клетки, УЗИ печени и остеосцинтиграфия и/или ПЭТ) до её начала. Дело в том, что если Вы проходили иные обследования с невысокой информативностью, а у Вас уже есть метастазы, то на фоне химиотерапии они могут стать незаметными. Они не исчезнут, но Ваше лечение может быть неправильным.
Подробнее о правильном обследовании
при раке молочной железы смотрите ЗДЕСЬ
Химиотерапия по протоколу (клиническое исследование) подразумевает, что Вам предлагают пройти лечение новым препаратом, либо уже известными препаратами (с доказанной эффективностью), но по новой схеме назначения. В наших условиях возможность пациенту попасть в клиническое исследование — шанс получить современное лечение или наблюдение.
Подробнее можно прочитать ЗДЕСЬ.
Наши зарубежные коллеги не прерывают химиотерапию. У нас нередко можно услышать, что химиотерапию нужно прервать для проведение лучевой терапии, а то «она будет неэффективна». Это не так. Вы получаете химиотерапевтическое лечение. Лучевую терапию следует начать через 3(4) недели после последнего введения химиопрепаратов (возможно, с одновременным получением таргетного лечения).
Важный момент лечения — используются ли оригинальные препараты для химиотерапии или дженерики. В ряде случаев пациенты лишены выбора: их лечат тем, что есть. Некоторые дженерики не отличаются по эффективности от оригинальных препаратов. Приобрести самостоятельно онкологические препараты можно, но не факт, что их будут применять для Вашего лечения в государственном учреждении: они не прошли через официальные механизмы закупок, и учреждение не всегда готово отвечать за возможные осложнения от применения «левых» препаратов. Кроме того, руководителю учреждению будет необходимо отчитаться о закупке на бюджетные средства нерасходуемых препаратов.
В 2014 году в одном государственном учреждении имели место достоверные случаи, когда его руководитель не обеспечил своевременную закупку лекарств. Для сокрытия отсутствия лекарств было прекращено разведение препаратов в процедурных отделений, а организован «кабинет централизованного разведения». При этом пациентов не предупреждали об отсутствии тех или иных химиопрепаратов в учреждении (чтобы не мешать карьере руководителя). Для проверяющих в аптеке учреждения находились купленные лично руководителем «демонстрационные» образцы лекарств. Чем лечили пациентов — . , только многие из них отмечали «необычно лёгкую переносимость» циклов химиотерапии в это время. Пациенту рекомендуется проявлять бдительность и быть уверенным в том, что ему действительно вводят назначенные препараты.
В процессе проведения химиотерапии у менструирующих женщин может сбиваться менструальный цикл, может даже наступить полная менопауза. Некоторые пациентки, озабоченные возможными проблемами (в перспективе) с беременностью до начала химиотерапии изымают и сохраняют свои яйцеклетки (как для ЭКО) — чтобы (если менструальная функция после химиотерапии не восстановится) иметь возможность иметь своих детей. В Санкт-Петербурге с этим Вам могут помочь в клинике «Мать и дитя», компании АВА-Петер, центрах ЭКО.
Ниже перечислены медицинские учреждения Санкт-Петербурга, в которых больные раком молочной железы могут получать химиотерапию:
- ПСПбГМУ им. акад. И.П. Павлова — Учреждение федерального подчинения – отделение химиотерапии – ул. Рентгена, 12, каб. 126: Зарембо Ирина Александровна, тел. 8 (921) 945-84-04 (оригинальные препараты)
или ул. Льва Толстого, д.17, 7 этаж – вход под арку с ул. Рентгена. Стельмах Лилия Владимировна : 8 (921) 748-24-62 (оригинальные препараты) - ЛООД — Ленинградский областной онкологический диспансер — Учреждение подчиняется администрации области. СПб, Литейный пр. 37. Только в этом учреждении пациентам предоставляют герцептин на весь курс лечения по полису ОМС (для пациентов с HER2+++). Для его получения необходимо быть (стать) прописанным в Ленинградской области. Химиопрепараты в учреждении в своём большинстве неоригинальные.
- ГКОД — Городской клинический онкологический диспансер — Учреждение городского подчинения (2 Берёзовая аллея 3/5). Лечение — по полису ОМС для жителей юга города, много неоригинальных препаратов, герцептин рутинно назначают не на весь курс лечения; лекарства персонал разводит в присутствии пациента;
- Клинический научно-практический центр специализированных видов медицинской помощи — КНПЦСВМПО — Учреждение городского подчинения (онкоцентр в пос. Песочный, ул. Ленинградская 68а, ЛИТ.А). Лечение по полису ОМС для жителей севера города. Много неоригинальных препаратов, герцептин рутинно назначают не на весь курс лечения, препараты для химиотерапии не растворяют в присутствии пациента.
- Частный онкологический центр «ДЕ-ВИТА» — Ул. Савушкина 14-б, тел. 8-981-864-20-27 – лечение равносильно лечению за рубежом, оригинальные препараты, препараты поддержки, европейские протоколы лечения. Иногда предлагают «лечение по протоколу» бесплатно, оригинальными препаратами.
- Онкологический диспансер Московского района (Новоизмайловский пр., 77) — Только для жителей Московского р-на, лечение аналогично таковому в ГКОД.
- Научно-исследовательский институт (НИИ) онкологии им. Н. Н. Петрова — Учреждение федерального подчинения (пос. Песочный, ул. Ленинградская, д.68).
- Медсанчасть № 122
- ЛДЦ МИБС (п. Песочный, ул. Карла Маркса, д. 43)
Если информация нашего сайта была Вам полезна — пожалуйста, оставьте свои отзывы о нём и рекомендации в интернете для других пациентов.
Автор: Чиж Игорь Александрович
заведующий, кмн, онколог высшей квалификационной категории,
хирург высшей квалификационной категории, пластический хирург
источник
У женщин, страдающих раком молочной железы на ранних стадиях, короткий курс лучевой терапии высокими дозами менее токсичен и обеспечивает лучшее качество жизни по сравнению с длительным курсом низкими дозами. Это подтверждают два недавних исследования, результаты которых опубликованы в JAMA Oncology.
Рак молочной железы (РМЖ) является наиболее частой опухолью у женщин, уступая по распространенности только раку кожи.
Лучевую терапию молочной железы часто назначают с целью профилактики рецидива женщинам с РМЖ на ранних стадиях, которые перенесли органосохраняющую операцию. При этом классически курс лечения продолжается достаточно долго, во время каждого сеанса грудь пациентки подвергают воздействию небольших доз излучения. Этот метод называется фракционированным облучением молочной железы (CF-WBI).
Другой вариант – короткие курсы лучевой терапии большими дозами — гипофракционированное облучение молочной железы (HF-WBI). Предыдущие исследования показали, что эта схема так же эффективна, как и предыдущая.
«Рандомизированные исследования, проведенные в Великобритании и Канаде, показали одинаковую выживаемость и частоту рецидивов в обеих группах», — говорит доктор Симона Шайтелман (Simona Shaitelman) из Онкологического центра Андерсона Техасского университета (Anderson Cancer Center at the University of Texas), соавтор одного из последних исследований. Несмотря на такие выводы, американское сообщество радиоонкологов (врачей, специализирующихся на лучевой терапии опухолей) не спешит менять свои подходы.
«Вопрос в том, — говорит доктор Шайтелман, — можем ли мы, обладая новыми технологиями и знаниями о том, что выживаемость и риск рецидива одинаковы, предложить пациенткам лучший вариант лечения?»
Доктор Шайтелман с коллегами проанализировали данные 287 женщин в возрасте 40 лет и старше, у которых был диагностирован рак молочной железы на ранних стадиях и проведена органосохраняющая операция.
149 пациенткам впоследствии назначили фракционированное облучение молочной железы, 138 – гипофракционированное.
В течение последующих 6 месяцев ученые наблюдали за токсическими эффектами и влиянием лучевой терапии на качество жизни женщин в краткосрочной и долгосрочной перспективе в обеих группах.
Исследователи обнаружили, что у пациенток, получавших HF-WBI, во время лечения были значительно менее выражены такие побочные эффекты, как острый дерматит, зуд, боли в груди, усиление пигментации кожи и усталость по сравнению с теми, кто получали CF-WBI.
У женщин из обеих групп в течение 6 месяцев отмечались токсические эффекты, но у тех, кто перенесли HF-WBI, было больше энергии, они реже жаловались на утомляемость.
Кроме того, пациентки после HF-WBI испытывали меньше проблем при возвращении к привычным повседневным делам. «Это очень важно для женщин, перенесших лучевую терапию по поводу РМЖ, — говорит доктор Шайтелман, — Многие из них являются работающими матерями, работают на дому или в другом месте. Важно, чтобы мы могли удовлетворить эту потребность».
Ученые считают, что женщины должны знать об этом и иметь возможность выбрать гипофракционированное облучение для лечения рака молочной железы. Соавтор исследования, доктор Бенджамин Смит (Benjamin Smith) добавляет:
«Теперь я считаю короткий курс лучевой терапии не дополнительным возможным вариантом, а, скорее, отправной точкой, предпочтительным методом, который врачи должны обсуждать с пациенткой, когда возникает необходимость в облучении груди».
Во время другого исследования, проведенного доктором Решмой Джагси (Reshma Jagsi) из Мичиганского университета в Энн-Арборе (University of Michigan-Ann Arbor), ученые оценили токсические эффекты CF-WBI и HF-WBI в течение 1 недели лечения.
Ученые проанализировали данные 2309 женщин, получавших лучевую терапию после органосохраняющей операции. 570 пациенток получали HF-WBI, 1731 — CF-WBI.
Ученые обнаружили, что у пациенток, перенесших CF-WBI, чаще возникали кожные реакции, боли в груди и повышенная утомляемость, — что соответствует результатам, полученным доктором Шайтелман.
Но после 6 месяцев наблюдения доктором Джагси не было обнаружено особой разницы между группами в плане токсических эффектов.
Резюмируя результаты этих двух исследований, ученые говорят, что они дополняют друг друга. Исследование Шайтелман строго рандомизированное, но в него было включено небольшое количество пациенток. Исследование доктора Джагси более масштабное, но нерандомизированное.
«Гипофракционированное облучение молочной железы должно быть рассмотрено для большинства пациенток с РМЖ на ранних стадиях», — подытоживают ученые.
Для того чтобы лечение рака было максимально эффективным, онколог должен четко придерживаться принципов доказательной медицины. Именно так работают врачи Европейской клиники. Мы постоянно сотрудничаем с коллегами из Америки, Израиля и других стран, всегда в курсе последних достижений мировой онкологии.
источник
Рак молочной железы является наиболее распространенным видом рака в Германии. Ежегодно в стране регистрируется более 70.000 новых случаев этого заболевания. Если рак распознается на ранней стадии, то очень многие женщины имеют шанс излечиться.
«Ранние стадии рака и не очень агрессивные формы заболевания сегодня практически всегда излечимы!»
В случае с раком молочной железы считается, что возраст пациента является наибольшим фактором риска развития заболевания. Чем старше становится человечество в целом, тем больше раковых заболеваний будет диагностироваться в будущем.
Наиболее частое онкологическое заболевание в целом
Кроме того, считается, что рак молочной железы является наиболее распространенным раковым заболеванием не только у женщин. Рак груди является наиболее распространенным видом рака в целом.
«Ранние стадии рака и не очень агрессивные формы заболевания сегодня практически всегда излечимы, однако это не означает, что можно преуменьшать серьезность этих заболеваний. Это означает то, что детально проработанные концепции хирургического, медикаментозного лечения и лучевой терапии хорошо работают», — говорит Доктор мед. наук Мануэла Зайферт, руководстводитель отделения сенологии и маммологиии Городской Клинической больницы г. Золинген, Германия.
Снижать риски
После химиотерапии, которая проводится до или после операции, и после самой операции многие женщины задаются вопросом: а нужно ли облучение вообще? И еще один вопрос: Не являются ли нагрузки вследствие лучевой терапии слишком высокими в соотношении с пользой от лечения? Ответ на этот вопрос очевиден – нет. «Польза от лучевой терапии практически всегда больше, чем риск. Поэтому на сегодняшний день почти все женщины с раком груди получают лучевую терапию, особенно в случае с так называемыми органосохраняющими операциями облучения в большинстве случаев являются обязательными», — подчеркивает доктор Зайферт. Риск того, что заболевание может возникнуть снова, становится вполовину меньше благодаря облучению. Этот факт уже давно был доказан результатами большого количества очень крупных исследований. В любом случае, этой возможностью следует воспользоваться.
Хорошая переносимость
Сегодня большинство женщин получают лучевую терапию в соответствии с золотым стандартом. В данном контексте золотой стандарт означает, что отличающиеся от него методы лечения, как минимум, должны давать хорошие результаты, соответствующие стандарту, и ни в коем случае худшие результаты. В зависимости от того, насколько высоко оценивается риск рецидива, классическая форма облучения длится от пяти до шести недель и состоит из 25 — 32 разовых облучений. Из них 25 разовых сеансов лучевой терапии включают в себя низкодозное облучение всей груди. В случае с некоторыми пациентками могут проводиться от пяти до восьми прицельных разовых облучений, направленных исключительно на ложе опухоли. В таком случае специалисты говорят о так называемом «прицельном облучении ложа опухоли» (boost-облучение). Доза за один сеанс boost-терапии идентична дозе при облучении всей груди. В качестве нового золотого стандарта сегодня многим женщинам предлагается сокращенная лучевая терапия, которая включает в себя от 15 до 20 сеансов облучения. Специалисты называют такое облучение гипофракционированным.
В большинстве случаев лечение проводится в амбулаторном режиме
Терапия проводится в основном в амбулаторном режиме. «Тяжелые побочные эффекты, которые возникали ранее, уже давно остались в прошлом. Современные приборы для лучевой терапии можно направлять на поле облучение абсолютно прицельно», — говорит доктор Зайферт.
Также сегодня можно регулировать интенсивность излучения, так что расположенные за полем облучения ткани совсем не затрагиваются. «На момент окончания облучения кожа всегда немного раздраженная, поэтому пациенткам необходимо хорошо ухаживать за кожей, применяя лосьоны без ароматизаторов, носить легкую и свободную одежду, а также отказаться от плавания и солнечных ванн», — рассказывает доктор Зайферт.
В принципе считается, что кожа полностью восстанавливается приблизительно в течение от четырех до восьми недель. Против синдрома усталости, который скорее редко возникает при лучевой терапии, доктор Зайферт рекомендует физическую активность на свежем воздухе, легкую средиземноморскую кухню, а также интересные встречи с друзьями знакомыми.
Выше золотого стандарта
Во многих центрах радиологической онкологии будущее для лучевой терапии уже началось. При этом, в основном, развиваются четыре новых пути, направленных на улучшение эффективности уже имеющегося золотого стандарта или на повышение комфорта для пациенток без ограничения эффективности лучевой терапии. «Краеугольным камнем этих рассуждений является адаптация лучевой терапии в зависимости от индивидуальной ситуации пациентов», — говорит доктор Зайферт. «Мы называем это режимом и видами облучения, адаптированными к индивидуальным рискам. Таким образом, мы можем создать персонализированную лучевую терапию».
источник
Говорят, что надежда умирает последней. Это верно во всех случаях жизни, а если касается онкологической патологии – то в первую очередь. Если не опускать руки и бороться, то часто приходит награда – выздоровление. Тем более что многие виды злокачественных опухолей, диагностированных на ранних стадиях, прекрасно поддаются лечению, которое, к сожалению, бывает достаточно сложным, а порой и мучительным. Однако зачастую человек и сам не знает своих способностей, это потом уже с гордостью можно сделать акцент на том, что пришлось выдержать и преодолеть, где лишь вера в победу помогала.
Учитывая, что рак молочной железы (РМЖ) – проблема всемирного значения, его лечению уделяется самое пристальное внимание. Даже те, кому посчастливилось никаким образом не встречаться с раком, знают слова: «химия», «лучевое лечение», « удаление железы», а вопрос: излечим ли рак молочной железы, на сегодняшний день является, пожалуй, самым актуальным, где ведущим методом лечения РМЖ всё-таки был и остаётся метод хирургический.
Радикальная мастэктомия преследует цель вырвать железу из «клешней» рака, где базой для этого являются следующие принципы:
- удаление всего злокачественного очага с участками возможного распространения (радикализм); профилактические приёмы, направленные против расселения злокачественных клеток в области раны и её пределов (абластика), которые предусматривают самое бережное отношение к органу, не допуская грубых пальпаторных манипуляций, многократной не всегда оправданной биопсии, неаккуратного проведения оперативного вмешательства; удаление из раны 100% злокачественных клеток, в том числе, поврежденных, которые впоследствии могут привести к рецидиву (антибластика).
Для осуществления этих мероприятий и приобретения уверенности, что со злом покончено, применяются пред — или послеоперационные методы, направленные на полную гибель раковых клеток: операция с применением лазера, лучевая и химиотерапия, фотодинамическая и гормонотерапия и другие.
Современная медицина уже имеет возможности проведения не просто радикальной мастэктомии, а органосохранной, с помощью всего двух разрезов, когда железа уже не вырывается полным блоком совместно с окружающими тканями, лимфоузлами и сосудами. Правда, если это возможно (с учетом расселения злокачественного процесса). Такая хирургия особенно эффективна для лечения рака на ранних стадиях, когда ещё и очаг небольшой и раковые клетки не рассеялись.
Мастэктомия предусматривает разные виды хирургического вмешательства в зависимости от стадии, локализации опухоли, размеров самой груди, возраста пациентки. Однако расширенную радикальную мастэктомию проводят в исключительных случаях, так как её в настоящее время заменили более эффективные модифицированные методы с последующим радиотерапевтическим воздействием на лимфатическую систему.
К щадящим методам относится лампэктомия, где удаляется небольшой участок железы с иссечением минимального объёма здоровых тканей вокруг зоны поражения. Операция считается органосберегающей, так как даёт незначительный косметический дефект. Несколько больший объем потери ткани железы предусмотрен при квадрант — или сегментэктомии, ввиду удаления целого сегмента.
После мастэктомии лимфообращение зачастую теряет свои основные пути, поэтому лимфатическая система (ЛС) должна проложить новые, сосудам неизвестные, о чём врач и предупреждает больную женщину, так как лимфостаз руки в таких случаях – дело обычное. Он бывает мягким и может продолжаться до года. Мягкий лимфостаз никакой угрозы для жизни не несёт, но качество её снижает существенно. Плотный лимфостаз называют необратимым отёком, он возникает позже, как осложнение мягкого, и требует обязательного лечения.
Кроме этого, современная онкохирургия позволяет производить реконструкцию или пластику удалённой части молочной железы, которая может быть выполнена параллельно основному вмешательству или несколько погодя. Восстановительная операция может быть осуществлена за счёт вживления имплантанта на месте потерянной части или путём пластики «живым» (собственным) материалом пациентки, используя близлежащие мышцы женщины (обычно это мышца спины) с изменением направления, но с сохранением кровоснабжения.
Чтобы операция прошла успешно и до неё, и после применяются другие методы борьбы с раком, которые призваны завершить этот процесс, потому что лечение РМЖ должно быть комплексным.
Лучевая терапия на злокачественный процесс воздействует локально-регионарно, то есть, на подавление роста не только вокруг удалённого очага, а и на зону, выходящую за пределы локализации опухоли. Её применяют и до оперативного вмешательства, где требуется максимально снизить степень злокачественности клеток, не дать им имплантироваться в других органах, и после для предотвращения рецидива на участке поражения и распространения метастазов в регионарной зоне.
Лучевая терапия рака молочной железы, применяемая до оперативного вмешательства, показана в случаях больших опухолей (более 5 см), отека МЖ, диффузных форм опухоли и при наличии метастатических лимфоузлов в подмышечной области. Однако она не снижает вероятность появления метастазов в отдалённых органах и повреждает не только раковые клетки, но и здоровые, что относят к недостаткам этого метода.
Всё о современных методах диагностики эрозии шейки матки можно узнать из этой статьи.
Показаниями к лучевому лечению в послеоперационном периоде являются:
- обнаруженные в ходе операции метастатические лимфатические узлы; все формы рака с метастазами, не зависимо от проведённой предоперационной терапии; наличие отёка кожи МЖ; многочисленные очаги инвазий в МЖ; радикальная резекция МЖ; не удалённые по различным причинам подмышечные лимфоузлы.
Лучевое лечение иногда может быть самостоятельным способом борьбы с недугом, правда, не единственным. Химио — и гормонотерапия дополняют его. Это происходит в случаях наличия противопоказаний к радикальному методу, при сложных формах рака (неоперабельный или отёчно-инфильтративный). Отказ пациентки от оперативного вмешательства также даёт основание ограничиться лучевым лечением.
Химиотерапия при раке молочной железы назначается до операции и называется неадъювантной.
Лечение химиопрепаратами после проведённого оперативного вмешательства называется адъювантной терапией, которое направлено на предотвращение рецидива за счёт метастазов, уже имеющихся, но ещё не проявивших себя. А коль они есть, то проявиться могут в разные сроки.
Лечебная химиотерапия назначается в случае выявления новых метастазов и появления рецидива, вопреки лечению.
Ввиду того, что опухоли часто имеют устойчивость к некоторым химиопрепаратам, широкое применение получила полихимиотерапия (ПХТ), которая отличается от монохимиотерапии (МХТ) более высокой эффективностью за счёт применения нескольких химиотерапевтических средств с различным механизмом действия.
Дозы лечебной ПХТ, как правило, выше, чем при адъювантной, при этом в обоих случаях отдельно рассчитывается доза препарата на весь курс и суммарная доза для каждого средства.
Адъювантная ПХТ предусматривает 5-6 курсов, а неадъювантная – по 3-4 курса до и после хирургического вмешательства.
Больные не вникают в сложные наименования, ибо запомнить их не каждому под силу, это дело специалистов, которые тоже называют их FAC, CAF, CMF, не перечисляя всю схему по дням. Однако любой больной, пройдя через ПХТ, может запросто ответить, каким воздействиям его подвергали, и назовёт, например, FAC или CAF красной химиотерапией, а CMF – жёлтой. Кроме этих, есть ещё и белая, и голубая ПХТ…
Нет смысла описывать каждый препарат или их составы в отдельности. Схему лечения определяет врач, он же и контролирует ход этого не очень приятного мероприятия.
Известно, что определенные гормоны желез внутренней секреции (щитовидная железа, яичники, гипофиз, надпочечники) оказывают существенное влияние на поведение опухоли МЖ. Более десяти гормонов «вносят свою лепту» в формирование и развитие рака, но превалирующее значение имеют эстрогены, прогестерон и фолликулостимулирующий гормон (ФСГ).
Либерины, вырабатываемые гипоталамусом направляются в гипофиз и там «решают» тормозить или возбуждать продукцию тех или иных гипофизарных гормонов. Это в первую очередь касается пролактина, который стимулирует лактацию и способствует развитию альвеолярного аппарата МЖ.
На функциональные способности МЖ оказывают влияние ФСГ и ЛГ (лютеинизирующий гормон) посредством количественных изменений эстрогенов и прогестерона.
Ликвидация этих гормонов или блокирование их влияния является задачей гормонотерапии при РМЖ. Следовательно, в таком случае нужны такие лекарства от рака молочной железы, которые могли бы воздействовать на гормоны. Конечно, лучше всего с такой проблемой справятся другие гормоны.
Однако прежде чем приступить к лечению, должны быть выполнены следующие мероприятия:
- выявление гормонорецепторов опухоли, то есть, при гормоноположительной, а их 35-50% от всех, лечение целесообразно; определение чувствительности к гормонотерапии, так как далеко не каждый рак, имеющий рецепторы, будет реагировать на лечение, то есть, гормонопозитивный, не значит, гормоночувствительный; не оставлять без контроля другие гормоночувствительные органы – матку и яичники; особый подход требует менопауза, где предпочтение будет отдано антиэстрогенам, тогда как в пременопаузе они применяются, если имеет место хирургическая, лучевая или химиотерапевтическая кастрация; соблюдение установленной последовательности в применении гормональных препаратов; при назначении ПХТ для проверки гормоночувствительности сначала проводится гормональная терапия.
В зависимости от возраста, состояния организма женщины, вида опухоли, метастазирования использование гормонотерапии может идти в четырёх направлениях:
- применение антиэстрогенов – хорошо переносится, редко осложняется, но вызывает развитие резистентности опухоли к лечению; назначение ингибиторов ароматазы – снижают количество активных эстрогенов на 85-90%; лечение прогестинами (гестагены, прогестагены) дают частоту ремиссии до 18%, но способны создать угрозу тромбоэмболий, влагалищных кровотечений, ожирения; терапия андрогенами предполагает отёки и «приливы», зато частота ремиссии до 20%.
Серьёзные средства для лечения онкологических заболеваний, убивая клетки рака, не могут быть абсолютно безобидными для других систем, а для иммунной – в первую очередь. Лечебные воздействия ПХТ, мастэктомия, лучевое лечение, сама опухоль, как правило, скажутся на состоянии иммуннитета и приведут к нарушениям реактивности организма.
Раньше с целью повышения иммунного ответа применялась вакцина БЦЖ, от которой пришлось отказаться, так как в ряде случаев имело место ухудшение эффективности лечебных мероприятий.
Современная иммуномодуляция предусматривает такие методики, как активная и пассивная, специфическая и неспецифическая. Неспецифическая стимуляция значительно дешевле, так как включает доступные и недорогие лекарственные средства типа декариса, тимолина, настойки элеутерококка. Что касается специфической иммуностимуляции, то в её основе заложены свойства человеческого интерферона, который, воздействуя на клетки опухоли, подавляет их размножение и мутацию.
Для стимулирования противоопухолевого иммунитета применяют лейкоцитарный человеческий интерферон, способствующий повышению фагоцитарной активности макрофагов, чтобы те, в свою очередь, начали активно «поедать» клетки опухоли. Достоинство интерферона состоит в том, что он практически не вызывает аллергических реакций и не сенсибилизирует организм пациентки, однако способ его выделения и производства достаточно сложен и требует определённых материальных затрат.
Высокая выживаемость при раке МЖ зависит не только от стадии рака, но и его формы. Однозначно: выявленный на ранних стадиях, рак молочной железы даёт почти 100% пятилетнюю выживаемость, и кроме этого, имеют место случаи полного излечения.
Когда уже рак становится очевидным, на что указывает яркая симптоматика, сдаваться также не следует, так как современные методы лечения позволяют во многих случаях остановить опухолевый рост. Неплохие результаты в онкологии показывает воздействие на злокачественный процесс сочетание низкоинтенсивного лазера и химиотерапии с применением кислорода – фотодинамическая терапия. Преимуществом метода является его направленное действие на саму опухоль, не повреждая при этом здоровые ткани.
Рассеивание рака по всему организму и проявление его в различных органах в виде метастазов, к сожалению, не утешает своим неблагоприятным прогнозом.
Дермоидная киста яичника и беременность. Читать подробнее
Лапароскопия маточных труб имеет ряд противопоказаний! Ознакомиться с ними можно здесь http://ladyinform. com/laparoskopiya-matochnih-trub
Самым первым и самым главным этапом в борьбе с раком является самодиагностика, которая требует обучения. Учиться профилактике должны все: начиная от любого медицинского работника, независимо от званий и регалий, и заканчивая девочками старших классов. Специальная литература в виде рекламных листовок, размещённых повсеместно, буклетов для выпускниц школ и университетов, напоминания для невест в белом платье – всё должно быть направлено на непримиримую борьбу со злом.
Обследования в медицинских учреждениях должны последовать при малейшем подозрении на патологию у молодых девушек и ежегодно (даже без каких бы то ни было признаков опухоли) – у взрослых женщин. Для профилактики.
Женщины, которым очень не повезло, обязаны строго подчиняться рекомендациям врача и на этапах стационарного лечения, и после выписки домой. Не следует забывать, что провоцировать рак или его рецидивы способны многие факторы, поэтому важно обратить особое внимание на состояние других систем организма. Питание при раке молочной железы должно быть полноценным и насыщенным витаминами, ведь любое лечение злокачественных опухолей приводит к угнетению иммунитета. А повышать его необходимо. Существенное влияние оказывает лечебный процесс на психоэмоциональный статус женщины, поэтому борьба с депрессией тоже относится к мерам профилактики.
От женщины не так уж много и требуется, всё можно выразить одним словом – контроль, а остальное – скажет врач. Но лучше б до этого не дошло.
В заключение, несколько слов о стоимости лечения рака молочной железы. Ежегодные материальные затраты на борьбу с ним огромны. Это предусмотрено государственными программами всех цивилизованных государств, жители которых имеют возможность получать онкологическую помощь бесплатно, что исходит из морально-этических общечеловеческих принципов. Но больному тоже нужно оставить выбор. Некоторые из них желают иметь особые условия пребывания в стационаре и готовы за это заплатить. И это их право.
Платные консультации онкологов в России осуществляются в частных клиниках и медицинских центрах, однако врачам зачастую приходится оправдываться и доказывать целесообразность платных приёмов, а тем более стационарного лечения. Поэтому многие едут по «проторенным дорожкам» в Германию, Израиль, где давно всё организовано и цена для многих россиян доступна. Например, полное обследование в Германии стоит 2000 евро, а лечение обойдётся в 10-12 тысяч, в Израиле стоимость обследования составляет 4000$ и лечение в 10 тысяч. В России цена операций на молочной железе колеблется от 20 до 200 тысяч рублей. А можно и бесплатно. Выбор есть.
Раком груди молочной железы называют злокачественную опухоль железистой тканевой основы молочной железы, которая является самым распространенным и часто встречающимся видом раковых заболеваний у женщин и вторым по количеству заболеваний после рака легких. В последние годы онкология молочной железы во многом стала более изученной и часто ее лечение проводится успешно как при помощи хирургического вмешательства, так и другими методами лечения (химиотерапия, лучевая терапия).
Главными критериями улучшения результатов лечения являются:
— диагностика на начальных стадиях развития;
— уверенность больного в своем выздоровлении — адекватность лечения.
Раком молочной железы могут в первую очередь заболеть те категории женщин, которые имеют данные факторы риска:
— женщины, не имеющие детей, у которых отсутствовали беременности и роды;
— поздние роды у женщин — после 30 лет;
— ранняя менструация (до 12 лет);
— поздний климаксический период — после 55 лет;
— непрерывное употребление экзогенных гормонов в лечебных целях, на протяжении 10 лет и более.
Каждой женщине надо знать, какие бывают первые признаки при раке молочной железы. При выявлении первых признаков надо сразу же обращаться к врачу, а это может проявляться:
— уплотнениями или опухолевидными образованиями в молочных железах (определить уплотнения можно самостоятельно, если тщательно пальцами ощупывать каждую грудь);
— выделениями любого вида из соска груди, если они не связаны с беременностью и лактацией;
— с появлением, в области соска, чешуйчатости, своеобразной эрозии, корочки и образований, подобных ареолам;
— различные отеки или деформации, увеличение или уменьшение размеров груди;
— увеличение подмышечных лимфатических узлов или над ключицей.
При выявлении хотя бы одного патологического изменения в области груди, необходимо обратиться за консультацией к врачу. Как и любой вид рака, так и рак груди молочной железы почти не выявляется на начальных стадиях развития заболевания, при тщательном обследовании первые стадии характеризуются появлением малочувствительных подвижных уплотнительных масс, с увеличением опухоли полностью фиксируется подвижность и появляются розоватые выделения из соска. Для своевременного выявления надо раз в два года проходить маммографию, УЗИ, а женщинам после 50 лет требуется ежегодное обследование.
Как лечить рак груди молочной железы химиотерапия и лучевая терапия.
Профилактикой рака молочной железы, считается устранение факторов, которые могут способствовать его развитию, при этом анализ крови на выявление маркеров играет очень большую роль. Тип опухоли определяется путем гистологического исследования тканей. Самым эффективным методом лечения рака молочной железы является мастэктомия — операция по удалению грудных мышц или лимфатических узлов, после такой операции может быть назначена химиотерапия, направленная на профилактические меры по уничтожению раковых клеток (остановка развития рецидива) и является дополнительным лечением.
Если рак распространил метастазы на другие близлежащие органы, то химиотерапия может быть назначена как основное лечение. Лечение химиотерапией представляет собой комплекс противораковых препаратов, которые вводятся внутривенно и параллельно проводится оральный прием лекарств. Введенные внутривенно, лекарственные препараты доставляются кровотоком во все органы, таким способ они достигают всех раковых клеток, находящихся вне молочной железы и поэтому считается самым эффективным методом в случаях уничтожения метастаз.
Весь лечебный курс химиотерапии делится на циклы с промежуточными восстановительными периодами. Такие циклы рассчитаны в основном на период от 6 месяцев до года, это зависит от степени развития заболевания и от применяемых препаратов. После каждого курса проводятся контрольные обследования.
источник
Рак груди – опасная онкопатология, значительно распространенная у женщин. На сегодняшний день состояние проблемы таково, что ее научились диагностировать на самых ранних стадиях, когда опухоль имеет еще величину не более горошины.
Эффективное лечение предполагает сочетание различных методик: операции, введения препаратов, уничтожающих опухолевые клетки, приема гормональных препаратов и тех, что блокируют гормоны, проводящие стимуляцию раковых клеток.
Лучевая терапия при раке молочной железы – давно использующийся, но от этого не ставший менее эффективным, метод борьбы с карциноматозной структурой. Основан он на прекращении размножения активно делящихся клеток (такие характеристики имеют раковые клетки) высокоэнергетическими пучками рентгеновских лучей или других радиоактивных частиц.
К настоящему моменту данный метод лечения максимально усовершенствован, чтобы минимизировать неизбежные при облучении побочные эффекты. Изобретены методики внутритканевого введения источника излучения, что дает возможность здоровым клеткам оставаться облученными в минимальном диаметре от радиоисточника. Кроме того, здоровые структуры умеют хорошо восстанавливаться, чего нельзя сказать о дефектных клетках.
Доказано, что при раке молочной железы лучевая терапия:
p, blockquote 8,0,0,0,0 —>
- уменьшает боли, вызванные сдавливанием нервных окончаний;
- снижает кровоточивость из аномальных сосудов, беспорядочная сеть которых питает опухолевые структуры;
- уменьшает риск возникновения патологического перелома, если произошло метастазирование рака в костные структуры;
- улучшается дыхательная функция;
- если метастазы находятся в позвоночнике, проводимое их облучение частично устраняет сдавливание ими структур спинного мозга или выходящих из него нервов.
Проведенная после резекции злокачественной опухоли, радиотерапия снижает вероятность повторного появления этих мутировавших клеток в 50-67%, что существенно сказывается на качестве жизни. Возникающие же после лучевого лечения побочные эффекты, в большинстве своем, временны: попавшие под облучение и погибшие нормальные клетки довольно быстро восстанавливаются, с ними пропадают и беспокоящие симптомы.
Лучевая терапия рака молочной железы уничтожает новообразование следующим образом:
p, blockquote 12,0,0,0,0 —>
- Радиоактивное излучение – это наподобие лазера, который выпаривает любые ткани, оказавшиеся на его пути. Оно «видит» активно делящиеся клетки и угнетает клеточный центр, дающий команду к делению. Так повреждаются не только раковые, но и «нормальные» для организма клетки, имеющие высокую скорость деления (это костный кроветворный мозг, слизистая оболочка кишечника).
- Лучи способствуют зарастанию большинства сосудов, питающих опухоль: отсутствие питания – гибель для раковых клеток. Из-за данного эффекта отекают и воспаляются здоровые ткани в каком-то (он зависит от вида выбранной лучевой терапии) радиусе вокруг новообразования.
Лучевая терапия в лечении рака молочной железы назначается радиотерапевтом. На основании истории болезни (указанных в ней данных о стадии болезни, гистологическом заключении) и осмотра пациентки он делает заключение, нужно ли облучать опухоль, какой выбрать режим терапии, дозу, периодичность и кратность излучения.
Совместно, лучевой терапевт и хирург-онколог обсуждают: радиоактивными веществами лучше воздействовать на новообразование до операции, после нее или вместо вмешательства (последнее применяется в неоперабельных случаях). Также этот узкий специалист определяет переносимость лучевого лечения, принимает решение об изменении его типа или отмене.
Предоперационная лучевая терапия прописывается в зависимости от нескольких критериев рака молочной железы:
p, blockquote 17,0,0,0,0 —>
- При Педжетовой болезни (карцинома сосково-ареолярного массива), если есть отдаленные (во внутренние органы или кости) или регионарные (в лимфоузлы) метастазы.
- При изъязвленной форме рака: за время проведения облучения язва может или затянуться, или очиститься. Удаление новообразования без лечения радиоактивными лучами сильно повышает риск того, что после операции рана будет постоянно инфицироваться и плохо заживать.
- Если опухоль – инфильтративно-отечная. Оптимальное решение в этом случае: вначале – неоадъювантная химиотерапия, после – радикальная лучевая терапия. Это повышает вероятность, что до операции опухоль сможет более четко очертить свои границы.
- При инфильтративной форме, когда раковая опухоль плотно спаяна с тканями: с сосково-ареолярным комплексом, фасцией (пленкой), покрывающей мышцы, лежащие под железой. Проведенная до операции, лучевая терапия при раке молочной железы может применяться, когда организм еще не «отравлен» продуктами опухолевого распада.
- При маститоподобной карциноме, но только – после химиотерапии.
2. Если груди стали источником нескольких раковых опухолей.
3. Обнаружено более четырёх метастатически-пораженных лимфоузлов.
После удаления рака молочной железы лучевая терапия должна подавить ростовую способность паталогических клеток, которые могли оставаться после оперативного вмешательства. Она чаще всего проводится:
p, blockquote 20,0,0,0,0 —>
- на 3 стадии любой формы рака;
- при болезни Педжета без метастазов;
- в случае узловой формы рака;
- если есть метастазы в подмышечной и подключичной областях;
- когда по гистологическому типу рак относится к тем, которые часто рецидивируют.
Чем больше органов планируется удалить во время операции, тем обширнее должна быть зона обработки радиоактивными лучами, тем длительнее курс лучевой терапии при раке молочной железы.
Читайте подробнее о раке молочной железы, его формах и методах лечения.
Обработке лучами также подвергаются (по показаниям):
p, blockquote 23,0,0,0,0 —>
- только молочная железа;
- лимфоузлы подмышечной ямки;
- лимфоузлы, расположенные над и под ключицей, захватывая ножки мышц, идущих от области за ухом к грудине (кивательная мышца).
При наличии метастазов до или после операции облучению подвергаются области, где они находились или находятся.
Интраоперационный облучатель «Intrabeam® PRS 500»
Эта методика дополнительного уничтожения клеток раковой опухоли непосредственно во время операции стала применяться относительно недавно. Она дает дополнительные гарантии, что те клетки новообразования, которые могли не быть иссечены, «умрут» от облучения. Такая технология лечения за последние 5 лет показала отличные результаты – менее 2% рецидивирования.
Дело в том, что при операции опухоль удаляется под визуальным контролем. «Страхование» от неполного ее резецирования дает только выполняемое во время операции (когда пациентка еще на столе и рана ее не ушита) гистологическое исследование, а оно в нашей стране выполняется крайне редко. При этом доказано, что рецидив рака почти всегда обнаруживается именно в том месте, где подобное образование уже однажды иссекалось.
Интраоперационное облучение показано также для лечения не очень агрессивных (когда рост и метастазирование идут годами) типов карциномы у пожилых пациенток – чтобы после операции обойтись без лучевой терапии, или уменьшить ее продолжительность на несколько недель. Показана она при небольших размерах опухоли, даже если есть 1-2 метастаза в регионарные лимфоузлы. Радионожом также можно удалять подмышечные лимфоузлы, если в них есть отсеянные из карциномы клетки.
Проведение лучевой терапии после химиотерапии рака молочной железы лучше всего позволяет избежать рецидива:
p, blockquote 30,0,0,0,0 —>
- препараты уничтожают скопления раковых клеток;
- облучение побеждает «оставшиеся в живых».
Показания к такой терапии: неоперабельный рак, инфильтративно-отечная форма рака, и отказ пациентки от операции.
Если для химиотерапии применялся Адриамицин, то с момента его последнего введения до применения радиации должен пройти месяц. При использовании других препаратов хватит 2-3 недель.
Лучевая терапия: линейный ускоритель «Elekta Synergy»
Она делится в зависимости от своей цели и может быть:
p, blockquote 34,0,0,0,0 —>
- Радикальной, которая (совместно с другими видами лечения) должна полностью очистить организм от рака.
- Паллиативной, назначаемой при наличии или метастазов, или больших объемов опухоли. В этом случае ни один из методов лечения, ни их сочетание не гарантирует полного избавления от новообразования. Но есть шанс сильно затормозить рост опухоли и распространение от нее метастазов с помощью лучевой терапии.
- Симптоматической. Это подразумевает облучение неоперабельной раковой опухоли для того, чтобы уменьшить боли и немного улучшить состояние.
В зависимости от расположения источника с радиоактивным материалом, лучевая терапия может быть наружной, когда источник расположен в стационарном устройстве и контактной внутренней (брахитерапия), при которой радиоактивное вещество с помощью катетера или баллона вводится в опухоль.
Последнюю используют, преимущественно, для обучения опухоли высокой дозой, чтобы окружающие ткани не пострадали очень сильно. При этом радиоактивный источник или вводят в новообразование на несколько суток, или убирают его через 10-20 минут после введения.
Хоть лучевой терапевт определяет сроки лучевой терапии индивидуально в каждом случае, можно привести некоторые усредненные параметры.
Так, перед операцией проводится короткий интенсивный курс облучения. Это примерно 4,5 недели (в зависимости от запланированной общей дозы и переносимости ее). Далее, через 3 недели, но не позже четвертой, может проводиться операция. Послеоперационная радиотерапия может проводиться через месяц после хирургического вмешательства. Ее длительность – 5 дней в неделю, 5-7 недель.
Последствия лучевой терапии при раке молочной железы обнаруживаются не сразу. Через время в 3-4 недели обычно наблюдаются:
p, blockquote 42,0,0,0,0 —>
- повышенная утомляемость;
- ноющие боли в облучаемой груди;
- изменения кожи груди: ее покраснение, отечность, сухость, зуд. Могут появиться волдыри или отслоение верхнего кожного слоя, как при солнечном ожоге. Кожа на облучаемой груди может потемнеть;
- боли в мышцах, лежащих под грудью;
- кашель;
- понос;
- изменения, связанные с воздействием на костный мозг, который временно перестает вырабатывать новые клетки крови, тогда как старые постепенно гибнут. Это кровоточивость, слабость и бледность, легкая подверженность инфекциям.
Эти последствия у большинства женщин уходят после окончания воздействия радиоисточником в течение полумесяца. Мышечные боли могут длиться до года.
При выполнении лучевой терапии при раке молочной железы могут быть и осложнения, к которым относятся:
p, blockquote 44,0,0,0,0 —>
- Отек подмышечной ямки и руки на облучающейся стороне.
- Радиационное воспаление легких.
- Потеря мышечной силы руки с больной стороны.
- Повреждение сердечной мышцы (повышенный риск отмечается у курящих и тех, кто уже страдает сердечными заболеваниями).
- Лучевые язвы на коже.
Радиотерапия имеет такие противопоказания, как:
p, blockquote 46,0,0,0,0 —>
- системные болезни (системная волчанка, склеродермия, дерматомиозит);
- тяжелый сахарный диабет;
- беременность;
- анемия;
- полученный ранее курс радиотерапии на любой другой зоне тела;
- тяжелая сердечно-сосудистая недостаточность;
- истощение;
- тяжелое состояние больного;
- лихорадочные состояния;
- активная фаза туберкулеза;
- перенесенный инфаркт;
- почечная или дыхательная недостаточности.
Во время, а также год после лучевого лечения женщине нужно больше отдыхать, гулять, получать позитивную информацию. Ей придется уделять повышенное внимание гигиене груди и руки: не купаться в горячей воде, не пользоваться парфюмерными изделиями, перед выходом на улицу использовать солнцезащитные препараты местного назначения.
Во время лучевой терапии при раке молочной железы, питание должно стать полноценным, богатым витаминами. Можно кушать супы на втором рыбном или мясном бульоне, отварные овощи, каши, запеченное или вареное мясо, пить кисели, отвары шиповника, черники, свежих спелых яблок и груш. Белый хлеб – высших сортов, лучше подсушить. Творог – только свежий и нежирный. Если есть анемия, в питание включить грецкие орехи, абрикосы, гранаты, мед, петрушку, кабачки. Белковой пищи – побольше, но она не должна быть жирной (сливочное масло – можно). Во время поноса свежие овощи и фрукты – ограничить. Прием пищи – четырехкратный или более частый.
Также важен объем суточной жидкости – не менее 2 литров. Сюда включают отвары шиповника, свежевыжатые фруктовые соки, морсы, зеленые и фруктовые чаи.
Алкоголь, консервы, маринованные и соленые продукты, а также газировку употреблять нельзя.
p, blockquote 52,0,0,0,0 —> p, blockquote 53,0,0,0,1 —>
источник