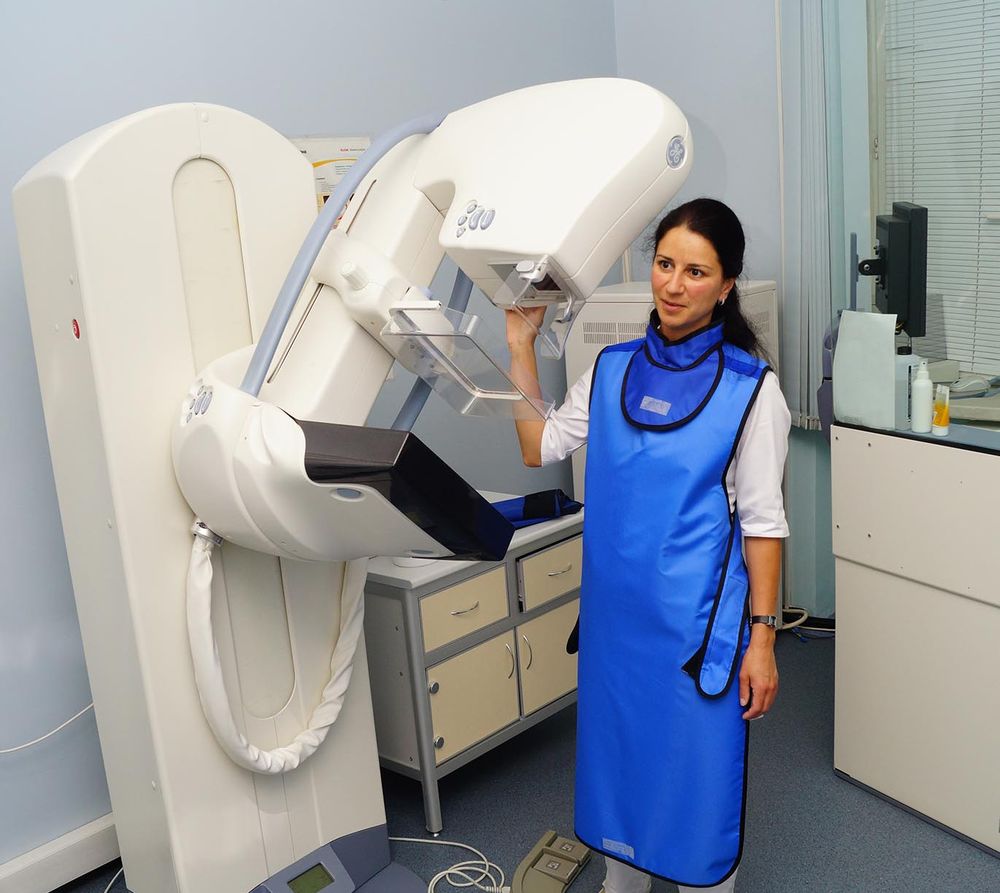
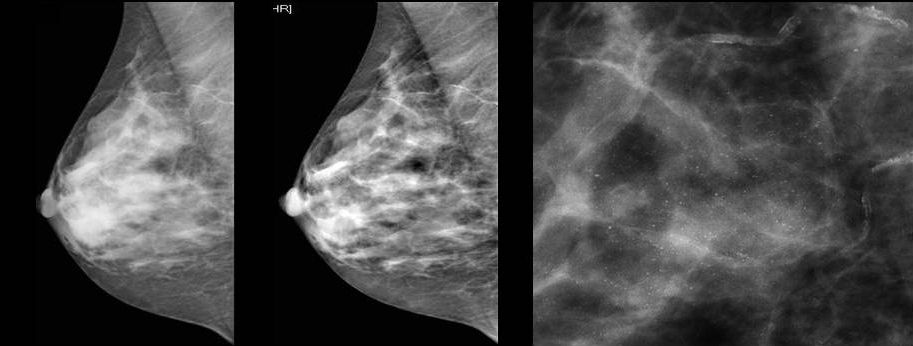
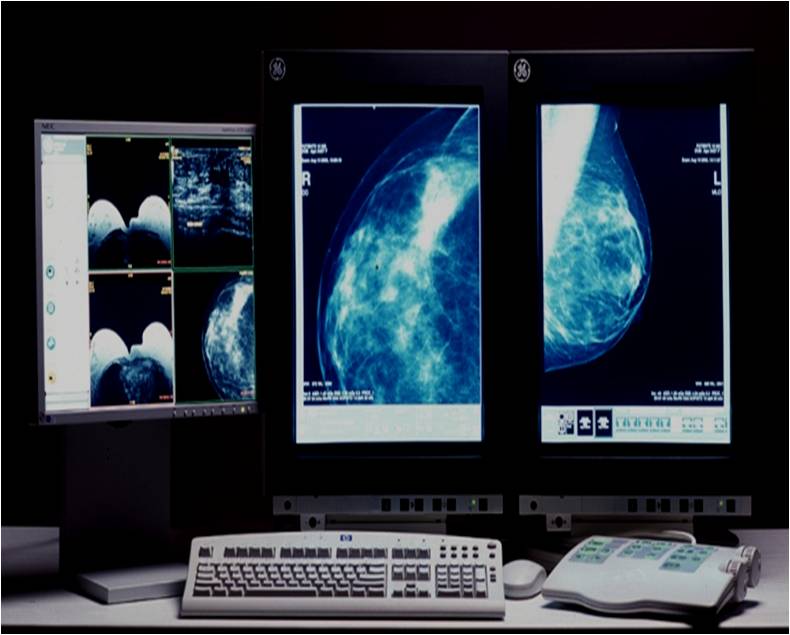
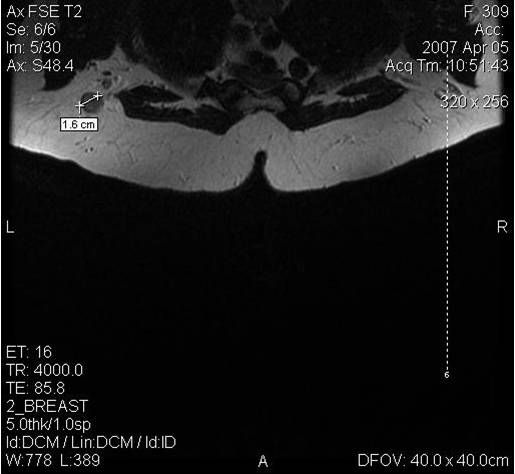
Карельская региональная общественная организация «Общество помощи больным заболеваниями молочной железы» была создана в 2002 году. Это пациентская организация: бывшие онкологические больные объединились, чтобы оказывать поддержку друг другу и вновь заболевшим женщинам. Проведенное нами ранее исследование подтвердило положительное влияние общения женщин, объединённых общими проблемами, между собой.
Основная цель организации — оказание помощи в реабилитации женщин с онкологическими заболеваниями молочной железы, оказание психологической и материальной поддержки.
Особое значение имеет установление контактов с другими организациями, подобными нашей. Так, в 2003-2005 годы были установлены связи со Шведской организацией «BROCANCER» в г. Шелефтео. Были проведены обучающие семинары по работе организации, занятия по профилактике лимфостаза и реабилитации. Шведская организация безвозмездно предоставила нашим женщинам парики, лечебное белье и экзопротезы.
В 2011 наша организация оказала поддержку подобной организации города Бишкека. В Киргизию мы отправили посылку с нашими буклетами («Рак молочной железы»), парики и лечебное белье.
Мы надеемся на установление новых контактов.
Thanks
Население нашего региона не слишком избаловано социальными льготами. Тем более ценным является тот факт, что неравнодушные инициативные люди продумали и осуществили проект, по которому выиграли Президентский грант, направленный на материальную помощь больным
людям.
Скажу про себя. Приобрести экопротез и соответствующий бюстгальтер ты просто вынуждена, чтобы выглядеть нормальной женщиной, а вот приобретение купальника, конечно откладываешь на потом — это ведь не предмет первой необходимости. Для меня возможность приобрести его практически бесплатно и хорошего качества — это большая материальная
поддержка. Да и моральная тоже — появились планы посещать бассейн, чувствуя себя там свободно и комфортно, настроение улучшилось. А когда настроение хорошее, то и болезни отступают. Душевное спасибо авторам проекта (Людмиле Григорьевне Симоновой и её коллегам) и успехов им в дальнейшей деятельности.
Даже очень сильные и самодостаточные люди нередко нуждаются в помощи и поддержке. Особенно, если они сталкиваются с проблемами онкологии. Возникает масса вопросов, страх и неизвестность. Как себя вести и как жить дальше так, чтобы не впадать в депрессии и отчаяние. Как убедить себя, что болезнь ещё не приговор. Организованная Людмилой Григорьевной встреча с человеком, который проходит все этапы лечения и при этом остаётся на позитиве, ведёт активный образ жизни и исходя из собственного опыта, наглядно нам показывает, что жизнь не закончилась. Организация подобных встреч очень важна, полезна, информативна и вдохновенна.
Благодарность
Хочу выразить благодарность общественной организации «Общество помощи больным заболеваниями молочной железы», республики Карелия. Силиконовый экзопротез молочной железы я получила за счёт гранта Президента Российской Федерации на развитие гражданского общества, предоставленного Фондом президентских грантов. Я молодая девушка, которая переживает страшную болезнь, РАК молочной железы. Не имея инвалидности мне выдали экзопротез. Я благодарна этой организации, так как покупка для меня не возможна, по причине его высокой стоимости.
Для молодой девушки очень важно чувствовать себя уверенной, а с одной грудью это не возможно. Экзопротез дал мне уверенности в том, что ни кто не узнает о моей болезни. Для психологического состояния это очень важно.
Большое, человеческое спасибо.
С уважением Елена Валентиновна.
Спасибо
Я член общественной организации КРОО «Общество помощи больным заболеваниями молочной железы» председателем правления которого являеться Симонова Л.Г. В этом году наша организация выиграла Президенский грант, благодаря которому не являясь инвалидом, я получила возможность бесплатно приобрести корректирующее белье и купальник для активного отдыха. Хочу высказать огромное СПАСИБО всем людям, кто с пониманием относится к нашей проблеме.
Особая благодарность
В моей жизни произошла большая беда. В преодолении её мне оказана помощь Карельской республиканской общественной организацией(КРОО) «Общество помощи больным
заболеваниями молочной железы». Отзывчивыми людьми этой организации и в частности Симоновой Людмилой Григорьевной мне жительнице Кемского района Коноваловой
Галине Петровне предоставлен экзопротез. Реализация проекта проводится на средства выделенные Президентом РФ на развитие гражданского общества из фонда
Президентских грантов. С уважением Г. Коновалова
В жизни каждого человека случаются разные ситуации. Так получилось, что мне пришлось перенести операцию по удалению груди, инвалидности не имею. Получить экзопротез молочной железы бесплатно и во время — это очень хорошо! Большое спасибо КРОО «Общество помощи больным заболеваниями молочной железы» и гранту Президента РФ за помощь, за проявление поддержки, за то, что не оставили меня наедине с моей проблемой. Отдельное спасибо за понимание, отзывчивость руководителю КРОО Симоновой Людмиле Григорьевне!
С уважением, Наталья Борисовна Казакова
«13 июля хирургическое отделение РОД г. Петрозаводска посетили члены КРОО «Общество помощи больным заболеваниями молочной железы». Пройдя по палатам, они пригласили женщин, которые перенесли операцию по поводу РМЖ, на беседу. Мы очень неохотно шли на эту встречу, а другие вообще не тронулись с кроватей. Но чем больше мы вникали в смысл беседы о преодолении послеоперационной депрессии, тем более заинтересованно мы слушали членов организации, уже преодолевших тяжелое послеоперационное состояние и вернувшихся к нормальной жизни. Мы узнали очень многое о работе общественной организации, которая реально помогает вновь заболевшим женщинам. Мы все получили Памятку для пациенток с РМЖ, в которой, как оказалось, мы много почерпнули для себя полезных рекомендаций и советов, как преодолеть психологическую послеоперационную депрессию. Особенно приятно было услышать приглашение на заседания Школы пациентов и другие мероприятия, проводимые общественной организацией. Когда в палатах мы рассказали об этой беседе, многие женщины пожалели, что не пошли на встречу. Большое спасибо членам этой организации за поддержку в трудный момент нашей жизни.»
источник
«Результаты УЗИ молочных желез выявили образование, подозрительное на онкологию», «результаты маммографии не позволяют однозначно исключить наличие злокачественного образования», «биопсия показала наличие раковых изменений в молочной железе и требуется расширенное обследование». Это лишь немногие из самых страшных слов, которые женщина может услышать от своего врача.
Молочные железы состоят из трех основных типов тканей — жировой, соединительной и железистой. Раком молочной железы (РМЖ) называют злокачественные опухоли, развивающиеся именно из клеток железистой ткани. Вопреки расхожему мнению, РМЖ заболевают как женщины, так и мужчины, однако у женщин он встречается примерно в 100 раз чаще.
Рак груди развивается так же, как и любая другая злокачественная опухоль в организме. Одна или несколько клеток железистой ткани в результате произошедшей в них мутации начинают аномально быстро делиться. Из них образуется опухоль, способная прорастать в соседние ткани и создавать вторичные опухолевые очаги — метастазы.
Мутации, которые приводят к РМЖ, бывают наследственными и приобретенными.
Распространенными наследственными генетическими причинами рака молочной железы становятся мутации в генах BRCA1 и BRCA2. Носительницы мутации BRCA1 имеют риск заболеть раком молочной железы 55–65%, а носительницы BRCA2 — 45%. Такие генетические дефекты передаются по наследству от родителей детям, они становятся причиной рака молочной железы примерно в 15% случаев.
Намного чаще опухоль возникает из-за приобретенных мутаций: они возникают в клетках молочной железы и не передаются по наследству. Например, в 20% случаев увеличено количество копий гена, кодирующего HER2 — белок-рецептор, который находится на поверхности клеток и стимулирует их размножение.
«Молекулярно-генетический портрет» опухоли имеет важное значение при выборе оптимального лечения.
Чаще всего опухоли молочных желёз развиваются из клеток молочных протоков — в этом случае врачи говорят о протоковом раке молочной железы или протоковой карциноме. Довольно часто злокачественные опухоли вырастают из клеток долек молочной железы, этот тип рака называют инвазивной лобулярной карциномой (инвазивный рак молочной железы). Стоит отметить, что рост опухоли возможен и из других клеток железистой ткани.
К сожалению, полной информации о причинах возникновения рака молочной железы у ученых пока нет. Существует список факторов риска, влияющих на вероятность появления опухоли, однако у некоторых болезнь диагностируют при отсутствии этих факторов, другие же остаются здоровыми при наличии сразу многих из них. Тем не менее, ученые все же связывают развитие рака груди с определенными обстоятельствами, наиболее часто предваряющими его появление. К ним относятся:
- Возраст. Большинство случаев РМЖ приходятся на женщин в возрасте 55 лет и старше.
- Наследственность. Если РМЖ диагностирован у кого-то из близких родственников, риск повышается вдвое.
- Рак молочной железы в анамнезе.
- Повышенная плотность ткани молочной железы по результатам маммографии.
- Некоторые доброкачественные новообразования в молочной железе.
- Раннее начало менструаций — до 12 лет.
- Поздняя менопауза — после 55 лет.
- Отсутствие детей или поздние (после 35 лет) первые роды.
- Воздействие радиации, например, в ходе лучевой терапии, проводимой для лечения другого типа рака.
- Курение и злоупотребление алкоголем. Если женщина ежедневно потребляет 28–42 г этилового спирта, ее риски повышаются на 20%.
- Лишний вес и низкая физическая активность.
- Использование гормональных препаратов: оральные контрацептивы, заместительная гормональная терапия в постменопаузе.
- Травмы молочных желез.
- Сахарный диабет.
- Работа по графику с ночными сменами.
Довольно часто на ранних стадиях рак молочной железы протекает бессимптомно. Но в ряде случаев признаки, указывающие на наличие заболевания, все же есть, и их можно заметить.
В первую очередь, к симптомам, которые должны насторожить, относят уплотнения в молочных железах, рядом с ними или в подмышечной впадине. В 9 случаях из 10 уплотнения бывают доброкачественными, однако установить это наверняка можно только на осмотре у маммолога.
К симптомам рака молочной железы относят:
- Отвердение кожи
- Участок втяжения кожи
- Эрозия кожи
- Покраснение кожи
- Выделения из соска
- Деформация молочной железы по типу ряби
- Припухлость кожи
- Увеличенные в размерах вены
- Втяжение соска
- Нарушение симметрии молочных желез
- Симптом лимонной корки
- Пальпируемый узел внутри молочной железы.
При появлении указанных симптомов, а также любых других изменений в молочных железах (например, необычных или болезненных ощущений) нужно немедленно проконсультироваться с маммологом.
В Европейской клинике ведёт консультативный приём и выполняет операции известный российский хирург-маммолог, доктор медицинских наук Сергей Михайлович Портной (автор более 300 печатных работ, член правления Российского общества онкомаммологов, автор трех патентов на изобретения).
Сергей Михайлович выполняет весь объем оперативных вмешательств на молочной железе, включая органосохраняющие и реконструктивные пластические операции.
Самостоятельно проверять грудь на наличие узелков или каких-либо других изменений стоит раз в месяц, по окончании менструации. Домашнюю диагностику удобнее всего проводить, принимая ванну или находясь под душем. О любых изменениях, которые удалось обнаружить, стоит как можно быстрее рассказать врачу.
Порядок проведения самообследования молочных желез:
- Разденьтесь выше пояса и встаньте перед зеркалом.
- Поднимите руки вверх и заведите их за голову. Внимательно осмотрите грудь. Повернитесь правым, левым боком.
- Ощупайте молочные железы в положении стоя сложенными указательным, средним и безымянным пальцем. Начинайте с верхней наружной части груди и двигайтесь по часовой стрелке.
- Сожмите сосок двумя пальцами. Проверьте, выделяется ли из него что-нибудь.
- Снова ощупайте молочные железы — теперь в положении лежа.
70% случаев рака молочной железы выявляются пациентами самостоятельно в результате самообследования груди.
О роли биопсии в диагностике рака молочной железы рассказывает врач Европейской клиники Портной С.М.:
Для подтверждения или исключения диагноза в первую очередь проводится мануальное обследование груди. Затем, при наличии подозрений или в качестве скрининговой процедуры, может быть назначена маммография, рентгенологическое исследование молочных желез. Как правило, женщинам до 35 лет ее выполнение не рекомендуется, в молодости ткань молочных желез особенно чувствительна к радиоактивному облучению.
Ультразвуковое исследование (УЗИ) молочных желез позволяет оценить структуру их ткани и отличить, например, опухоль от кисты, наполненной жидкостью.
Если результаты маммографии или УЗИ указывают на наличие новообразований в молочной железе, врач, как правило, назначает биопсию, лабораторное исследование образца тканей из молочной железы. Биопсия позволяет выяснить, является ли опухоль злокачественной, а также определить ее тип и стадию. Кроме того, исследование биопсийного материала дает ответ на вопрос, является ли опухоль гормонозависимой, что также влияет на схему лечения.
При необходимости могут использоваться и другие диагностические методы, например, магнитно-резонансная томография (МРТ).
После постановки диагноза основной задачей лечащего врача является определение стадии онкологического заболевания, то есть размера опухоли, ее расположения, наличия метастазов и агрессивности. От этих факторов зависит прогноз лечения и подбор оптимальных методов терапии. Как правило, для уточнения стадии проводятся анализы крови, маммография другой молочной железы, сканирование костей, а также компьютерная или позитронно-эмиссионная томография. В некоторых случаях определить стадию опухоли можно только при проведении операции.
Стратегия лечения рака молочной железы зависит от многих факторов — типа рака, стадии, чувствительности клеток опухоли к гормонам, а также общего состояния здоровья пациентки.
Основной метод лечения рака груди — хирургическая операция. Если болезнь удалось диагностировать на ранней стадии, хирург может выполнить лампэктомию, удаление тканей опухоли и небольшой части окружающей ее здоровой ткани. При более крупных опухолях молочная железа удаляется целиком (такая операция называется мастэктомией), равно как и ближайшие к ней лимфатические узлы. Если по оценке врача риск развития рака во второй молочной железе достаточно высок, пациентке может быть рекомендовано удаление обеих молочных желез сразу.
Чтобы разобраться, распространились ли раковые клетки в лимфатические узлы, и определиться с объемом хирургического вмешательства, может быть проведена сентинель-биопсия, или биопсия сторожевого лимфоузла. Во время операции в опухоль вводят радиофармпрепарат или флуоресцентный краситель — это помогает визуализировать лимфоузел, который первым принимает лимфу от ткани молочной железы. Его удаляют и проводят гистологическое исследование. Если в сторожевом лимфоузле не обнаруживают опухолевых клеток, можно ограничиться удалением очага в молочной железе. В противном случае показано иссечение регионарных лимфоузлов.
Лучевую терапию (то есть воздействие на опухоль ионизирующим излучением) при раке молочной железы, как правило, используют после проведения хирургической операции. Терапия проводится с целью уничтожения раковых клеток, которые могли остаться в организме.
Химиотерапия, то есть использование препаратов, убивающих раковые клетки, может проводиться после операции по удалению опухоли, как и лучевая терапия. В некоторых случаях химиотерапию проводят до оперативного лечения для того, чтобы уменьшить размер слишком крупной для удаления опухоли.
В Европейской клинике для лечения рака молочной железы применяются наиболее современные, оригинальные европейские и американские химиопрепараты. У нас есть возможность составить «молекулярный отпечаток» опухоли, подобрать на основании его анализа наиболее эффективные и безопасные комбинации лекарств.
Для лечения рака молочной железы, чувствительного к гормонам, используют гормональную терапию — к ней относится несколько разных методов, останавливающих выработку гормонов в организме или блокирующих их поступление к опухоли. Гормональная терапия позволяет снизить вероятность рецидива опухоли, а также, в случае выявления неоперабельной опухоли, помогает контролировать ее рост.
Для лечения рака молочной железы применяют также таргетную терапию — препараты, поступающие непосредственно к тканям опухоли и минимально воздействующие на здоровые клетки организма. Таргетную терапию используют либо отдельно, либо в комбинации с другими методами лечения — в зависимости от того, какая схема лучше всего подойдет пациенту.
Если рак молочной железы диагностирован на ранних стадиях (0-I), пятилетняя выживаемость приближается к 100%. То есть, можно сказать, что удается вылечить практически всех женщин. Далее, в зависимости от стадии, прогноз относительно пятилетней выживаемости ухудшается:
- На II стадии — 93%.
- На III стадии — 72%.
- На IV стадии — 22%.
Совокупность имеющихся в арсенале онкологов методов лечения рака молочной железы позволяет в большинстве случаев добиться ремиссии заболевания или, как минимум, продлить жизнь с сохранением ее качества. Однако следует помнить, что эффективность лечения в целом напрямую зависит от того, было ли лечение начато своевременно, то есть на ранних стадиях заболевания.
Максимальная эффективность противоопухолевого лечения достигается только в том случае, если оно проводится в соответствии с международными протоколами, при этом учитываются индивидуальные особенности каждого пациента. Именно так назначают лечение онкологи Европейской клиники.
источник
Уважаемые участники группы !
Огромная просьба рассказать как можно большему количеству людей об истории Татьяны! Вместе мы победим болезнь!
Каждый способ — реальная помощь Татьяне!
Показать полностью…
1. Перепостом (нажать под аватаром группы «Рассказать друзьям») — 1-2 секунды .
2. Пригласить друзей в группу https://m.vk.com/club127940764 2-3 минуты!
3. Распространить пост в других социальных сетях: в Одноклассниках, в Твиттере, на Фейсбуке и в др.- 5-6 минут!
4. Лично рассказать коллегам и друзьям об этой истории болезни Татьяны и предложить каждому передать через Вас сколько возможно, даже по 10-50 рублей — 1-2 минуты во время чаепития!
5. Может быть, у Вас есть мелочь (раскидана по карманам, дому, в кошельке или висят копейки на электронных кошельках)? Даже рубль-два тоже необходимы, заверяем Вас, любая сумма очень нужна! Реквизиты — https://m.vk.com/topic-127940764_34225531
ПОЖАЛУЙСТА, не пройдите мимо! ДАЖЕ МИНИМАЛЬНАЯ ПОМОЩЬ ОЧЕНЬ НУЖНА! СПАСИБО ВАМ!
Опубликовано из Контакта для iPhone – http://vk.cc/4Vbr0j
Минздрав РФ закрыл госпрограмму по борьбе с онкологией
Министерство здравоохранения РФ приняло решение не продлевать Федеральную национальную онкологическую программу.
В минувший четверг, 13 ноября, в Москве представители медицинского сообщества обсудили итоги этой программы за пять лет, что она реализовывалась, с 2009 по 2014 год. За это время было потрачено 47 миллиардов рублей.
Показать полностью…
Сами медики оценивают программу как успешную и нуждающуюся в развитии. На выделенные государством средства было закуплено и установлено 400 тысяч единиц высокотехнологического медицинского оборудования, такого как компьютерные и магнитно-резонансные томографы, рентгенологические приборы, видеоэноскопические комплексы. Новые приборы позволяют проводить более точечное и точное лечение, за счет чего эффективность лечения увеличивалось, а побочные эффекты лучевой терапии снижались.
Однако, при всем при этом оказалось, что на суперсовременной технике попросту некому работать и следующим шагом в борьбе с онкологическими заболеваниями должна стать подготовка квалифицированных специалистов. Так, во всей России работают только около тысячи лучевых терапевтов. Также наблюдается существенный дефицит медицинских физиков, так как многие выпускники по данной специальности не работают по профессии, а другие уезжают за пределы России или в частные клиники, так как в бюджетной медицине зарплаты низкие.
«Нужно выйти на средний уровень по Европе. Количество физиков у нас меньше, чем в США, в 28 раз. Необходимо удерживать этих штучных специалистов в России. Особенно кадровая проблема касается регионов: вместо комнаты в коммуналке и зарплаты в 20 тыс. руб. нужно предоставлять им отдельное жилье и достойные зарплаты», – цитирует специалистов «Коммерсантъ».
В целом за пять лет, что проводилась программа, смертность от рака сократилась только на 1 процент. Минздрав считает этот показатель очень низким. В свою очередь медики говорят, что смертность остается на прежнем уровне в первую очередь из-за поздней диагностики рака, тогда как процент излечившихся от онкологии пациентов увеличился.
С 2015 года Минздрав РФ переводит систему здравоохранения на самофинансирование, а это означает, что расходы на лечение раковых больных лягут на систему ОМС и самих пациентов, так как страховка не покроет все затраты на лечение. Стоимость одного курса лечения может достигать 1,5 миллионов рублей.
В качестве альтернативы специалисты рекомендуют включить онкологию в перечень заболеваний, лечение которых будет оплачиваться за счет работодателя, а в случае, если работодатель не может оплачивать это лечение, то большую часть расходов должно оплачивать государство.
По мнению представителей Минздрава, федеральная национальная онкологическая программа выполнила поставленные задачи, а потому ее продолжения не планируется. В ведомстве заявили, что проблемы диагностики и лечения рака решаются в других федеральных и региональных программах. Приоритетным направлением на 2015 год являются работы по развитию сети первичных онкологических и смотровых кабинетов.
«Активная работа по повышению онконастороженности проводится с медицинским персоналом первичного звена здравоохранения. Кроме того, мы разрабатываем другое важное направление — информирование населения о необходимости профилактики онкологических заболеваний», – приводит «Коммерсантъ» слова представителей министерства.
источник
По распространенности рак молочной железы (РМЖ) занимает первое место среди онкологических заболеваний. Он поражает ежегодно 1 млн. 600 тыс. женщин в мире и свыше 66 тыс. в Российской Федерации.
В ближайшие 20 лет во всех странах прогнозируется почти двукратное увеличение заболеваемости женщин раком груди, что объясняется увеличением продолжительности жизни и улучшением методов диагностики.
За последние годы, благодаря более раннему выявлению опухолей, смертность от рака груди у женщин снижается. В развитых странах, где применяется маммографический скрининг населения, этот показатель снизился на 30–50%.
Рак молочной железы – это не единообразное заболевание. При лечении клиницисты учитывают принадлежность опухоли к конкретному подтипу. Генетическое тестирование и иммуногистохимический метод, позволяют надежно определить биологические подтипы РМЖ. Эти подтипы сами по себе включают многие факторы риска и предсказывающие признаки, что позволяет выбрать наиболее эффективную терапию для больного.
Доказанное с помощью молекулярно-генетического анализа и иммуногистохимического исследования патогенетическое разнообразие РМЖ позволяет индивидуализировать лечение.
Увеличение выживаемости при раке молочной железы связано не только с широкомасштабным внедрением маммографического скрининга, но и адекватным использованием системных видов лечения.
Для выявления злокачественных опухолей молочной железы существует определенный алгоритм диагностики, и его первичный элемент — маммографический скрининг. Чувствительность этого метода диагностики для опухолей от 2 мм до 5 мм составляет около 85%. Маммографическое исследование выполняют в двух проекциях.
Молодым женщинам с плотным строением молочной железы необходимо включение в программу наблюдения методов УЗИ и МРТ.
Поскольку традиционный маммографический скрининг у женщин до 40 лет малоэффективен, для скрининга может понадобиться альтернативная методика — МРТ. Современная контрастная магнитно-резонансная томография — высокочувствительный метод диагностики заболеваний молочной железы.
МРТ-диагностика рака молочной железы
У женщин с мутациями BRCA1 или BRCA2 при проведении МРТ возможно диагностировать рак молочной железы на самых ранних стадиях.
При ряде показаний женщинам назначается биопсия молочной железы под контролем УЗИ. Это исследование позволяет прицельно брать биологический материал для гистологического исследования, определения уровня экспрессии стероидных гормонов и статуса Her-2.
Известно множество факторов, повышающих риск возникновения рака молочной железы. На некоторые из них повлиять невозможно:
- семейная история по РМЖ,
- раннее менархе (начало месячных),
- позднее наступление менопаузы.
В то же время существуют и модифицируемые факторы, такие как:
- избыточный вес в постменопаузе,
- использование заместительной гормонотерапии,
- потребление алкоголя,
- курение
Стратегические шаги, направленные на снижение риска возникновения РМЖ включают контроль веса и борьбу с ожирением, регулярную физическую активность, уменьшение потребления алкоголя.
Большинство факторов риска рака молочной железы связано с действием гормонов на ткань молочной железы (раннее менархе, позднее наступление менопаузы, ожирение, применение гормональных препаратов). Считается, что именно женские половые гормоны, стимулируют процессы клеточного роста и повышают риски повреждения ДНК, что может привести к развитию злокачественного новообразования.
Только 5–10% случаев рака молочной железы обусловлены унаследованными мутантными генами BRCA. Но при этом, среди носителей мутаций риск возникновения заболевания может достигать 80%.
Чем младше возраст выявления первичного заболевания рака груди, тем выше вероятность заболеть контралатеральным раком, т.е. противоположной молочной железы.
Семейная история с наличием заболеваний раком молочной железы у кровных родственников, даже без ассоциации с мутациями BRCA, также повышает риск возникновения РМЖ.
Ожирение
Различными исследованиями доказано существование связи между заболеваемостью первичным РМЖ в постменопаузе и ожирением. Есть подтверждение связи между избыточным весом и низкой выживаемостью при всевозможных видах РМЖ.
Алкоголь
Алкоголь — также установленный фактор риска возникновения первичного РМЖ. Достоверность его отрицательного воздействия на пациентов, перенесших рак молочной железы, убедительна, так как он влияет на увеличение количества циркулирующих эстрогенов.
Только врач может оценить значимость различных симптомов. Однако каждой женщине необходимо знать, при каких симптомах надо обращаться к маммологу:
- «Образование», уплотнения, узел, инфильтрат, опухоль, «шарик» — что-то подобные этому вы обнаружили. Это еще не повод решить, что у вас РМЖ, но повод показаться специалисту.
- Деформация контура молочной железы, ареолы или соска (втяжение кожи или наоборот выбухание)
- Втяжение соска; особенно, если появилось недавно
- Выделение крови из соска
- Отек кожи всей молочной железы или ее локального участка
- Появление раздражения, мокнутые «ранки», язвочки, корочки на соске или ареоле
- Изъязвления (длительные, без видимой причины) на коже груди
- Дискомфорт в подмышечной области и обнаружение лимфоузлов ( «шариков» ) в подмышечной области
- Изменение цвета кожи молочной железы — покраснение, повышение температуры кожи в этой области.
Все эти симптомы могут быть проявлениями различных заболеваний (их насчитывается несколько десятков), возможно, не злокачественной природы. Однако, это может решить только специалист по заболеваниям молочной железы.
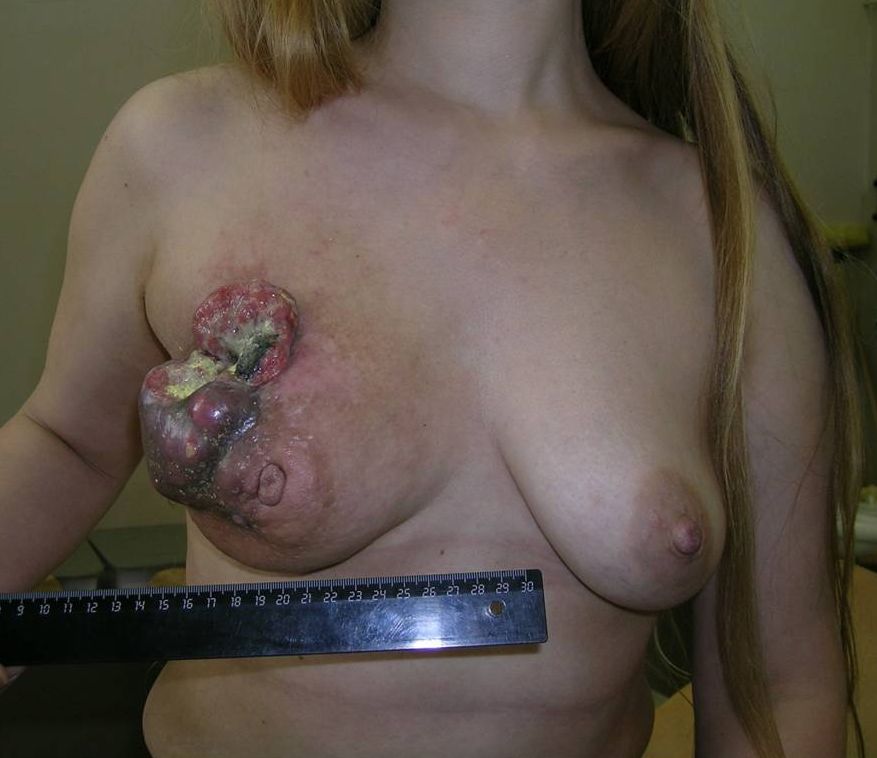
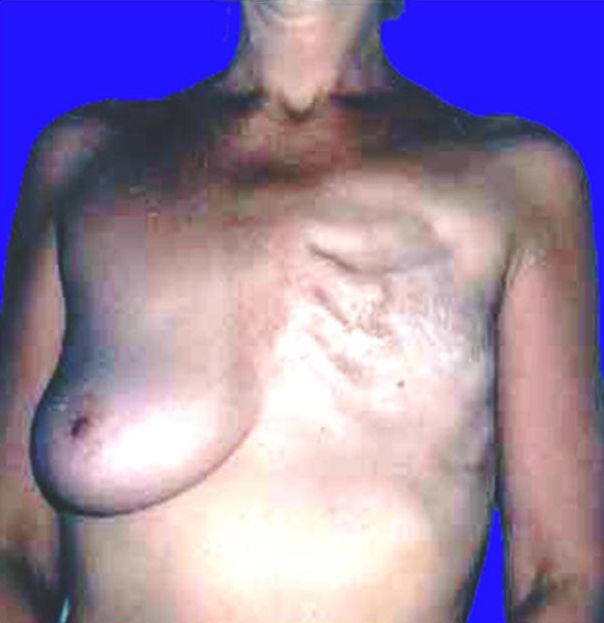
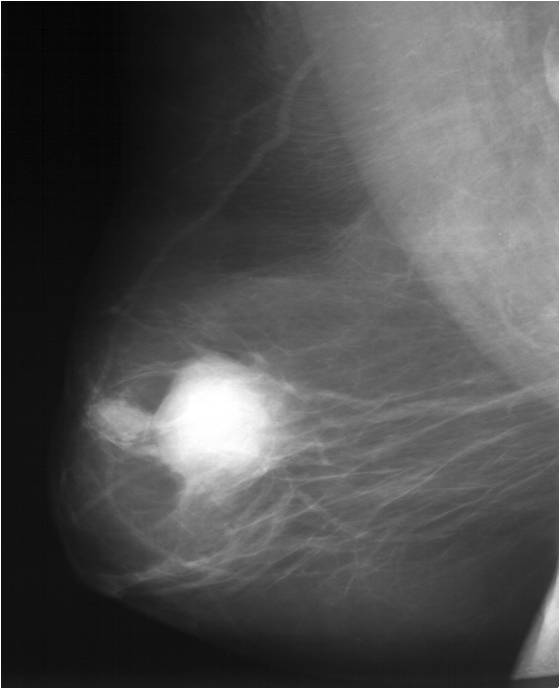
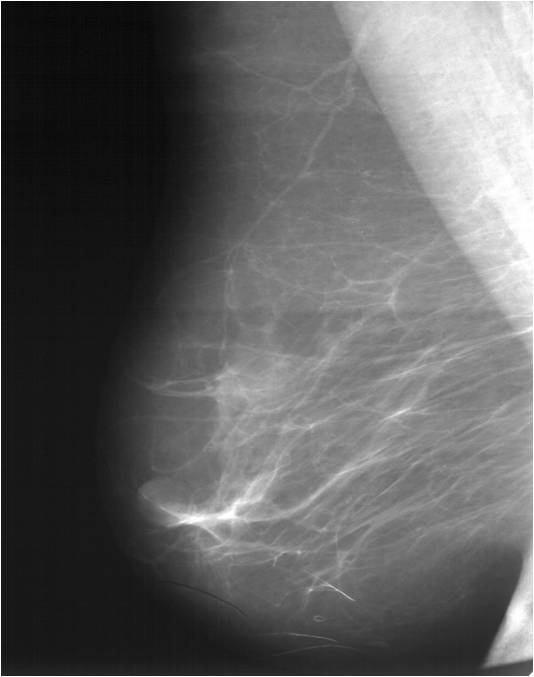
Признаки и симптомы рака молочной железы
0 стадия
Это стадия, когда не выявлена первичная опухоль, или она не может быть оценена, а также в случае неинвазивного рака молочной железы (что означает опухоль не выходит за границы своего появления, так называемый рак in situ).
1 стадия
Раковые клетки в этой стадии инвазируют или прорастают в соседние ткани. Опухолевый узел не более 2 см, лимфоузлы при этой стадии не поражены.
2 стадия
В этой стадии опухолевый узел превышает 2см и может достигать до 5см. При этой стадии могут быть поражены лимфоузлы, но поражение лимфоузлов носит одиночный характер, они не спаяны друг с другом и находятся на той же стороне, что и опухоль. В случае поражения лимфоузлов размер опухоли может быть и менее 2см.
3 стадия
Инвазивный рак, более 5 см или с явным и значительным поражением лимфатических узлов. При этом лимфоузлы могут быть спаяны между собой.
4 стадия
На этой стадии опухоль прорастает в кожу груди, грудную стенку либо во внутренние грудные лимфатические узлы. Она может быть любых размеров.
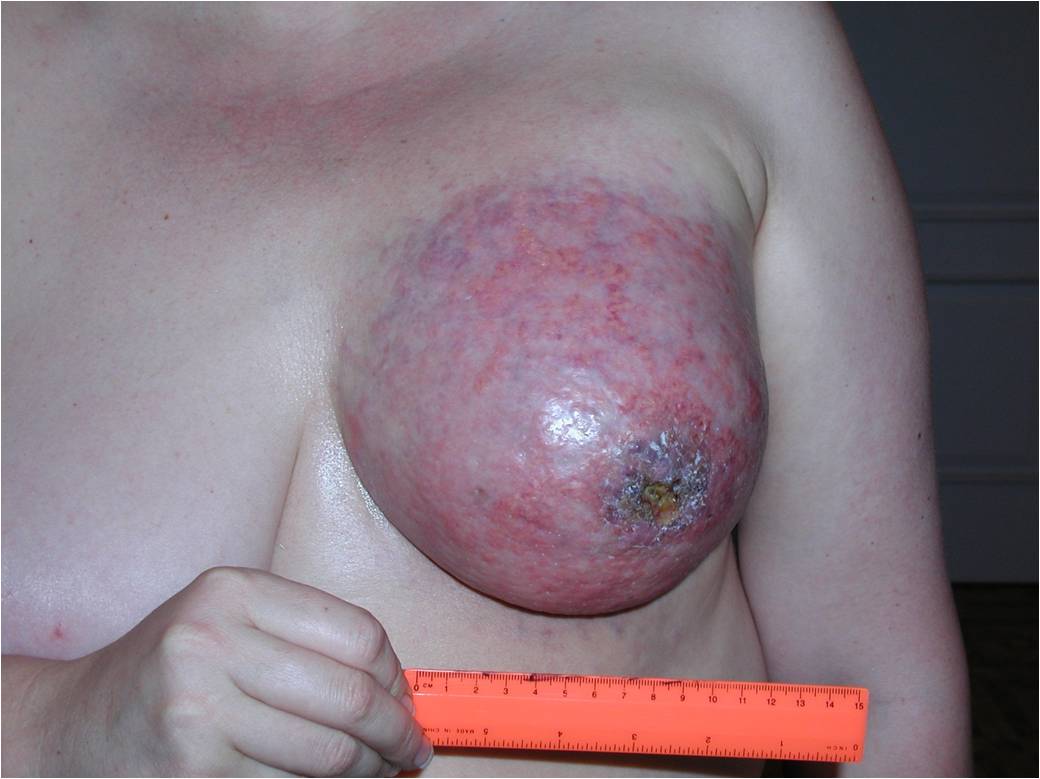
К 4 стадии рака молочной железы относится воспалительный рак, он встречается до 10 % всех случаев. Симптомы воспалительной формы рака груди это покраснение кожных покровов, железа становится теплой, отмечается увеличение и/или уплотнение части либо всей молочной железы. Кожа приобретает вид апельсиновой корки. Эту форму рака надо дифференцировать с воспалением молочной железы – маститом.
Также при 4 стадии опухоль может распространяться за пределы грудной клетки, в подмышечную область, внутренние грудные лимфатические узлы. Возможны метастазы в надключичные лимфатические узлы, а также в легкие, печень, кости или головной мозг.
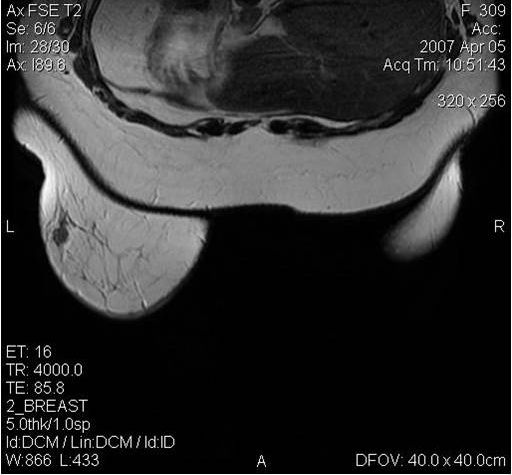
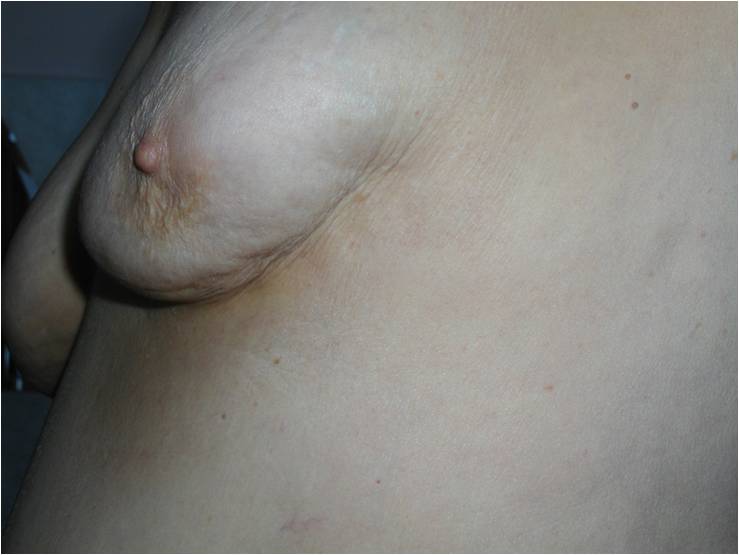
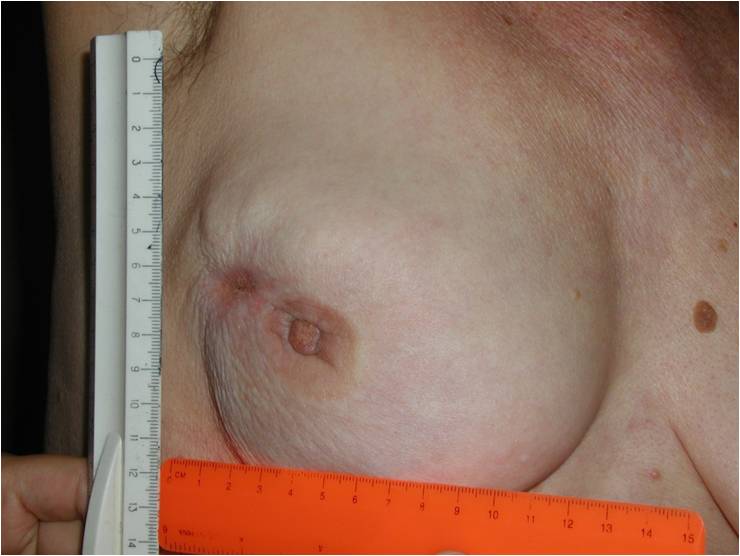
Как выглядит рак груди в разных стадиях:
Хирургическая операция — основной метод лечения при опухолях груди, и от качества его проведения во многом зависит исход заболевания. По данным некоторых штатов Индии, в которых по религиозным мотивам не проводится хирургическое лечение, показатели заболеваемости практически равняются показателям смертности. Обычно смертность от РМЖ в два — четыре раза уступает заболеваемости.
Однако, после хирургического лечения чаще всего следует лучевое. Местное лечение без послеоперационной лучевой терапии часто приводит к локально-регионарным рецидивам заболевания. Дело в том, что после завершения хирургической операции невозможно исключить существования скрытых отдаленных метастазов. Даже у больных с опухолями менее 1 см в диаметре в 10% случаев возможен рецидив заболевания.
Локализация отдаленных метастазов при РМЖ
Сейчас во всем мире наблюдается тенденция к сокращению объема хирургического вмешательства без потери эффективности. Хирургическое и лучевое лечение РМЖ развивается и совершенствуется в направлении органосохранения.
Благодаря внедрению маммографического скрининга, резко возросло число больных с ранней стадией заболевания, когда лимфоузлы не поражены метастазами. В этом случае «классическое» удаление всех уровней лимфоузлов было бы избыточной калечащей процедурой. На помощь хирургам пришел метод биопсии сигнальных (сторожевых) лимфатических узлов.
Поскольку, метастазы в подмышечных лимфоузлах появляются последовательно от первого ко второму, затем к третьему уровню, то достаточно определить наличие метастазов именно в первом лимфоузле. Его назвали «сигнальным»: если сигнальный лимфатический узел не содержит метастазов, то другие лимфоузлы также не метастатические.
Благодаря этому органосохраняющему методу, тысячи пациенток избежали избыточной полной хирургической диссекции, удаление раковой опухоли не привело к удалению груди.
Последние результаты клинических испытаний, в том числе и при участии НИИ онкологии им. Н.Н. Петрова, подтвердили безопасность отказа от полной подмышечной диссекции. Биопсия сигнальных (сторожевых) лимфатических узлов постепенно вытесняет подмышечную диссекцию как стандартную процедуру стадирования РМЖ.
Концепция биопсии сигнальных лимфатических узлов приобретает все большее признание и введена для многих локализаций опухолей в стандарты хирургического лечения Европейской Организацией по Изучению и Лечению Рака (EORTC).
Химиотерапия, наряду с хирургическим вмешательством, является одним из основных методов терапии рака. Послеоперационная химиотерапия улучшает результаты хирургического лечения, как и прогноз заболевания.
Ранее решение о назначении химиотерапии основывалось на двух факторах:
- стадия заболевания
- состояние регионарных лимфоузлов.
Благодаря многочисленным исследованиям ученых изменяются представления о биологии рака молочной железы, и выбор режимов химиотерапии значительно расширяется. И сегодня химиотерапевтическое лечение назначают даже при отсутствии метастазов в лимфоузлах, если небольшие по размеру опухоли обладают агрессивными биологическими характеристиками.
Люминальный А рак
При люминальном А раке избегают назначать проведение химиотерапии, особенно при негативных лимфоузлах, и применяют одну эндокринотерапию.
Люминальный В рак
Люминальные В опухоли характеризуются высокой агрессивностью. В этом случае чаще всего будет назначена химиотерапия, а выбор лечения основывается на оценке риска развития рецидива.
HER2-позитивный рак молочной железы
Лечение HER2-позитивного рака молочной железы основано на применении стандартных схем химиотерапии – трастузумаб и ХТ, основанная на антрациклинах и таксанах. Однако, только небольшой процент пациентов выигрывает от лечения, но все подвержены связанной с этим токсичностью.
Трижды негативный РМЖ
Трижды негативный рак молочной железы обычно ассоциируется с плохим прогнозом. Из-за редкой встречаемости особых типов РМЖ нет достаточных данных о роли адъювантной химиотерапии.
Химиотерапия при РМЖ у очень молодых женщин
Рак молочной железы в молодом возрасте обычно протекает агрессивно, часто встречаются гормонорезистеные и HER2-позитивные опухоли с иными свойствами, чем у более пожилых женщин. Для таких пациенток, моложе 35 лет, адъювантная полихимиотерапия почти всегда является необходимым методом лечения.
Химиотерапия пожилых пациенток
У пожилых пациенток (старше 65 лет) при решении вопроса о назначении адъювантной химиотерапии обязательно учитываются общее состояние организма и наличие сопутствующих хронических заболеваний.
В идеале пожилые пациенты должны подвергаться гериатрической оценке для определения их «пригодности» к адъювантому лечению. Потенциальный эффект лечения должен быть сбалансирован с теми рисками для организма, которые несет химиотерапия. Врач определяет наиболее эффективный и при этом наиболее безопасный специфический режим, основываясь на подтипе опухоли и индивидуальных характеристиках пациента.
Гормонотерапия
Молодые женщины с гормоноположительным раком молочной железы сохраняют риск рецидива заболевания на протяжении по крайней мере 15 лет после первичного заболевания. Онкологи должны определить, кто из пациентов нуждается в долгосрочной адъювантной терапии тамоксифеном или ингибиторами ароматазы.
Неоадъюватная (предоперационная) терапия
Неоадъюватная терапия занимает ведущую роль в лечении женщин с неоперабельным раком молочной железы, а также имеет важное значение при операбельных опухолях, когда выполняются органосохраняющие операции.
Эффект неоадъювантного лечения ДО (слева) и ПОСЛЕ (справа)
Лучевое лечение после проведенного хирургического вмешательства играет важную роль в терапии рака молочной железы и прогнозе заболевания. В НМИЦ онкологии им. Н.Н. Петрова было проведено исследование роли лучевой терапии после органосохраняющих операций (секторальная резекция с аксиллярной лимфоаденэктомией) у пациенток с минимальным РМЖ.
Анализ десятилетней безрецидивной выживаемости доказал более высокую эффективность лечения в группе больных, где применялась послеоперационная лучевая терапия.
Использование лекарственных препаратов для снижения риска заболевания называется химиопрофилактикой. На сегодняшний день одобренными препаратами для профилактики рака молочной железы являются тамоксифен и ралоксифен.
Тамоксифен может использоваться как пременопаузальными, так и постменопаузальными женщинами. Прием тамоксифена приводит к снижению риска РМЖ на 38% на более чем 10 летний период. Наиболее распространенными нежелательными явлениями на фоне приема препарата являются приливы.
В настоящее время клинические исследования изучают роль другого класса препаратов – ингибиторов ароматазы для оценки эффектов снижения риска РМЖ, которые сегодня используются только для лечения РМЖ. Предварительные результаты оказываются многообещающими. Ингибиторы ароматазы действуют только у женщин с нефункционирующими яичниками.
Профилактические хирургические операции по удалению молочных желез проводятся только в одном случае – если женщина является носителем мутаций в генах BRCA1 и BRCA2, известных как «синдром Анджелины Джоли». Мировой практикой доказано, что при удалении ткани обеих молочных желез риски РМЖ снижаются более чем на 90%. Такие операции выполняются в клиниках США и Израиля. В Европе подход к этому вопросу более консервативный.
В НМИЦ онкологии им. Н.Н. Петрова при проведении хирургического лечения женщинам с мутациями BRCA1 предлагается профилактическое удаление и реконструкция молочной железы.
Московского
Онкологического
Общества
КОМБИНИРОВАННО-РАСШИРЕННЫЕ ЗАСЕДАНИЯ МОСКОВСКОГО ОНКОЛОГИЧЕСКОГО ОБЩЕСТВА – НОВЫЙ ФОРМАТ ОБСУЖДЕНИЯ РАЗРАБОТОК СОВРЕМЕННОЙ ОНКОЛОГИИ
ЗАСЕДАНИЕ 567
состоится в четверг 22 апреля 2010 г. в 17:00
в конференц-зале Клиники
Российского онкологического научного центра им. Н.Н. Блохина
Председатели: проф. А.И. Пачес, чл.-корр. РАН, проф. М.Р. Личиницер
ЛЕЧЕНИЕ БОЛЬНЫХ РАКОМ МОЛОЧНОЙ ЖЕЛЕЗЫ
1) ПЕРВИЧНО-ОПЕРАБЕЛЬНЫЕ ОПУХОЛИ
СОВРЕМЕННЫЕ ПРИНЦИПЫ ЛЕЧЕНИЯ БОЛЬНЫХ
ПЕРВИЧНО-ОПЕРАБЕЛЬНЫМ РАКОМ МОЛОЧНОЙ ЖЕЛЕЗЫ
Портной С.М.
(Российский онкологический научный центр им. Н.Н. Блохина)
Дискуссия, фиксированные выступления в прениях
Принципы лечения больных первично-операбельным
раком молочной железы
Бурлаков А.С. (Московская онкологическая клиническая больница № 62)
Колесников Р.В., Хмелевский Е.В. (РНЦ рентгенорадиологии)
Соболевский В.А. (РОНЦ им. Н.Н. Блохина)
Строяковский Д.Л. (Московская онкологическая клиническая
больница № 62)
Трофимова О.П. (РОНЦ им. Н.Н. Блохина)
НОВЫЙ ФОРМАТ ЗАСЕДАНИЙ ОБЩЕСТВА
Проблемы лечения больных раком молочной железы лишь фрагментарно обсуждались в 2000-х гг. на заседаниях Московского Онкологического общества: «Сигнальный («сторожевой») лимфоузел рака молочной железы» (заседание №474; 25.01.01); «Рак молочной железы и беременность» (заседание №486; 28.03.02); «Хирургия рака молочной железы» (заседание №490; 26.09.02); «Лучевая терапия рака молочной железы» (заседание №508; 20.05.04); «Реабилитация после мастэктомии» (заседание №527; 20.04.06).
Разумеется, представляет интерес попытка обсуждения всей необъятной проблемы в целом. В этой связи организационный комитет Общества предлагает вначале – в апреле – рассмотреть вопросы (принципы; «стандарты») преимущественно хирургического лечения больных первично операбельными опухолями. См. формулировку повестки дня:
ЛЕЧЕНИЕ БОЛЬНЫХ РАКОМ МОЛОЧНОЙ ЖЕЛЕЗЫ. 1) ПЕРВИЧНО-ОПЕРАБЕЛЬНЫЕ ОПУХОЛИ. При этом предполагается придать информационное насыщение следующей лечебной схеме:
Лечение при I стадии (T1NM) предусматривает мастэктомию с сохранением грудных мышц (либо – радикальную органосохраняющую операцию) ± гормонотерапию. При II стадии (T1N1M; T2N0-1M; T3NM) проводится неоадъювантная химиотерапия + операция вышеуказанного объема (в случаях центральной локализации – мастэктомия + 6 курсов САF). В отдельных случаях при IIIа стадии (T1-2N2M; T3N1-2M) назначается неоадъювантная химиотерапия (4-6 курсов) + мастэктомия + химио-лучевая терапия. Подлежат обязательному обсуждению возможности реконструкции молочной железы при I-III стадиях.
В последующем, после анализа тематических предложений и дополнений появляется возможность органично перейти ко второй части заседания:
ЛЕЧЕНИЕ БОЛЬНЫХ РАКОМ МОЛОЧНОЙ ЖЕЛЕЗЫ. 2) МЕСТНОРАСПРОСТРАНЕННЫЕ И ДИССЕМИНИРОВАННЫЕ ПОРАЖЕНИЯ. Обсуждение на этом заседании преимущественно затронет следующие жизненно важные вопросы:
Возможности лечения отечно-инфильтративных форм рака молочной железы. Результаты «санационных» мастэктомий. Показания, возможности, результаты лечения при церебральных, костных, легочных метастазах; отдаленных метастазах рака молочной железы иных локализаций.
Вниманию специалистов будет представлен разносторонний опыт Российского онкологического научного центра по обсуждаемой проблеме, состоится выявление положений, уязвимых для критики, и обсуждение преимуществ прогрессивных разработок.
Организационный комитет Общества полагает, что состоящее из двух частей («комбинированное») заседание, кроме того, станет еще и «расширенным» – по разнообразию тематических направлений, количеству онкологических учреждений, численности привлеченных к участию в нем заинтересованных специалистов.
Имеются весомые основания считать, что дополнения предложенной тематики, представления результатов собственных исследований, как правило, отражают рейтинг специалистов в нашем профессиональном сообществе.
PROCEEDINGS OF THE MOSCOW CANCER SOCIETY
№ 567 (April 22, 2010)
THE-STATE-OF-THE-ART IN THE TREATMENT OF BREAST CARCINOMA
1) PRINCIPLES OF MANAGEMENT IN OPERABLE,
STAGED I-II (IIIA) CASES
Report: THE-STATE-OF-THE-ART IN THE TREATMENT OF OPERABLE BREAST CARCINOMA. By Prof. S. Portnoi (The N.N. Blokhin Cancer Research Center).
Discussion: TREATMENT PRINCIPLES IN PATIENTS WITH OPERABLE, STAGED I-II (IIIA) BREAST CARCINOMA. By Prof. A. Burlakov, Prof. D. Stroiakovsky et al. (Moscow Cancer Hospital #62); Dr. R. Kolesnikov, Prof. E. Khmelevsky (Russian Research Center of Roentgenology and Radiology); Prof. V. Sobolevsky, Prof. O. Trofimova (The N.N. Blokhin Cancer Research Center).
СОВРЕМЕННЫЕ ПРИНЦИПЫ ЛЕЧЕНИЯ БОЛЬНЫХ
ПЕРВИЧНО-ОПЕРАБЕЛЬНЫМ РАКОМ МОЛОЧНОЙ ЖЕЛЕЗЫ
Портной С.М.
(Российский онкологический научный центр им. Н.Н. Блохина)
Резюме: Современная лечебная тактика при первично-операбельном раке молочной железы (I-II стадий) предусматривает хирургическое лечение в объеме органосохраняющей операции. В случае противопоказаний к органосохраняющему лечению (мультицентрический рост опухоли, признаки внутрипротокового роста значительной протяженности, невозможность проведения послеоперационной лучевой терапии) выполняется модифицированная радикальная мастэктомия ± одномоментная реконструкция. Основной критерий радикализма органосохраняющей операции – отсутствие элементов опухоли по линии резекции. Если размер опухоли не позволяет выполнить органосохраняющую операцию с приемлемым косметическим результатом, возникает необходимость неоадъювантной химиотерапии. Её вариант выбирается с учетом гистологических и иммуногистохимических характеристик опухоли. Органосохраняющая операция признается адекватным вариантом местного лечения только в сочетании с лучевой терапией. Адъювантная системная терапия проводится в соответствии с рекомендациями Консенсусной конференции экспертов (Сан-Галлен; 2009).
Определение. Первично-операбельным следует считать рак молочной железы (РМЖ) I-II стадии.
Заболеваемость и смертность от рака молочной железы в России за 30 лет возросли в 4 раза. Стандартизованные показатели заболеваемости и смертности на 100.000 населения составляли в 1970 г. 9,6 и 4,2; в 2000 г. – 38,3 и 17,2 соответственно. Статистика 2000-х гг. подтверждает дальнейший рост заболеваемости, но стабилизацию смертности от рака молочной железы. В 2007 г. в России РМЖ диагностирован у 51.865 женщин, умерло от этой болезни 23.064 пациентки (Давыдов М.И., Аксель Е.М., 2009).
Факторы прогноза. Помимо общеизвестных факторов прогноза – критерии TNM, число пораженных лимфатических узлов, гистологическая форма, рецепторы эстрогенов и прогестерона (РЭ и РП) – сравнительно новым фактором неблагоприятного прогноза стала гиперэкспрессия HER-2/neu. Рецепторы РЭ, РП и HER-2/neu являются также сильными предиктивными факторами, позволяющими планировать системную терапию.
Стандарт хирургического лечения. Общепринятым стандартом лечения, наряду с модифицированной радикальной мастэктомией, является выполнение органосохраняющих операций: 1) «широкие» клиновидные резекции (радикальная резекция, квадрантэктомия); 2) лампэктомия (от «lump» – кусок, комок; экономная резекция железы, выполняемая из двух доступов: через дугообразный разрез, ориентированный по кожным складкам, производится удаление опухоли, а через горизонтальный разрез в подмышечной области выполняется лимфодиссекция); 3) онкопластические резекции – хирургические вмешательства с одномоментным восстановлением формы и объема железы.
Радикальность органосохраняющих операций. Основным требованием к органосохраняющим операциям является их онкологическая безопасность, что подразумевает невысокую частоту местных рецидивов наряду с отсутствием проявлений отдаленных метастазов. Однако, неумелое выполнение органосохраняющих операций сопровождается значительной частотой местных рецидивов, сравнительно с аналогичным показателем после мастэктомий. Частота местных рецидивов после органосохраняющих операций достигает 20,7% за 3 года наблюдения (Добренький М.Н., 2004). Более того, при возникновении местного рецидива повышается вероятность диссеминации опухоли (возможно, рецидивная опухоль является источником диссеминации).
Отсутствие элементов опухоли по краю резекции – важнейший показатель адекватности органосохраняющей операции. Напротов, у больных с «позитивными» краями, по сравнению с больными, у которых не определялось элементов опухоли по краю резекции, в 3,7 раза чаще развивались отдаленные метастазы и в 3,9 раза – летальные исходы вследствие прогрессирования заболевания (Meric F. et al.; 2003). Еще один фактор, ставящий под сомнение радикальность органосохраняющих операций, – выявление опухолевых клеток в лимфатических/кровеносных сосудах. По нашим данным наличие клеток опухоли в сосудах повышает вероятность развития отдаленных метастазов после органосохраняющих операций и в этой связи, обусловливает необходимость назначения адъювантной терапии (Портной С.М., Лактионов К.П., 2005).
Органосохраняющие операции заслуженно являются одним из стандартов лечения раннего РМЖ, однако они не всегда могут обеспечить эффективность, равную эффективности модифицированной радикальной мастэктомии. Тщательный отбор больных, контроль краев резекции, проведение лучевой терапии – компоненты, позволяющие проводить адекватное органосохраняющее лечение. Дополнительные показания к выполнению органосохраняющих операций появляются в результате успешной неоадъювантной терапии по поводу больших по размеру опухолей, при которых невозможно планировать органосохраняющую операцию на I этапе лечения.
Возможности органосохраняющего лечения при центральной локализации опухоли ограничены следующими обстоятельствами: 1) после резекции центрального отдела происходит выраженная деформация железы; 2) удаление соска и ареолы наносит дополнительный косметический ущерб; 3) органосохраняющая операция является в абсолютном большинстве случаев неприемлемой при раке Педжета из-за внутрипротокового распространения опухоли. Ифильтративное внутрипротоковое распространение рака Педжета является причиной значительной частоты местных рецидивов: 14-40% за 5-6 лет клинического наблюдения (Pezzi С. et al.; 2004). В исследовании Европейской организации по исследованию и лечению рака (Bijker N., et al. 2001) отмечен один из наименьших показателей частоты рецидивов после органосохраняющего лечения по поводу рака Педжета: 5,2% за 6 лет наблюдения. Операции были выполнены 61 женщине; признаков инвазивного роста не определялось, опухолевого узла в железе у большинства из них (97%) не выявлялось. Всем пациенткам производилось удаление сосково-ареолярного комплекса с конической резекцией ткани центрального отдела железы. Подлежащий внутрипротоковый компонент не распространялся более чем за 5 см от соска, в краях резекции не выявлялось элементов опухоли. Во всех случаях проводилась лучевая терапия на молочную железу в стандартной дозе 50 Гр.
Очевидно, столь ранняя форма рака Педжета представляет большую редкость. Группа больных, соответствовавших вышеперечисленным критериям, была составлена в рамках кооперированного исследования, в котором принимали участие 14 Европейских онкологических центров в течение 11 лет (с 1987 по 1998). Таким образом, выявление одного случая, соответствовавшего критериям, при которых возможно выполнение органосохраняющей операции, происходило, в среднем, в течение 2,5 лет.
Реконструктивные одномоментные операции после мастэктомии к началу 2000-х гг. стали применяться достаточно часто. В настоящее время возросла необходимость в максимально точной оценке онкологической безопасности таких операций. Кроме того, важно уточнить, насколько успешно реконструкция устраняет психологическую проблему.
Для оценки онкологического риска 124 операций с первичной реконструкцией молочной железы –экспандером (14), лоскутом широчайшей мышцы спины с использованием эндопротеза (18), поперечным лоскутом прямой мышцы живота (92) – проведено сравнение сведений о течении заболевания после выполнения маммопластики с аналогичными показателями в группе из 379 больных, которым реконструкция железы не выполнялась. Группы были сопоставимы по основным прогностическим факторам (возраст, значения критериев «T» и «N»), методам противоопухолевого лечения. Повышения частоты местных рецидивов и прогрессирования заболевания в группе пациенток с одномоментной реконструкцией железы не отмечено. Многофакторный анализ не выявил влияния реконструктивной операции на возникновение рецидивов.
У больных, перенесших реконструкцию молочной железы существенно реже наблюдалась депрессия; достоверно выше оказались оценки показателей по критериям «общительность», «радость», «активность», «счастье», «удовлетворенность профессией», «возможности для отдыха и развлечений» (Ткаченко Г.А. с соавт.; 2008). Таким образом, реконструктивные операции не ухудшают течения болезни и значительно улучшают психологическое состояние пациенток.
Адъювантная терапия. Согласно консенсусному решению экспертов Международной конференции по адъювантной терапии рака молочной железы (Сан-Галлен; 2009) адъювантная системная терапия в случае инфильтративного РМЖ может не проводиться при наличии совокупности благоприятных факторов прогноза: размер новообразования до 2,0 см при отсутствии поражения регионарных лимфоузлов (T1NM), I степень злокачественности опухоли, наличие в опухоли рецепторов эстрогенов и/или прогестерона, отсутствие выраженной перитуморальной инвазии сосудов, отсутствие гиперэкспрессии HER-2/neu, возраст пациентки более 35 лет. Остальным больным назначается адъювантная системная терапия. Адъювантная эндокринная терапия показана при наличии в опухоли РЭ и/или РП. Гормональная зависимость опухоли не исключает ее чувствительности к адъювантной химиотерапии. В случаях наличия показаний к адъювантной химиотерапии и к адъювантной эндокринной терапии в первую очередь проводится химиотерапия (Goldhirsch A. et al., 2009).
При РМЖ, имеющем характеристики РЭ-РП-HER-2/neu химиотерапия показана практически всем больным. Исключение составляют пациенты с pT1аNM и с редкими морфологическими формами опухоли (медуллярный, апокриноклеточный и аденокистозный) при отсутствии поражения лимфатических узлов и других признаков значительного метастатического потенциала.
Гиперэкспрессия HER-2/neu является показанием к применению (помимо химиотерапии) трастузумаба (герцептина) в течение 1 года (за исключением случаев pT1аNM) . Как было показано в серии рандомизированных исследований, применение трастузумаба в качестве адъювантной терапии на 50% снижает риск рецидива (Baselga J. et al., 2006).
Больным с гормонально-зависимыми опухолями (РЭ+ и/или РП+) помимо эндокринной терапии может проводиться и адъювантная химиотерапия, причем рекомендация по ее проведению является результатом анализа ряда дополнительных факторов. Возможно не проводить химиотерапию при высоких уровнях РЭ и РП, I степени злокачественности опухоли, низкой пролиферативной активности опухолевых клеток, отсутствии выраженной инвазии сосудов, размере опухоли не более 2,0 см, желании пациентки избежать химиотерапии, низкой вероятности прогрессирования болезни по данным анализа генов опухоли (Goldhirsch A. et al., 2009).
Адъювантная эндокринная терапия может проводиться самостоятельно или после завершения адъювантной химиотерапии. Больным репродуктивного периода назначается тамоксифен в дозе 20 мг/сут. в течение 5 лет. Альтернативы могут рассматриваться при наличии противопоказаний к приему тамоксифена (хронический флеботромбоз, рецидивирующий полипоз эндометрия) или осложнений, связанных с терапией. Вариантом является сочетание любого вида подавления функции яичников с ингибиторами ароматазы (аримидекс, фемара, метрозол, др. препараты). Продолжительность терапии составляет не менее 5 лет. У больных, находящихся в постменопаузе, ингибиторы ароматазы показали свои преимущества перед тамоксифеном и могут быть использованы в виде единственного средства адъювантной эндокринной терапии, либо в виде препарата второй линии после 2-3-летнего применения тамоксифена. При этом общая продолжительность терапии должна быть не менее 5 лет. Если после 5-летнего применения тамоксифена назначается препарат второй линии, то продолжительность эндокринной терапии может составлять до 10 лет.
У мужчин стандартом адъювантной эндокринной терапии является прием тамоксифена по 20 мг в сутки в течение 5 лет (Goldhirsch A. et al., 2009).
Дискуссия. Фиксированные выступления в прениях
ЛУЧЕВАЯ ТЕРАПИЯ – ОБЯЗАТЕЛЬНЫЙ КОМПОНЕНТ ЛЕЧЕНИЯ ПОСЛЕ ОРГАНОСОХРАНЯЮЩИХ ОПЕРАЦИЙ ПО ПОВОДУ
РАКА МОЛОЧНОЙ ЖЕЛЕЗЫ
Трофимова О.П.
(РОНЦ им. Н.Н. Блохина)
Лучевая терапия – обязательный компонент комплексного лечения больных после органосохраняющих операций. Стандартом является облучение оставшейся части молочной железы с целью предотвращения развития местного рецидива РОД = 2 Гр 5 раз в неделю, суммарно до 50 Гр. Подведение указанной дозы связано с тем, что именно она, по мнению ряда исследователей, достаточна для разрушения микроскопических опухолевых очагов, возможно, располагающихся в поражённом органе. Проведение лучевой терапии после органосохраняющего лечения снижает частоту локальных рецидивов в 3-4 раза, что подтверждают результаты многих рандомизированных исследований.
С учетом факторов риска развития локального рецидива определяются и показания к облучению ложа удалённой опухоли («boost») в дозе 10-20 Гр, что особенно актуально для пациенток моложе 50 лет. После выполнении адекватной лимфаденэктомии до II уровня при раннем раке молочной железы (не менее 10 удалённых л/узлов должно быть подвергнуто гистологическому исследованию) проведение адъювантной лучевой терапии на зоны регионарного метастазирования показано при поражении 4-х и более лимфатических узлов; облучение нецелесообразно при отсутствии метастазов в лимфатических узлах. Назначение адъювантной лучевой терапии пациенткам с поражением 1-3 лимфатических узлов определяется индивидуально.
РОЛЬ ЛЕКАРСТВЕННОЙ ТЕРАПИИ
В ЛЕЧЕНИИ РАННЕГО РАКА МОЛОЧНОЙ ЖЕЛЕЗЫ (рРМЖ)
Строяковский Д.Л.
(Московская городская онкологическая больница №62)
«Ранним» традиционно считается рак молочной железы I и II стадии; «ключевым» лечебным методом при данной распространенности опухоли является хирургический. Однако, в значительном числе наблюдений, несмотря на диагностику опухоли в «ранней» стадии и выполнение считавшейся «радикальной» операции, выявляется местный рецидив и/или отдаленные метастазы. Основной целью адъювантной или неоадъювантной лекарственной терапии рРМЖ является снижение риска прогрессирования заболевания.
Определение показаний к проведению адъювантной химиотерапии и/или гормонотерапии после радикальной операции, (а также сочетаний неоадъювантной и адъювантной терапии) остается еще нерешенной задачей. Даже при нынешнем уровне знаний, нередки случаи, когда трудно дать ответ на многочисленные вопросы: Нужно ли проводить адъювантную (неоадъювантную) терапию? Если да, то какую именно и как долго?
Причиной столь сложных вопросов является гетерогенность рака молочной железы. Этот факт известен очень давно, но только в последнее время, становятся понятными молекулярные основы этой гетерогенности.
По сути, при одной локализации процесса – в молочной железе – имеются несколько заболеваниий, которые различаются причинами возникновения злокачественного роста, генетическими нарушениями, клиническим течением и разным прогнозом болезни. Поэтому, при выборе адъювантной (или неоадъювантной) терапии рРМЖ должны учитываться следующие факторы: морфология и клинические проявления опухоли (инфильтрация, мультицентричность роста), значения символов TNM, иммуногистохимические (ER, PR, Her-2, Суt 5/6, EGFR1) и молекулярно-генетические маркеры (BRCA, профиль генов, Topo2), возраст больной.
На основании вышеуказанных данных, предложено определять несколько молекулярно-генетических форм рака молочной железы:
1. Рак молочной железы соответствующий уровню стволовой клетки молочной железы. Гены «Cloudin» семейства «отключены». Эта форма встречается у 5-10% больных, чаще в молодом возрасте. Она определяется следующими характеристиками: генетический профиль опухоли сходен с профилем стволовых клеток молочной железы; часто выявляются: лимфоцитарная инфильтрация, ER-, PR-, Her-2-, Grade III, др. Данную форму отличает относительно меньшая химиочувствительность, отсутствие эффекта после применения таргетных препаратов, неблагоприятный прогноз. При данной форме требуется проведение агрессивного лечения.
2. Рак молочной железы соответствующий уровню бипотентного и раннего ламинального предшественника (BRCA1 – мутирован или его экспрессия резко снижена); базальный вариант. Эта форма встречается у 10-25% больных, чаще в молодом возрасте. Она определяется следующими характеристиками: ER-, PR-, Her-2-, Grade III, иногда с экспрессией рецепторов стероидных гормонов, Cyt 5/6 – 60%, EGFR1- в 50-70% случаев.
Гистологически – инфильтративный протоковый или (реже) дольковый рак, метапластический рак, миоэпителиальная карцинома, овсяноклеточный рак. Форму характеризуется особым генетическим профилем, неблагоприятным прогнозом. Часто выявляются метастазы в висцеральные органы и головной мозг.
Однако, при данной форме отмечена относительно высокая химиочувствительность опухоли. Эффективно назначение препаратов платины, ингибиторов PARP (новый класс лекарств), ингибиторов ангиогенеза, дозоинтенсивной терапии. Отмечено быстрое развитие химиорезистентности. При данной форме требуется проведение агрессивного лечения.
3. Рак молочной железы соответствующий уровню позднего ламинального предшественника. Her-2+ вариант. Эта форма встречается у 10-15% больных, от молодого возраста до менопаузы. Она определяется следующими характеристиками: ER-, PR-, Her-2+, Grade II-III; у 1/3 больных выявляется гиперэкспрессия Topo2α. Форма характеризуется неблагоприятным прогнозом. Часто выявляются метастазы в висцеральные органы и головной мозг. При данной форме отмечена высокая химиочувствительность опухоли. Высока эффективность адъювантной и неоадъювантной химиотерапии с назначением трастузумаба (анти-Her-2 моноклонального антитела) и лапатиниба (ингибитора тирозин-киназы Her-1 и Her-2). При данной форме требуется проведение агрессивного лечения.
4. Рак молочной железы ( ламинальный В), соответствующий уровню дифференцированных клеток. Форма встречается у 10-15% больных. Выявляется в молодом, перименопаузальном и раннем постменопаузальном возрасте. Характеристики: ER±, PR±, Her-2±, Grade II-III; возможна гиперэкспрессия Topo2α, в сочетании с гиперэкспрессией Her-2. Форма характеризуется неблагоприятным прогнозом. Часто выявляются метастазы в висцеральные органы, головной мозг, кости и мягкие ткани, кожу, лимфоузлы. Высокая химиочувствительность опухоли отмечена к антрациклинам (при гиперэкспрессии Topo2α), таксанам, другим препаратам. Эффективность гормонотерапии не выражена, особенно у больных с высокой пролиферативной активностью опухоли. Возможно сочетание гормонотерапии (ингибиторы ароматазы) в сочетании с трастузумабом – при трипл-позитивном фенотипе опухоли. Высока эффективность адъювантной и неоадъювантной химиотерапии с назначением трастузумаба (анти-Her-2 моноклонального антитела) и лапатиниба (ингибитора тирозин-киназы Her-1 и Her-2). Форма требует проведения агрессивного лечения.
5. Рак молочной железы (ламинальный А), соответствующий уровню высокодифференцированных клеток. Форма встречается у 30-50% больных. Чаще встречается в пожилом, позднем постменопаузальном возрасте. Избыток эстрогенов – одна из важнейших причин возникновения данной формы (ожирение, гормонозаместительная терапия, эстрогеновые контрацептивы, алкоголь). Теоретически, нормализуя уровень эстрогенов возможно снизить заболеваемость (!) Характеристики: ER+, PR+, Her-2-, Grade I-II; часто выявляется инфильтративный протоковый или дольковой рак. Форма характеризуется благоприятным прогнозом у большинства больных. Основная мишень метастазов – кости. Многие пациентки имеют ограниченные прогрессирования, при которых эффективны локальные виды лечения (операции, лучевая терапия). Продолжительные сроки общей выживаемости при проявлениях прогрессирования. Высокая эффективность гормонотерапии, химиочувствительность – не выражена, но назначаются традиционные цитостатики. Форма не требует проведения агрессивного лечения.
Адъювантная терапия раннего рака молочной железы, является общепринятой. Неоадъювантная терапия, решает задачи, связанные с оценкой возможности выполнения органосохранной операции (без ущерба радикальности операции), оценки индивидуальной чувствительности опухоли к химиотерапии (оценки патоморфоза), определения прогноза (и, возможно, преодоления неблагоприятного прогноза применением иного варианта терапии).
Таким образом, исходя из наличия вариантов рака молочной железы, для улучшения результатов лечения, следует руководствоваться следующими положениями: Женщины в глубокой постменопаузе, имеют меньший риск неблагоприятных типов рака молочной железы, поэтому для данной возрастной группы приемлема такая последовательность лечения: операция, затем лекарственная терапия. Чем старше возраст, тем большее влияние на выживаемость оказывает локальное (в том числе циторедуктивное) воздействие. Роль адъювантной (и неоадъювантной) химиотерапии снижается c возрастом; роль гормонотерапии возрастает.
Все формы РМЖ при размере опухоли более 1 см, кроме ламинального А и редких благоприятных форм, нуждаются в неоадъювантной терапии, для оценки патоморфоза, как важнейшего прогностического фактора. При слабом патоморфозе, необходим переход на альтернативную линию химиотерапии, для снижения риска прогрессирования. Выполнение органосохранной операции оправдано при невысоком риске рецидива.
Сведения о форме опухоли являются неотъемлемой частью диагноза. Эта информация должна быть востребована для принятия решения о выработке оптимального плана лечения в каждом конкретном случае.
ОДНОМОМЕНТНЫЕ РЕКОНСТРУКТИВНЫЕ ОПЕРАЦИИ
ПРИ РАКЕ МОЛОЧНОЙ ЖЕЛЕЗЫ
Соболевский В.А.
(РОНЦ им. Н.Н. Блохина)
В 2000-х гг. одномоментная реконструкция молочной железы после радикальной мастэктомии общепризнанно является неотъемлемой частью лечения и важным этапом реабилитации больных раком молочной железы. По данным Американского общества пластических и реконструктивных хирургов в 1990-х гг. одномоментно выполнялись 38% реконструктивных операций, в 2000-х гг. на долю одномоментных реконструкций приходится уже 75% восстановительного хирургического лечения.
Реконструкция молочной железы выполняется применением аллопротезов, собственных тканей, а также – сочетанием этих методов. Реконструкция железы собственными тканями предусматривает применение перемещенного TRAM-лоскута (Тransverse Rectus Abdominis Musculocutaneous flap), свободных TRAM- или DIEP-лоскутов (Deep Inferior Epigastric Perforator) на микрососудистых анастомозах, LD-лоскута (Latissimus Dorsi musculocutaneous flap), лоскута Рубенса, др. Эндопротезирование молочной железы выполняется одноэтапно (установкой экспандра-эндопротеза Беккера), либо двуэтапным методом (применением экспандера с последующей его заменой на эндопротез).
По данным конференции IPRAS (International Plastic Reconstructive Aestetic Surgery; 2009), в настоящее время собственные ткани являются оптимальным материалом для реконструкции. Свободный TRAM- или DIEP-лоскут позволяют создать железу любого объема с удовлетворительным эстетическим результатом.
Методы эндопротезирования проще в техническом плане, менее травматичны, требуют меньшего срока послеоперационной реабилитации. Проведение лучевой терапии (ЛТ) после эндопротезирования неизбежно ведет к увеличению числа осложнений и реопераций. Одноэтапное эндопротезирование оптимально при отсутствии показаний к лучевой терапии, при реконструкции железы небольшого объема, без ее птоза. При необходимости лучевой терапии предпочтительно двуэтапное эндопротезирование.
С 2006 г. в отделении реконструктивной и сосудистой хирургии РОНЦ выполнено 110 одномоментных реконструктивных операций, в том числе с применением перемещенного TRAM-лоскута (49), свободного TRAM-лоскута (11), одноэтапного (26) и двуэтапного эндопротезирования (26). Не отмечено клинически значимых осложнений.
ПРОБЛЕМА ВЫБОРА МЕТОДА РЕКОНСТРУКЦИИ МОЛОЧНОЙ ЖЕЛЕЗЫ
Бурлаков А.С.
(Московская городская онкологическая больница №62)
Еще 10-15 лет назад проблема реконструкции молочной железы сводилась к примитивному противостоянию онкологов и пластических хирургов. Хирурги под знаменами эстетических и реабилитационных идей стремились восстановить молочную железу всем пациенткам, перенесшим радикальную мастэктомию. Было официально признано, что качество жизни онкологических больных так же важно, как и ее продолжительность. Однако стремление к повышению качества жизни стало приводить не к развитию восстановительной хирургии, а лишь к расширению показаний к выполнению органосохраняющих операций (не всегда оправданному). Восстановительные же операции в практической онкологии по-прежнему применяются в ограниченном объеме.
Проблема реконструкции молочной железы достаточно сложна и многогранна. Нужно ли восстанавливать молочную железу после радикальной мастэктомии? Следует ли это делать одномоментно с мастэктомией или после окончания лечения? Какой способ реконструкции предпочтителен? Вот вопросы, ответы на которые приходится искать при совместном обсуждении с пациенткой плана лечения.
Начиная внедрять 15 лет назад реконструкцию молочной железы в практику московской городской больницы №62, мы считали, что практически все женщины, прошедшие радикальное хирургическое лечение по поводу рака, нуждаются в реконструктивной хирургии. На сегодняшний день, анализируя опыт более 400 реконструкций, мы считаем, что в хирургической реабилитации нуждаются лишь 3-5% пациенток. В начале работы мы безапеляционно заявляли, что одномоментные реконструкции молочной железы значительно лучше отсроченных, а использование лоскута собственных тканей предпочтительнее протезирования. По мере накопления опыта мы стали менее категоричны в своих суждениях и нередко предпочитаем эндопротезирования аутотрансплантатам. На практике, в каждом случае приходится выбирать (при активном участии пациентки) лечебно-реабилитационную программу, состоящую из онкологической и реконструктивной частей. Дополняя друг друга, они позволяют достичь основной цели лечения – максимального онкологического результата при минимальном ущербе качеству жизни.
источник