Автореферат и диссертация по медицине (14.00.14) на тему: Рак молочной железы в сочетании с опухолевыми заболеваниями матки и яичников
1.1. Некоторые особенности клинического течения диагностики лечения и прогноза первично-множественных злокачественных новообразований молочной железы, шейки матки, тела матки и яичников.
Глава II. МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
РЕЗУЛЬТАТЫ СОБСТВЕННЫХ ИССЛЕДОВАНИЙ.
Глава III. ПЕРВИЧНО-МНОЖЕСТВЕННЫЙ РАК МОЛОЧНОЙ
III. 1. Общая характеристика материала.
111.2. Синхронный рак молочной железы и шейки матки.
111.3. Метахронный рак молочной железы и шейки матки.
Актуальность проблемы. Среди множества проблем клинической онкологии в настоящее время одной из основных остается проблема своевременной диагностики и эффективного лечения первичной множественности L злокачественных опухолей.
Для практического врача остаются спорными и нерешенными вопросы этой проблемы. Практические врачи лечебно-профилактических учреждений общего профиля и врачи-онкологи недостаточно осведомлены о методах диагностики и лечения больных с первично-множественными злокачественными опухолями. Противоречивость публикуемых материалов по данной проблеме, большой процент врачебных ошибок и низкие показатели ранней выявляемости заболевания, особенно опухолей второй- локализации,- а также- высокий процент-смертности этой категории больных указывают на необходимость обобщения накопленных к настоящему моменту сведений. В полной мере все сказанное относится к случаям сочетанных опухолевых поражений молочной железы, матки и яичников. На наш взгляд, среди данной категории больных особо следует вьщелигатрушу жешцшг на тему «Рак молочной железы в сочетании с опухолевыми заболеваниями матки и яичников»
1. Общая и безрецидивная выживаемость больных первично — множественным раком молочной железы и шейки матки в сроки 5 ( 56,7% и 53,7%) и 10 (28,3% и 8,6%) лет достоверно хуже аналогичных показателей выживаемости больных раком молочной железы контрольной группы в сроки 5 лет (81,7% и 69,1%) и 10 (65,3% и 51,3%) лег (р по медицине, диссертация 2005 года, Лещев, Василий Васильевич
1. Абдурасулов Д.М Вопросы этиопатогенеза, эпидемиологии и клиники множественных опухолевых поражений.— Ташкент: Медицина, 1977. с 14-144
2. Абдурасулов Д.М., Никишин К.Е. -Множественные опухолевые поражения Т. 1.//Первично множественные опухоли — Ташкент: Медицина,. 1968 — 652с.
3. Артюх Г.Ф. О множественных первичных опухолях.//Клинич. медицина -1972 33 №5. с.24-29.
4. АтласШМ: Иллюстрированное руководство по TNM / pTNM -классификация злокачественных опухолей/. Пер. с англ. 4-го издания/. Под ред. В. Е. Кратенка, Е. А. Короткевича.- Минск: Белорусский центр науч. Мед. Информации, 1998.-381с., стр. 201-244.
5. Бохман Я.В., Лившиц М.А., Винокуров В.Л, и др.— Новые подходы к лечению гинекологического рака. // Первично-множественные опухоли гениталий, молочной железы и толстой кишки — СПб.: Гиппократ, 1993,- 221с.
6. Бохман Я.В. — Руководство по онкогинекологии.// Первично-множественные опухоли. Л.Медицина 1989.- 464с.
7. Бохман Я.В., Рыбин Е.П. Патогенические аспекты первично-множественных опухолей толстой кишки, тела матки, молочной железы//Гл. в кн.: Первично-множественные злокачественные опухоли. — Л. 1987.-C47-56.
8. Бохман Я.В., Мерабишвили В.М. Семиглазов В.Ф.Патогенетические подходы к профилактике и лечению гормонозависимых опухолей. -Л. Медицина, 1983.-cl 1-22.
9. Бохман Я. В., ЛютраУ. К. Рак шейки матки, Кишинев: Штиипца, -1991.-240 стр.
10. Василенко И. Я., Москалева Ю. И., Стрельцова В. Н. Канцерогенный эффект ионизирующего излучения в комбинации с химическими и другими физическими агентами // Вонр. Онкологии. — 1996 . № 2 —с. 3 14.
11. Верморкен Я. — Эпителиальный рак яичников: состояние проблемы.// Материалы второй ежегодной конференции «Современные тенденции развития лекарственной терапии опухолей». М., 1998. — стр. 85-88.
12. Винокуров В.Л., Ливший М.А., Митрохина М.В., Максимов С.Я. — Рак яичников в сочетании с другими злокачественными опухолями// Первично-множественные злокачественные оиухоли. Л. 1987г. с. 120123.
13. Вихляева Е.М., Палладии Г.А. Патогенез, клиника и лечение миомы матки. Кишинев, 1982.-300с.
14. Вишневская Е.Е., БохманЯ.В. Ошибки в онкогинекологической практике// Ошибки в диагностике первично-множественных злокачественных опухолей и метастатических поражений,- Минск: Беларусь, 1987.-237с.
15. Высоцкая И.В. Прогностическое значение опухолевых маркеров РЭА, СА-15-3,МСА, ферритина, ТПА и ПТГ при раке молочной железы.//Автореф. дисс на соиск. учен степ. канд. мед. наук, М.,1993 С19-21.
16. Габуния М.С., Братик А.В., Олимпиева С.П. — Факторы риска развития доброкачественных заболеваний молочной железы на фоне гинекологических заболеваний. Маммология №2: с. 21-30, 1998.
17. Ганина К.П., Коханевич Е.В., Винокур M.J1. Диагностика предопухолевых и опухолевых процессов шейки матки. — Киев: Наукова думка, 1984 .с.48-51
18. Ганцев Ш.Х., Мерабишвили В.М., Куликов Е.П. и др. -Распространенность и риск возникновения первично-множественных опухолей по материалам популярного канцер-регистра. Рос. Онкол. Ж. №5: 4-7,199&
19. Годорожа Н.М. — Аспекты профилактики рака молочной железы: Автореф. Дисс на соиск. ученой степ.д-ра мед. наук, Киев, 1991г.с16-21.
20. Гумилевская Е.П. О первично-множественных злокачественных опухолях// Вопр. Онкологии.-1966 № 9- с84-88
21. Дарьялова СЛ., Чиссов В.И. Диагностика и лечение злокачественных опухолей. Москва, 1993г., стр.238-250.
22. Давыдов М. И., Аксель Е. М, — Злокачественные новообразования в России и странах СНГ в 2000г., Москва, 2001г.
23. Двойрин В.В., Аксель Е.М., Трапезников Н.Н. Статистика злокачественных новообразований в России и некоторых других странах СНГ в 1994 г. — М., 1995.
24. Демидов В.П., Островцев Л.Д. — Первично-множественный рак молочной железы. Рос. Онкол. Ж. № 5: 21-26, 1998.
25. ДильманВ.М. Эндокринологическая онкология. М.; Медицина, 1983г. C149-167
26. Железнов Б.И., Стружаков А.Н. Генитальный эндометриоз. -М.,1985г.-160 с.
27. Злокачественные новообразования в России в 1998 г. (заболеваемость и смертность). /Под ред. Акад. В.И. Чисова, проф. В.В. Старинского, канд. Мед. Наук Л.В. Ременкик. М., 1999. стр. 284.
28. Иванов В.М. Рак молочной железы у больных пожилого и старческого возраста.// Автореферат диссертации на соискание учепоий степени доктора мед. паук., М.Д993. с 18-20.
29. Имянитов Е.Н., Хансон К.П. Молекулярные аспекты патогенеза первично-множественных опухолей // Рос. Онкол. Ж. — 1998. — №5. стр. 47-51.
30. Косгромина К.Н. Современное состояние и перспективы развития лучевой терапии гинекологического рака// Мед.радиол.-2001 .T.46,№ 1. С.48-51.
31. Кузьмина З.В., Бассалык Л.С. Муравьева Н.И. Цитоплазматические рецепторы стероидных гормонов в опухолях больных раком эндометрия//Акуш. и.гинек.-1998.-№4.с29-32.
32. Куликов Е.П., Лебедев A.M., Антонова Т.П. и др. Анализ заболеваемости и результаты лечения первично-множественных злокачественных опухолей. — Рос. Онкол. Ж. №5: 39-41, 1998.
33. Летягин В.П., Высоцкая И.В. Первичный рак молочной железы(диагностика, лечение, прогноз).М.,1996, 160.
34. Летягин В.П., Высоцкая И.В., Легков А.А. Лечение доброкачественных и злокачественных заболеваний молочных желез. М., 1997.С23-29.
35. Максимов С.Я. Возможности современного выявления первично-множественного рака тела матки и молочной железы: Автореф.дисс. на соиск. ученой степ. канд. мед. паук. — Л., 1990.cr.9-I9
36. Международная гистологическая классификация опухолей.Второе издание ВОЗ, «Женева», 1984.
37. Мельников Р. А., Рыбин Е.П., Бохман Я.В. //Первично-множественные злокачественные опухоли. Л., 1987.-стр. 120-123.
38. Новикова Е.Г., Антошечкина Е.Т. В кн.: Ошибки в клинической онкологии., иод ред. В.И. Чиссова, А.Х. Трахтенберга — М.: Медицина, 1993г. -С.442-451, 426-441.
39. Новикова Е.Г. Диагностика предраковых заболеваний и начальных форм рака шейки матки. Заболевания шейки матки,влагалиша и вульвы (клинические лекции).М.,Медпресс 1999;с153-9.
40. Новикова Е.Г., ЧулковаО.В., Беляева И.Г. Особенности первично-множественных опухолей репродуктивной системы у женщин.Росс.Онкол.Журнал №5 1998. С. 18-21.
41. Огнерубов Н.А., Летягин В.П., Подцубная И.В. с соав. Рак молочной железы: неоадъювантная химиолучевая терапия. — Воронеж, 1996.с64
42. ПорхановаН.В. Рецидивы серозного рака яичников(факторы прогноза и диагностика).Дисс. канд. мед. наук. М.,1999. стр47-84.
43. Сельчук В.Ю. Первично-множественные опухоли (клиника, лечение и закономерности развития). — Автореферат диссертации на соискание ученой степени докторской дисертации. Москва, 1994.
44. Сидорова И.С., Караулов А.В., Курашвили Ю.Б.//Вестн. Российской Ассоциации акушеров-гинекологов-1998.-№4.-С.87-88.
45. Слинчак С.М. Множественные злокачественные опухоли. Киев: Здоровья-1968-191с.
46. Толокиов Б.О. Современная комплексная диагностика и лечение больных хориокарциномой матки .Онкогинекология Т2 №2 с.49-50.
47. Тюляндин С. А. — Рак Яичников: Вчера, сегодня, завтра.// Материалы конференции «Современные тенденции развития лекарственно терапии опухолей». М., 1997. — стр. 66-70.
48. Ханов A.M. Эпидемиология, факторы риска и оптимизации диагностики первично-множественных злокачественных опухолей: Автореф.дис. на соискание уч. ст. канд. мед. наук. — М., 1994.
49. Харитонова Т.В. Опухоли яичников: клинические проблемы. Русский медицинский журнал Том 6, № 10 1998 с667-676
50. Холин В.В. Оценка результатов лучевого и комбинированного лечения рака шейки матки //Мед.радиолог.-1978.-№8.-С. 75-78.
51. Цель Е. А. Первично-множественные злокачественные опухоли: Автореф. дисс. на соиск. учен. степ. канд. мед. наук.-М., 1947.-18 с.
52. ЧекаловаМ.А. Ультразвуковая диагностика злокачественных заболеваний тела матки. Автореф. на соискание учен, степени, д-ра. мед. наук. М.,1999
53. Чиссов В.И., Трахтенберг А.Х., Первично-множественные злокачественные опухоли, Москва, «Медицина», 2000г.Гл.11.с.251-273.
54. Ягунова JI.B. К вопросу о сочетании рака молочной железы и карциномы других локаштзаши1//Х1фургия.-1968 №1-с86-89.
55. Adamopoulos D.A.,Loraine J.A., Dove G.A.Endocrinological studies inwomen approaching the menopause// J. of Obstetr. And Gynaecol/ of the
56. British Commonwealth.-1971.-vol. 78.-p.62-79.
57. Anaslassiades O., Lakovou E., Slravridou N. el al. Multi-centricily in breast cancer. A study of 366 cases// Amer. J.clin.path. 1993. — Vol.99, N 3. -P.238 -243.
58. Bertelsen K.,Jakobsen A., Stroyer J. et al. A prospective randomized comparison of 6 ad 12 cycles of cyclophosphamide,adi iamycin and cisplatin in advanced epithelial ovarian cancer :a Danish Study Group trial (DACOVA). Gyn Oncol 1993; 49:30-6
59. Billrot С.A.T. Die algemeine Chirurgie, Pathologie und Therapie.-Berlin: G.Reimer.- I889.-P. 908/
60. Bonle J., Jde P., LillelG., Wynanls P. //Gynecol. Oncol.-1981.-Vol.l 1.-Р.140-161/
61. Blatt J., Olshon A., Gula M. J. et al. Second malignancies in very-long term survivors of childhood cancer// Amer.J. Med.-1992.-Vol.93,Nl-P.57-60.
62. Bokhman J.B., Maximov S.J. Relative risk of development and active detection of primary multiple endometrial, breast and ovaria cancer // Eur. J. Gynaecol.Oncol.-1993.-Yol. 14,N2.-P. 114-118.
63. Buist M.R., Golding R.P., Burger C.W. et al.//Gynecol.Oncol.-1994.-Vol.52.-№ 2.-P. 191-198.
64. Caldas C., Ponder B.A.J. Cancer genes and molecular oncology in the clinic//Lancet.- 1997.-Vol. 14.-P.574.
65. Casey G. The BRCA1 and BRCA2 breast cancer genes// Curr. Opin. Oncol. -1997. Vol.9. — P.88-93.
66. Champault G., Loygue J. Cancer multiples et familieux //Med.chir.gig/1977.-Vol.276.-P.404-407/
67. Chassagne D., Sismondi P.J.C. et al. A glossary for complications of ment in gynecological cancers //Radiother.Oncol.-1993.-Vol.26.-P. 195-202/
68. Chlebowski R.T., Butler J., Nelson A., Lillington L. Breast cancer chemoprevention. Tamoxifen: current and future prospective. //Cancer,1993, 72 (3 suppl): 1032-7
69. Crowe J.P Jr., Godon N.H., Stenk R.R. et al.Short-term tamoxifen plus chemotherapy: Superior results in node-positive breast cancer.// Surgery,1990,108/4,619-628.
70. Di Saia P.J., Creasman W.T. Clinical Gynecologic Oncology.-St/ Louis: Mosby Cjmr any ,1992
71. Eng C., Mulligan L. M. Mutations of the RET proto-oncogene in the multiple endocrine neoplasia type 2 syndromes, related sporadic tumours, and hirschsprung disease// Hum. Mutat. 1997. — Vol. 9. -P.97-109.
72. Fisher В Experimental and clinical justification for the use of tamoxifen in a breast cancer prevention trial: a description of the NSABP effort(meeling abstract). //Proc. Annu Meet. Am. Assoc. Cancer. Res., 1992,33:A 567-8
73. Fisher B.,Carbone P., Economon S.G. L-Phenilalanine mustard (L-PAM) in the management of primary breast cancer.N. Engl.Med.,1975,292,117.
74. FribergB. et al.,//ActaObstet.Gynecol.Scand.-1997.-Vol.76.Suppl.l67.
75. Fritsche H.A. Serum tumor markers for patient monitoring : a case-oriented approach illustrated with carcinoembryonic antigen.Clin.Chem., 1993,39, IIB, Pi 2, p.2431 2434.
76. Gben S., Lee L. Incidence of paraaortic and pelvic lymph node metastases in epithelial carcinoma of the ovary. Gyn Oncol 1983; 16: 95-100.
77. Grimes E.M. Richardson M.R. //Gynecology and Obstetrics./Eds J .J.Sciarra.-Philadelphia,l992.-Vol. 5 .-P.65.
78. Halsted W.S.: The results of Operations for the Care of Cancer of the Breast Performed at the Johns Hopkins Hospital from June 1889 to January 1894. Arch.S urg., 1894,20:497.
79. Hata K„ Hata T.,Kitao M.//Am.J.Obstet.Gynecol. 1995.-Vol 172.-№5.-P. 1469-1500.
80. Hickey J., Goldberg F. Ultrasound Review of Obstetrics and Gynecology.-Philadelphia; New York,l996/
81. Hurt H.H., Broders A.C. Multiple primary malignant neoplasms //J. Lab. Clin.Med.-1953.-Vol.13.-P.765.
82. Kennedy A. W., Markman M., Webster K. D., et al. Combination chemotherapy of ovarian and fallopian tybe cancer and primary peritoneal carcinoma with carboplatin and docetaxel.//Proc. ASCO. 2000.
83. Lee Т.К., Myers R.T., Schaiyj M., Marshall R.B. Multiple primary malignant tumors (MPMT): study of 68 autopsy cases (1963-1980)//J.Amer.Geriat.Soc.-1982.-Vol.30.-P.744.
84. Jordan V.C. Preclinical and clinical pharmacology of tamoxifen (meeting abstract). // CCPC-93: Second International Cancer Chemo Prevention Conference. April 28-30, 1993, Berlin, Germany,p.51,1993
85. Jurkovic D., Jauniaux E., Campbell S.// The Fetus as a Patient / Eds A.KuijakF.A. Chervenak. 1994. P. 135.
86. Madden J.L. Modified radical mastectomy. Surg. Gynec. And Abstr. Dec. 1965, Vol.121, 1221-1231.
87. Madden J.L., Kandalaf Z.S., Bourgue R. Modified Radical Mastectomy. Ann. Surg., May 1972, vol. 175, №5, 624-634.
88. Mauriiac L., Durand M., Avril A. Effect of primary chemotherapy in conservative treatment of breast cancer patients with operable tumor larger than 3 cm: results of a randomized trial in a srugle center. Am. Oncol., 1991, 2, 347.
89. Malrnio K.Multiple primary cancer.A clinical-statistical investigation based on 650 cases //Ann. chirurgie Gynecol. Penniae.Helsinki.-1959.-Vol.48, N3.-P.56-60.
90. Markman M. Intraperitoneal therapy of ovarian cancer.// Semin. Oncol. — 1998. Vol. 25. — P. 356 — 360.
91. Markman M., Bookman M. A., Second-line treatment of ovarian cancer.// The Oncologist. 2000 — Vol. 5. — P. 26 — 35.
92. Minderhoud-Bassie W., Treurniet F.E., Koops W et al.//Acta Obstet.Gynecol.Scand.-1995.-Vol.74.-№10.-P.827-831.
93. Moertel С., Dockerty M., Baggenstoss A.//Cancer.-1961-Vol.l4.-P.238-248/
94. Morrow G.P., Curtin J.P. Gynecologis Cancer Surgery. Cburcbill Livingstone 1996.
95. Nengut A., Robinson E. Multiple primary neoplasms // Cancer J. -1992-Vol. 5, N 5.- P.245-248.
96. Paley D., Dyson W. The prognosis of carcinoma of the breast in relation to the type of operation performed. Brit. J. Cancer, 1948,v.2,7-13/
97. Pearl M., Johnston C., Frank Т., Roberts I.//Int. J. Gynaecol. Obstetr.-1993/-Vol 43, N 3.-P.305-312.
98. Powell D.E., Puis L., Ragell I. Current concept in epithelial ovarian tumours: does benignto malignant transformation occur? Human Pathol., 1992, v. 23, p.846-847.
99. Rose P.G., Fraire A.E. Multiple primary gynaecologic neoplasms in a young HIV-positive patient.- J. Surg/Oncol.-1993.-Vol.53, N 4.-P.269-272.
100. Rubagotti A., Perrota A., Casella C.,Boccardo F. Risk of primaries after chemotherapy and/or tamoxifen treatment for early breast cancer//
101. Ann. On col. -1996. Vol .7. -P.239-244/
102. Rusin G. J. S., Nelstrop A. E., Benzen S. M. et al. Use of tumor markers in monitoring the course of ovarian cancer.// Ann. Oncol. 1999. — Vol. 10 (suppl. 1).-P. 21-27.
источник
Смертность от рака яичников стоит на 8-м месте среди причин смертности женщин от онкологических заболеваний. Из-за отсутствия свойственных только этому заболеванию симптомов, рак яичников до сих пор диагностируют довольно поздно. Что может современная медицина, с ее генетическими исследованиями и новыми препаратами, а что зависит от самих женщин, рассказывает Светлана Викторовна Хохлова, д.м.н., старший научный сотрудник отделения химиотерапии РОНЦ им. Н.Н. Блохина.
Почему большинство случаев рака яичников у женщин приходится на возраст после 50 лет? Как связан рак яичников с отсутствием беременности и грудного вскармливания? С раком груди?
На сегодняшний день выделяют несколько факторов, которые повышают риск развития рака яичников: гормональный, генетический, алиментарные факторы, к которым относится экология и питание, и социальные факторы.
Многочисленные эпидемиологические исследования показывают влияние гормональных факторов в группах пациенток, у которых либо раньше начиналась менструация, либо поздно наступала менопауза.
Прямой связи с гормональными нарушениями в организме в этих исследованиях не наблюдалось. Однако установлено, что повышенное количество эстрогенов, во-первых, участвует в развитии рака молочной железы, а во-вторых, может повысить риск развития рака яичников.
Эти гормональные нарушения связаны, в основном, с процессами овуляции. При выходе яйцеклетки из яичника в каждом менструальном цикле происходит незначительное повреждение коркового слоя яичника. Эти повреждения эпителия накапливаются и могут приводить к перерождению эпителия в рак, поэтому женщины в возрасте после 40 лет и попадают в группу риска. Также приводить к перерождению ткани в рак могут воспалительные процессы, кисты яичников, эндометриоз.
Напротив, беременность и грудное вскармливание уменьшают количество овуляций в жизни женщины, с чем и связано предположение, что материнство снижает риск развития онкологии. Это подтверждает статистика: установлено, что в странах с низкой рождаемостью (а это, как правило, развитые страны) рак яичников встречается чаще. В развивающихся странах с высокой рождаемостью риск развития рака яичников намного ниже.
Сейчас проверяются гипотезы о том, насколько повышают риск развития рака препараты, стимулирующие работу яичников, например, эстрогены. В то же время, имеются данные, что контрацептивы с эстрогенами и прогестинами уменьшают риск развития данного заболевания.
Что такое гены BRCA и как они связаны с раком яичников и раком груди? Надо ли носителям мутировавших генов на всякий случай удалять яичники, как Анджелина Джоли удалила грудь?
Наиболее важным фактором развития рака яичников последние годы считают генетический. Всевозможные повреждения ДНК происходят в организме каждую секунду и могут приводить к развитию опухоли. Однако выявлены определенные гены-супрессоры, которые блокируют опухолевый рост. К таким генам, которые участвуют в восстановлении ДНК и сдерживают развитие опухолевого процесса, как раз и относятся BRCA1 и BRCA2.
Если же в этих генах имеются мутации, то механизм, который восстанавливает поврежденные ДНК, не работает, количество мутаций в ДНК накапливается и развивается злокачественная опухоль. По имеющейся статистике, к 70 годам у 44% носителей мутированного гена развивается злокачественная опухоль яичников. А частота мутации гена BRCA среди больных раком яичников превышает 15%.
Генетические мутации BRCA1/2 наследуемы и часто встречаются в семьях, где кто-то болел или болеет раковым заболеванием. Не обязательно раком яичников или молочной железы — сейчас уже есть данные, что меланома, рак поджелудочной железы и ряд других опухолевых заболеваний в семьях также влияют на предрасположенность к развитию рака яичников. Поэтому члены таких семей должны быть на особом учете и проходить обследования.
Что касается таких решительных мер, как профилактическое удаление яичников и молочных желез, то исследования действительно показывают значительное снижение риска развития опухоли в этих случаях. Однако в нашей стране юридически данные виды операции не разрешены.
Какие есть способы ранней диагностики рака яичников? Диагностируется ли он на УЗИ?
К сожалению, скрининг для рака яичников не показал свою значимость. Ни УЗИ, ни определенные маркеры не показывают на ранних этапах данную патологию. С помощью ультразвукового исследования можно увидеть кисты, опухолевые изменения, и если есть подозрения на злокачественную опухоль, то пациентку обязательно нужно направить к онкологу и сделать анализ крови на маркер CA125.
Так что на сегодняшний день раннюю диагностику ракового заболевания может обеспечить онконастороженность самих женщин.
Действительно ли симптомы рака яичников могут напоминать расстройство желудка? Если женщина пойдет с болью в животе к гастроэнтерологу, он заподозрит неладное?
Рак яичников имеет имплантационный характер прогрессирования: метастазирование идет по серозной оболочке кишечника, желудка, печени, также появляется жидкость в брюшной полости. Поэтому часто пациентка жалуется на расстройство желудка, боли в эпигастральной области, в правом подреберье. Такие симптомы, как увеличение живота и запоры, появляются уже на 3-4-й стадии рака.
Проблема своевременной постановки диагноза заключается в отсутствии уникальных симптомов. Даже в Москве, где медицина на достаточно высоком уровне, с момента появления у женщины жалоб до первого визита к онкологу проходит от 4 месяцев до полутора лет. Все это время она может проходить обследования по месту жительства у терапевта, но правильный диагноз установлен не будет. 80% пациенток попадают к онкологу уже на 3-4-й стадии рака яичников. Единственный путь, который может изменить скорбную ситуацию — это информирование и обучение медицинских работников первичного звена.
Если опухоль обнаружена, то операция обязательна? Существуют ли варианты лекарственной терапии?
Да, основным методом лечения рака яичников является, конечно, оперативное: удаление первичной опухоли, большого сальника, всех видимых опухолевых изменений в брюшной полости.
Вне зависимости от стадии заболевания после операции пациенты проходят химиотерапию. Обойтись без химиотерапии можно только на очень ранней стадии, но из-за сложности обнаружения заболевания таких случаев мало. Часто во время операции оказывается, что стадия рака гораздо больше, чем предполагалось по данным обследования.
За многие годы большое количество всевозможных таргетных (или целевых) препаратов изучалось при раке яичников, но на сегодня из этой группы только один препарат зарегистрирован для лечения данной патологии.
С увеличением наших познаний в биологии рака ученые обнаружили, что в опухолевых клетках с мутацией гена BRCA ряд механизмов восстановления ДНК выключены. Для пациенток — носителей данных мутаций разработали препараты, которые блокируют другие механизмы восстановления ДНК, ДНК не восстанавливается, и опухолевая клетка погибает.
Это так называемые PARP-ингибиторы. Практическое применения этих препаратов показало преимущество использования их в поддерживающем режиме у пациенток с рецидивом рака яичников с мутацией гена BRCA1/2, у которых удалось достичь полного или частичного ответа на химиотерапию с применением препаратов платины. Такие препараты выводят лечение пациенток, страдающих раком яичников, на качественно новый уровень и улучшают их выживаемость.
Иммунотерапия — новое модное на сегодня направление, которое при раке яичников только изучается. Иммунная система человека очень сложная, и, к примеру, сейчас уже установлено, что рак «прячется» от иммунного ответа организма. В последние годы активно изучается группа препаратов — ингибиторов контрольных точек (checkpoint-ингибиторы), которые делают опухоль «видимой» для собственной иммунной системы, и уже сам организм человека подключается к уничтожению рака. Ингибиторы контрольных точек уже зарегистрированы в лечении меланомы и рака легкого, и нам остается лишь держать руку на пульсе современных медицинских исследований и ожидать выхода новых инновационных препаратов.
Можно ли сформулировать порядок действий для профилактики рака яичников — в каком возрасте какие обследования проходить женщине?
Профилактика рака яичников связана с уже упомянутыми факторами риска: правильное питание, своевременное лечение воспалительных процессов, обследование и лечение кист, лечение эндометриоза и других предраковых заболеваний.
Те, у кого выявлена генетическая мутация, встают на учет к генетику и проходят специальную скрининговую диагностику с раннего возраста. Мутация BRCA1/2 может проявляться и в виде рака молочной железы, и виде рака яичников, поэтому женщины группы риска должны проходить осмотр у гинеколога и маммолога регулярно с 25 лет. С 25-30 лет раз в год необходимо делать МРТ молочных желез и маммографию, с 35 лет — УЗИ яичников, малого таза и брюшной полости, а также анализ крови на определение маркера CA125.
Главным помощником женщины может быть ее собственная информированность и онконастороженность. Рекомендую каждой женщине после 30-35 лет регулярно проходить осмотр у гинеколога и проверять молочные железы.
источник
Этиология и встречаемость наследственного рака молочной железы и яичников. Мутации основных генов предрасположенности к опухолям составляют от 3 до 10% случаев рака груди и имеют предполагаемую распространенность от 1 на 300 до 1 на 800. Два таких гена — BRCA1 и BRCA2.
В общей популяции Северной Америки распространенность мутаций в гене BRCA1 — от 1 на 500 до 1 на 1000; распространенность мутаций в гене BRCA2 приблизительно в два раза выше. Тем не менее существуют значимые различия в этническом распределении патогенных мутаций среди семей с двумя или более случаев опухолей груди и/или яичника.
Мутации BRCA1 или BRCA2 вызывают приблизительно 70-80% семейного рака груди, но только небольшую долю рака груди в целом.
Гены BRCA1 и BRCA2 кодируют повсеместно экспрессируемые ядерные белки. Полагают, что они поддерживают целостность генома, регулируя репарацию ДНК, транскрипционную трансактивизацию и клеточный цикл.
Несмотря на повсеместную экспрессию BRCA1 и BRCA2, мутация этих генов предрасполагает преимущественно к новообразованиям молочных желез и яичников. Утрата функции BRCA1 или BRCA2, вероятно, приводит к накоплению других мутаций, уже непосредственно ответственных за новообразования. В соответствии с этой гипотезой, карциномы груди и яичников у больных с мутациями BRCA1 или BRCA2 имеют хромосомную нестабильность и частые мутации в других генах-супрессорах опухолевого роста.
Образование опухолей у носителей мутаций BRCA1 или BRCA2 в половых клетках соответствует «двухударной» гипотезе; т.е. в клетках опухоли оба аллеля гена BRCA1 или BRCA2 теряют функцию. Соматическая потеря функции вторым аллелем происходит при потере гетерозиготности, внутригенной мутации или гиперметилировании промотора. Из-за высокой частоты утраты функции вторым аллелем генов BRCA1 или BRCA2 семьи несущие мутации BRCA1 или BRCA2 проявляют аутосомно-доминантное наследование новообразований.
Популяционная распространенность наследуемых мутаций генов BRCA1 или BRCA2 сильно варьирует и часто демонстрирует эффект родоначальника. В Исландии мутация BRCA2 999del5 встречается в специфическом гаплотипе и имеет распространение 0,6%. Среди евреев ашкенази мутации BRCA1 185delAG и 5382insC и мутация BRCA2 6174delT также встречаются в специфических гаплотипах и имеют распространенность 1; 0,4 и 1,2% соответственно.
Пациенты с наследуемыми мутациями генов BRCA1 или BRCA2 имеют повышенный риск развития нескольких типов опухолей. Кроме повышенного риска рака молочной железы и яичников у женщин, мутации BRCA1 вызывают повышенный риск рака простаты и, возможно, опухоли кишечника. Аналогично, кроме женского рака груди и яичников, мутации гена BRCA2 увеличивают риск рака простаты, поджелудочной железы, желчных протоков, желчного пузыря и мужского рака груди.
Среди носительниц наследуемых мутаций генов BRCA1 или BRCA2 общую пенетрантность рака молочной железы, яичников или и того и другого оценивают приблизительно в 50-80% для мутаций BRCA1 и несколько меньше для мутаций BRCA2 (40% для рака груди и 10% для опухоли яичников). Приблизительно две трети семей с анамнезом рака молочной железы и яичников у женщин передают мутацию в гене BRCA1, тогда как приблизительно две трети семей с наличием в анамнезе мужского и женского рака молочной железы имеют мутацию в гене BRCA2.
Особенности фенотипических проявлений наследственного рака молочной железы и яичников:
• Возраст начала: зрелость
• Рак молочной железы
• Опухоли яичников
• Опухоли простаты
• Многочисленные первичные опухоли
Текущие рекомендации для женщин с наследуемыми мутациями в генах BRCA1 или BRCA2 включают частые осмотры груди и яичников, включая визуализационные исследования. Оказание помощи мужчинам группы риска включает частые обследования простаты и молочных желез и лабораторные тесты для подтверждения опухоли простаты. В семьях с известными мутациями молекулярный анализ помогает сфокусировать наблюдение или профилактику на носителях мутации.
Полная двусторонняя мастэктомия может уменьшить риск рака молочных желез более чем на 90%, хотя полностью риск не устраняется, поскольку часто остается некоторое количество железистой ткани. Аналогично двусторонняя сальпингоофорэктомия может снизить риск опухоли яичников более чем на 90%.
Женский пол, возраст и семейный анамнез — наиболее важные факторы риска рака молочных желез. В популяциях западных стран совокупная встречаемость женского рака молочной железы — 1 на 200 в 40 лет, 1 на 50 в 50 лет и 1 на 10 к 70 годам жизни. Если пациенты имеют родственников первой степени родства с раком груди, возникшим после 55 лет, их риск возрастает в 1,6 раза относительно возрастного риска, тогда как относительный риск возрастает в 2,3 раза, если рак груди развился у одного из членов семьи ранее 55 лет, и в 3,8 раза, если ранее 45 лет.
Если родственник первой степени родства имел двусторонний рак молочной железы, относительный риск возрастает в 6,4 раза.
Дети пациентки с наследуемой мутацией в генах BRCA1 или BRCA2 имеют 50% риск унаследовать эту мутацию.
Вследствие неполной пенетрантности и переменной экспрессивности точно предсказать факт развития или возраст появления опухоли невозможно.
Пример наследственного рака молочной железы и яичников. С.М., 25-летняя прежде здоровая женщина, направлена в клинику онкогенетики ее гинекологом, после того как у нее диагностирован рак груди. Она была обеспокоена риском развития опухолей у ее детей и собственным риском развития рака яичников. Ее мать, две тетки по матери и дед по матери имели рак груди; у ее матери также была опухоль яичников.
Генетический консультант объяснил, что семейная история рака груди свидетельствует об унаследованной склонности, и вычислил, что риск у пробанда оказаться носительницей мутации предрасположенности к раку груди в генах BRCA1 или BRCA2 значительно выше порогового для направления на секвенирование гена. На основе последующего обсуждения прогноза и рисков повторения СМ. решила сделать секвенирование генов BRCA1 и BRCA2.
Исследование показало, что у нее мутация преждевременного завершения считывания в одном аллеле BRCA2, которая ранее была описана у других пациентов с ранним раком груди. При обсуждении полученных результатов СМ. захотела обследовать своих дочерей 6 и 7 лет. Генетический консультант объяснил, что, поскольку мутация приводит лишь к незначительному риску в детстве, решение провести генетическое тестирование лучше оставить до того времени, когда дети будут достаточно зрелыми, чтобы самим принять решение о полезности такого исследования, и пациентка согласилась с этим доводом.
Пять взрослых родственников захотели провести тестирование, и четверо из них, включая одного мужчину, оказались носителями мутации; одна из них, женщина, решила провести профилактическую двустороннюю мастэктомию; также со всеми носителями мутации обсужден риск опухолей другой локализации.
источник
Кандидат биологических наук А. ЛУШНИКОВА, кандидат медицинских наук Л. ЛЮБЧЕНКО, ГУ Российский онкологический научный центр имени Н. Н. Блохина РАМН.
Рак молочной железы — наиболее распространенный вид опухолей среди женского населения Европы, Америки и некоторых стран Азии. Ежегодно в мире регистрируется более одного миллиона случаев этого заболевания, а при средней продолжительности жизни 80 лет риск заболеть раком молочной железы составляет 12,5%. В течение последних 20 лет в мире, а также в России наметилась устойчивая тенденция к росту заболеваемости этим видом рака, особенно в городах и мегаполисах. С 1985 года он занимает первое место среди онкологических заболеваний у женщин, составляя 31,2%. Хорошо известно, что ежегодный профилактический осмотр способствует раннему выявлению опухолей. Однако часто пациентки обращаются к врачу уже с явными признаками опухоли, а это затрудняет последующее лечение. Одна из причин — непонимание важности ранней диагностики заболевания. Сейчас ученые глубоко проникли в механизмы возникновения раковой клетки, хотя многое до сих пор неясно. Как и другие онкологические заболевания, рак молочной железы по-прежнему остается коварным и агрессивным. Поэтому любому человеку очень важно иметь представление о развитии этого заболевания: предупрежден, значит, вооружен. Откуда такая напасть?
Вряд ли найдется однозначный ответ на этот вполне законный вопрос. Рак молочных желез известен с незапамятных времен: его случаи описаны, например, в древнеегипетских папирусах врача Имхотепа (3000 лет до н.э.), в вавилонском врачебном кодексе Хаммурапи (2250 лет до н.э.); о нем неоднократ но упоминает Гиппократ (400 лет до н.э.), а Гален (130-200 гг.н.э.) называет опухоли молочной железы раком из-за их внешнего сходства с крабом (по-гречески слова «краб» и «рак» звучат одинаково: karkinos). В отличие от множества заболеваний, причины которых выяснены, в основе развития злокачественных опухолей лежат более сложные механизмы и целый ряд причин, включая генетические особенности, факторы окружающей среды и многие другие.
Опухоли молочной железы могут быть как доброкачественными, так и злокачественными, или раковыми. Последние встречаются гораздо реже. Злокачественные опухоли возникают случайно или связаны с наследственностью. В 10% случаев заболевание передается из поколения в поколение и обусловлено врожденными мутациями в генах предрасположенности BRCA1 или BRCA2 (от англ. BReast CАncer).
Наиболее распространенное доброкачественное заболевание молочных желез — различные мастопатии, которые относятся к большой группе дисгормональных гипер-плазий (разрастания ткани молочных желез, обусловленные гормональными нарушениями) и связаны с нарушениями функций яичников, надпочечников, гипофиза, щитовидной железы или с нарушениями гормонального обмена в связи с заболеваниями печени, ожирением и т.д. Эти разрастания ткани молочных желез могут быть в виде плотных узелков, кист или диффузных образований. Некоторые из таких изменений можно отнести к предраковым.
И вот что удивительно, рак молочных желез встречается не только у женщин, но и у мужчин, но гораздо реже: с мужским населением связано около 1% всех случаев заболевания. Среди причин опухолей молочных желез у мужчин — редкие мутации в гене предрасположенности BRCA2, ожирение, гормональные нарушения. В отличие от доброкачественного разрастания ткани молочных желез злокачественное перерождение обязательно требует оперативного лечения.
Известно, что в отличие от нормальных клеток опухолевые не переходят после деления в фазу покоя, а продолжают бесконтрольно размножаться. Образование опухоли — многоступенчатый процесс. Рост и прогрессия опухоли, то есть ее переход от начальной к более агрессивной стадии, врастание опухоли в окружающие ткани, или инвазия, зависят от клеточных генов. Они контролируют клеточный цикл, межклеточные взаимодействия, старение и гибель клетки, а также отвечают за восстановление ДНК и стабильность клеточного генома.
Под действием различных факторов в нормальных генах могут возникать мутации. Чем дольше делятся клетки, тем вероятность таких мутаций выше, а значит, вероятнее злокачественное перерождение клеток под действием канцерогенов. Накопление повреждений в клеточном геноме связано как с ошибками репликации ДНК, так и с внешними, внеклеточными факторами.
К факторам риска на уровне человеческого организма можно отнести повышенный уровень эстрогенов (женских половых гормонов), нарушения менструального цикла, функций щитовидной железы и надпочечников, аборты и отсутствие грудного вскармливания. Эти особенности нередко встречаются в анамнезе больных раком молочной железы. К факторам, повышающим риск заболевания им, относятся также ранний возраст менархе (11-12 лет); поздние первые роды (28-30 лет); большие площадь и вес плаценты, усиливающие риск возникновения рака молочной железы у дочерей; аборты, особенно до первых родов; хроническое воспаление придатков; эндометриоз (разрастание клеток, выстилающих матку); кисты яичников и другие заболевания.
В возрасте после 65 лет наблюдается второй пик заболеваемости злокачественными опухолями молочной железы, связанный с эстрогенами надпочечников и повышенной массой тела. В общем разнообразные факторы риска этого заболевания можно условно разделить на три группы:
связанные с репродукцией (рождение детей/аборты, лактация, возраст менархе), сопутствующие гинекологические заболевания;
связанные с генетической предрасположенностью: злокачественные опухоли, особенно женских репродуктивных органов и молочных желез у близких родственников;
связанные с нарушениями обмена веществ и гормональными нарушениями, в том числе с приемом гормональных препаратов, содержащих эстрогены.
Развитию рака молочной железы предшествует разрастание ее ткани гиперплазия (увеличение числа клеток) и появление в протоках железы нетипичных клеток. Эти изменения называются предраковыми. К таковым относится и упомянутая нами мастопатия — кистозно-фиброзные и диффузные изменения ткани молочной железы. Хотя злокачественное перерождение при мастопатии происходит довольно редко, все же появление первых признаков мастопатии, выявляемых при пальпации, то есть осторожном прощупывании железы, — это повод для обращения к маммологу.
Маммография (рентгеновское обследование) и УЗИ — основные методы раннего выявления опухолей молочной железы и мастопатии. Результаты этих исследований нередко подтверждают ся с помощью пункции молочной железы, когда взятый иглой шприца образец предполагаемого новообразования исследуется под микроскопом. Очень часто изменения молочной железы обнаруживают сами пациентки при осмотре желез в первые 6-10 дней после начала менструаций.
Какие же признаки должны насторожить при самостоятельном обследовании? Во-первых, ощутимые уплотнения в молочной железе; изменение контура железы и ее плоская, а не округлая поверхность над уплотнением; отек железы, когда кожа напоминает пористую лимонную корку; втяжение соска внутрь. При запущенной злокачественной опухоли большая часть молочной железы отекает и краснеет, а при прорастании опухоли в кожу появляются язвы. Опухолевые клетки через лимфатические сосуды попадают в ближайшие лимфатические узлы, которые увеличиваются в размерах, нарушается отток жидкости из молочной железы, и развиваются отеки. Через кровеносные сосуды опухолевые клетки разносятся по организму и дают начало новым злокачественным очагам — метастазам.
Нередко предположение или заключение врача-маммолога о наличии патологических изменений в молочной железе порождает у пациенток самые неприятные опасения, а порой и панику. Однако на сегодняшний день уже имеется немало методов, позволяющих уточнить диагноз рака молочной железы и назначить соответствующее лечение, если диагноз подтвердится. Речь идет, прежде всего, о маркерах (факторах риска) опухолевого роста, обнаруживаемых в крови пациенток. Основное их предназначение — раннее выявление злокачественных новообразований и рецидивов, а также оценка эффективности лечения заболевания. При направлении в диспансер или специализированную клинику пациентке предложат сдать кровь на анализ таких маркеров. В отношении рака молочной железы пока не существует строго специфичного маркера, поэтому применяется комплекс тестов на несколько маркеров. Концентрации этих маркеров в сыворотке крови пациенток зависят от степени злокачественности и стадии заболевания и поэтому важны для диагноза и прогноза заболевания. Существуют и другие параметры, позволяющие специалисту заподозрить прогрессирование заболевания или метастатическое поражение других органов. Анализ этих показателей, в той или иной степени связанных с опухолями молочной железы, дает возможность спланировать дальнейшие действия: назначить химио- или гормональную терапию, хирургическое лечение либо лечебно-профилактические препараты в случае мастопатии или доброкачественных новообразований, к примеру фиброаденомы молочной железы. Перечень диагностических тестов меняется в зависимости от материальных возможностей клиники и пациенток, а также от конкретного случая заболевания.
Главное — своевременно и профессионально сделать анализы, руководствуясь рекомендация ми специалистов. В жизни, к сожалению, нередки случаи обращения пациенток к разного рода целителям и к так называемой народной медицине. Не умаляя значения фитотерапии и гомеопатии, врачи-онкологи настоятельно советуют обращаться именно в профильные учреждения: специализированные диспансеры и клиники, где пациентке помогут квалифицированные врачи. Промедление в выборе правильного метода терапии очень опасно.
В основу лечения рака молочной железы положен комбинированный комплексный подход в сочетании с хирургическим лечением. На опухоль воздействуют лекарственными препаратами, облучением, гормонами. Удаление всей молочной железы, или мастэктомию, зачастую заменяют компромиссным органосохраняющим лечением: удалением сегментов железы с подмышечными лимфатическими узлами. Сохранить и восстановить форму молочной железы позволяют реконструктивные операции, важность которых очевидна, особенно для молодых пациенток. Операбельны (подлежащие операции) обычно первая-вторая стадии рака. При запущенных опухолях или неоперабельном раке требуется дополнительное лечение, которое затормаживает рост опухоли и дает возможность хирургического вмешательства. Однако в большинстве случаев одного хирургического лечения недостаточно. Если риск рецидива низок, то есть опухоль мала (менее 1 см), отсутствуют метастазы в близлежащие и отдаленные лимфатические узлы, степень злокачественности низкая, а опухолевые клетки несут рецепторы опухолевых клеток к эстрогенам и прогестерону (главным половым гормонам женщины), то хирургическое лечение нередко дает устойчивый положительный эффект. Но иногда развиваются послеоперационные осложнения в виде кровотечений и нагноения раны. Вследствие удаления лимфатических узлов нарушается отток лимфы из тканей и развивается лимфостаз, обычно это происходит спустя несколько недель после операции. Нередко лимфостаз провоцируется инфекциями, горячими и солнечными ваннами, физическими нагрузками. Вот почему больным, перенесшим мастэктомию, не рекомендуются инъекции в руку на оперированной стороне, противопоказаны солярии и сауны, им нужно избегать инфицирования кожи через трещины или царапины. Полезны специальный массаж рук и гимнастика, улучшающие циркуляцию лимфы и восстанавливающие работу суставов.
Успех зависит от прогноза
Наиболее эффективное лечение опухолей молочной железы возможно лишь с учетом прогноза течения заболевания и реакции пациента на тот или иной препарат, то есть имеется ряд факторов, указывающих на благоприятный или неблагоприятный исход заболевания, а также на чувствительность опухоли к проводимому лечению. К таким факторам относятся размер опухоли, наличие метастазов в лимфатические узлы, гистология опухоли (ее строение, определяющее злокачественность), уровень эстрогеновых и прогестероновых рецепторов в опухолевых клетках и другие.
Морфологические и молекулярно-биологические факторы прогноза рака молочной железы и эффективности лечения
Количество пораженных метастазами лимфатических узлов
Прорастание опухоли кровеносными и лимфатическими сосудами
Показатели активности синтеза ДНК
Плоидность опухолевых клеток
Интенсивность деления опухолевых клеток (уровень ядерного белка митозина, уровень ядерного антигена Ki-67 и т.д.)
Наличие рецепторов эстрогенов и прогестерона
Уровень активаторов и ингибиторов (блокаторов) плазминогена (белка, участвующего во многих клеточных взаимодействиях, в инвазии и метастазировании и др.).
Исследованию этих и других факторов посвящены многие монографии, мы отметим лишь принципиально важные для развития рака молочной железы у женщин. Во-первых, это рецепторы стероидных гормонов — специфические белки, которые избирательно связывают молекулы соответствующих стероидов, проникающих в клетки (рис. 2). Наличие в опухолевых клетках рецепторов к эстрогенам и прогестерону говорит о чувствительности опухоли к гормональной терапии и о малой возможности метастазирования. На чувствительность опухоли к лечению гормонами указывает также наличие в опухолевой ткани эпидермальных факторов роста (веществ, способствующих росту определенных типов клеток). Когда в опухолевых клетках нет рецепторов к стероидным гормонам, то лечить опухоли с помощью гормональной терапии бессмысленно.
В передаче сигналов к делению клеток участвует также рецептор HER2/neu (рис. 3). Его блокирование может замедлить или остановить деление опухолевых клеток и рост опухолей, которые зависят от этих сигналов. Для такой блокировки был разработан препарат герцептин. Когда ген, кодирующий этот рецептор, активно транскрибируется (переписывается), то целесообразно использовать химиотерапию с применением герцептина, а лечение гормонами в этом случае неэффективно.
Злокачественные опухоли способны к метастазированию и инвазии. В этих процессах главную роль играют белки uPA и PAI-1. Если их уровни превышают определенные минимальные значения, то риск рака молочной железы увеличивается в 1,5-2 раза, поэтому данные важны для прогноза.
Рост злокачественной опухоли сопровождается формированием в ней разветвленной сети капилляров — сравнительно мелких кровеносных сосудов. Процесс регулируется фактором роста эндотелия сосудов. Высокий уровень этого белка в опухоли свидетельствует о неблагоприятном прогнозе как при раннем, так и при прогрессирующем злокачественном процессе. Анализ активности фактора роста эпителия стимулировал создание новых препаратов, блокирующих рост злокачественных клеток, например перспективного препарата авастин.
В последнее время выяснилось, что в ткани молочной железы с помощью фермента ароматазы синтезируются собственные эстрогены. Поэтому подавление синтеза этого фермента с помощью препаратов, например аримедекса и аромазина, может снизить риск рака молочной железы. Таким образом, благодаря исследованиям биохимиков и молекулярных биологов в распоряжении врачей оказались биологически значимые параметры, позволяющие прогнозировать течение заболевания на различных стадиях и подбирать подходящую терапию при распространяющемся раке молочной железы. Во-первых, это уровни рецепторов к эстрогенам и прогестерону в опухоли, которые дают возможность оценить целесообразность гормональной терапии и предвидеть ее результат. Во-вторых, уровень активности гена Her2/neu (см. рис.3), позволяющий обнаружить пациенток с повышенным риском рецидива опухоли молочной железы и риском ее метастазирования на ранних стадиях заболевания. В-третьих, уровень фактора роста эпителия, указывающий на прогноз развития опухоли как в начале, так и на более поздних стадиях заболевания.
Молекулярно-биологическая подоплека рака молочной железы
Какие молекулярные механизмы лежат в основе рака? Известно, что развитие опухоли связано с нарушением роста и дифференцировки клеток и злокачественным их перерождением. Во многих случаях такие нарушения обусловлены мутациями или резким повышением активности клеточных онкогенов — нормальных генов, которые участвуют в регуляции клеточного цикла, передаче сигналов и в других процессах жизнедеятельности клеток. Сейчас известно немногим более 100 различных протоонкогенов — нормальных клеточных генов, повышенная активность изменения которых или изменение их структуры приводит к синтезу онкобелков, играющих ключевую роль в клеточной жизнедеятельности. Такая активация протоонкогенов и превращение их в онкогены возможны в результате мутаций, хромосомных перестроек и других механизмов. В клетке человека около 50 000 функционирующих генов, поэтому доля потенциальных онкогенов, ответственных за злокачественный рост клеток, достаточно велика. В случае рака молочной железы, вероятно, задействовано не более 10 онкогенов.
Кроме того, нарушения клеточного цикла и бесконтрольное размножение клеток могут быть связаны с мутациями в генах-супрессорах, или подавителях опухоли. К ним относятся, например, мутации в уже упомянутых нами генах BRCA1 и BRCA2. Эти гены кодируют высокомолекулярные ядерные белки, которые исправляют повреждения ДНК и поддерживают стабильность генома, а продукт гена BRCA1 участвует в правильном распределении хромосом при делении клеток, подавляет чрезмерное гормонозависимое размножение клеток молочной железы, которое происходит, например, при половом созревании и подготовке к лактации у беременных женщин. Вот почему мутации этого гена приводят к целому спектру нарушений, начиная от новых генных мутаций и хромосомных перестроек и кончая безудержным размножением клеток эстрогензависимых органов, определяю щим развитие опухолей молочной железы и яичников. Таким образом, мутации в генах BRCA1/BRCA2 нарушают контроль за повреждениями ДНК и поддержанием целостности клеточного генома, что обусловливает появление злокачественных клеточных клонов.
Помимо мутаций активность генов-супрессоров опухоли и других генов, ответственных за регуляцию, может изменяться в результате нарушений в молекуле ДНК. Это справедливо и по отношению к раку молочной железы.
В некоторых лабораториях с помощью специальных микрочипов исследуются профили изменений клеток опухолей молочной железы. Например, французские исследователи сравнили профили таких изменений в разных образцах злокачественных клеток до и после лечения препаратом доксорубицин, что позволило наметить и обосновать стратегию химиотерапии. Они выделили группу из 496 генов, активность (экспрессия) которых отличается от экспрессии этих генов в нормальной ткани молочной железы. Несколько лет назад были опубликованы результаты исследования экспрессии 200 генов, полученные на 122 образцах опухолевой ткани молочной железы. Выделили несколько групп генов рака молочной железы, начиная с экспрессии генов близкой к норме и кончая генами с экспрессией, дающей наихудший прогноз.
Во многих лабораториях проводятся эксперименты по созданию «молекулярного портрета» опухолей молочной железы. Японские исследователи, например, получили молекулярный профиль генов в процессе лечения пациенток препаратом доцетаксел. Оказалось, что чувствительные и устойчивые к этому препарату опухоли четко различаются по активности 76 генов.
Конечно, эти подходы пока очень трудоемки и дороги для применения на практике, однако они важны для разработки более специфичных и простых методов анализа эффективности лечения. Такие данные помогут в дальнейшем прогнозировать течение заболевания и чувствительность опухоли к терапии.
Возникновение рака может быть связано не только с нарушением работы онкогенов и других генов, но и с вирусными инфекциями.
В последние 10 лет появились веские доказательства того, что в организме человека циркулирует ретровирус, родственный вирусу опухолей молочных желез мышей, или MMTV (от англ. Mouse Mammary Tumor Virus). Их активация — сложная цепочка биохимических процессов, похожая на активацию некоторых ретровирусов, вызывающих лейкозы у человека и животных.
Сначала в сыворотках крови многих больных раком молочной железы обнаружили антитела к белкам, родственным структурным белкам оболочки MMTV. Затем в ДНК лимфоцитов периферической крови и в опухолевой ткани примерно у 40% больных спорадическим раком молочной железы с помощью высокочувствительных методов обнаружили последовательности, похожие по строению на гены этого ретровируса. Из генома опухолевых клеток, попадающих в плевральную полость больных раком молочной железы, были выделены и клонированы последовательности ДНК, на 95-97% соответствующие полноразмерному провирусу.
MMTV-родственный провирус человека, или hMTV (от англ. human Mammary Tumor Virus), был обнаружен в геноме лимфоцитов и опухолевых клеток, но не в нормальных тканях человека (рис. 4). Это указывает на внешний источник ретровирусной инфекции. Частота встречаемости MMTV-гомологичных последовательностей меняется от 0-1% (Великобритания) до 75-80% (Тунис). По нашим оценкам, в России она составляет от 39-42% при спорадическом раке молочной железы до 52-56% при семейном раке и у беременных женщин со злокачественной опухолью груди. Высказано несколько предположений о путях попадания вируса в организм человека, в том числе инфицирование через лимфоидную ткань желудочно-кишечного тракта из загрязненных мышиными фекалиями продуктов. Это предположение, по-видимому, небезосновательно, так как MMTV-гомологичные последовательности были выявлены в лимфоидной ткани больной раком молочной железы и раком толстой кишки, а провирусные последовательности обнаружены у домовых мышей Mus musculus sp.domesticus, обитающих в московском регионе. Более того, распределение MMTV-гомологичных последовательностей в человеческих популяциях соответствует распространению этого вида мышей. Не исключена передача MMTV человеку от мыши как непосредственно, так и через промежуточных «хозяев» (кошек, приматов).
Недавно группа исследователей из США под руководством доктора С. Росс показала, что первичной мишенью для ретровирусной инфекции могут быть древовидные клетки — определенные лимфоидные клетки, которые поглощают чужеродные белки и вирусные частицы путем пиноцитоза — процесса поглощения жидкостей и инородных тел (рис. 5). Оказалось, что эти клетки могут затем продуцировать инфекционный вирус и передавать его другим клеткам, в частности В- и Т-лимфоцитам. При отсутствии дендритных клеток эффективность инфекции MMTV резко ослабевает; несомненно, она зависит и от других причин. Для циркуляции в организме как мышей, так и человека MMTV использует лимфоциты периферической крови. На этом этапе число копий провируса в геноме сравнительно мало. Во время активного деления эпителиальных клеток молочной железы, растущей под действием гормонов, встроенный в клеточный геном провирус получает возможность быстрого умножения копий в тысячи раз. По-видимому, провирус может встраиваться в клетки молочной железы, обладающие свойствами стволовых клеток, которые впоследствии дают начало множественным очагам опухолевого роста. Есть данные о возможном прямом или опосредованном участии hMTV в развитии рака молочной железы. В экспериментах с культурами клеток рака молочной железы человека, содержащими (+) и не содержащими (-) провирусные последовательности, группа американских исследователей обнаружила, что в (+)-клетках наблюдается высокая активность генов, связанная с иммунным ответом на инфекцию. Кроме того, в этих (+)-клетках активировались восемь генов, которые были совершенно неактивны в (-)-клетках. Сравнение картин генной экспрессии с помощью микрочипов показало, что суммарная активность генов в инфицированных hMTV клетках соответствует активности генов при воспалительном процессе с участием интерферонов, то есть вирусная инфекция играет в развитии рака молочной железы вполне определенную роль.
Чем же отличаются инфицированные и не инфицированные hMTV опухоли? Ответить на этот вопрос попытались австралийские биологи. Они показали, что на ранних стадиях рака молочной железы у пациенток одной из клиник Сиднея инфицированные этим ретровирусом опухоли по своему строению и росту сходны с опухолями молочной железы у мышей. Однако определенное сходство в развитии рака молочной железы мышей и человека было замечено задолго до этой работы. И у человека и у мышей известны опухоли молочной железы, в которых очень быстрый рост начинается сразу в нескольких очагах. Есть основания предположить, что такие опухоли возникают из клеток типа стволовых, которые приобрели способность к злокачественному росту вследствие либо геномных нарушений в клетках, либо вирусной инфекции. Новым в исследовании австралийских ученых стал факт накопления в ядрах инфицированных hMTV опухолей молочной железы человека неактивного белка — продукта гена р53, подавляющего рост опухоли, о котором мы упоминали выше. Почему этот белок не работает, еще предстоит разобраться, но для таких опухолей характерен более быстрый рост, чаще всего они локализованы в области протоков молочных желез.
В то же время группа исследователей под руководством проффесора Сельмона из Австрии с помощью генно-инженерных конструкций показала, что продукт одного из генов МMTV содержит последовательность аминокислот, соответствующую последовательностям аминокислот в иммунорецепторах, или ITAM (от англ. Immunoreceptor Tyrosine-based Activation Motifs), участвующих в передаче сигналов, регулирующих развитие клеток. Гиперактивация этих сигнальных путей вследствие проявления провируса в эпителиальных клетках молочной железы может привести к перерождению клеток и развитию рака молочной железы. Возможность появления морфологически измененных клеток, способных к трехмерному росту в культуральной среде in vitro, проверена нами в экспериментах с клетками эпителия эмбриональной почки человека, которые культивировали с вирус-продуцирующими клетками мышей. Было показано, что вирусные последова тельности действительно встраиваются в клеточный геном и на них образуются транскрипты РНК. Внедрение провируса в геном клетки может повлечь изменение активности генов в области такого объединения. Кроме того, в геноме мышиного ретровируса имеются чувствительные к действию гормонов регуляторные элементы, которые также могут изменить или полностью нарушить работу клеточных генов. Вспомним также о кодируемых MMTV аминокислотных последовательностях в составе ITAM, которые могут опосредовать существенные изменения в инфицированных вирусом клетках. Однако при последующих делениях клеток в результате хромосомных перестроек некоторые из хромосом утрачиваются вместе со встроенными в клеточный геном копиями провируса. Таким образом, опухолевое перерождение вероятно лишь в ограниченном числе клеток. Другими словами, кроме горизонтальной передачи hMTV, по-видимому, существует и вертикальная: от матери к детям. При этом лимфоидная ткань кишечника человека может служить «воротами» ретровирусной инфекции, а лимфатические узлы — резервуаром. Важно, что при умножении числа провирусных копий в составе клеточного генома наблюдается минимальный иммунный ответ на инфекцию, хотя в инфицированных клетках и обнаруживаются признаки, характерные для воспаления. Например, как уже говорилось, активны гены, кодирующие белки, которые участвуют в регуляторных процессах вместе с интерфероном. По мнению некоторых исследователей, само воспаление в молочных железах, равно как и их резкая инволюция, то есть массовое уменьшение тканей (например, после аборта или внезапного прекращения лактации), может повышать риск злокачественного перерождения клеток.
Участие МMTV в развитии злокачественной опухоли, а возможно, и опухолей других локализаций позволяет выделить носительниц hMTV в группу риска наряду с пациентками из наследственно отягощенных семей, несущими мутации в генах предрасположенности.
Итак, благодаря усилиям специалистов в области клинической биохимии и генетики, молекуляр ной биологии, вирусологии и иммунологии удалось составить довольно емкий «молекулярный портрет» рака молочной железы. В то время как усилия ученых сосредоточены на выяснении причин и механизмов возникновения опухолей, врачи стремятся распознать опухоли на возможно ранних стадиях, которые хорошо поддаются лечению и прогнозу. Вот почему число параметров для диагностики рака и оценки его развития продолжает расти. О некоторых из них мы рассказали в предлагаемой читателю статье. Какие из таких маркеров окажутся наиболее эффективными и найдут применение в клинике, покажет ближайшее будущее.
Хотя неумолимая статистика говорит о росте заболеваемости раком молочной железы, у специалистов есть повод для оптимизма. Как заметил доктор Сельмон: «Насколько коварен рак, настолько изобретателен человеческий разум…» Несомненно, ранняя предклиническая диагностика уже сейчас позволяет значительно улучшить результаты лечения и добиться лучшей выживаемости пациенток, вернуть их к активной жизни и вселить надежду на полное выздоровление.
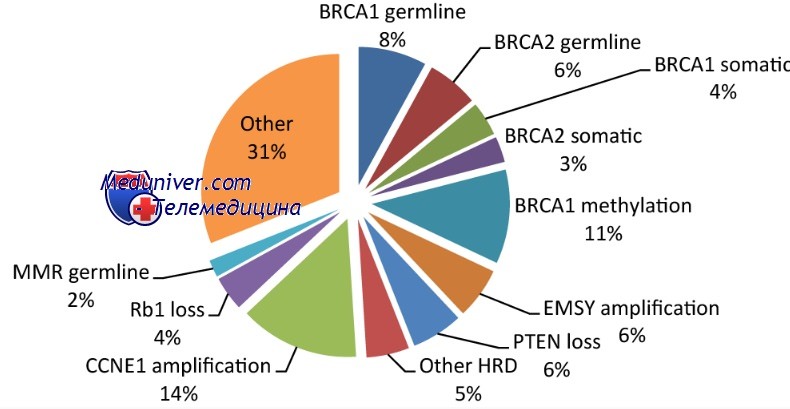
Рак молочной железы в 10% случаев передается по наследству. Если одна из двух копий, или аллелей, гена BRCA1 у женщины несет мутацию, то вероятность развития у нее рака молочной железы возрастает до 85%, а рака яичников — до 40%. У носителей таких мутаций возрастает и риск рака толстой кишки, а у мужчин — рака предстательной железы. В гене BRCA1 выявлено до 700 различных мутаций, которые характерны для жительниц определенных географических регионов. В случае мутаций в гене BRCA2 риск развития злокачественных опухолей груди и яичников сравнительно ниже. Показано, что в России частота мутаций в гене BRCA1 у пациенток с семейным раком молочной железы примерно на порядок выше, чем в гене BRCA2. Мутации в гене BRCA1 обнаруживаются в 16% семей с двумя и более близкими родственника ми, страдающими злокачественными опухолями груди в отсутствие рака яичников. Сочетание этих двух заболеваний в семье также обусловлено мутациями в генах BRCA1/BRCA2 (см. схему на стр. 21). Оказалось, что мутации в гене BRCA1 встречаются у 61% российских пациенток с семейными случаями рака молочной железы и яичников. Мутации в генах BRCA1/BRCA2 могут обусловить и другие формы рака. Если одни и те же мутации в гене BRCA2 у российских пациенток встречаются очень редко, то в гене BRCA1 преобладает особая мутация, которая характерна для европейской части России и встречается также в странах Европы.
Носительницы этих мутаций нуждаются в регулярном посещении маммолога, поскольку риск рака молочной железы у них достигает 80-90%, а их ближайшим родственникам рекомендована консультация врача-генетика. Кроме указанных имеются и другие гены, мутации или определенные аллельные варианты которых могут способствовать развитию опухолей молочной железы и некоторых других злокачественных новообразований. Однако этот вклад не столь значителен, как в случае генов BRCA1/BRCA2.
Предположение о возможной мутации возникает у генетика, если среди ближайших родственников пациентки обнаруживаются две и более больных раком молочной железы, если заболевание развивается в возрасте до 45 лет, при опухолях в двух молочных железах или при раке с множественными очагами опухоли, а также при наличии рака яичников.
Спорадический рак молочной железы развивается без особых очевидных причин, хотя имеются определенные, не связанные с наследственной предрасположенностью факторы, повышающие риск его возникновения.
источник