Рак молочной железы – онкологическое заболевание, наиболее часто встречающееся у женщин старше 60 лет. Ежегодно в Росси регистрируется 50 тысяч новых случаев рака молочной железы. Наиболее часто на начальных стадиях рак молочной железы протекает бессимптомно, поэтому развивается незаметно.
Молочная железа – гормонзависимый орган. В течение жизни она подвергается регулярным гормональным атакам: во время менструального цикла, беременности, лактации. Дополнительными предрасполагающими факторами к возникновению рака молочной железы относятся прием контрацептивов, аборты, выкидыши, резкие изменения веса, стрессы и депрессии. Наступление климакса сопровождается полной гормональной перестройкой организма:
- функция яичников затухает;
- происходит замещение железистой ткани молочной железы на жировую.
И все это сопровождается изменением структуры и объема груди.
Обязательно нужно пройти профилактический осмотр маммолога в нашем медицинском центре, если вы:
- переживаете климакс;
- никогда не рожали;
- делали аборты или у вас были выкидыши;
- принимали или принимаете оральные контрацептивы.
В период климакса ваша грудь испытывает колоссальную гормональную нагрузку, поэтому нуждается в тщательном и регулярном обследовании.
Чем старше женщина, тем больше риск возникновения рака молочной железы. У женщин старше 60 лет рак молочной железы выявляется в 400 раз чаще, чем у молодых 20-ти летних девушек. Основной причиной возникновения рака молочной железы является перенасыщенность организма эстрогенами – женскими половыми гормонами, которая происходит во время климакса. Именно поэтому после менопаузы наступает период наибольшей вероятности развития опухолевых заболеваний.
Факторы риска возникновения рака груди:
- пожилой возраст (старше 60 лет);
- наследственность (выявление онкологических заболеваний в семье);
- отсутствие родов или первые роды после 30 лет;
- позднее наступление менопаузы (после 55-летнего возраста);
- фиброзно-кистозная мастопатия молочных желез;
- болезни гинекологических органов;
- травмы груди;
- проживание в зоне повышенной радиоактивности;
- частые стрессы и депрессии.
Если вы уже достигли менопаузы, посетите врача-маммолога в клинике «Витамед», чтобы исключить рак молочной железы. Вовремя выявленная патология позволит нам наиболее эффективно провести лечение и сохранить здоровье, а нередко и саму жизнь!
Согласитесь, в нашей стране женщины преклонного возраста редко посещают гинеколога, а тем более маммолога, не проходят профилактических врачебных осмотров, поэтому рак у них зачастую выявляют случайно и на поздних стадиях. У пожилых пациенток течение болезни осложняется общим состоянием здоровья и наличием хронических заболеваний, поэтому процент смертности растет вместе с возрастом. Кроме того, больных этой категории лечат более щадящими методами, что тоже влияет на результат. У женщин 65-74 лет рецидив возникает в 7% случаев, старше 75 у каждой третьей пациентки.
Симптомы заболевания:
- втянутость соска и кровянистые выделения из него;
- уплотнение в молочной железе с нечеткими краями;
- отечность груди;
- увеличение лимфоузлов в подмышечных впадинах;
- раздражение, шелушение кожи молочных желез, эффект апельсиновой корки.
Если вы заметили у себя один или несколько из этих симптомов, немедленно звоните в нашу клинику! Залог успешного лечения рака – обнаружение болезни на ранних стадиях и незамедлительное лечение. Рак молочной железы – не приговор, но промедления не терпит. Выявление рака на начальной стадии на 70 % повышает шансы на полное излечение. Поэтому женщинам, особенно пожилого возраста, необходимо два раза в год посещать узких специалистов, чтобы предупредить возможное развитие болезни.
В медицинском центре «Витамед» вы получите консультацию онколога-маммолога, кандидата медицинских наук. После внимательного осмотра при необходимости вам будет назначено диагностическое обследование для контроля состояния молочных желез и выявления возможных отклонений. Помните, что раковое заболевание на начальных стадиях незаметно, но именно в этот момент лучше всего поддается излечению. Звоните нам прямо сейчас!
источник
24.03.2009 12:22 При ранней диагностики рака груди, заболевание успешно лечится в 98% случаев. Современные ученые продолжают делать впечатляющие открытия как в области диагностики, так и в области терапии рака молочной железы. Однако для пожилых женщин рак груди представляет более серьезную угрозу, чем для женщин молодого и среднего возраста. Особенно это касается проблем с выявлением рака на ранних этапах развития опухоли. И эта проблема не будет решена, пока пожилые женщины не будут строго придерживаться рекомендаций медицинских специалистов и в обязательном порядке проходить ежегодное рекомендуемое обследование. Последние исследования свидетельствуют, что именно из-за отказа от ежегодного обследования у пожилых пациенток настолько низкий процент ранней диагностики рака груди.
По оценкам Национального института рака (США) ежегодно рак груди диагностируется у 225 тысяч американок, около 40 тысяч пациенток погибает каждый год. Среди погибших большое количество пожилых пациенток.
Невозможно переоценить важность раннего выявления рака груди. Ранняя диагностика позволяет добиться практически стопроцентного излечения заболевания. Однако добиться от женщин регулярного прохождения маммографии пока не представляется возможным, около 70% пациенток пожилого возраста не проходили обследование в течение нескольких лет до диагностики рака.
Риск развития рака груди повышается при следующих факторах:
— в подростковом возрасте пациентка страдала от ожирения;
— женщина не рожала детей или рожала старше 38-летнего возраста;
— длительное применение оральных контрацептивов;
— увеличение массы тела в пожилом возрасте;
— позднее наступление менопаузы (после 50-летнего возраста);
— операции по увеличению груди.
Также фактором риска принято считать повышение эстрогена в крови женщины, а также влияние комбинации эстрогена и прогестерона на ткани молочной железы.
Вторичные факторы — это прежде всего курение, ожирение, употребление алкоголя, неправильное питание и стресс — также оказывают сильнейшее негативное влияние.
Наследственность может значительно повышать риск развития рака груди (около 10% всех случаев).
Восемьдесят процентов всех случаев рака молочной железы диагностируется у женщин старше 50 лет, около 60 процентов приходится на женщин старше 65 лет. Вероятность заболевания раком груди растет после 50-летнего возраста с каждым годом. Средний возраст пациенток, у которых диагностируют рак груди — это 62 года. Что касается женщин старше 70-ти лет, ситуация по диагностике крайне сложная. После 70-ти лет женщины вообще не посещают маммографию. Такое халатное отношение к диагностике резко повышает летальность в возрастной группе от 70-ти лет. Нельзя снимать вину в этой проблеме с медиков, так как отсутствует механизм ведения информационно-разъяснительной работы о необходимости регулярного прохождения маммографии с пожилыми женщинами. Если бы удалось наладить нормальный контакт по этому вопросу, скорее всего ситуация изменилась бы в лучшую сторону.
После того, как у пациентки обнаруживается опухоль, проводится консилиум из нескольких медицинских специалистов (включая хирурга) для выбора метода лечения. Метод лечения рака груди зависит от стадии развития злокачественного процесса, возраста и общего состояния пациентки. Существует четыре традиционных метода лечения рака:
При условии ранней диагностики рака груди у пожилой пациентки, лечение начинается с проведения хирургической операции и дальнейшей химиотерапии и лучевой терапии. Однако в данный метод могут быть внесены некоторые изменения, например химиотерапия может быть начата до проведения операции, чтобы подавить злокачественные клетки. Читать подробнее о лечении рака груди
источник
Когда-то амазонками называли храбрых воительниц, отрезавших себе грудь, чтоб не мешала метко стрелять из лука. Нынче же так называют женщин, которым из-за рака молочной железы удалили грудь, но этим спасли жизнь.
Это одно из самых распространенных заболеваний, которое имеет каждая пятнадцатая украинка, и по большинству – в преклонном возрасте. От рака никто не застрахован, и все же, в каждом возрасте он имеет свои особенности возникновения. Поэтому, зная их, как молодые девушки, так и те, кому за шестьдесят пять, могут свести к минимуму риск услышать страшный диагноз.
Как распознать болезнь и предотвратить ее – специально для читательниц газеты «Здоров’я і довголіття» расскажет ведущий специалист одного из известнейших в Украине учреждений по диагностике и лечению рака груди – врач-маммолог Киевского областного онкологического диспансера Сергей Грибач.
— Сергей Михайлович, почему в зависимости от возраста женщины течение заболевания и факторы возникновения рака молочной железы несколько отличаются?
— Рак молочной железы занимает первое место среди всех злокачественных заболеваний у женщин. По прогнозам и наблюдениям, с 2020-го ежегодно в мире будет регистрироваться около миллиона новых случаев выявления рака молочной железы, и незначительный процент среди таких больных – мужчины. То есть, количество выявленных случаев будет стремительно возрастать, и нет ни малейшего повода относиться к проблеме несерьезно, особенно женщинам 60-65 лет.
По данным последних исследований, рак грудной железы имеет возрастные особенности и является гормонозависимым. Условно можно выделить три группы больных: до 35 лет, от 35 до 65-ти и старше 65 лет. Как ни странно, но наихудшие показатели выживаемости после обнаружения и лечения наблюдаются у больных первой и третьей групп. То есть, в эти годы жизни рак имеет самое агрессивное течение, но факторы, влияющие на развитие патологии в эти периоды, – разные.
Так, у женщин до 35 лет рак молочной железы обусловлен генетически. То есть, если у кого-то в семье, особенно у мамы или бабушки, был рак молочной железы, то вероятность, что подобная мутация генов передастся по наследству, достигает 30-40%.
Среди известнейших мутаций – мутации двух генов: так называемые BRCA1 и BRCA2. Их можно обнаружить, проведя генетическое обследование. Оно сравнительно недорогое, его достаточно сделать лишь раз в жизни и знать, есть ли сбой и риск заболеть раком груди.
Сейчас даже существует так называемый синдром Анджелины Джоли. Голливудская знаменитость попала именно в эту группу риска: ее бабушка, мама и тетя умерли от злокачественной опухоли молочной железы. Поэтому, когда у звезды обнаружили мутацию BRCA, чтобы минимизировать риск возникновения рака, она удалила грудь и призвала женщин сдавать анализ, чтобы снизить риск этой угрозы.
У второй группы женщин – в возрасте от 35 до 65 лет – показатели заболеваемости несколько ниже, а выживаемость после лечения рака груди значительно выше. Примерно такая же тенденция возникновения и течения заболевания наблюдается и у женщин, которым за 70.
— То есть, мы видим волнообразный рост пиков возникновения рака молочной железы. Следующий пик после возраста до 35 лет приходится на период жизни 60-65 лет, когда женщины пребывают в менопаузе, и, казалось бы, гормоны уже не вырабатываются. Но рак груди – гормонозависим. Что же происходит в организме женщины, которой за 60, и что провоцирует рак?
— Есть несколько факторов, вызывающих рост показателя заболеваемости после 65 лет. Действительно, в этом возрасте у женщин наступает уже постменопауза. И клиническими исследованиями доказано, что рак молочной железы имеет доклиническое течение, которое составляет 10-15 лет. То есть, опухоль возникла раньше, но была «спящей» все эти годы. Что же может ее разбудить и способствовать перерождению в злокачественное образование?
Сегодня всё больше исследований показывают, что существенную роль в возникновении и клиническом течении играет синдром Х, или метаболический синдром. Это – повышенные артериальное давление и уровень сахара в крови, нарушение липидного обмена, ожирение. Если взглянуть на наших бабушек, то большинство из них имеют этот синдром. При его наличии риск заболеваемости возрастает на 20%, с соответствующим уменьшением выживаемости.
Второй фактор возникновения злокачественных опухолей – гормоны. Даже во время менопаузы половые гормоны вырабатываются, но не привычным, как в молодом возрасте, путем, образуясь в яичниках, – они продуцируются внегонадно. То есть, гормоны бесконтрольно начинают образовываться в коже, печени, мышцах и в жировой ткани. Таким образом, чем больше масса тела, тем больше внегонадных эстрогенов и прогестерона, и именно эти половые гормоны как прямо, так и косвенно стимулируют образование злокачественных опухолей в грудной железе.
— Какой избыток массы тела уже опасен после 60 лет и может, на фоне перевыработки гормонов, спровоцировать рак груди?
— Действительно, поддержание оптимальной массы тела является первичной и действенной профилактикой заболевания раком молочной железы. Свою идеальную массу тела можно вычислить с помощью несложной формулы – так называемого индекса массы тела. Для этого следует разделить массу тела (в килограммах) на рост (в метрах), возведенный в квадрат. Величина, полученная после деления, равна индексу массы тела и показывает, есть ли лишние килограммы.
Например, возьмем средний рост женщины – 1,72 м, массу тела – 65,3 кг. Согласно формуле расчета: 1,72 х 1,72 = 2,9584; 65,3 : 2,9584 = = 22,07. Это нормальный индекс массы тела. Он колеблется от 19 до 24. Если индекс превышает 25 – это уже избыточная масса. Свои индивидуальные расчеты человек легко может сделать и на специальных сайтах в Интернете с помощью автоматических калькуляторов массы тела.
Действительно важно сделать такой тест, и в зависимости от его результатов сбалансировать вес. Ведь даже при увеличении массы тела на 10%, не говоря уже об ожирении 1-й, 2-й или 3-й степени, наблюдается рост числа случаев заболевания раком молочной железы и летальных исходов.
— Какой диеты и образа жизни следует придерживаться, чтобы сбалансировать массу тела и провести профилактику заболевания рака молочной железы, особенно в преклонном возрасте? Могут ли резкие изменения массы тела спровоцировать возникновение рака?
— За массой тела необходимо следить, ведь резкая потеря или наращивание килограммов сказывается и на гормональном балансе. Поэтому желательно придерживаться правильного питания, богатого витаминами и клетчаткой, и делать оздоровительные упражнения, и благодаря этому нормализовать свои показатели массы тела и поддерживать здоровье.
Сейчас этому аспекту в мировой медицинской общественности уделяется значительное внимание. Специалисты авторитетного агентства Food and Drug Administration, подведомственного Министерству здравоохранения и социальных служб США, в одном из последних исследований прослеживали взаимосвязь между наиболее употребляемыми продуктами питания и сроком жизни с раком молочной железы. В течение 20 лет они наблюдали за почти 40 тысячами пациенток и определили, что диета с уменьшением жиров и углеводов увеличивает на 15% показатель выживаемости. Таким образом, благодаря сбалансированному питанию и контролю массы тела, женщины держали под контролем и производство гормонов, и увеличивали продолжительность жизни.
— Помимо внутренней выработки, гормоны могут поступать в организм женщины и с продуктами питания. Какой пищи следует избегать в рационе, чтобы не допустить гормонального перенасыщения?
— Крупных фундаментальных научных исследований на эту тему нет. Но наблюдения показывают: если в рационе человека есть значительное количество модифицированных продуктов, при производстве которых применяются новейшие методики увеличения массы и урожайности, это значительно повышает поступление в организм половых гормонов. Поэтому лучше промышленно выращенное мясо не употреблять.
Еще один фактор может вызывать относительное увеличение гормонов – нарушение работы пищеварительного тракта. В частности, из-за заболевания печени гормоны не выводятся быстро из организма, а трансформируются в клетках печени в неактивные формы и дольше циркулируют в организме, оказывая более длительное действие.
Поэтому людям с заболеваниями органов пищеварения, чтобы нормализовать свой гормональный фон, необходимо пройти курс лечения. А также придерживаться так называемой «печеночной диеты» (стол № 5), где ограничено потребление жареного, копченого, соленого, острого, кофе, шоколада, какао.
Очень советую всем женщинам увеличить в рационе количество морских продуктов. Дело в том, что микродозы йода уменьшают чувствительность клеток молочной железы к половым гормонам.
Дополнительным источником поступления эстрогенов является пиво. Больше всего фитоэстрогенов содержится в темных сортах. Наглядно увидеть, что пиво – очень богатый гормонами напиток, можно по фигурам мужчин – пивных алкоголиков. У них растут грудь и живот по женскому типу. Поэтому с употреблением пива следует быть осмотрительными.
— Какую нужно проводить самодиагностику и обследование молочной железы, и есть ли здесь определенные особенности в пожилом возрасте?
— Женщинам, пребывающим в менопаузе, раз в 2 года стоит делать маммографические обследования. А также следует выбрать один из дней месяца, например, первое число, и в это время ежемесячно осматривать грудную железу. Две трети больных раком груди именно так, путем нажатий на грудь и осмотра, обнаружили уплотнение, асимметрию, деформацию молочной железы, фиксировали выделения из соска. Это дает возможность своевременно выявить признаки неблагополучия и обратиться к врачу-маммологу, не запуская болезнь.
Интервью вела Валентина Берник.
источник
Это статья открытого доступа, распространяемая в соответствии с лицензией Creative Commons Attribution License (), которая допускает неограниченное использование, распространение и воспроизведение на любом носителе при условии, что оригинальная работа была правильно указана.
Экономически эффективное лечение рака в развивающихся странах остается сложным. В пожилых людях с возможной ограниченной продолжительностью жизни следует тщательно учитывать расходы на здравоохранение, связанные со стандартными режимами лечения. Мы представляем результаты консервативного лечения рака молочной железы у пожилых людей в среде с ограниченными ресурсами.
Пациенты в возрасте 70 лет и старше с ранним раком молочной железы лечились опухолевым иссечением или простой мастэктомией и адъювантом тамоксифена. Были отобраны записи пациентов, представляющих Группу груди в период с января 1990 года по декабрь 2004 года, и были проанализированы демографические, клинические, патологические и онкологические данные. Статистика выживания рассчитывалась с использованием метода таблицы жизни.
Было выявлено 483 пациента старше 70 лет. В соответствии с консервативным протоколом управлялось сто восемьдесят восемь пациентов. Сорок один имел простую мастэктомию и 147 удаление опухоли. Их средний возраст составлял 77,3 года. Среднее последующее наблюдение составляет 62 месяца. Тридцать один пациент (16,4%) не соответствовал применению тамоксифена. Стадия TNM составляла 0 у 4 пациентов, у 42 — у II, у 116 — у 116, у III — у 26 пациентов. Не было 30-дневной смертности. Кумулятивная частота локального рецидива составила 3,3% через 5 и 10 лет. Кумулятивная частота регионального рецидива составила 3,3% через 5 лет и 4,5% в 10 лет. Кумулятивная частота отдаленного рецидива составляла 6,2% через 5 лет и 12,2% через 10 лет. Совокупная общая, заболеваемость и безрецидивная выживаемость в течение 10 лет составляли 59%, 88% и 81% соответственно.
Ограниченная хирургия и тамоксифен обеспечивают превосходный контроль над раком молочной железы у пожилых людей в среде с ограниченными ресурсами. Лучевая терапия и подмышечная диссекция и могут быть безопасно опущены, что снижает использование ресурсов здравоохранения.
Лечение рака молочной железы у пожилых людей противоречиво [1-6]. Ожидаемая продолжительность жизни пожилых пациентов в развивающихся странах может быть меньше, чем в развитых странах [7], и следует тщательно рассмотреть расходы на здравоохранение, связанные со стандартными режимами лечения.
Некоторые авторы из развитых стран рекомендуют менее агрессивные варианты у пожилых людей [2,8,9], тогда как другие выступают за стандартное лечение для всех пациентов независимо от возраста [3,5,9].
С возрастом заболеваемость хорошо дифференцированными видами рака и особыми гистопатологическими подтипами, связанными с благоприятным прогнозом, увеличивается [8]. Потенциал локального рецидива уменьшается с возрастом [10-12].
Из-за этих факторов и повышенной смертности от сопутствующих заболеваний может быть возможным избежать заболеваемости, связанной с подмышечной диссекцией и лучевой терапией у пожилых людей, не увеличивая риск локального и регионального рецидива и выживания [10,12-16].
Мы представляем здесь обновление предварительной проверки консервативного лечения рака молочной железы у пожилых людей в среде с ограниченными ресурсами [17] с упором на взаимосвязь патологических данных с формами локального и отдаленного отказа. Насколько нам известно, это единственные данные о результатах рака молочной железы в аналогичных обстоятельствах.
У пациентов в возрасте 70 лет и старше было выполнено удаление опухоли или простая мастэктомия для небольших грудей и адъювантного тамоксифена для положительных опухолей рецептора эстрогена. Пациенты с положительными T3 и T4b рецепторами эстрогеновых расстройств рассматриваются для неоадъювантного тамоксифена в попытке уменьшить опухоль перед операцией. Ни лучевая терапия, ни подмышечная диссекция не предлагаются, даже у пациентов с N1-статусом.
Были проанализированы записи 483 женщин в возрасте 70 лет и старше на момент постановки диагноза, которые были представлены Группе груди в период с января 1990 года по декабрь 2004 года. Записи пациентов, которые лечились с ограниченной хирургией и тамоксифеном, были проанализированы для переменных, суммированных в таблице 1. Данные были собраны из предполагаемой базы данных рака молочной железы.
Клиническая постановка проводилась в соответствии с шестой редакцией Международного классификационного совета Союза по борьбе с раком / Американского совместного комитета по раку TNM [18]. Резекция всей валовой опухоли проводилась у всех пациентов. Опухоли были проанализированы на патологические переменные, приведенные в таблице 1. Из-за ограничений на ресурсы, гормональный рецептор и статус c-erb B2 не были определены в нашем учреждении до марта 2004 года. Следовательно, эти переменные известны только у нескольких пожилых пациентов с ранней грудью рак.
Наблюдение за телефоном проводилось для всех пациентов, которых не видели в больнице в течение предыдущих 6 месяцев. Умершие пациенты классифицировались как умершие от болезни или умершие от других причин, основанные на информации от врача первичной медико-санитарной помощи, опекунов или членов семьи. Статистика выживания рассчитывалась с использованием метода таблицы жизни [19].
Из 3681 пациента с диагнозом рака молочной железы в больнице Тигерберга 483 пациентам было старше 70 лет. Двести тридцать три опухоли (48%) считались слишком продвинутыми для протокола. Из них восемь имели стадию IIA-заболевания, 20 имели стадийное заболевание IIB, а 22 имели стадию IIIA-заболевания, 75 имели стадию IIIB-заболевания, а 108 пациентов были представлены со стадией IV заболевания. Из 125 пациентов со стадией II и III заболевания 85 были исключены из-за громоздкой подмышечной болезни, требующей полного подмышечного вскрытия и 40 из-за передового характера их повреждений молочной железы, требующих лучевой терапии для местного контроля. Тридцать пять пациентов (7,2%) считались слишком хрупкими для любой операции. В девяти (1,9%) пациентах были выбраны другие варианты лечения: у одного пациента были осязаемые подмышечные узлы и получил полный подмышечный клиренс, поскольку из-за крайне плохих социально-экономических условий соблюдение регулярного режима наблюдения было невозможным. Четыре пациента были частично обработаны в другом месте до направления в наш центр. У одного пациента было послеоперационное излучение для многоцентровой опухоли. Один пациент просил модифицированную радикальную мастэктомию. У двух пациентов были плоскоклеточные карциномы и они были исключены из исследования. У четырнадцати пациентов была либо послеоперационная лучевая терапия (2 пациента), либо модифицированная радикальная мастэктомия в рамках международных многоцентровых испытаний. Четыре пациента отказались от операции. Сто восемьдесят восемь пациентов лечились согласно протоколу. Сорок один имел простую мастэктомию (SM) и 147 опухолевые выделения (TE).
Возраст варьировался от 70 до 95 лет. Средний возраст составил 77,3 года. Сопутствующие сопутствующие заболевания были распространены со средним уровнем заболеваемости 1,4 пациента на одного пациента. Таблица 2 и 3 отражают эти сопутствующие заболевания.
Число пациентов с сопутствующими заболеваниями
Количество сопутствующих заболеваний на одного пациента
Клиническая TNM-классификация опухолей отражена в Таблицах 4 и 5.
Двадцать один пациент (14%), получавший терапию ТЭ и десять пациентов (24%), получавших SM, имели небольшие подвижные узлы.
Типы опухолей Всемирной организации здравоохранения отражены в таблице 6 [20]. У всех пациентов была достигнута полная маржа без опухолей. У 126 пациентов гистопатологические поля были более 3 мм. У 38 пациентов маржи составляли менее 3 мм, а у 24 пациентов показатели резекции были связаны с опухолью при микроскопическом исследовании; дальнейшие резекции не проводились для достижения свободных от опухоли полей. Средний размер опухоли у пациентов с ТЕ был 22,2 мм (диапазон: 570 мм) и 47,25 мм для тех, у кого была простая мастэктомия (диапазон: 10-150 мм).
Тип опухоли Всемирной организации здравоохранения [20]
Сто опухолей (53%) не было на месте. Тридцать четыре опухоли имели обширную карциному протоков in situ, 24 в группе TE и десять в группе SM. Лимфососудистая инфильтрация была обнаружена у 16 (9%) опухолей. Не было 30-дневной смертности.
Среднее наблюдение за всей группой составляет 62 месяца (от 4 до 166 месяцев). Пять из них живут с признаками заболевания на 43, 62, 75, 95 и 128 месяцев соответственно. Двадцать пациентов умерли от рака молочной железы, 93 живы без признаков заболевания, а 53 умерли от других заболеваний. Из 188 пациентов 17 были потеряны для наблюдения. Тридцать один пациент (16,4%) не соответствовал применению тамоксифена.
Ни у одного из пациентов, у которых были СМ и 6 пациентов с ТЭ, не было местного повторения. У четырех из этих пациентов болезнь контролировалась с последующим местным иссечением через 7, 23, 27 и 50 месяцев после первоначального лечения. Двое из этих пациентов умерли от интеркуррентных заболеваний. Они были без болезней во время смерти. Остальные два пациента живы и здоровы без признаков заболевания через 55 и 62 месяца после первоначального лечения. Местное рецидивирование одного пациента контролировалось лучевой терапией через 8 месяцев после первоначального лечения. Пациент жив без признаков заболевания через 43 месяца. У одного пациента были параллельные региональные метастазы, и он был обработан мастэктомией с подмышечной вскрытием через 55 месяцев. Этот пациент продолжал развивать отдаленные метастазы через 86 месяцев и умер от рака молочной железы через 166 месяцев.
Все 6 пациентов имели инфильтрацию проточной карциномы. У 3 пациентов показатели резекции были четкими. В 2 они были маргинальными, и в 1 были задействованы поля. Пациент с вовлеченной маржой развил рецидив через 8 месяцев после начальной операции и обсуждается выше. Ни у одного из пациентов с локальным рецидивом опухоли имели обширный компонент in situ.
Пациент, который также развивал региональные и отдаленные метастазы, имел проникающую проточную карциному 2-го уровня с лимфоваскулярной инфильтрацией. Ни у кого из пациентов с локальным рецидивом не было опухолей с инфильтрацией лимфомы. Средний размер опухоли 6 опухолей составлял 14,8 мм (диапазон 10 мм-20 мм)
Ни один из пациентов, которые не соответствовали применению тамоксифена, развивал локальный рецидив.
Кумулятивная частота локального рецидива составляет 3,3% через 5 и 10 лет. Локальная скорость управления отражена на рисунке 1.
Локальная скорость управления.
Региональный рецидив развился у одного пациента, у которого был СМ через 47 месяцев. Ее рецидив контролировался подмышечным вскрытием. Она разработала отдаленные метастазы и умерла через 67 месяцев после первоначального диагноза рака молочной железы. Восемь пациентов, у которых было иссечение опухоли, развивали региональный рецидив в 4, 19, 23, 35, 45, 55, 64 и 112 месяцах соответственно. У 6 пациентов рецидив контролировался подмышечным расслоением. Два из этих пациентов продолжали развивать отдаленные метастазы. У одного был региональный рецидив через 35 месяцев и отдаленные метастазы через 96 месяцев и вскоре он умер. Другой пациент уже обсуждался. Один пациент отказался от подмышечной диссекции, когда у нее появился региональный рецидив через 23 месяца. Она умерла от интеркурентной болезни через 75 месяцев. Один пациент считался слишком хрупким для любого вмешательства, когда у нее развился региональный рецидив в 112 месяцев и умер от интеркурентной болезни через 7 месяцев. Остальные 4 живы без признаков болезни. Кумулятивная частота регионального рецидива составляет 3,3% через 5 лет и 4,5% в 10 лет. Региональный контрольный показатель отражен на рисунке 2. Ни один из пациентов с пальпируемыми узлами на момент постановки диагноза не нуждался в подмышечной диссекции для регионального контроля в ходе их наблюдения. У двух пациентов, у которых была ТЕ и была локальная рецидива, не соблюдалось использование тамоксифена.
Дистальные метастазы развились у 16 пациентов с ТЭ (10,8%) и у 5 пациентов с СМ (12,2%), то есть в 21 группе. Один пациент развил метастазы в кости через 83 месяца и все еще жив с болезнью через 95 месяцев после первоначального диагноза; 20 умерли от метастатического рака молочной железы. Кумулятивная частота отдаленного рецидива составляет 6,2% через 5 лет и 12,2% в 10 лет. Дальнейшая скорость управления отражена на рисунке 3.
Из пациентов, у которых развился отдаленный рецидив, 15 имели инфильтрацию протоковой карциномы, у трех были папиллярная карцинома, у двух — муцинозная карцинома, у одного — пролекарственная дольковая карцинома. У пациентов с инфильтрацией протоковой карциномы три были опухолями 1-го класса, десять имели опухоли 2-го класса, а у двух были опухоли 3-го класса. Один пациент, у которого развился отдаленный рецидив, не соответствовал применению тамоксифена.
Кумулятивная общая выживаемость, выживаемость, связанная с конкретными заболеваниями и безрецидивная выживаемость, отражены на рисунках 4-6.
В развитых странах более трети всех случаев рака молочной железы приходится на женщин старше 70 лет [1,2,4]. В докладе из Южной Африки очевидно, что заболевание наблюдается в более раннем возрасте у негров (в среднем 49 лет) и цветных (в среднем 53 года), чем у белых (в среднем 60 лет). В этой серии 15% цветных пациентов, 5% пациентов с черным и 30% белых пациентов старше 70 лет на презентации [21]. Население, которое мы обслуживаем, преимущественно окрашено.
Рак молочной железы у пожилых людей является более ленивым заболеванием, чем у молодых женщин [1,4,16]. В анализе гистопатологических данных в 1869 году после менопаузальных женщин с раком молочной железы в развитой стране Фишер и др. Продемонстрировали более благоприятные признаки с возрастом. Эти особенности включают менее сосудистую инвазию и лимфоплазматическую стромальную реакцию. У пожилой женщины также есть более высокая частота положительных опухолей с рецепторами гормонов (85% положительных рецепторов эстрогена против 67% у более молодых пациентов). Пятьдесят восемь процентов (по сравнению с 50%) были диагностированы с отрицательной болезнью узла, хотя 20% имели опухоли> 5 см (против 13% из тех, кто моложе 65). Частота опухолей 3-го класса также уменьшалась с возрастом [8]. Эти результаты сопоставимы с низкими показателями распространенности лимфоваскулярной инвазии (9%) и 3-го класса (9%) в нашей серии. В серии из 572 образцов мастэктомии женщин всех возрастов из Пакистана аналогичные патологические особенности были обнаружены, как в западной серии неэкранированных популяций [22].
Потенциал локального рецидива уменьшается с возрастом [10-12], эффект усиливается тамоксифеном [23]. Добавление облучения к частичной мастэктомии у более молодых пациентов снижает частоту ипсилатерального рецидива, не влияя на выживание [24-27].
В большой итальянской серии, оценивающей сохранение груди у женщин всех возрастов, лучевая терапия не улучшала местные контрольные показатели у пациентов старше 65 лет [12]. Результаты трех исследований, оценивающих роль лучевой терапии при раннем раке молочной железы у пожилых людей, приведены в таблице 7. Эти результаты сопоставимы с нашими данными.
Частота рецидивов и выживаемости с упущением лучевой терапии.
L + T: Lumpectomy и Tamoxifen. L + T + R: лумпэктомия, тамоксифен и полное облучение груди
Q: Четырехэктомия. A: подмышечный клиренс R: полное облучение груди C; CMF. Т: Тамоксифен
Даже в развитых странах пожилые женщины часто не получают лучевую терапию: у женщин старше 60 лет, которые лечились от рака молочной железы стадии I или II с сегментарной мастэктомией, только 39,2% были направлены на послеоперационную лучевую терапию, тогда как 82% подобных пациентов менее 60 лет были упоминается. У пожилых пациентов, получивших лучевую терапию, осложнения были минимальными. Значительная польза от облучения в достижении местного и регионального контроля. Данные даже предположили, что послеоперационное облучение может быть более полезным при распространении на пожилых пациентов после сегментарной мастэктомии, чем среди молодых женщин. Эти результаты контрастируют с большинством других серий, оценивающих лучевую терапию у пожилых людей, и эти различия трудно объяснить. Однако не проводился анализ факторов, отличных от возраста (т. Е. Сопутствующих заболеваний, статуса рецепторов и использования тамоксифена) в качестве причин для направления на лучевую терапию. Значительное число пациентов, не предназначенных для лучевой терапии, также имели опухоли с неизвестным статусом кратности резекции [9].
У наших пациентов кумулятивная частота локального рецидива составляет 3,3% через 5 и 10 лет. Он сравнивает благоприятные данные о местных показателях рецидива у более молодых пациентов, получающих излучение после удаления опухоли [27-32]. Это демонстрирует ценность выбора подходящего пациента. Резекция инфильтрированных подмышечных узлов не влияет на выживаемость, но обеспечивает прогностическую информацию для планирования послеоперационной терапии. Еще одна роль для подмышечной диссекции — это региональный контроль [13,14,27,33,34].
Martelli et al., [13] сообщили о 321 пожилых пациентах с оперативным раком молочной железы и клинически не пальпируемых подмышечных узлах, рандомизированных для хирургического вмешательства (S + AD) или без подмышечной вскрытии (S). Все пациенты получали тамоксифен. Не было выявлено существенных различий в общей смертности от рака молочной железы или кумулятивной заболеваемости грудных детей между этими двумя группами. Авторы пришли к выводу, что пожилые пациенты с небольшими опухолями без клинической подмышечной активности могут быть удовлетворительно обработаны консервативной хирургией и тамоксифеном.
У 20% пациентов, у которых была подмышечная диссекция, была метастатическая инфильтрация узлом. Тем не менее, только 1,8% пациентов, у которых было иссечение опухоли, потребовали отсроченной подмышечной диссекции для клинически открытого подмышечного заболевания. Эти данные свидетельствуют о том, что подавляющее большинство микроскопических подмышечных узловых метастазов клинически не имеет значения.
У наших пациентов прогностическая информация, полученная подмышечным вскрытием, не изменила бы управление. Из-за ограничений ресурсов до марта 2004 года пациенты получали тамоксифен независимо от статуса рецептора гормонов и не предлагали химиотерапии. В нашей серии 16,4% пациентов имели осязаемые подмышечные узлы. Разумеется, узлы были микроскопически задействованы во многих других случаях. Однако кумулятивная частота регионального рецидива сравнима с наблюдаемой Martelli et al., [13], упомянутой выше. Тот факт, что ни один из пациентов с ощутимыми узлами не нуждался в подмышечной диссекции для регионального контроля, также подтверждает эффективность тамоксифена в контроле над этими узлами.
Адъювантная терапия тамоксифеном существенно улучшает выживаемость женщин с положительными опухолями рецептора эстрогена [35]. Тамоксифен значительно снизил скорость отказа лечения на локальных и отдаленных участках, второй рак молочной железы и частоту рецидива опухоли после лумпэктомии и облучения молочной железы [36,37]. Тамоксифен также оценивался как единственное лечение рака молочной железы у пожилых людей, и более ранние исследования показали, что только тамоксифен является достаточным лечением [38-40]. Однако недавний метаанализ показывает, что выживаемость рака молочной железы и выживаемость без прогрессирования хуже у женщин, получавших только тамоксифен [41-45]. Мы поддерживаем идею о том, что тамоксифен сам по себе является неадекватной терапией, которую следует зарезервировать для очень слабых пациентов.
Соответствие применению тамоксифена не оценивалось ни в одной из вышеупомянутых серий. Одной из причин низкой скорости лечения в целом у наших пациентов может быть использование адъювантного тамоксифена и высокий уровень долгосрочного соблюдения его применения.
Использование тамоксифена у пациентов с неизвестными или отрицательными рецепторами гормонов является спорным, поскольку оно может подвергать пациентов побочным эффектам препарата без какой-либо клинической пользы [35]. Вероятность появления опухолей у пожилых людей, являющихся положительными на рецепторы эстрогена, составила 85% [8]. Стоимость определения гормональных рецепторов в нашем учреждении примерно в десять раз превышает стоимость тамоксифена на один месяц. Поэтому можно утверждать, что нецелесообразно определять статус рецептора с учетом выделения 15% пациентов, которые не получат тамоксифена. Несмотря на свои неблагоприятные последствия, тамоксифен хорошо переносится у пожилых людей и может оказать благоприятное влияние на уровень липидов в крови и минеральную плотность костей [4,8,42-44,46,47].
К 2010 году большинство из примерно 1,5 миллионов ежегодных новых случаев рака молочной железы будут диагностированы у женщин в странах с ограниченными ресурсами [48]. Проблемы лечения этих пациентов несколько.
Адъювантная системная и лучевая терапия становятся все более дорогостоящими, и необходимо тщательное рассмотрение экономической эффективности.
Дальнейшая продолжительность жизни южноафриканских женщин в возрасте от 70 до 74 лет составляет 10,4 года, женщин — от 75 до 79 лет — 8 лет, а для 80-48 лет — 5,9 года против США — 14,8 года, 11,2 года и 8,5 лет соответственно [7 ]. Это показывает, что даже в развивающейся стране у пожилых женщин может быть значительная дальнейшая продолжительность жизни, и следует тщательно рассмотреть варианты лечения, чтобы не ставить под угрозу локальный или дистанционный контроль заболеваний.
По сравнению с лечением раннего рака молочной железы лечение прогрессирующего рака молочной железы является более ресурсоемким и имеет более низкие результаты. Это подчеркивает потенциальную выгоду раннего обнаружения и диагностики, особенно в странах с ограниченными ресурсами [49].
В исследовании, посвященном изучению рака молочной железы и шейки матки среди южноафриканских женщин, почти пятая часть женщин не слышала об этих раках, и почти половина не знали о методе самоанализа груди. Более низкие уровни осведомленности были также обнаружены у женщин старшего возраста и сельских районов [50]. В нашем исследовании 48,2% пациентов представили слишком развитую болезнь для консервативного лечения, продемонстрировав необходимость раннего выявления рака молочной железы в развивающихся странах.
В стране с ограниченными ресурсами ограниченная хирургия и тамоксифен обеспечивают превосходный контроль над раком молочной железы у пожилых людей, сравнимый с результатами, полученными в условиях ограниченного ресурса.
Автор (ы) заявляют, что у них нет конкурирующих интересов.
LJW собрал данные, выполнил статистический анализ и составил рукопись. JPA задумала исследование и участвовала в его разработке и координации. JDO собрал некоторые данные и выполнил некоторый статистический анализ. Все авторы прочитали и утвердили окончательную рукопись.
источник
При раннем выявлении рака молочной железы успешно проходят лечение в 98% случаев. Исследователи продолжают добиваться впечатляющих успехов в диагностике и лечении рака молочной железы.
Тем не менее, рак молочной железы у пожилых людей остается очень распространенным заболеванием, риски которого будут минимизированы только в том случае, если женщины будут следовать рекомендованному графику и проходить ежегодные маммограммы.
За последние тридцать лет количество новых случаев заболевания увеличивается с каждым годом, хотя смерть от рака молочной железы несколько снизилась. Рак молочной железы остается второй ведущей причиной раковой смерти после рака легких.
Как и все виды рака, рак молочной железы начинается с аномального роста клеток. Эти «плохие» клетки развиваются слишком быстро, распространяются или метастазируются по всей груди, часто входя в лимфатические узлы, расположенные под мышкой или даже движутся в другие части тела.
Существует несколько признаков потенциального рака молочной железы, включая кровопролитие или отвод соска; изменение размера или контура груди; сплющивание, покраснение или питтинг кожи над грудью. Наиболее распространенным признаком является опухоль на груди.
Если женщина обнаруживает отвердение кожи, она должна посетить врача.
Считается, что несколько основных факторов риска повышают вероятность рака молочной железы. Тем не менее, важно иметь в виду, что большинство людей с одним или несколькими из этих факторов риска не имеют рака молочной железы.
- Возраст
- Травма грудной клетки в детстве
- Начало менархе(первой менструации) до 12 лет
- Увеличение веса в подростковом возрасте
- Отсутствие беременности или поздняя беременность (после 30 лет)
- Длительное использование оральных контрацептивов
- Увеличение массы тела после менопаузы
- Поздняя менопауза (после 50 лет)
- Повышенная плотность ткани груди
Чрезмерное воздействие эстрогена, гормона, который способствует появлению женских вторичных половых признаков, является ведущим фактором в развитии рака молочной железы. Воздействие комбинации эстрогена и прогестерона в течение четырехлетнего периода также увеличивает риск развития рака молочной железы. Это особенно важно из-за тенденций в терапии лечения эстрогенами, чтобы предотвратить предменопаузальный синдром и другие болезни. Более недавнее сокращение заместительной гормональной терапии, возможно, привело к недавнему небольшому сокращению случаев рака молочной железы у женщин старше 50 лет.
Также важны вторичные факторы, такие как: курение, ожирение, алкоголь, диета и стресс. Как и при снижении риска всех видов рака, рекомендуется здоровый образ жизни, включая сбалансированное питание, частые физические нагрузки и умеренный стресс.
Генетика также может играть большую роль в развитии рака молочной железы. Несмотря на то, что менее 10% случаев рака молочной железы унаследованы, женщины с семейной историей заболевания имеют гораздо больший риск рака груди (и яичников).
Как только рак будет обнаружен, то врач определит его стадию и опубликует отчет о вашем заболевании. Этот подробный отчет должен включать все, начиная от мест и описаний каждого образца ткани до клинической истории пациента с заболеванием до современного времени.
Лечение рака молочной железы варьируется в зависимости от стадии рака, количества или диапазона злокачественных клеток. Режим лечения также будет зависеть от этого.
Четыре традиционных метода лечения включают:
- Хирургию
- Радиационную терапию
- Химиотерапию
- Гормональную терапию
Более 100 лет хирургия считалась основным методом лечения рака молочной железы. Только недавно этот подход изменился, так как появились новые методы первой ответной реакции, и врачи во многих случаях начали применять целевые стратегии лечения. Однако хирургическое вмешательство остается важным способом лечения.
Lumpectomyis — наименее инвазивная хирургическая процедура, так как удаляется только опухоль. Lumpectomies рекомендуются, когда нет признаков распространения рака на другие участки груди или тела. За этим обычно следуют пять-семь недель лучевой терапии в качестве меры предосторожности.
Существует три уровня мастэктомии или удаление груди. Общая мастэктомия приводит к полному удалению груди. Амодифицированная радикальная мастэктомия, наиболее распространенная хирургическая процедура, включает удаление груди и вспомогательных лимфатических узлов. Радикальная мастэктомия, длительная и стандартная процедура, которая требует удаления всей груди, подмышечных лимфатических узлов и грудной стенки под грудью. После операции врачи изучают образцы из каждой тканевой группы, для определения дальнейшего лечения, хотя лучевая терапия является обычной процедурой последующего наблюдения.
По данным Национального института рака, лучевая терапия, использование интенсивных световых лучей для уничтожения раковых клеток, имеет 50-70% шанс уменьшить рецидив. Но большинство пациентов осознают, что радиация убивает не только раковые клетки, но и здоровые клетки.
Химиотерапия, то есть использование препаратов, убивающих раковые клетки. Химиотерапия быстро атакует клетки, как раковые, так и здоровые клетки. Хотя последние разработки способствовали снижению печально известных побочных эффектов. Важно отметить, что каждый режим лечения химиотерапией уникален и зависит от многих факторов, включая историю болезни пациента и его наследственности, текущее состояние здоровья и множество других факторов.
Гормональная терапия, использование определенных гормонов, поражающих раковые клетки, представляет собой систематическое лечение, предназначенное для избавления всего организма от рака. Врачи используют специальные препараты, чтобы ингибировать эстроген или прогестерон от развития рака молочной железы или, в некоторых случаях, отключить производство гормонов яичников.
Гормональная терапия обычно используется, когда пациент является положительным гормональным рецептором. Его можно использовать для снижения риска возникновения рака у женщин с высоким риском рака, для снижения риска рецидива, для сокращения большой опухоли или для лечения распространенного заболевания.
Существует также недавно разработанная схема направленного лечения тиммун, которая имитирует естественные антитела, которые атакуют специфические характеристики раковой клетки. Целенаправленная терапия добавляется к химиотерапии, хотя исследователи также разрабатывают методы снижения интенсивности химиотерапии и даже потенциально исключают ее из режима лечения.
Постепенно учеными разрабатываются новые методы лечения рака, а также совершенствуются старые. Развивается комбинация высокодозной химиотерапии и замены разрушенных клеток трансплантацией стволовых клеток, хотя метод остается еще не доказанным. Также изучаются использование определенных ингибиторов киназы, которые блокируют сигналы, которые необходимы для роста опухоли.
Наш пансионат сможет обеспечить вам ежегодный осмотр, который поможет в диагностике ранних стадий заболеваний, в том числе, таких как рак молочной железы.
источник
Наибольшая заболеваемость раком молочной железы отмечается среди женщин 50 — 60 лет, причем 30 — 45% заболевших находятся в возрасте 60 лет и старше Рак молочной железы (РМЖ) занимает одно из первых мест в заболеваемости населения злокачественны
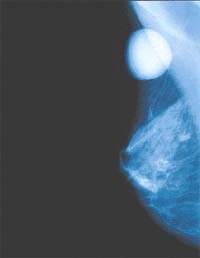 |
Наибольшая заболеваемость раком молочной железы отмечается среди женщин 50 — 60 лет, причем 30 — 45% заболевших находятся в возрасте 60 лет и старше
Рак молочной железы (РМЖ) занимает одно из первых мест в заболеваемости населения злокачественными опухолями. Пик этой патологии приходится на 50 —60 лет, но 30 — 45% пациенток, заболевших этой формой рака, находятся в возрасте 60 лет и старше. При определении тактики лечения заболевания приходится ориентироваться не только на достижение наилучших результатов выживания, но и на оценку риска применения того или иного метода лечения.
В зависимости от степени распространенности РМЖ проводят хирургическое, лучевое или химиотерапевтическое лечение, а также комбинации этих методов. В последнее время все больший удельный вес приобретает химиотерапия в качестве метода общего воздействия на организм. Рекомендации по лечению рака молочной железы у пожилых противоречивы — от максимально радикального подхода до сугубо сдержанного.
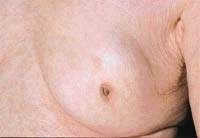 |
Статистические данные, приводимые многими авторами, свидетельствуют о том, что при отсутствии метастазов в регионарные лимфоузлы отдаленные результаты лечения не зависят от объема оперативного вмешательства. Анализ 5-летней выживаемости пожилых больных в зависимости от объема оперативного вмешательства показал, что после радикальных операций 5 лет жили 56%, после мастэктомии с подмышечной лимфаденэктомией — 46%, простой мастэктомии — 60%, а среди неоперированных больных данный показатель составил 45%.
Статистической разницы между этими показателями нет. При наличии метастазов (Т1 — 3 N1 М0 ) выживаемость после радикальной мастэктомии (по Patey или Halsted) составляет 56%, а среди неоперированных больных — 45%.
Все это заставляет врачей очень строго относиться к определению тактики лечения, в первую очередь хирургического.
На выбор предстоящего лечения влияет и отношение к нему больной. Пожилые пациентки, как правило, настороженно воспринимают возможность радикального хирургического вмешательства и часто от него воздерживаются, отдавая предпочтение органосохраняющим операциям в комбинации с лучевым и химиогормональным методами.
| При отсутствии метастазов в региональных лимфоузлах отдаленные результаты не зависят от объема оперативного вмешательства |
Задачей врача-онколога на догоспитальном этапе является возможно более раннее выявление опухолевой патологии с использованием доступных методов обследования — пальпаторного осмотра, маммографии, ультразвукового исследования. Правильно ориентировать больного в плане предстоящего лечения, рассказать о возможных осложнениях — это задача онкологов специализированных учреждений. Рекомендации должны быть основаны на объективной оценке риска операции и знании этих осложнений с учетом функциональных особенностей организма пациента.
В доступной нам литературе мы не нашли сообщений, касающихся хирургических осложнений у больных РМЖ пожилого возраста.
Нами было прослежено течение послеоперационного периода у 206 женщин, страдавших РМЖ, у 112 из которых была выполнена радикальная мастэктомия по Patey, а у 94 — по Halsted. Среди указанных больных 64 имели возраст старше 60 лет (табл. 1).
Как видно из табл. 1, на долю пожилых больных пришелся 31% от общего числа пациентов. Практически все они имели сопутствующую патологию, выраженность которой, однако, была не настолько велика, чтобы отказаться от операции. Среди сопутствующих заболеваний чаще всего отмечались: ИБС, гипертоническая болезнь, хронические воспалительные процессы в легких и бронхах.
Послеоперационный период считался осложненным, если наблюдались обильная лимфорея, некрозы кожи, нагноения раны, осложнения со стороны терапевтического статуса, потребовавшие лечения (табл. 2).
У больных старше 60 лет среднее значение послеоперационных койко-дней составило 21 день. Средние показатели лимфореи: незначительная —28%, умеренная — 26%, обильная — 45%. Некроз кожи у всей группы больных встретился в 24% наблюдений.
читель-
ная
нная
ная
читель-
ный
нный
ный
итель-
ное
нное
ное
Оценивая изложенные результаты, следует отметить тенденцию к увеличению лимфореи с возрастом. Если у больных 60—65 лет обильная лимфорея отмечена в 42% случаев, то у больных 66—70 лет — в 62%. У больных в возрасте 71—75 лет обильная лимфорея встретилась в 25% наблюдений, но частота умеренной лимфореи возросла до 42% (для сравнения: частота умеренной лимфореи в возрасте 60—65 лет составила 25%, в возрасте 66—70 лет — 18%). Некоторое снижение частоты появления обильной лимфореи в возрасте 71 — 75 лет можно объяснить тем фактом, что практически всем этим больным выполняли операцию по Patey, а не по Halsted. Из пяти больных старше 75 лет у троих наблюдалась обильная лимфорея.
Частота некрозов кожи также увеличивалась с возрастом: 9% у пациентов 60 — 65 лет, 37% в 66 — 70 лет и 25% в 71 — 75 лет. У двоих из больных старше 75 лет были некрозы кожи. В появлении этих осложнений, безусловно, большую роль играет степень поражения сосудов атеросклеротическим процессом и ангиопатия, связанная с сахарным диабетом. Квалификация хирурга, выполняющего операцию, также немаловажна. Для сравнения в табл. 3 приведены данные по таким же осложнениям у больных моложе 60 лет.
Среднее значение послеоперационных койко-дней у больных моложе 60 лет составило 15 дней.
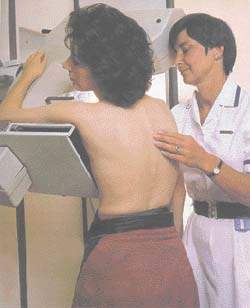 |
Сравнивая данные, приведенные в табл. 2 и 3, можно отметить следующее: пациенты старше 60 лет находились в стационаре после операции примерно на 6 дней больше, чем больные моложе 60 лет, что связано с более выраженной лимфореей. Некроз кожи также чаще встречался у больных старше 60 лет, по сравнению с более молодыми пациентами (24% и 5% соответственно). Частота возникновения инфекционных осложнений существенно не различалась, так как это осложнение скорее связано с соблюдением асептики и антисептики при выполнении операции и послеоперационных хирургических процедур. Это можно объяснить и частым назначением антибактериальных препаратов, препятствующих развитию нагноений. Отметим, что 17% пожилых пациентов страдали ожирением, а 7,8% сахарным диабетом. Практически у всех больных с данной патологией мы отмечали обильную лимфорею, некроз кожи, в отдаленном периоде — выраженный отек руки.
Учитывая большую частоту послеоперационных осложнений у больных старше 60 лет, требуется более дифференцированно подходить к отбору больных на операцию — с точки зрения не только хирурга, но и анестезиолога-реаниматолога. Все больные данной группы должны осматриваться анестезиологом на догоспитальном этапе, в поликлинике диспансера. При этом нужно оценивать функциональные возможности организма, назначать дополнительные консультации специалистов (эндокринолога, терапевта, невропатолога).
Мы считаем, что таким больным необходимо проводить более поверхностное обезболивание (отказаться от опиатов, снизить дозы нейролептиков). Учитывая возрастную чувствительность к наркотическим веществам и снижение обменных процессов в послеоперационном периоде, мы применяем с целью обезболивания ненаркотические анальгетики (трамал). Для профилактики тромбозов и пневмоний большое внимание уделяем ранней активизации больных (на фоне адекватной инфузионной терапии, включающей переливание свежезамороженной плазмы, альбумина, протеина). При травматичных операциях, сопровождающихся кровопотерей более 400 мл, проводим переливание эритроцитарной массы. Учитывая большую частоту возникновения кожных некрозов, используем в инфузионной терапии препараты, улучшающие микроциркуляцию (реополиглюкин, трентал).
Из 64 наблюдавшихся больных старше 60 лет в послеоперационном периоде только у 2 пациенток имели место нарушения сердечного ритма, потребовавшие медикаментозного лечения, а у 1 больной возникла тяжелая субэндокардиальная ишемия миокарда. Послеоперационных пневмоний, тромбоэмболий не отмечено. Таким образом, частота терапевтических осложнений составила 4,7%.
Проведенные нами исследования позволили сделать следующие выводы:
источник
Автореферат и диссертация по медицине (14.00.27) на тему: Особенности лечения рака молочной железы в пожилом и старческом возрасте
Автореферат диссертации по медицине на тему Особенности лечения рака молочной железы в пожилом и старческом возрасте
ПЫНЗАРЬ ВИТАЛИЙ АЛЕКСЕЕВИЧ
ОСОБЕННОСТИ ЛЕЧЕНИЯ РАКА МОЛОЧНОЙ ЖЕЛЕЗЫ В ПОЖИЛОМ И СТАРЧЕСКОМ ВОЗРАСТЕ
14.00.27 — Хирургия 14.00.14 — Онкология
диссертации на соискание ученой степени кандидата медицинских наук
Работа выполнена в Государственном Образовательном Учреждении Высшего Профессионального Образования «Московский Государственный медико-стоматологический Университет» Федерального агентства по здравоохранению и социальному развитию Российской Федерации и Государственном Учреждении «Российский Онкологический Научный Центр имени H.H. Блохина» Российской Академии Медицинских Наук.
доктор медицинских наук, профессор
Емельянов Сергей Иванович
доктор медицинских наук, профессор
Нечушки н Михаил Иванович
Доктор медицинских наук, профессор
Доктор медицинских наук, профессор
Ведущее учреждение: Институт хирургии им. A.B. Вишневского РАМН
Защита диссертации состоится «СЪюксах 2007 г. в » » часов на заседании диссертационного совета Д 212.203.09 при Российском Университете дружбы народов по адресу: 117198, г. Москва, ул. Миклухо-Маклая, д. 8.
С диссертацией можно ознакомиться в библиотеке Российского Государственного Университета дружбы народов (117198, ГСП, Москва, ул. Миклухо-Маклая, д. 6). Автореферат разослан « / / » ^¿-¿/¿¿¿^ 2007 г.
Учёный секретарь диссертационного совета, доктор медицинских наук, профессор
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Ежегодно в мире регистрируется 8 млн. новых случаев злокачественных новообразований и более 5,2 млн. смертей от них. В России в 2000 г. выявлено 448,6 тыс. больных с впервые в жизни установленным диагнозом злокачественного новообразования.
Продолжительность жизни во многих странах увеличивается, и вместе с этим возрастает заболеваемость злокачественными опухолями пожилых людей (согласно классификации, принятой европейским региональным бюро ВОЗ (Киев, 1963) возраст от 60 до 74 лет признан пожилым, от 75 до 89 -старческим, а 90 лет и более — возрастом долгожителей). За период с 1980 по 2000 год заболеваемость повысилась почти на 70%: с 22,6 до 38,3%0000.
В России заболеваемость в возрастных группах после 50 лет резко возросла. На конец 2004 г. на учёте состояло 408,4 тыс. больных РМЖ, из них 55,1% — в течение 5 лет и более (Давыдов М.И., Аксель Е.М., 2005).
Рак молочной железы в России занимает третье место среди всех причин смерти женского населения после болезней системы кровообращения и несчастных случаев во всех возрастных группах, составляя в среднем 2,1%, прогрессивно увеличиваясь с возрастом. Общее число умерших от РМЖ увеличилось с 12,5 тыс. (1983г.) до 22,7 тыс. (2003г.), т.е. прирост составил 10,2 тыс. (85%) (Давыдов М.И., Двойрин В.В., 2005).
Не смотря на очевидную актуальность проблемы, до последнего времени разработке рациональных методов лечения пожилых не уделялось достаточного внимания. Так, в международных научных исследованиях возраст 65-70 лет часто является критерием исключения. По существу, лишь недавно появились специальные научные программы по этой проблеме.
Как известно, онкологические заболевания у пожилых имеют некоторые особенности. Состояние здоровья таких пациентов существенно отличается от больных других возрастных групп, что обусловлено наличием сопутствующих заболеваний (Hillen H.F., Mäher ML, Dreyfus H., 2000).
Несомненно, имеются определенные успехи в комбинированном и комплексном лечении рака молочной железы связанные с внедрением в широкую медицинскую практику новых методов лучевой и лекарственной терапии, однако доминирующее значение продолжает занимать хирургическое вмешательство, которое до настоящего времени остается той основой, с учетом которой строится план всех лечебных мероприятий (Иванов В.М. 1993).
Хиругическое лечение всегда должно соответствовать сформулированному в 1960 г. А.И. Раковым принципу онкологического радикализма, который при раке молочной железы предусматривает удаление не только органа с первичной опухолью и окружающими тканями, но также широкое иссечение регионарных лимфатических узлов и клетчатки — первый этап регионарного метастазирования (Баженова А.П., 1983).
Эволюция хирургической тактики привела к постепенному отказу хирургов — онкологов от выполнения калечащих операции типа Урбана -Холдина и предпочтению органо- и функционально-сберегающих вмешательств в сочетании с химио- и лучевой терапией (Иванов В.М., 1993). Однако, постоянно появляющиеся сообщения о возникновении различных серьезных осложений после проведения дистанционной гамма-терапии со стороны органов, попадающих в зону облучения (Кудрявцев Д.В. 2001), ведет к постоянному поиску новых методик облучения и определению более узких показаний к проведению дистанционной лучевой терапии (ДЛТ) на зоны регионарного метастазирования при раке молочной железы, особенно у больных пожилого и старческого возраста.
Благодаря достижениям маммографического скрининга и успехам ранней диагностики рака молочной железы, стало возможно выполнение хирургических вмешательств меньшего объема, что имеет немаловажное значение при лечении рака у пожилых, позволяет добиться быстрой реабилитации оперированных пациентов и улучшить качество их жизни.
Изменение хирургической тактики в сторону органосохранных операций связано и с появлением биологической системной модели рака молочной железы В^зЬег, (1977) показавшей, что данное заболевание на этапе клинической манифестации является системным заболеванием, сопровождающимся скрытой диссеминацией опухолевых клеток. Эта гипотеза сделала необходимым смещение акцента при выборе тактики лечения в сторону системной терапии (Пак Д.Д., 2001).
В настоящее время существует ряд нерешенных проблем, связанных с оптимизацией дальнейшего лечения пожилых пациентов, перенесших органосохраняющие операции. Лучевая терапия несет определенный риск, учитывая наличие сопутствующей патологии. Лекарственная терапия может быть высокоэффективной, хотя ее применение так же проблематично в большинстве случаев, из-за повышенного риска токсичности препаратов. В пожилом возрасте становится значительнее роль гормонотерапии, что определяется более частым содержанием рецепторов эстрогенов и прогестерона в опухоли. При ранних стадиях рака молочной железы у женщин в возрасте старше 70 лет при ЭР+ и/или ПР+ лечение вообще может быть начато с применения тамоксифена (Тюляндин С.А., 2003).
По сути, нет четкого алгоритма лечебной тактики при раке молочной железы у пациентов старшего возраста. Как упоминалось ранее, в международных научных исследованиях возраст пациенток старше 65-70 лет обычно является критерием исключения.
Все вышеизложенное и побудило нас предпринять настоящее исследование особенностей лечения рака молочной железы у пациенток в возрасте 70 лет и старше.
Улучшить результаты лечения рака молочной железы у больных пожилого и старческого возраста за счет разработки алгоритма хирургического и комплексного лечения.
1. Сравнить результаты лечения больных раком молочной железы старше 70 лет при различных объемах оперативного вмешательства.
2. Определить эффективность послеоперационного лечения в данной возрастной группе с применением адъювантной терапии и без нее.
3. Выявить особенности влияния прогностических факторов на общую и безрецидивную выживаемость пациентов в данной возрастной группе.
4. Изучить по-стадийно трех- и пятилетнюю выживаемость больных раком молочной железы, вошедших в исследуемую группу.
5. Изучить причины смерти больных раком молочной железы пожилого и старческого возраста.
6. На основе полученных данных разработать объемы оперативного вмешательства и сформировать алгоритм послеоперационного лечения пациенток, в возрасте 70 лет и старше.
На собственном клиническом материале изучены результаты лечения пожилых больных раком молочной железы. Произведена сравнительная оценка результатов лечения в зависимости от объема оперативного вмешательства и разработан алгоритм комбинированного и комплексного лечения рака молочной железы в данной возрастной группе. Практическая ценность
Данное исследование позволяет применять рекомендации по выбору объема оперативного вмешательства и комплексному лечению больных раком молочной железы пожилого возраста; применению адъювантной эндокринотерапии, что приводит к оптимальной тактике лечения больных раком молочной железы пожилого и старческого возраста. Основные положения, выносимые на защиту
1. Оптимальным объёмом оперативного вмешательства при раке молочной железы в стадиях 1-И, является радикальная резекция, при стадиях Ш-1У — радикальная мастэктомия с сохранением грудных мышц.
2. Необходимость проведения дополнительного адъювантного лечения при ранних стадиях рака молочной железы.
3. При местно-распространённом раке лечение должно быть комплексным, но соответствовать общесоматическому статусу пациента.
4. При раке молочной железы у пожилых пациенток, факторами, обладающими высокой прогностической значимостью являются: возраст; критерии: Т, N. гормональный статус, центральная локализация опухоли.
5. Проведение открытой биопсии парастернальных лимфатических узлов является важным элементом операции, позволяющим правильно сталировать заболевание и назначать дополнительную терапию.
6. При наличии в опухоли положительных рецепторов стероидных гормонов, необходимо назначать гормонотерапию в адъювантном режиме.
7. Структура смертности больных раком молочной железы в пожилом и старческом возрасте различна в зависимости от стадии заболевания.
Апробация диссертации состоялась 3 ноября 2006 года на межкафедральной научной конференции с участием сотрудников кафедры общей хирургии, сотрудников Дорожной клинической больницы им. H.A. Семашко ОАО «РЖД», сотрудников отделения радиохирургии ГУ РОНЦ им. H.H. Блохина.
Публикации по теме диссертации
По теме диссертации опубликовано 11 научных работ.
Объем и структура диссертации
Материалы диссертации изложены на 125 страницах машинописного текста и включают введение, 4 главы, заключение, выводы, практические рекомендации и указатель литературы. Работа иллюстрирована 24 рисунками, 41 таблицей. Указатель литературы содержит 140 источников, из них 78 — отечественных и 62 — зарубежных.
В основу работы положен анализ лечения 272 больных раком молочной железы женщин в возрасте 70 лет и старше, оперированных и получавших дальнейшее лечение на клинических базах кафедры общей хирургии лечебного факультета МГМСУ и в отделении радиохирургии ГУ РОНЦ им. H.H. Блохина РАМН за период с 1998 по 2003 гг.
Математическая обработка материала произведена на персональном компьютере с использованием статистических программ STATISTICA 6.0, SPSS 13.0.
Распределение по возрасту показало, что заболевание наиболее часто встречается у лиц в возрасте 71-75 лет (54,4%), меньше было больных в возрасте 70 лет (14,7%) и 76 — 80 лет (25,7 %). В Возрасте 81 и старше, всего 5,1 % больных. Медиана возраста в группе исследования составила 74 года (интерквартильный размах 71-76 лет).
На основании данных амбулаторного обследования, изучения операционного материала и гистологических препаратов, были установлены следующие стадии онкологического заболевания, согласно Международной классификации опухолей (TNM, 2002г.): рак молочной железы I стадии установлен у 77 пациенток, что составило 28,3% от всей группы наблюдения. Рак молочной железы стадии IIA был выявлен у 104 (38,2%) пациенток, стадии IIb — у 25 (9,2%), IIIA стадии- у 24 (8,8%), ШЬ — у 18 (6,6%) и IIIC — у 17 пациенток (6,3%). Рак молочной железы IV стадии был установлен в 4 случаях, что составило 1,5% от всей исследованной группы, а 0 st — у 3 (1,1%). (табл. 1).
Выявление сопутствующих заболеваний, их числа и выраженности проводилось на основании анамнеза, жалоб больных, данных осмотра терапевта и инструментальных методов обследования. Важно отметить, что абсолютно все больные имели какую-либо сопутствующую патологию, а большинство 2 диагноза и более.
Большинство больных (185 — 68,0%) страдали заболеваниями сердечнососудистой системы, куда вошли ИБС, гипертоническая болезнь,
недостаточность кровообращения, перенесенные инсульты и инфаркты миокарда. У 65 (23,9%) наблюдалась патология эндокринной системы -тиреотоксический зоб, сахарный диабет, ожирение 3-4 ст. Заболевания дыхательной системы (бронхиальная астма, хронический бронхит) отмечены у 22 больных, что составило 8,1%.
У большинства пациенток размеры опухоли соответствовали критериям Т1-43,8% и Т2-44,9%. Наличие метастазов в регионарные лимфатические узлы выявлено в 106 (39,0%) случаях. В основном имелось единичное метастазирование в аксиллярные лимфатические узлы N1 — 57 (21,0%) наблюдений; а наличие метастазов в парастернальную зону в сочетании с аксиллярными метастазами выявлено у 9 (3,3%) пациенток. Не имели регионарных метастазов -166 (61,0%) больных.
Распределение больных раком молочной железы пожилого возраста по стадиям заболевания
Стадия Количество больных
НА ТШ1М0 тгшмо 28 76 10,3 27,9
ПЬ Т2И1М0 тзиомо 24 1 8,8 0,4
ША ТШ2аМ0 Т2К2аМ0 тзтмо ТЗЮаМО 10 12 1 1 3,7 4,4 0,4 0,4
ШЬ Т41Ч0М0 Т4ШМ0 Т4№аМ0 7 4 7 2,6 1.5 2.6
ШС ТШЗаМО ТШЗЪМО Т2ЮаМ0 Т2ШЬМ0 ТЗЫЗЬМО Т4ШаМ0 Т4ЫЗЬМ0 2 1 5 4 3 1 1 0,7 0,4 1,8 1,5 1,1 0,4 0,4
Отдалённое метастазирование, было выявлено у 4 (1,5%) больных. Из них у 3 — метастазы в кости, у 1 — в лёгкие.
Морфологические формы опухоли определены после операции при плановом гистологическом исследовании и представлены в основном инфильтративно-протоковым раком — 184 (67,6%) наблюдения.
Исследование рецепторного статуса опухоли показало, что опухоли по рецепторам эстрогена и/или прогестерона были рецептор-положительными в 133 (48,9%) случаях, а рецептор-отрицательными в 79 (29,0%). В 60 (22,1%) случаях рецепторный статус не определялся, в связи с техническими проблемами.
Количество выполненных радикальных резекций (132) и мастэктомий (140) было примерно одинаковое. При наличии ТЗ-4 выполнялись только мастэктомии, а при Т1-2 выполнялись как мастэктомии, так и радикальные резекции. Таким образом, одним из факторов, определяющих выбор объёма операции, явился размер первичного опухолевого узла, критерий Т.
Диагностика реального состояния парастернальной лимфатической цепочки на дооперационном периоде крайне затруднительна, в связи с ее расположением непосредственно за грудиной. Таким образом, показания к проведению лучевой терапии на парастернальную зону, в настоящее время, основываются на локализации и размере первичной опухоли и состоянии аксиллярного лимфатического коллектора. Само же проведение лучевой терапии может неблагоприятно сказаться на общем состоянии больных пожилого и старческого возраста, особенно при поражении левой молочной железы, когда в зону облучения попадает сердце.
В связи с этим, в случае выполнения радикальной резекции и локализации опухоли во внутренних квадрантах молочной железы, операция дополнялась открытой биопсией парастернальных лимфатических узлов на стороне поражения, и была выполнена у 17 больных. При мастэктомии, независимо от локализации первичной опухоли, данная манипуляция проводилась в 115 случаях. В 9 случаях подтверждено наличие MTS рака молочной железы в парастернальные лимфатические узлы. У этих больных была произведена коррекция стадии заболевания и только у них послеоперационная дистанционная лучевая терапия была дополнена полем на парастернальную зону. Остальным пациенткам, в послеоперационном периоде лучевая терапия на парастернальную зону не проводилась.
В послеоперационном периоде у пациенток имелось 20 (7,4%) осложнений различного характера и локализации. Со стороны п/о шва отмечено 12 воспалительных осложнений (по 6 после мастэктомии и резекции). К общим, не хирургическим осложнениям, мы отнесли возникшую у пациенток в послеоперационном периоде патологию: ЦНС (инсульт — 2), сердечно-сосудистой системы (инфаркт миокарда 2), лёгочной системы (пневмония) — 3 случая, лимфатический отёк верхней конечности — 1. Таким образом, по отношению к послеоперационным осложнениям, между группами больных по объёму оперативного вмешательства нет значимой разницы и выбор типа операции не может быть продиктован тем или иным возможным послеоперационным осложнением.
Лучевая терапия является важным компонентом лечения рака молочной железы. Проведённая операция в 72 (26,47%) случаях была дополнена ДЛТ. После радикальной резекции ДЛТ проводилась на оставшуюся часть молочной железы и регионарные зоны (при наличии метастазов опухоли в 4 и более лимфатических узлах) РОД 2-2,5 Гр. до СОД 50 Гр. В 7 случаях (после радикальной мастэктомии) только на аксиллярную зону (Ш-1У стадии). В 9 случаях на парастернальную зону до СОД 46 Гр. Учитывая возраст и наличие сопутствующей патологии, далеко не всем пациенткам, кому это было необходимо, было возможно провести курс послеоперационной ДЛТ. Поэтому распределение больных по признаку проведения послеоперационной лучевой терапии было особым. При выполнении радикальной мастэктомии и отсутствии регионарных метастазов (рЫО), ДЛТ у пациенток с наличием критерия рТ1-3 не проводилась (63 пациентки). В 4 случаях, при наличии критерия рТ4 — лучевая терапия проводилась на область послеоперационного рубца (табл. 2).
Распределение назначения ДЛТ в группах по типу операции
с наличием/отсутствием регионарных MTS
Критерий рт Тип операции Регионарные МТБ Лучевая терапия Итого
рТ1-2 радикальная резекция нет 57 (59,4%) 39 (40,6%) 96 (100%)
Итого 72 (54,5%) 60 (45,5%) 132(100%)
рТ1-2 мастэктомия нет 59(100%) 0 59(100%)
рТЗ-4 мастэктомия нет 4 (50,0%) 4 (50,0%) 8 (100%)
Всего 198(73,6%) 71 (26,4%) 269 (100%)
Адъювантное полихимиотерапевтическое лечение назначалось пациенткам при раке молочной железы в стадиях IIB, III, IV. Однако, при наличии выраженной сопутствующей патологии, а так же, достаточно частым отказом пациенток от данного вида лечения, плохой переносимостью химиотерапии, всего получили химиотерапевтическое лечение по схеме CAF (6 курсов) только 23 пациентки — 8.5%). При назначении химиотерапии, обращалось внимание на стадию, критерии Т и N.
Гормонотерапия тамоксифеном по 20 мг. в сутки проводилась всего 156 (57,4%) пациенткам (133 — с положительными рецепторами стероидных гормонов и 23 — с длительным анамнезом заболевания, после радикальной резекции и получавшим ДЛТ. Три пациентки, имевшие Ш-Г/ стадии основного заболевания, получали химиолучевое и гормональное лечение в адъювантном режиме после открытой биопсии опухоли для определения гормонального статуса.
При дальнейшем наблюдении за оперированными пациентками, было выявлено 10 (3,7%) локальных рецидивов основного заболевания. При сравнении групп при рТ1-2 по типу операции, выявляется, что разница между группами статистически не значима, р=1,0 и р=0,26 соответственно (использовался двухсторонний точный критерий Фишера). Имелось 4 рецидива после мастэктомии и 1 после радикальной резекции и ДЛТ. Таким образом, объём оперативного вмешательства не повлиял на частоту появления локального рецидива в группах пациенток при рТ1-2, где выполнялись и резекции и мастэктомии. В группах с критерием рТ 3 имелся 1 рецидив, с критерием рТ 4 имелось 4 рецидива, но по критерию объёма операции они статистически не сравнивались в связи с тем, что при данных показателях Т, выполнялись только мастэктомии.
Выполненные радикальные резекции (132 случая), при наличии показаний и возможности проведения, дополнялись послеоперационной ДЛТ (в 60 случаях). Разница между группами пациенток, которым проводилась или не проводилась ДЛТ по статусу локального рецидива отсутствует, р=1,0 (двухсторонний точный критерий Фишера). Вынужденный отказ от проведения ДЛТ после радикальных резекций в исследуемой нами группе пожилых пациенток в связи с соматическими противопоказаниями, не повлиял на частоту появления локальных рецидивов по сравнению с теми больными, которым в подобной ситуации ДЛТ проводили.
Важнейшим критерием, характеризующим правильность диагностики и лечения больного, является показатель выживаемости. В нашей работе приведены данные 3- и 5- летней выживаемости, для расчета показателей которой использован метод Каплан-Мейера (одномерный анализ). Анализировалась общая выживаемость (учитывающая смерть как от рака молочной железы, так и от другого заболевания) и безрецидивная выживаемость (учитывающая факт любого проявления прогрессирования рака молочной железы). При сравнении полученных показателей общей и безрецидивной выживаемости, выявлена необычная ситуация их взаимораспределения, когда показатели 3- и 5- летней безрецидивной выживаемости несколько выше, чем общей, что отличается от привычной картины распределения показателей этих видов выживаемости. Этот факт можно объяснить влиянием особенности рассматриваемых больных, а именно большой частотой смерти от других заболеваний, что связано с пожилым возрастом пациенток. Для объяснения особого распределения показателей выживаемости в исследуемой группе пожилых пациентов, проведён расчёт показателей болезньспецифической выживаемости
(выживаемости, учитывающей смертность только от рака молочной железы). Сравнивая показатели болезньспецифической и безрецидивной выживаемости, мы увидели привычную картину, когда болезньспецифическая выживаемость выше безрецидивной. Данное распределение показателей выживаемости подтверждает влияние большой частоты смерти от других заболеваний в данной группе больных на снижение показателей общей выживаемости по сравнению с безрецидивной.
Влияние прогностических факторов рака молочной железы на показатели выживаемости в исследуемой группе пациентов следующее: фактор возраста, критерии Т и N являются главенствующими, т.к. влияют на все виды выживаемости. Гормональный статус имеет статистически значимое влияние на безрецидивную и болезньспецифическую выживаемость. При расчёте общей выживаемости гормональный статус всё же оказывал своё влияние, но оно было статистически не значимо. Можно однозначно подтвердить вывод, что при наличии положительных рецепторов стероидных гормонов, выживаемость выше, чем при отрицательных.
Наличие сопутствующей патологии, как фактора прогноза, естественно, влияет на болезньспецифическую выживаемость. Однако, влияние данного фактора на другие виды выживаемости, по-видимому, нивелируется мощным влиянием фактора возраста в данной группе пациентов, который, наряду с другими особенностями пациентов, включает в себя и наличие сопутствующей патологии у пожилых. Степень злокачественности влияет на общую выживаемость у пациенток в нашей группе исследования. Влияние центральной локализации рака молочной железы на все виды выживаемости является важным фактором прогноза значительного ухудшения выживаемости в данной возрастной группе.
Полученные при одномерном анализе результаты были оценены посредством многофакторного анализа, т.е. изучено взаимное влияние прогностических факторов на выживаемость. При оценке показателей общей, безрецидивной и болезньспецифической выживаемости при мультифакторном анализе, выявляется, что при расчёте общей выживаемости, влияющими факторами прогноза были: возраст пациенток (р=0,048), критерии Т (р 0,2). Однако, отказ от проведения системной терапии при III стадии рака молочной железы, оказывает статистически значимое влияние (р=0,009) на общую выживаемость и приводит к значительному снижению её показателей. При отказе от системной терапии при III стадии, показатели 3- и 5- летней общей выживаемости составили 27,3±13,4 и 9,1±8,7 соответственно, по сравнению с показателями 3- и 5-летней общей выживаемости в группе больных, которым проводилась гормонотерапия 66,3±8,8 и 47,6±10,2 соответственно (табл 5, 6).
Безрецидивная выживаемость в зависимости от системной терапии.
Стадия Абс. число 3 летняя (ст. ошибка) 5 летняя (ст. ошибка) Р (log-rank)
1.нет терапии 30 96,6(3,4) 1 91,5(5,9) 0,39
2.гормонотерапия 47 97,4 (2,6) 1 97,4 (2,6)
1 .нет терапии 49 93,2 (3,8) 93,2 (3,8) 0,92(1-2)
2.гормонотерапия 74 92,5 (3,3) 92,5 (3,3) 0,51 (2-3)
З.химиотерапия 6 100 100 0,53 (1-3)
1.нет терапии 11 62,3 (15,0) 62,3 (15,0) 0,24(1-2)
2.гормонотерапия 32 68,8 (8,7) 68,8 (8,7) 0,67 (2-3)
З.химиотерапия 16 62,5 (14,5) 62,5 (14,5) 0,56(1-3)
Таблица 6 Общая выживаемость в зависимости от системной терапии.
Стадия Абс. число 3 летняя (ст. ошибка) 5 летняя (ст. ошибка) Р (log-rank)
1 .нет терапии 30 92,7 (5,0) 92,7 (5,0) 0,329
2.гормонотерапия 47 90,7 (4,5) 85,6 (6,5)
1.нет терапии 49 89,1 (4,6) | 61,5 (9,2) 0,79(1-2)
2.гормонотерапия 74 88,3 (3,9) 60,8 (8,2) 0,26 (2-3)
З.химиотерапия 6 100 100 0,20(1-3)
1.нет терапии 11 27,3 (13,4) 9,1 (8,7) 0,009(1-2)
2.гормонотерапия 32 66,3 (8,8) 47,6(10,2) 0,141 (2-3)
З.химиотерапия 16 43,8 (12,4) 26,3 (12,1) 0,298 (1-3)
Из 272 (100%) пациенток, 55 (20,2%) умерли от прогрессирования рака молочной железы, 27 (9,9%) — от других заболеваний (сопутствующей патологии), 190 (69,9%) пациенток на момент последнего наблюдения (начало 2006 года) были живы.
Анализируя данные по-стадийного распределения статуса больных и причин их смерти, выявлено, что среди больных, у которых опухолевый процесс на момент операции был в начальных стадиях, живых значительно больше — 168 (80,1%), чем погибших — 41 (19,9%). Причём отмечено, что смерть чаще наступала от сопутствующей патологии — в 23 случаях (11,2%), чем от рака — в 18 (8,7%). При рассмотрении группы пациенток с Ш-1У стадиями процесса, выявляется, что у них смерть наступает чаще — 41 (65%) случай, при 22 (34,9%) живых. Причём структура смертности такова: от рака умерло 37 (58,7%) больных, что почти в 10 раз чаще, чем от сопутствующей патологии — 4 (6,3%) и, в основном, в сроки до Зх лет наблюдения.
Учитывая полученные нами данные, мы можем рекомендовать следующий алгоритм лечения рака молочной железы у пациенток в пожилом и старческом возрасте: при наличии стадии 1-П, выполняется радикальная резекция молочной железы. Далее, при стадиях 1-Иа имеется возможность отказаться от проведения дополнительного лечения в адъювантном режиме, т.к. оно не оказывает статистически значимого улучшения показателей 3- и 5-летней выживаемости. При стадии Пб — послеоперационное дополнительное лечение сводится к применению гормонотерапии при наличии положительных рецепторов стероидных гормонов, а при их отсутствии, если возможно, необходимо проводить химиотерапевтическое лечение. При раке молочной железы III стадии, необходимо выполнение радикальной мастэктомии. В случае наличия тяжёлой сопутствующей патологии, когда риск объёмной операции высок, возможно выполнение радикальной резекции молочной железы с последующим облучением оставшейся части молочной железы и зон регионарного метастазирования в адъювантном режиме. При наличии положительных рецепторов стероидных гормонов, необходимо назначить гормонотерапию, при их отсутствии -химиотерапию. Лечение пациенток с IV стадией опухолевого поражения молочной железы, сводится к выполнению мастэктомии с последующим химиолучевым лечением. Гормонотерапия при наличии положительных рецепторов стероидных гормонов.
1. Ведущим методом лечения рака молочной железы в пожилом и старческом возрасте является хирургический метод. Оптимальным объёмом оперативного вмешательства является: при стадиях 1-П — радикальная резекция молочной железы, при стадиях Ш-1У — радикальная мастэктомия с сохранением грудных мышц.
2. При раке 1-Н стадии хирургический метод лечения обеспечивает стойкое пятилетнее выздоровление в 80,1% случаев. Проведение дополнительного адъювантного лечения не улучшает показатели выживаемости.
3. При местно-распространённом раке лечение должно быть комплексным и соответствовать общесоматическому статусу пациента. Риск адъювантного лечения не должен превышать возможный лечебный эффект.
4. Одномерный анализ позволил выделить факторы, обладающие высокой прогностической значимостью. При 3- и 5-летнем прогнозе это — возраст, критерии Т и И, гормональный статус, центральная локализация опухоли.
5. Многофакторный анализ позволил выделить факторы, обладающие высокой прогностической значимостью. При 3- и 5-летнем прогнозе это -критерии Т и N. гормональный статус.
6. Проведение открытой биопсии парастернальных лимфатических узлов на стороне поражения является важным элементом операции (в случае возможности выполнения), позволяющим правильно сталировать заболевание и назначать дополнительную терапию.
7. При наличии положительных стероидных рецепторов, необходимо назначать гормонотерапию в адъювантном режиме.
8. При 1-П стадиях процесса структура смертности такова: смерть чаще наступает от сопутствующей патологии (11,2%), чем от рака (8,7%). При III-IV стадиях от рака умирают 58,7% больных, что почти в 10 раз чаще, чем от сопутствующей патологии (6,3%) и, в основном, в сроки до Зх лет наблюдения.
Данные, полученные при выполнении работы, могут быть использованы специалистами при выборе объёма операции у пациенток пожилого возраста. Наш опыт проведения послеоперационного дополнительного лечения может явиться помощью для специалистов, которые проводят адъювантное лечение оперированных по поводу рака молочной железы пожилых пациенток. Дальнейшего углубленного изучения требует метод открытой биопсии парастернальных лимфатических узлов у пациенток пожилого и старческого возраста.
Список работ по теме диссертации.
1. Пынзарь В.А., Емельянов С.И., Нечушкин М.И., Уйманов В.А. Рак молочной железы у пожилых женщин. Современное состояние проблемы // Вестник РОНЦ им. H.H. Блохина РАМН, т. 17, №4, 2006. -С. 13-18.
2. Пынзарь В.А., Емельянов С.И., Нечушкин М.И., Уйманов В.А Отличительные особенности лечения рака молочной железы у пациенток пожилого и старческого возраста // Материалы конференции, посвященной 60-летию Национального Центра Онкологии. — Ереван. — 2006. — С. 167-168.
3. Пынзарь В.А., Емельянов С.И., Нечушкин М.И., Уйманов В.А Современное состояние проблемы рака молочной железы в пожилом возрасте // Иероглиф. — 2006. — Том 9, 31.- С.1272-1274
4. Стельмах O.K., Нечушкин М.И., Тюляндин С.А., Пынзарь В.А., Геворкян B.C. Адъювантное химиолучевое лечение больных раком молочной железы после органосохранных операций // Материалы Российской научно-практической конференции с международным участием «Новые технологии в онкологической практике». — Барнаул. -2005.-С. 105-106.
5. Пынзарь В.А., Емельянов С.И., Нечушкин М.И, Геворкян B.C. Рак молочной железы у женщин в возрасте старше 70 лет. Особенности лечения // Материалы Российской научно-практической конференции с международным участием «Новые технологии в онкологической практике». — Барнаул. — 2005. — С. 162-163.
6. Пынзарь В.А., Емельянов С.И., Нечушкин М.И. Особенности лечения рака молочной железы у женщин в возрасте старше 70 лет // Материалы Межрегиональной научно-практической конференции с международным участием, посвященной 110-летию со дня рождения проф. Ю.А. Ратнера «Лечение рака и предраковых заболеваний молочной железы». — Казань. — 2005. — С. 255-257.
7. Пынзарь В.А., Емельянов С.И., Нечушкин М.И. Особенности лечения рака молочной железы у пациенток пожилого возраста // Материалы III конгресса онкологов закавказских государств. Национальный Центр Онкологии им. В.А. Фанарджяна. — Армения. — 2004. — С. 200.
8. Пынзарь В.А., Емельянов С.И., Нечушкин М.И Лечение рака молочной железы у женщин, старше 70 лет // Материалы первой международной ежегодной онкологической конференции «Проблемы диагностики и лечения рака молочной железы». «Белые ночи Санкт-Петербурга». -С.Пб. — 2004.-С.133-134.
9. Пынзарь В.А. Лечение рака молочной железы у женщин старше 70 лет // Тез.докл. III конф. молодых учёных России с международным участием Научно-исследовательский центр ММА им. И.М. Сеченова. » Фундаментальные науки и прогресс клинической медицины». — М. -2004.-С. 217.
10. Пынзарь В.А., Нечушкин М.И., Уйманов В.А. Лечение операбельного рака молочной железы у пациенток, старше 70 лет // Тез. докл. 50-ой науч.-практич. Конф. Таджикского государственного медицинского университета имени Абуали ибни Сины с международным участием «Актуальные проблемы клинической онкологии». — Таджикистан. -2002,-С. 51-52.
11. Петровский A.B., Триголосов A.B., Нечушкин М.И., Пынзарь В.А. Роль открытой биопсии парастернальных лимфоузлов в стадировании рака молочной железы // Тез. докл. 50-ой науч.-практич. Конф. Таджикского государственного медицинского университета имени Абуали ибни Сины с международным участием «Актуальные проблемы клинической онкологии». — Таджикистан. — 2002.- С. 33-37.
Пынзарь Виталий Алексеевич (Россия) • Особенлофи-дачешш рак» молочной железы в ложилом и старческом
Рак молочной железы — одно из самых распространенных онкологических заболеваний у женщин. С учётом увеличивающейся продолжительности жизни, эта патология всё чаще встречается у пожилых пациенток. Течение онкологических заболеваний и их лечение у пожилых пациентов имеют некоторые особенности. В свете проблем пожилого возраста и наличия широкого спектра сопутствующей патологии, рассмотрены основные характеристики опухоли, а так же основные методы лечения рака молочной железы, такие как хирургическое вмешательство, послеоперационная лучевая терапия, адъювантная химиотерапия и гормонотерапия.
Pynzar Vitaly Alexeevich (Russia) The particulars treatment of breast cancer in elderly females.
Breast cancer is one of the commonest female malignancies. The disease occurrence in females of advanced age is increasing with the rise in life span. The course and treatment of malignancies in elderly patients have certain specific features. The dissertation considers principal characteristics of the tumor and main treatment approaches in breast cancer such as surgery, postoperative radiotherapy, adjuvant chemotherapy and hormonotherapy in light of specific problems of advanced age and the associated broad range of concurrent diseases.
Подписано в печать 1 ?. Q2.0 7 г. Формат 60×84/16. Тираж 100 экз. Заказ № 12.1
Отпечатано в службе множительной техники ГУ РОНЦ РАМН им. Н.Н. Блохина РАМН 115478, Москва, Каширское ш., 24
1 I Актуальность проблемы рака молочной железы у жешлнн в пожилом вотрэстс
J .2 Особенности он колотичеекнх заболеваний у пожилых IО
13 Общепринятая тактика лечения рака молочной железы 11 1 4 Виды оперативных вмешатышв при роке молочной железы, юс эволюция
1,5 Вехирурп1чсскис способы лечебного (ютдействиа
I 6 Выбор тзктн кн лечения у больных гюжилого шчрастп
Глава 2. Материалы и методы
2.1 Техника типичных оперативных вмешательств, выполняемых при роке молочной железы
2.2 Морфологическое изучение операционного материала
2.3 Характеристика исследуемой группы бальных
Глава 3. Аиалв* нровелённого лечение н ouiiciihui реп.зыя юв 50 Пива 4, Ад ыиваишое .течение пожилых больных, перенесши! оперативное вмгшательство
4,1. flocttecHipeaiiKOHiioe лечение больных, алгоритм лечении пожилых пациенток % включение
П рактн чески е ре ко ч енд а ни и
Ежегодно в мире регнсфнруется S млн, новых случае» злокачественных новообразований м более 5,2 млн. смертей or них. В России в 2000 г выявлено 448,6 тыс. больных с впервые в жнзин установленным диагнозом злокачественного новообразования
По сведениям ВОЗ каждый год в мире выявляют около I млн, новых случаев рака молочной железы, прогнозируя рост заболеваемости к 2010 году до 1,45 млн.
На протяжении жнши 1 из Я женщин в США страдает ттим заболеванием. В структуре онкозаболеваемосгн женщин доля этой локализации в России составила в 2000 году 19т3%.
В России ежегодно регистрируется более 46 тыс. новых случаев РМЖ, что в структуре онхологичеекой -заболеваемости женского населения составляет 19% За период с 1980 но 2000 юл заболеваемость повысилась почти на 70%: с 22,6 до ЭК,3%40М. Начиная с 1990 года, в России показатели качества онкологической помощи больным раком молочной железы, в том числе, доля выявления ранних стадий, практически не менялись, Однако, заболеваемость в возрастных t-рунпах после 50 лег резко возросла. На конец 2004 г на учСте состояло 408.4 тыс больных РМЖ, из них 55,1% — в течение 5 лет и более [ 17>.
Рак молочной железы является одной Ю наиболее частых причин смерти женщин, по сравЕкнню с другими формами злокачественных новообразований По уровню смертности от рака этой локализации первые три места занимают Дания, Ирландия и Нидерланды Россия в этом списке находится на 28-ом ранговом месте. В России зга форма рака занимает третье место среди всех причин смерти женского населения после болезней системы кровообращения и несчастных случаев во всех возрастных группах, составляя в среднем 2,1%, прогрессивно увеличиваясь с возрастом, гак, например, составляя в возрасте 35-54 лет — 9,0% Общее число умерших от РМЖ увеличилось с 12,5 тыс. (1983г.) до 22,7 тыс. (2003г X т.е прирост составил 10,2 тыс (85%) |17,19].
Продолжительность жншн но многих странах увеличивается, и вместе с я им, возрастает заболеваемость злокачественными опухолями у пожилых людей. Согласно классификации, принятой европейским региональным бюро ВОЗ (Киев, 1963) возраст от 60 до 74 лег признан пожилым, от 75 до 89 — старческим, а 90 лет к более — возрасюм долгожителей Не смотря на очевидную актуальность проблемы, до последнего времени разработке рациональных методов лечения пожилых не уделялось достаточное внимания Так, в международных научных нс&ммюваниях вотрасг старше 65-70 лет обычно является критерием исключения. Но существу, только недавно 1юявнлись специальные научные программы для разработки этой проблемы
Как известно, онкологические заболевания в данной возрастной категории имеюг некоторые особенности Состояние здоровья таких паннеитов существенно отличается от больных других возрастных групп, что обусловлено наличием сопутствующих заболеваний! 110,) 18J, lie смотря па определенные успехи в комбинированном н комплексном .течении рака молочной железы связанные с внедрением в широкую медицинскую практику новых методов лучевой н лекарственной терапии, доминирующие значение занимает хируршчсское вмешательство, которое до настоящего креме) ut остается той основой, с учетом которой строится план лечебных мероприятий Jl 30, 31, 35, 38, 39, 51, 52, 59. 60, 77, 87, 96, 117, 130], Хиругическое лечение всегда должно соответствовать сформулированному в I960 г. ЛИ Раковым принципу онкологического радикализма, который при раке молочной железы предусматривает удаление не только органа с первичной опухолью и окружающими тканями, но также широкое иссечение регионарных лимфатических углов н клетчатки — первый этап регионарного метастаз нровання (21.
В 50 — 70с голы получила распространение расширенная частил омня по Урбану — Ходдину. включающая в себя подмышечную, подключичную, подлопаточную лнмфаденэктомию, резекцию хряхцекых частей ребер на стороне поражения для вьптолнсния нарастерналыюй лнмфоднееекцнн 5, 27, 59, 72, 73J, Несмотря на очевидный радикализм, тто вмешательство являлось калечащим, приводило к выраженным косметическим дефектам, а по эффективности было сопоставимо с результатами «снес 17×10матичных операций (Холстсда), дополненных лучевой терапией на юны регионарного мсгастазирования
Традиционно считается, что современная история лечения больных раком молочной железы начинается с гипотезы W. IIaisled (1895) об этапном процессе мегасгазироаання В течение 70 лет операция Halsied (радикальная масгзктомня), предусматривающая удаление в одном блоке молочной железы, большой и малой грудных мышц, подмышечио-подключнчно-поддопаточноЙ клетчатки, содержащей соответствующие регионарные лимфатические коллекторы, считалась станлартом хирургического лечения рака молочной железы Предложенная в 1948 году Р Patey и W.Dyson «модифицированная* масгэктомня с сохраненном большой грудной мышцы явилась более функционально щадя шей операцией, как и разработанная в 1958 году модификация радикальной масгжгомнн J. L. Madden с сохранением обеих грудных мышц |1. 27, 59, 70, 861.
Эволюция хирургической тактики привела к гюстспсшюму откату хирургов — онкологов от выполнения калечащих операции типа Урбана -Холдннз н предпочтетоо органе- и функщюнатыю-сбсрсгающих вмешательств в сочетании с хнмно- н лучевой терапией [5» II, 30, 31, 34, 38, 40,51.52,54, 59,63,108, I39J
Однако, постоянно появляющиеся сообщения о возникновении различных серьезных «сложений после проведения дистанционной гамма-терапии со стороны органов, попадающих а зону облучения [9, 18, 32, 37,
44, 112>, ведеi к постоянному поиску новых мсюлнк облучения н определен ню более узких показаний к проведению ДЛТ на юны регионарного метастатнрования при раке молот нон железы, особенно у больных пожилою н старческого возраста.
Ьлагодаря достижениям маммографического скрининга и успехам ранней дн&люсгнкн рака молочной железы, стало возможно выполнение хирургических вмешательств меньшего объема, что имеет не маловажное значение при лечении рака у пожилых, позволяет добиться быстрой реабилитации оперированных пациентов и улучшить качество их жишн
Изменение хирургической тактики в сторону оргаиосохранных операций связано так же и с появлением биологической системной модели рака молочной железы В. Fisher, показавшей, что данное заболевание на этане клинической манифестации является системным заболеванием, сопровождающимся скрытой днсссмшшдоей опухолевых клеток. Эта гипотеза сделала необходимым смещение акцепта при выборе тактики лечения рака молочной железы в строну системной терапии [59, 96, 97|,
В настоящее время существует ряд нерешенных проблем, связанных с оптимизацией дальнейшего лечения пожилых пациентов, после оргоносохрадонжих операций Лучевая терапия несет определенный риск, учтивая наличие сопутствующей патологии. Лекарственная терапия может быть высокоэффективной, хогя ее применение так же проблематично в большинстве случаев, из-за повышенного риска токсичности препаратов В пожилом возрасте становится значительнее роль гормонотерапии, что определяется более частым содержанием рецепторов эстрогенов ЭР+ и прогестерона ПР+ в опухоли. При ранних аадиях рака молочной железы у женщин в вотрасте старин: 70 лет при ЭР+ и/или ПР+ лечение яообще может быть начато с применения тамокенфена [67].
По сути, нет четкою алгоритма лечебной тактики при раке молочной железы у пациентов дайной возрастной группы.
Существует надежда мл го, что пожилые пациент в ближайшие годы смогут получить эффективное цйИВМЩПШПОв лечение Большинство авторов отмечают необходимость проведения дальнейших исследований для решения вышеозначенного вопроса
Целью данного исследования является улучшение результатов лечения ракв молочной железы у больных пожилого и отеческого возраста за счет разработки алгоритма хирургического н комплексного лечения. В сяятн с ттим поставлены следующие задачи
1. Сравнить результаты лечения больных раком молочной железы старше 70 лет при различных объемах оперативного вмешательства
2 Определить эффективность послеоперационного лечения в данной возрастной группе с применением адъювантной терапии и без нее.
3 Выявить особенности влияния прогностических факторов на общую н безрецмднниую выживаемость нацистов в данной возрастной группе.
4. Изучить гю-сталийно трех- и пятилетнюю выживаемость больных раком молочной железы, вошедших в исследуемую группу,
5. Изучить причины смерти больных раком молочной железы пожилого возраста.
6 На основе полученных данных разработать объемы оперативного вмешагсльства и сформировать алгоритм послеоперационного лечения пожилых папненток Объектом исследовании явились истории болезни, амбулаторные карты, а так же непосредственное участие в лечебном процессе в общей сложности 272 больных раком молочной железы пожилого возраста на тему «Особенности лечения рака молочной железы в пожилом и старческом возрасте»
I Ведущим методом лечения рака молочной железы в пожилом и старческом возрасте является хирургический метод Оптимальным объёмом оперативного вмешательства является при стадиях 1-М • радикальная резекция молочной железы, при стадиях III-IV — радикальная масгжгомня с сохранением грудных мышц.
2. При раке 1-П стадии хирургический метод лечения обеспечивает стойкое пятилетнее выздоровление в 80,1% случаев Проведение дополнительного алыовантного лечения не улучшает показатели выживаемости.
3. При мсстно-распространСшюм раке лечение должно бьггь комплексным и соответствовать общссомагичсскому статусу пациента. Рнск дополнительного лечения не должен превышать возможный лечебный эффект
4 Одномерный анализ позволил выделить факторы, обладающие высокой прогностической значимостью. При 3- и 5-летнем прогнозе это — возраст, критерии Т и N, гормональный статус, центральная локализация опухоли,
5. Многофакторный анализ позволил выделить факторы, обладающие высокой прогностической значимостью. При 3- и 5-летнем прогнозе это — критерии Т и N, гормональный статус.
6. Проведение открытой биопсии парастернальных лимфатических узлов на стороне поражения является важным тле ментом операции (в случае возможности выполнения), позволяющим правильно сталировать заболевание и назначать дополнительную тераштю.
7 При наличии положительных стероидных рецепторов, необходимо назначать гормонотерапию в адыовангном режиме
8. 11рн I—II стадиях процесса структура смертности такова: смерть чаще наступает от сопутствующей патологии (11,2%), чем от рака (8,7%) При ГП-IV стадиях, от рака умирают 58,7% больных, что почти в 10 рат чаще, чем от сопутствующей патологии (6,3%) и, в основном, в сроки до Зх лет наблюдения
Данные, полученные пачп при выполнении работы, могут быть использованы в дальнейшем специалистами при выборе объема операции у пациенток пожилого возраста Так же наш опыт проведения послеоперационного дополнительного лечения может явиться помощью дня специалистов, которые проводят адьювангное лечение оперированных но поводу рака молочной железы пожилых пациенток Дальнейшего углубленного изучения по применению у пожилых патдоентов требуют метод открытой биопсии парастсрнальных лимфатических узлов и методика выявления сторожевых аксиллярных узлов
Список использованной литературы по медицине, диссертация 2007 года, Пынзарь, Виталий Алексеевич
1. Александров Н.Н., Пантюшенко ТА, Козел Т.С. Расширенные операции при раке молочной железы // Вопросы онкологии 1982. -№3 -С. 102-109
2. Баженова А.П. Островцев Л.Д., Хаханшианли Г.Н, Рак молочной железы -М. Медицина, 1985. 269 с.
3. Барановский Г И,, Забродина А Н., Петра осо В.А., Черепанов Ф.С. и лр О хнрурт-ическом лечении больных раком молочной железы if Вопросы онкологии. -1975. № 2. — С. 93-97,
4. Бсрезкнн Д.П., Семнгдазов В.Ф., Филатов ВН., Якимов В.И. Выживаемость больных раком молочпоЙ железы (по материалам ВЦИЭЛ)//Вопр онкологии 1986 -Т, 32, Ж> -С. 17-24.
5. Бнланишвили Г В Изменения лимфатической системы молочной железы при раке П Тезисы докладов VIII Международного онкологического конгресса -М , 1962 -С. 459
6. Богуш ЛК, Иванов А.В. Стсрнотомия как хирургический доступ при операциях на бронхах, легких и внутригрудных лимфатических узлах // Груд хирургия. 1980 — Jfel — С. 44-49
7. Ш Вушмакни Н.Д. Лимфатически железы подмышечной впадины и их питание. Автореф дне . капа, мед. наук. Казань, 1910. — 26 с.
8. Веронези У., Коста А., Гранд» С. Объем хирургического лечения рака молочной железы а зависимости от распространения о пуходе вою процесса Национальный институт по изучению и лечению опу холей (Милан) // Вопросы онкологии. 1977 — №12 — С 20-25.
9. Вишнево ткая ЕМ Расширенная радикальная ампутация грудной железы с удалением лимфатической парастернальной цепочки при раке (непосредственные результаты) // Хирургия. 1962, — №8, — С. 52-56.
10. Волченко Н.Н., Кармакова Т.А., Якубовская Р.И. О некоторых формах рака молочной железы // Арх патологии -1994, Т, 56, №4. -С. 18-22
11. М.Высоцкая И В Лечение рака молочшзй железы О—П стадий; Автореф. докт мед наук, —М,, 1999 -С. 31-35.
12. Гельфгот М.М. Клиническое применение цветной лнмфографнн при оперативном лечении рака молочной железы // Вопр. онкологии. -1969. Т. 15. №3, — С. 20-26
13. Гордеева Л.И. Состояние лимфатического русла молочной железы человека при мастопатиях н при раке Н Арх анатомии, теологии и эмбриологии -1961. Т. 41, №9. — С. 67-75.
14. Давыдов М.И. Аксель Е М Злокачественные новообразования в России и странах СНГ в 2003 г. — М., 2005. 268 с,
15. Дацснко B.C. Эволюция методик предоперационной лучевой терапии при раке молочной железы И Вопр онкологии 1990 — Т 36, №12 -С 1448-1453
16. Двойрнн В.В., Аксель Трапезников HJi Статистика злокачественных новообразований в России и некоторых других сфанах СНГ а 1994 г М., 1995, Ч. 2. — 193 с.
17. Дегрель И- Атлас заболеваний молочной железы. Будапешт: Изд-во Акад Наук Венгрии, 1977 -173 с,
18. Демидов ГСП, Острой но в Л Д., Ковалев Б.Н. и др. Кооперированные исследования по лечению рака молочной железы // Вопр онкологии -1987 -№2 -С. 33-37.
19. Демин. В Н. Лечение рака молочной железы Н Хирургия. 1977. — № 2. — С.23-26
20. Дружков О Б., Дружков Б.К. Способ медиальной радикальной резекции молочной железы И Тезисы докладов 1 съезда онкологов СНГ М , 1996 -Ч. 2 -е 490
21. Дымарски£ Л.Ю. Рак молочной железы. М. Медицина. 1980. 200 с.
22. Дымарскнй Л.Ю. Расширенная мастэктомия при раке молочной железы // Хирургия -1978 >&4 — С. 3*4.
23. Жданов Д.А. Анатомия сосудов н опухолей. Душанбе: Ирфон. 1974 — 191 с,
24. Жданов ДА. Общая анатомия и физиология лимфатической системы. Л.: Медицина, 1952. -336с.
25. Иванов В.М. Рак молочной железы у больных пожилого н старческого возраста Авторсф. дне. д-ра. мед наук. М, 1993. — С. 18-27,
26. Иванов ВМ, Погодина Е.М., Высоцкая И В, Буйденок Ю.В., Новохацкая В.В. Рак молочной железы у больных пожилого и старческого возраста // Маммология 2006 — №1. — С 15-22
27. Кантин А В. Возможности раднохнрургического лечения рака молочной железы // Вести, хирургии. 1967, — Т. 99, № 9. — С, 46-49
28. Кожевников А,И., Яхонтов Н.Е., Панксгьянов А.И. Эффективность лечения больных раком молочной железы // Вопр онкологии 1975 -JG2.-C. 88-93
29. Козлова А.В. Лучевая терапия рака молочной железы // Мед. радиология 1965. — №4 -С. 12-18
30. Комиссаров А.Б- Варианты хирургических методов лечения локализованных форм рака молочной железы // Випр. онкологии -1985 .-№7 -С. 53-57,
31. Кошаровскнй ТТ. Кулакоаскнй А,А Замечания по удалению ретростернальных лимфатических узлов при радикальной операции рака молочной железы // Вогр. онкологии. 1959. — Т, 5. Jfe II. — С, 520-523.
32. Кудрявцев Д.В., Гумснецкая Ю.В Лучевая терапия больных раком молочной железы (( Вопр онкологии. 2001. — Т. 3, №2. — С. 144-145
33. Летягнн В П. Современные тенденции в лечении первичною рака молочной железы // Вестник ВОНЦ АМН СССР, 1990. — №1 -С 40-42
34. Летягнн ВII Лечение первичного рака молочной железы //Тер арх. — 1992 -№ 10. С. 33-37.
35. Лсгягнн В Л, Голдобснко Г В. ‘Эффективность комбинированною н комплексного методов лечения первичною рака молочной железы // Мед. радиол, и радиан безопасность. 1994.-№6,-С. 31-33
36. Летя | ни В.П., Высоцкая И В Первичный рак молочной железы диагностика, лечение, прогноз. М,, 1996. — 161 с.
37. Легягнн В.П., Лакгнонов К.П., Высоцкая И,В., Котов В.А- Рак молочной железы: (этиология, клаесиф, лечение, прогноз.) М, 1996.-150 с.
38. Личнннцер М.Р., Гормонотерапия рака молочной железы материалы V российской онкологической конференции 27-29 ноября 2001 г„ Москва — С.23-24,
39. Лучевая терапия злокачественных опухолей / Под ред. ЕС Киселевой -М Медицина, 1996.-С, 146-165
40. Малыгин СЕ, Сан-Антондо 2001 Новые решения а хирургии молочной железы И Практическая онкология Т. 2 2001.- №1,- С. 2022
41. Макаренко Н.П. Эндокринная терапия рака молочной железы у женщин //РМЖ -1998 №10. — С. 643*647.
42. Марготтинн М., Якобелли Г.т Kay М. Отдаленные результаты расширенной радикальной масгэктомнн // Труды VIII Международного противоракового конгресса, М , 1962 — Т I , — С, 385*388
43. Надь Д., Каласи И Хирургическая анатомия Грудная клетка. -Будапешт Изд-во Акад. Наук Венгрии, 1959. 428 с.
44. Найденов В За раезшнрената маоектмня при рак на млечната жлеза // Онкология (София). 1970 — Т. 7, № 2. — С. 65-69.
45. Маркович Ф.В. Роль расшнрешюй маегзктомин в лечен ни рака медиальной половины и центра молочной железы // Актуальные проблемы онкологии и медицинской радиологин. Минск, 1970. Т 2, -С 256-258
46. НевожаЙ В.И., Лихобабин В,Я., Апанаеевич ВИ. Оргаиосохраняющие операции при раке молочной железы И
47. Скрининг в раннем выявлении опухолей репродуктивной системы и проведение органосохраняющего лечения. Л. 1991 -С. 63-64.
48. Нечушкнн МИ Лечение больных раком молочной железы центральной и медиальной локализации с использованием раднохнрургнчсских методик: Авторсф. дне. д-ра. мед. наук. М., 2001 -4» с
49. Нсчушкнн М.И., Анлросов Н.С., Пароконная А.А-, Карапстяи Я.Р. Комплексное леченне больных раком молочной железы медиальной и центральной локализации // Материалы 7 Всероссийского конгресса рентгенологов и радиологов М., 1996. С. 152.
50. Орлов О.А. Способ радикальной резекции молочной железы при раке, локализующемся в се внутренних квадратах // Тезисы докладов юбилейной научной конференции к 50-легню оккослужбы Пермской обл Пермь, 1997-С. 46-48
51. Павлов А.С., Даушко B.C. Роль лучевой терапии при хирургическом лечении больных раком молочной железы Н Вопр онкологии. -1987 -Ш -С. 40-45.
52. Пак Д.Д От свсрхраднкальных масгэкгомий до органосохрашющих операций Н Практическая онкология Т. 3 2001 — №1.- С. 29-33
53. Семиглазов ВФ, Нургазисв КИТ, Арзуманов А-С. Опухоли молочной железы
54. Сигая М.З., Дружков Б К, Балд про на Н.Г., и др. Операция Урбана-Холдина в лечении рака молочной железы // Тезисы докладов VII Республиканской онкологической конференции. Казань, 1987. — С. 129-I3L
55. Слоинм ДА, Шницер А.В. // Лечащий врач 1998 2, -С. 61-63,
56. Трапезников Н.Н., Амирасланов А.Т., Гафур-Ахунов МА-I (оражение лимфатических узлов надключичной области без выявленного первичного очага // Мед. журн, Узбекистана. 19919. -С. 6-8
57. Трапезников Н.Н. Лстягин В.П., Алиев ДА. Лечение опухолей молочной железы М Медицина. 1989. 174 с.
58. Тюляклин С А. Химиотерапия днссемннкроваюкчо рака молочной железы // Практическая онкология избранные лекции / Под pea С. А. Тюляндизю. В.М Монссенко -СПб, 2004 -С. 104-105.
59. Тюлянднн С, А, Рекомендации восьмой конференции по адъювантной терапии рака молочной железы (Ст.-Галден, Швейцария, февраль 2003 года) // Практическая онкология Т. 2 -2003,-№1 С. 27-32.
60. Холднн С.А. Злокачественные опухоли молочной железы // Злокачественные опухоли: Руководство / под ред Н.Н. i 1строва. Л., 1962.-Т. 3,4. U — С. 31*167,
61. Холдни С.А. Многотомное руководство но хирургии под ред. Б.В Петровского. М Медицина, 1960. — Т. 5. — С 273,336.
62. Холднн С,А Принципы н границы хирургического лечения рака молочной железы Н Вопр онкологии 1969. — Т. 15. № 7. — С. 10-16.
63. Холднн С.А. Пути прогресса в лечении рака молочной железы И Хирургия -1957. №3 — С. 3-16.
64. Холднн С.А Расширенная подмышечно-грудинная мастэктомия при раке молочной железы // Проблемы онкологии (Труды института онкологии АМН СССР). Л,, I960, — Т. 3, — С. 14-24
65. Холднн С.А Сравнительная оценка оперативно-лучевых методов лечения рака молочной железы // Труды института онкологии АМН СССР Вопросы онкологии Л,. 1953. — Вып 6. — С. 184-201
66. Холдин С,А . Дымэрский Л.Ю. О лимфогенном мстжлазнровании и его значение для выработки плана рационального лечения рака молочной железы // Вопр онкологии. 1963, — Т.9- — № 3. — С. 96-102.
67. Холдин с.а., Дымаре кий Л.Ю. Опыт применения расширенных подмышечно-грудинных масгжгомнй прн раке молочной железы // Вести хирургии 1968 — № 9 — С, 34-39.
68. Холднн С.А , Дымарскнй Л.Ю Расширенные радикальные операции прн раке молочной железы. Л.: Медицина, 1975. — 231 с.
69. Яиишеаскмн Ф И Рак молочной железы. Клиника, диагностика, лечение. М. Медицина, 1966. — 331 с,
70. Aaronson N.K. el al Evaluation of breast conserving therapy; clinical methodological and psychosocial perspectives Europ. J. Surg, Onool -1988 — Vol 14 — P. 133- 140
71. Abrao A. Biopsia da cadeia ganglionar mammana interna contralateral cm 20 eases dc carcinoma opera ve I da mama com metastases na cadeia homolateral H Rev bras Cirug. -1959 Vol 38 1. — P 72-74
72. Abrao A., Da Stlva Neto J.B. Esludo Anatomico da Cadenia ganglionar Mam aria Interia tm 100 casos // Rev Paul Med 1954. — Vol, 45 -P. 317-326.
73. Albenni J.L, Meunier В , DenzJcr B. el al. Somatostatin receptor ui breast cancer and axillary nodes, study with scintigraphy, histopathology and receptor autoradiography // Breast Cancer Res Treat 2000. — Vol. 61 -P, 21-32,
74. Allen В. Campbell I., Desai S. ct al. Pilot study comparing the accuracy of lymphoscintigraphy sentinel lymph node localisation with axillary node dissection in women with operable breast cancer // N. Z Med J. 2001 -Vol 114. -P 233-236
75. Amagada R., Le M. G., Cjuincbreliere J. M. et al. Lale local recurrences in a randomised trial comparing conservative treatment with total mastectomy in early breast cancer patients // Ann Onool- 2003.- N11,-P 1617-1622.
76. Baumgarthcr E, Wcisz C, Mesier A ft Magy oncol 1990; 34:2.78-94
77. Butcher H Radical mastectomy for mammary carcinoma // Ann. Surg. -1969 -Vol 170. m P 883-888
78. Caceres E. Incidence of metastasis in the internal mammary chain in 600 consecutive operable eases of cancer of the breast and 5 year survival m 425 cases U Proc Ninth Inter Cancer Congress Tokyo. 1966 — P 699
79. Caceres fc Radical mastectomy with resection of the internal mammary lymph node chain // Proc Seventh Inter. Cancer Congress. London, 1958.-P. 1061-1067,
80. Christensen В., Bli chert-Toft M., Stemssen OX, Nielsen S.Z. Reliability of axillary lymph node scintigraphy in suspected carcinoma of the breast tf Brit J. Surg 1980 — Vol, 67, № 9 — P 667-668
81. Clark R M, Wilkinson R H , Miceli P N. el a3 Breasi cancer experiences with conservative therapy U Arner J. Clinical Oncotogy.-1987.-Vol. 10-P 461-468,
82. De Frenza N„ Falko G., Traversa A ct al. Tamoxifene e patologia genitals Femminile correlate H C. Hal ostet e ginecol 1998, 9: 416421
83. Di Vito F. D’Onorio 0., Chiappara C„ Grasso F Melastasi Imfonoduli mframammana quale pnmo segno cltnicodi carcinoma dclla mammcla // Problem di diagnosi e tcrapia adiuvantc. 1986. — Vol. 7, № 3. — P. 167173.
84. Early Breasi Cancer Trial istis Collahoralive Group H Lancet. 1998, 351 1451-1467
85. Fisher B. Biological and cons iderations regarding the use of surgery and chemotherapy in the treatment of primary breast cancer // Cancer. 1977 -Vol. 40, Suppl 1-P 574-587
86. Ftshcr В, Anderson S., Biyanl J. el al. Twenty-year follow-up of a randomized tnal comparing total mastectomy, lumpectomy, and lumpectomy plus inadiation for the treatment of invasive breast cancer H M, Engl, J Med -2002; 347 (16): 1233-1241
87. Flanagan F L , Pehdashti p., Siegel В A, PET in breast cancer (Review. // Semin Nucl Med 1998 — Vol 28 — P 290-302.
88. Fodor J., Pol gar C., Ncmcth G. Evidence-based radiotherapy m the treatment of operable breast cancer results in the 1990-res Review. // Orv. Hetil 2000. — Vol. 141, -P, 1551-1555,
89. Frcdriksson I., Liljcgrcn G, Amesson L. et al. Local recurrence tn the breast afler conservative surgery-a study of prognosis and prognostic factors in 391 women // Eur J Cancer -2002-Vol 38, N 14 -P I860
90. Haagensen CD Metastasis of carcinoma of the breast to the periphery of the regional lymph node filter//Ann. Surg. 1969. — Vol. 169, №2 — P 174-190
91. Haagensen C D Treatment оГ early mammary carcinoma A cooperative International Study // Ann. Surg 1963, — Vol, 157, № 2. — P 157-179.
92. Haagensen C.D., Cooley F, Radical mastectomy for mammary carcinoma tt Ann Surg -1963 Vol 157, № 2 — P 166-169
93. Handley R.S. Current concepts tn the prtmary treatment of operable carcinoma of the breast If Cancer 1969 — Vol 24, >fe 6 — P 1270-1271.
94. Handley R.S The results of radical operations for the cure of carcinoma of the breast // Ann. Surg. -1967. Vol- 46 — P. 1-19.
95. Handley R.S., Trackray Л.С. Invasion of mammary lymph nodes in carcinoma of the breast // Brit, med J, 1954 — Vol, 4854 * P 61-63.
96. Handley W.S. Cancer of the breast and its treatment. New York, 1922
97. Henderson I Craig//Cancer — 1994,1:40 M09.
98. ПО, lltllen H.F., Hupperets PS Breast cancer in patients, 70 years or older //Ned. Tijdsehr Geneeskd 2000; 144(23): 1099-1104
99. Hovnanian A.p. A technique for the biopsy of intercostal parasternal lymph nodesftSurgery I960. — Vol 47.№6.-P 891-894
100. Johansson S„ Svensson H , Denekamp J Dose response and latency for radiation-induced fibrosis, edema, and neuropathy in breast cancer patients // Int J Rad Oncol Biol Phys, 2002. Vol. 52, N5, — P. 12071219.
101. Johansson S. Svensson H. Larsson LG Denekamp J Brachial plexopathy after postoperative radiotherapy of breast cancer patients—a long-term follow-up // Acta Oncol 2000. — Vol. 39, N3. — P. 373-382.
102. Johansson S„ Lofroih P,0„ Denekamp J. Left sided vocal cord paralysis a newly recognized late complication of mediastinal irradiation // Radiothcr. Oncol 2001 — Vol. 58, — P. 287-294.
103. Jordan U. Long-term adjuvant «Tamoxifen therapy for breast cancer // Breast cancer Res And Treat — 1990; 15:125-136.
104. Kerukowske K., Grady D, Rubin S.M. et al: Efficacy оГ screening mammography // JAMA 1998. Vol 273. — P 149-154
105. Laeons J.f Bucalossi P, Cacers E, et al Radical mastectomy versus radical mastectomy plus internal mammary dissection И Cancer. 1976. -Vol 37.-P. 206-214,
106. Maher ML, Dreyfus H , Сатрапа F et al Management of breast cancer in the eldery // Eur. J Cancer Care(Engl). — 1995,4
107. MaigaitUni M The problem of regional metastases of carcinoma of breast U VI Inter Cancer Congress, San Paolo, 1954 — Vol. I — P 6164
108. McDonald E, Haagcnscn C D. In Diseases of the breast 2nd ed Philadelphia W В Saunders; 1971
109. McPherson K., Steel C M . Dixon J M, Breast cancer Epidemiology, nsk factors and genetics // Brit mcd J. 1994 — Vol 309 — P 10031006
110. Moore R.D., Chapmck R, Schoenbcrd M Lymph node metastases associated with carcinoma of the breast // Cancer, 1960 — Vol. 13, № 3. — P. 545-549
111. Parker S, Tong T, Botden S. el al: Cancer statistics. 1996 // CA Cancer J. Clin. 1996. — Vol 46 — P 5-27.
112. Pierquin В., Raynal M. Olmezquine Y. et al Ije traitement conservateur des cancars du Sein. Results a 10 ans // Prese. Med. 2001 -Vol 15. № 8 -P. 375-377
113. Powles T.J. Chcmoprevention of breast cancer using tamoxifen if Endocr Relal Cancer 1997; 3 225-260
114. Schnitt S. J., Connolly J. L , Hams V R et al Pathologic predictors of early local recurrence in stage I and II breast cancer treated by primary radiation therapy // Cancer -1984-Vol 53,-P, 1049-1057
115. Tamoxifen and menopausal status Risks and benefits / Sasco Annie H Lancet-1996; 9003: 761.
116. Urban J What in the rationale for au extended radical procedure in early cases? // JAMA -1967 Vol 199, №10 — P 742-743
117. Urban J.A Extended radical mastectomy for breast cancer I/ Am. J Cancer -1963 Vol. 106, № 3 — P 399-404
118. Urban J. A Radical excision of the chest wall for mammary cancer // Cancer -1951 -Vol 4. P. 1263-1285
119. Urban J.A. Radical excision of the chest wall m women with mammary cancer // Cancer 1953 -Vol 2, — P, 863 — 875.
120. Urban J. A. Changing patterns of breast cancer// Cancer * 1976. -Vol 37 -P 111-117
121. Veronesi U. The sentinel node and breast cancer // BriL J- Surg. 1999. -Vol. 86. №1 -P. 1-2.
122. Veronesi U. Conservative treatment of breasi cancer H Current perspectives in breast cancer New Delhi, 1998. -P. 164-170.
123. Veronesi U-, Voltterram F., Luini A. Guadrantcctomy versus lumpectomy for small size breast cancer // Eur I Cancer -1990 -Vol. 26. N6.-P. 671-673.
124. Veronesi (j., Csscmelli N. Mariam L. et al Twenty-year follow-up of a randomized study comparing breast-eonscrving surgery with radical mastectomy for early breast cancer ti N Engl J Med -2002 -Vol 347,-P. 1227-1232
125. Wahl R-L. Current status of PET in breast cancer imaging, staging, and therapy Review. U Semin Roentgenol 2001. — Vol. 36. — P 250-260
126. Wangensteen O.H , Bell H,G. Cancer of the breasi // Surgeiy -1949 -Vol 130.-P 315-316.
источник