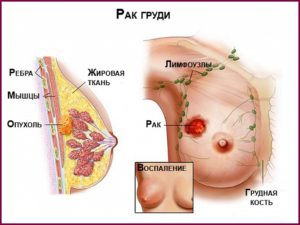
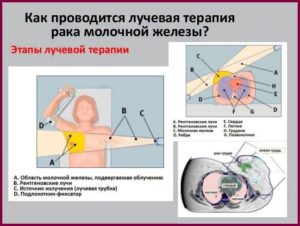
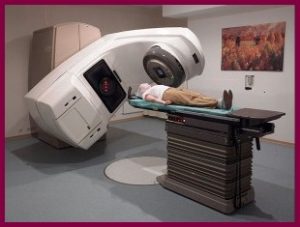
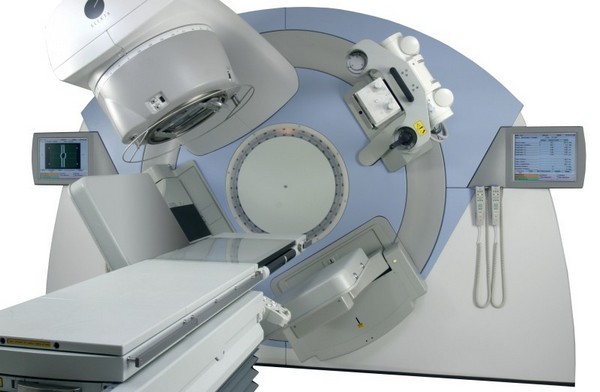
Рак молочной железы характеризуется образованием опухоли злокачественного характера, которая образовалась в тканях молочной железы. К огромному сожалению в настоящее время довольно часто встречаемая патология. Как показывает статистика, рак молочной железы встречается у каждой 12-ой женщины. При чем, возраст абсолютно разнообразный. Рак регистрируется у женщин в возрасте от 16 до 90 лет.
На сегодняшний день медицина не стоит на месте. Доктора могут диагностировать рак на ранних стадиях, когда новообразование довольно маленького размера. После диагностирования рака молочной железы, врач назначает лечение. Одним из видов лечения является лучевая терапия.
Лучевая терапия, иначе можно увидеть такое название как радиотерапия или радиационная терапия. Лечение данным способом основывается на воздействие рентгеновским бета-излучением, нейтроным излучением, гамма-излучением, которые воздействуют на злокачественные новообразования. Благодаря облучению прекращается активное размножение патологических клеток. Терапия довольно распространена и модернизирована. Это помогло снизить риски появления побочных эффектов. Так, например, для избежания уничтожения здоровых клеток, начали применять внутритканевое излучение. При постановки диагноза рака молочной железы лучевая терапия способствует:
- восстановлению дыхательной функции;
- уменьшению болевого синдрома;
- снижению риска возникновения перелома (в случае метастазирования в костные структуры);
- снижению риска появления кровотечений.
После курса лучевой терапии риск появления матировавших клеток снижается на 55-70%, что позволяет женщине жить полноценной жизнью. Но также не стоит забывать, что после такой терапии имеется ряд побочных эффектов.
Лучевая терапия подразделяется и зависит от цели и области воздействия. Так терапия делится на:
- Радикальную — применяется совместно с сопутствующим лечением. Целью является полное очищение организма от новообразований.
- Паллиативную — данный вид терапии применяется, если существуют метастазы или, если опухоль достигла больших размеров. Целью является остановить или затормозить рост и развития опухоли.
- Симптоматическую — применяется в случае, если опухоль неоперабельная. Цель: уменьшение болевого синдрома, продление жизни пациента.
Также лучевая терапия делится в зависимости от расположение злокачественной опухоли:
- Наружная — источник облучения расположен в специальном приборе.
- Внутренняя — источник облучения с помощью специального катетера вводят непосредственно в опухоль.
Лучевая терапия при раке молочной железы
По многим критериям лучевая терапия абсолютно противопоказана, при таких состояниях, как:
- беременность;
- любой вид сахарного диабета;
- анемия;
- дефицит массы тела;
- заболевание сердечно-сосудистой системы (сердечно-сосудистая недостаточность);
- туберкулез (активная фаза);
- перенесенный ранее инфаркт;
- почечная недостаточность;
- дыхательная недостаточность;
- лихорадка;
- тяжелое состояние женщины;
- системная волчанка (склеродермия).
Перед назначением проводится тщательный осмотр пациентки, который происходит строго на базе стационара. Непосредственно, на этом этапе подготовке, пациентку предупреждают о рисках возникновения осложнений, побочных эффектов. Доктор расспрашивает женщину подробно, чтобы она все ему рассказывала о всех изменениях после курса и во время курса лучевой терапии.
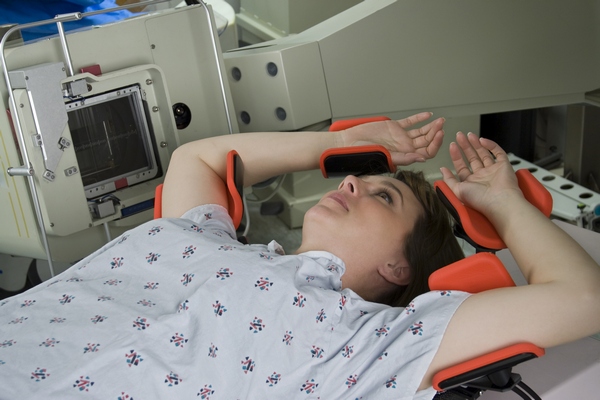
Во время проведения курса женщина лежит на твердой поверхности, тело фиксируется. При этом пациентка лежит на спине, а её рука отведена. Все это необходимо для точного попадания лучей в необходимую зону.
Когда начинается сеанс из комнаты все выходят и женщина остается одна, но связь с доктором не теряется. Общение происходит с помощью специального прибора.
Сама процедура абсолютна безболезненна и довольно короткая по времени.
При назначении операции и сохранении органа назначаются:
- Облучение молочной железы (или фрагмента молочной железы) по методу MammoSite.
- Облучение молочной железы + подключичная область + надключичная область + подмышечная область. Может также назначаться в различных комбинациях.
Так, например, после полного удаление пораженного органа (мастэктомии), лучевое облучение назначается подмышечной области, подключичной области, грудной стенке, надключичной области. Все это определяется по показаниям.
Курс лучевой терапии длиться от трех дней до трех недель.
Для того, чтобы лучевая терапия прошла успешной, врачи рекомендуют придерживаться несложной диеты. Так как правильное питание снижает риск появлений осложнений. Также радиотерапия способна нарушить работу пищеварительной системы, что может спровоцировать запор, рвоту, понос, тошноту.
Врачи рекомендуют начинать диету за две недели до начала курса лучевой терапии.
Диета заключается в полном отказе от:
- жирной пищи;
- жаренной пищи;
- консервации;
- острых специй;
- молочной продукции;
- алкоголя;
- копченостей;
- грибов;
- свежей капусты;
- газированных напитков;
- соленных продуктов.
Рекомендуется в свой рацион включить:
- не менее 2 л воды в день;
- сок яблочный;
- суп на втором бульоне;
- каши;
- зеленый чай, компот, отвар шиповника;
- творог нежирный;
- запеченное мясо, рыбу;
- грецкие орехи;
- зелень;
- мёд;
- яблоки;
- тыкву;
- гранат.
Питание должно быть дробное.
Лучевая терапия ведет за собой огромное количество последствий. Терапия способна воздействовать на:
- мягкие ткани кожи;
- мягкие ткани молочной железы;
- ткани подмышечной области (также грудной стенки);
- на кости части скелета грудной области;
- на легкие;
- на сердечно-сосудистую систему.
Также во время и после лучевой терапии, возможно у женщины могут наблюдаться такие последствия, как:
- отечность одной из рук или подмышечной области;
- может появиться небольшое уплотнение на молочной железе;
- отечность молочной железы;
- небольшое местное раздражение кожи в области облучения;
- высокий риск переломов;
- снижается мышечная сила руки.
Зачастую последствия терапии начинают проявляться через 2-3 недели после курса. Это проявляется в следующих моментах:
- в проявлении ноющей боли в области грудной клетки;
- повышенном чувстве утомляемости;
- изменении цвета кожи на груди (кожные покровы могут: покраснеть, появиться отёк, сухость, волдырь, потемнеть);
- кашле;
- расстройстве стула;
- болевых ощущениях в мышцах;
- нарушениях со стороны ЖКТ;
- алопеции;
- снижении иммунитета;
- нарушении сна.
Обычно данные недомогания начинают пропадать после полного выведения из организма радиоисточников. Это происходит через 6-7 недель после курса лучевой терапии. Но надо помнить, что боль в мышцах может остаться на более длительный срок. Так, например, болевой синдром женщина может ощущать в течении одного года.
Одними из самых распространенных реакций со стороны дыхательной системы являются: кашель, одышка, затрудненное дыхание. Часты инфекционные заболевания, сильная утомляемость. Появление этих признаков и симптомов возможно по истечении двух-трех месяцев после курса лучевой терапии.
Профилактика лучевых поражений легочной области заключается:
- в ингаляции;
- лечебной гимнастике;
- магнитотерапии;
- электрофорезе;
- специальном массаже.
Обычно, как показывает практика, кожные реакции проявляются в виде:
- сильного раздражения;
- зуда;
- жжения;
- сухости кожи;
- изменения цвета;
- появления волдырей.
При появлении кожных реакций необходимо незамедлительно сказать своему лечащему врачу. Так как, если вовремя не начать правильный уход, то заживление может проходить довольно долгое время, что приносит большой дискомфорт.
Женщина во время прохождения курса лучевой терапии, а также после окончании курса, ощущает болевой синдром. При этом болевой синдром проявляется резкими стреляющими точками. Это все происходит в следствии раздражения нервных волокон непосредственно в тканях молочной железы.
При этом врач обычно назначает противовоспалительные средства, которые приносят облегчение. После окончании курса лучевой терапии боли постепенно пропадают.
Иногда в области новообразования наблюдается уплотнение молочной железы. Так, например, мышцы становятся плотными и тугоподвижными. В основном, данное осложнение характерно для мышц, которые соединяют плечо и грудную стенку. Все это происходит в следствие образования рубцов.
Врач для облегчения данной патологии назначает обезболивающие препараты.
Лучевая терапия приводят к большому риску переломов. Это является следствием прямого удара в грудную клетку. При этом переломы заживают сами по себе, но, как показывает практика, данное осложнение встречается довольно редко.
Для того, чтобы уменьшить последствия после лучевой терапии надо:
- исполнять все рекомендации лечащего врача;
- пациент должен вести здоровый образ жизни;
- прогулки на свежем воздухе;
- правильное питание;
- употребление воды не менее 2-х литров;
- не пользоваться крема, дезодоранты, лосьоны;
- полностью исключить посещение саун;
- не делать компрессов, не применять грелок;
- избегать воздействие солнечных лучей в течении года.
Все стандартные последствия после курса лучевой терапии мы описали ранее, но также существуют осложнения, которые необходимо наблюдать у специалиста, а также их лечить. Так как многие осложнения могут нанести огромный вред здоровью, если их не лечить. К ним относятся:
- Лимфодерма — отек одной из верхней конечности. Является следствием терапии, которая непосредственно была направлена на подмышечные лимфоузлы. Также может образоваться после операбельного удаление подмышечных лимфоузлов.
- Хронические боли с парестезиями — при этом наблюдается сильное снижение мышечной силы, практически потеря чувствительности. Все это — следствие дегенерации нервного волокна.
- Пневмонит радиационной природы — следствие сильного облучения, которое возникает в легких. Начинает развиваться после курса облучения через 5-6 месяцев.
- Лучевые незаживающие раны — в основном не несут угрозы для жизни, но являются открытыми воротами для проникновения инфекции, так как считается открытой раной, к тому же доставляют дискомфорт.
После окончании курса лучевой терапии, если не произошло никаких побочных реакций и осложнений, то восстановление организма происходит довольно быстро. Через две недели женщина уже возвращается в свое привычное русло.
Для того, чтобы организм быстрее пришел в строй, необходимо строго придерживаться всех рекомендаций лечащего врача во время терапии.
- контроль динамики метастаз для пациентов со 2, 3, 4- ой стадии заболевания;
- сцинтиграфия скелета для пациентов с метастазами в кость;
- МРТ для контроля динамики опухоли;
- раз в год маммография;
- посещение врача маммолога не реже чем раз в 3 месяца первый год, в последующим — не реже двух раз в год.
источник
Здравствуйте дорогие читатели. Сегодня наша статья посвящена одному из методов, нацеленных на «добитие» раковых клеток после оперативного удаления основного их ядра. Итак, что такое лучевая терапия (ЛТ), и к каким результатам она приводит.
Лучевая терапия при раке молочной железы после операции используется для повышения выживаемости пациента, так как оставшиеся после «грубого» вмешательства скальпеля «отломки» опухоли подвергаются губительному воздействию корпускулярного или волнового излучения.
К корпускулярным типам относят:
- α и β — частицы;
- нейтронное;
- ионы углерода;
- протонное,
К волновому относят γ и рентген-излучение.
Метод предусматривает не разрушение опухолевых клеток, как думают многие, то есть некроз, что было бы очень печально для организма и привело бы его неминуемому отравлению, а инактивацию раковых клеток.
Инактивация в данном случае — это прекращение деления атипичной клетки, разрушение связей на уровне молекулы из-за:
- ионизации атомарной структуры ДНК;
- радиолиза воды в жидкой части патологической клетки.
Радиолиз означает, что вода в цитоплазме клетки формирует перекись и свободные радикалы, воздействующие на структуру ДНК.
Повреждает ли здоровые клетки такая терапия? Конечно. Облучение можно использовать потому, что оно наиболее действенно в отношении быстро делящихся и стремительно растущих клеток. Такими качествами обладают:
- раковые клетки;
- нормальные клетки красного костного мозга.
Направленное излучение сильнее повреждает раковые клетки, как активно растущие. Окружающие здоровые ткани тоже пострадают, но меньше. Во-первых, благодаря «прицельности» облучения здоровые ткани страдают в небольшом объеме. Во-вторых, даже подвергаясь той же дозе излучения, здоровые ткани (если это не костный мозг) повреждаются меньше, чем раковые клетки. Тем не менее им понадобиться некоторый период на восстановление.
Лучевая терапия в зависимости от времени ее проведения делится:
- на адъювальную (постоперационную);
- неадъювадьную (предоперационную) или индукционную.
Адъювадьное лечение нацелено на предотвращение рецидива болезни. Женщинам после органосохраняющей операции на молочных железах часто назначается ЛТ для предотвращения рецидива.
Неадъювальная терапия проводится до операции. Ее цель облегчить проведение процедуры для врача, снизить скорость роста опухоли на период подготовки к операции и повысить выживаемость пациента.
В лечении онкобольных применяют терапию:
- контактную (брахивальную);
- дистанционную;
- радионулкидную.
В первом случае облучается непосредственно опухоль. То есть источник излучения прикладывается к опухолевым тканям:
- интраоперативно;
- на поверхностную опухоль;
- в интерстициальную (закрытую тканями) опухоль в виде игл, шариков и т.п.
Метод щадящий, но на практике применяется редко. Дистанционное воздействие имеет больше побочных эффектов. Проводится сквозь здоровые ткани ради разрушения глубоко лежащих опухолей. Этот метод самый распространенный. Он универсальный и его можно использовать при разных новообразованиях.
В его рамках разрабатывается перспективная протонная терапия, позволяющая целенаправленно уничтожать именно рак на любой глубине. Вся доза выделяется в «теле» опухоли на последнем миллиметровом «рывке» пробега частиц. Окружающие ткани страдают минимально. Недостатком метода является его дороговизна (нужен дорогой циклотрон).
Последний метод предполагает введение радионудлида или составного фармпрепарата в сосуд или через рот. Радионуклид накапливается в опухолевых тканях и разрушает его.
ЛТ может быть элементом комплексного лечения и использоваться после химиотерапии или совместно с ней. Иногда такого курса достаточно, и можно избежать оперативного вмешательства.
Для лечения опухолей локализующихся вне молочной железы могут использоваться и другие методы ЛТ (РТМИ, РТВК, стереотаксическая радиохирургия).
В ЛТ входит предлучевой этап (выбор дозы, подготовка к облучению), лучевой и постлучевой. Лучевой этап после операции длится 14-21 день, при самостоятельном лучевом лечении курс пролонгируется до 4-6 недель.
Обычно сеансы проводят ежедневно пять дней подряд с интервалом в два дня ради восстановления тканей. Постлучевой этап начинается сразу после окончания процедур. Этот период требует щадящего режима, правильного питания и позитивного эмоционального настроя.
Лечение рака молочной железы обычно предполагает постоперационную ЛТ. Такое лечение должно уничтожить очажки неоплазии, оставшиеся после операции. Если у вас есть метастазы, цель ЛТ — уменьшение размера опухолевого очага и уменьшения боли при развитии рака.
Питание при ЛТ своеобразное:
- дробное;
- полноценное;
- высококалорийное;
- витаминизированное;
- с достаточным количеством минералов.
Пить нужно при лучевом лечении много, порядка 3 литров, включая соки, витаминные чаи, минеральную воду.
При ЛТ нельзя курить или принимать алкоголь. Вредные привычки при раке вообще противопоказаны. Также стоит убрать из своего рациона всевозможные сласти. Косметика и парфюмерия в период лечения могут полежать на полочке. Когда принимаете душ, не заливайте водой места облучения и не используйте мыло. Оно сушит кожу.
Если ткани в месте облучения зудят и краснеют, обратитесь к врачу. Не нужно самостоятельных мер (приложения холодных примочек или смазывания мазями). Носите одежду из натуральных тканей, свободного покроя, избегая трения облучаемых мест. Участки, подверженные облучению, нужно защищать от прямого солнечного света.
В процессе лечения, не пренебрегайте обычными рекомендациями для выздоравливающих: гуляйте, полноценно спите. Умеренная физическая активность вам только на пользу.
Последствия обработки ракового очага при ЛТ в основном связаны с одновременным повреждением здоровых тканей. Побочные эффекты могут быть:
К местным осложнениям относят явления, связанные с тем, что под «удар» попадает не только рак, но и здоровая ткань. К основным проявлениям относят:
- зуд;
- шелушение;
- гиперемию кожи;
- появление волдырей в зоне облучения, затем их изъязвления;
- усиление ломкости сосудов, кровоизлияния.
Системные осложнения развиваются, потому что опухолевые клетки погибают под воздействием излучения, продукты их распада попадают в системный кровоток, развиваются лучевые реакции:
- повышенная утомляемость и слабость;
- ЖКТ-расстройство (тошнота, рвота);
- ухудшение качества кожи и ее придатков (ломкость ногтей и выпадение волос);
- угнетается кроветворение и нарушение системы крови.
Кроме описанного разделения, специалисты делят последствия от ЛМ на лучевые:
Первые развиваются в течение первых 3 месяцев после лечения, вторые — после трехмесячного рубежа.
Реабилитация начинается сразу после окончания терапии. Первая консультация онколога проводится в промежутке с 1 по 3 месяц. Все последующие консультации проводятся раз в полугодие. Сроки реабилитации и специфические меры зависят от степени развития осложнений и интоксикации здоровых тканей.
В этот период важна диета (витамины, минералы и белки), здоровый сон и умеренная физическая активность. Обязателен контроль за состоянием тканей с помощью УЗИ и МРТ методов. Некоторые пациенты не ощущают серьезных последствий после ЛТ. Их беспокоит легкая слабость, которая быстро проходит при правильной диете и полноценном отдыхе. Реже развивается полноценная лучевая реакция.
На этом мы прощаемся с вами. Надеемся, наша статья помогла вам понять суть лучевого лечения при раке молочной железы. Читайте наши новые тексты и приглашайте друзей через социальные сети.
источник
Рак груди – опасная онкопатология, значительно распространенная у женщин. На сегодняшний день состояние проблемы таково, что ее научились диагностировать на самых ранних стадиях, когда опухоль имеет еще величину не более горошины.
Эффективное лечение предполагает сочетание различных методик: операции, введения препаратов, уничтожающих опухолевые клетки, приема гормональных препаратов и тех, что блокируют гормоны, проводящие стимуляцию раковых клеток.
Лучевая терапия при раке молочной железы – давно использующийся, но от этого не ставший менее эффективным, метод борьбы с карциноматозной структурой. Основан он на прекращении размножения активно делящихся клеток (такие характеристики имеют раковые клетки) высокоэнергетическими пучками рентгеновских лучей или других радиоактивных частиц.
К настоящему моменту данный метод лечения максимально усовершенствован, чтобы минимизировать неизбежные при облучении побочные эффекты. Изобретены методики внутритканевого введения источника излучения, что дает возможность здоровым клеткам оставаться облученными в минимальном диаметре от радиоисточника. Кроме того, здоровые структуры умеют хорошо восстанавливаться, чего нельзя сказать о дефектных клетках.
Доказано, что при раке молочной железы лучевая терапия:
p, blockquote 8,0,0,0,0 —>
- уменьшает боли, вызванные сдавливанием нервных окончаний;
- снижает кровоточивость из аномальных сосудов, беспорядочная сеть которых питает опухолевые структуры;
- уменьшает риск возникновения патологического перелома, если произошло метастазирование рака в костные структуры;
- улучшается дыхательная функция;
- если метастазы находятся в позвоночнике, проводимое их облучение частично устраняет сдавливание ими структур спинного мозга или выходящих из него нервов.
Проведенная после резекции злокачественной опухоли, радиотерапия снижает вероятность повторного появления этих мутировавших клеток в 50-67%, что существенно сказывается на качестве жизни. Возникающие же после лучевого лечения побочные эффекты, в большинстве своем, временны: попавшие под облучение и погибшие нормальные клетки довольно быстро восстанавливаются, с ними пропадают и беспокоящие симптомы.
Лучевая терапия рака молочной железы уничтожает новообразование следующим образом:
p, blockquote 12,0,0,0,0 —>
- Радиоактивное излучение – это наподобие лазера, который выпаривает любые ткани, оказавшиеся на его пути. Оно «видит» активно делящиеся клетки и угнетает клеточный центр, дающий команду к делению. Так повреждаются не только раковые, но и «нормальные» для организма клетки, имеющие высокую скорость деления (это костный кроветворный мозг, слизистая оболочка кишечника).
- Лучи способствуют зарастанию большинства сосудов, питающих опухоль: отсутствие питания – гибель для раковых клеток. Из-за данного эффекта отекают и воспаляются здоровые ткани в каком-то (он зависит от вида выбранной лучевой терапии) радиусе вокруг новообразования.
Лучевая терапия в лечении рака молочной железы назначается радиотерапевтом. На основании истории болезни (указанных в ней данных о стадии болезни, гистологическом заключении) и осмотра пациентки он делает заключение, нужно ли облучать опухоль, какой выбрать режим терапии, дозу, периодичность и кратность излучения.
Совместно, лучевой терапевт и хирург-онколог обсуждают: радиоактивными веществами лучше воздействовать на новообразование до операции, после нее или вместо вмешательства (последнее применяется в неоперабельных случаях). Также этот узкий специалист определяет переносимость лучевого лечения, принимает решение об изменении его типа или отмене.
Предоперационная лучевая терапия прописывается в зависимости от нескольких критериев рака молочной железы:
p, blockquote 17,0,0,0,0 —>
- При Педжетовой болезни (карцинома сосково-ареолярного массива), если есть отдаленные (во внутренние органы или кости) или регионарные (в лимфоузлы) метастазы.
- При изъязвленной форме рака: за время проведения облучения язва может или затянуться, или очиститься. Удаление новообразования без лечения радиоактивными лучами сильно повышает риск того, что после операции рана будет постоянно инфицироваться и плохо заживать.
- Если опухоль – инфильтративно-отечная. Оптимальное решение в этом случае: вначале – неоадъювантная химиотерапия, после – радикальная лучевая терапия. Это повышает вероятность, что до операции опухоль сможет более четко очертить свои границы.
- При инфильтративной форме, когда раковая опухоль плотно спаяна с тканями: с сосково-ареолярным комплексом, фасцией (пленкой), покрывающей мышцы, лежащие под железой. Проведенная до операции, лучевая терапия при раке молочной железы может применяться, когда организм еще не «отравлен» продуктами опухолевого распада.
- При маститоподобной карциноме, но только – после химиотерапии.
2. Если груди стали источником нескольких раковых опухолей.
3. Обнаружено более четырёх метастатически-пораженных лимфоузлов.
После удаления рака молочной железы лучевая терапия должна подавить ростовую способность паталогических клеток, которые могли оставаться после оперативного вмешательства. Она чаще всего проводится:
p, blockquote 20,0,0,0,0 —>
- на 3 стадии любой формы рака;
- при болезни Педжета без метастазов;
- в случае узловой формы рака;
- если есть метастазы в подмышечной и подключичной областях;
- когда по гистологическому типу рак относится к тем, которые часто рецидивируют.
Чем больше органов планируется удалить во время операции, тем обширнее должна быть зона обработки радиоактивными лучами, тем длительнее курс лучевой терапии при раке молочной железы.
Читайте подробнее о раке молочной железы, его формах и методах лечения.
Обработке лучами также подвергаются (по показаниям):
p, blockquote 23,0,0,0,0 —>
- только молочная железа;
- лимфоузлы подмышечной ямки;
- лимфоузлы, расположенные над и под ключицей, захватывая ножки мышц, идущих от области за ухом к грудине (кивательная мышца).
При наличии метастазов до или после операции облучению подвергаются области, где они находились или находятся.
Интраоперационный облучатель «Intrabeam® PRS 500»
Эта методика дополнительного уничтожения клеток раковой опухоли непосредственно во время операции стала применяться относительно недавно. Она дает дополнительные гарантии, что те клетки новообразования, которые могли не быть иссечены, «умрут» от облучения. Такая технология лечения за последние 5 лет показала отличные результаты – менее 2% рецидивирования.
Дело в том, что при операции опухоль удаляется под визуальным контролем. «Страхование» от неполного ее резецирования дает только выполняемое во время операции (когда пациентка еще на столе и рана ее не ушита) гистологическое исследование, а оно в нашей стране выполняется крайне редко. При этом доказано, что рецидив рака почти всегда обнаруживается именно в том месте, где подобное образование уже однажды иссекалось.
Интраоперационное облучение показано также для лечения не очень агрессивных (когда рост и метастазирование идут годами) типов карциномы у пожилых пациенток – чтобы после операции обойтись без лучевой терапии, или уменьшить ее продолжительность на несколько недель. Показана она при небольших размерах опухоли, даже если есть 1-2 метастаза в регионарные лимфоузлы. Радионожом также можно удалять подмышечные лимфоузлы, если в них есть отсеянные из карциномы клетки.
Проведение лучевой терапии после химиотерапии рака молочной железы лучше всего позволяет избежать рецидива:
p, blockquote 30,0,0,0,0 —>
- препараты уничтожают скопления раковых клеток;
- облучение побеждает «оставшиеся в живых».
Показания к такой терапии: неоперабельный рак, инфильтративно-отечная форма рака, и отказ пациентки от операции.
Если для химиотерапии применялся Адриамицин, то с момента его последнего введения до применения радиации должен пройти месяц. При использовании других препаратов хватит 2-3 недель.
Лучевая терапия: линейный ускоритель «Elekta Synergy»
Она делится в зависимости от своей цели и может быть:
p, blockquote 34,0,0,0,0 —>
- Радикальной, которая (совместно с другими видами лечения) должна полностью очистить организм от рака.
- Паллиативной, назначаемой при наличии или метастазов, или больших объемов опухоли. В этом случае ни один из методов лечения, ни их сочетание не гарантирует полного избавления от новообразования. Но есть шанс сильно затормозить рост опухоли и распространение от нее метастазов с помощью лучевой терапии.
- Симптоматической. Это подразумевает облучение неоперабельной раковой опухоли для того, чтобы уменьшить боли и немного улучшить состояние.
В зависимости от расположения источника с радиоактивным материалом, лучевая терапия может быть наружной, когда источник расположен в стационарном устройстве и контактной внутренней (брахитерапия), при которой радиоактивное вещество с помощью катетера или баллона вводится в опухоль.
Последнюю используют, преимущественно, для обучения опухоли высокой дозой, чтобы окружающие ткани не пострадали очень сильно. При этом радиоактивный источник или вводят в новообразование на несколько суток, или убирают его через 10-20 минут после введения.
Хоть лучевой терапевт определяет сроки лучевой терапии индивидуально в каждом случае, можно привести некоторые усредненные параметры.
Так, перед операцией проводится короткий интенсивный курс облучения. Это примерно 4,5 недели (в зависимости от запланированной общей дозы и переносимости ее). Далее, через 3 недели, но не позже четвертой, может проводиться операция. Послеоперационная радиотерапия может проводиться через месяц после хирургического вмешательства. Ее длительность – 5 дней в неделю, 5-7 недель.
Последствия лучевой терапии при раке молочной железы обнаруживаются не сразу. Через время в 3-4 недели обычно наблюдаются:
p, blockquote 42,0,0,0,0 —>
- повышенная утомляемость;
- ноющие боли в облучаемой груди;
- изменения кожи груди: ее покраснение, отечность, сухость, зуд. Могут появиться волдыри или отслоение верхнего кожного слоя, как при солнечном ожоге. Кожа на облучаемой груди может потемнеть;
- боли в мышцах, лежащих под грудью;
- кашель;
- понос;
- изменения, связанные с воздействием на костный мозг, который временно перестает вырабатывать новые клетки крови, тогда как старые постепенно гибнут. Это кровоточивость, слабость и бледность, легкая подверженность инфекциям.
Эти последствия у большинства женщин уходят после окончания воздействия радиоисточником в течение полумесяца. Мышечные боли могут длиться до года.
При выполнении лучевой терапии при раке молочной железы могут быть и осложнения, к которым относятся:
p, blockquote 44,0,0,0,0 —>
- Отек подмышечной ямки и руки на облучающейся стороне.
- Радиационное воспаление легких.
- Потеря мышечной силы руки с больной стороны.
- Повреждение сердечной мышцы (повышенный риск отмечается у курящих и тех, кто уже страдает сердечными заболеваниями).
- Лучевые язвы на коже.
Радиотерапия имеет такие противопоказания, как:
p, blockquote 46,0,0,0,0 —>
- системные болезни (системная волчанка, склеродермия, дерматомиозит);
- тяжелый сахарный диабет;
- беременность;
- анемия;
- полученный ранее курс радиотерапии на любой другой зоне тела;
- тяжелая сердечно-сосудистая недостаточность;
- истощение;
- тяжелое состояние больного;
- лихорадочные состояния;
- активная фаза туберкулеза;
- перенесенный инфаркт;
- почечная или дыхательная недостаточности.
Во время, а также год после лучевого лечения женщине нужно больше отдыхать, гулять, получать позитивную информацию. Ей придется уделять повышенное внимание гигиене груди и руки: не купаться в горячей воде, не пользоваться парфюмерными изделиями, перед выходом на улицу использовать солнцезащитные препараты местного назначения.
Во время лучевой терапии при раке молочной железы, питание должно стать полноценным, богатым витаминами. Можно кушать супы на втором рыбном или мясном бульоне, отварные овощи, каши, запеченное или вареное мясо, пить кисели, отвары шиповника, черники, свежих спелых яблок и груш. Белый хлеб – высших сортов, лучше подсушить. Творог – только свежий и нежирный. Если есть анемия, в питание включить грецкие орехи, абрикосы, гранаты, мед, петрушку, кабачки. Белковой пищи – побольше, но она не должна быть жирной (сливочное масло – можно). Во время поноса свежие овощи и фрукты – ограничить. Прием пищи – четырехкратный или более частый.
Также важен объем суточной жидкости – не менее 2 литров. Сюда включают отвары шиповника, свежевыжатые фруктовые соки, морсы, зеленые и фруктовые чаи.
Алкоголь, консервы, маринованные и соленые продукты, а также газировку употреблять нельзя.
p, blockquote 52,0,0,0,0 —> p, blockquote 53,0,0,0,1 —>
источник
Рак молочной железы является наиболее распространенным видом рака в Германии. Ежегодно в стране регистрируется более 70.000 новых случаев этого заболевания. Если рак распознается на ранней стадии, то очень многие женщины имеют шанс излечиться.
«Ранние стадии рака и не очень агрессивные формы заболевания сегодня практически всегда излечимы!»
В случае с раком молочной железы считается, что возраст пациента является наибольшим фактором риска развития заболевания. Чем старше становится человечество в целом, тем больше раковых заболеваний будет диагностироваться в будущем.
Наиболее частое онкологическое заболевание в целом
Кроме того, считается, что рак молочной железы является наиболее распространенным раковым заболеванием не только у женщин. Рак груди является наиболее распространенным видом рака в целом.
«Ранние стадии рака и не очень агрессивные формы заболевания сегодня практически всегда излечимы, однако это не означает, что можно преуменьшать серьезность этих заболеваний. Это означает то, что детально проработанные концепции хирургического, медикаментозного лечения и лучевой терапии хорошо работают», — говорит Доктор мед. наук Мануэла Зайферт, руководстводитель отделения сенологии и маммологиии Городской Клинической больницы г. Золинген, Германия.
Снижать риски
После химиотерапии, которая проводится до или после операции, и после самой операции многие женщины задаются вопросом: а нужно ли облучение вообще? И еще один вопрос: Не являются ли нагрузки вследствие лучевой терапии слишком высокими в соотношении с пользой от лечения? Ответ на этот вопрос очевиден – нет. «Польза от лучевой терапии практически всегда больше, чем риск. Поэтому на сегодняшний день почти все женщины с раком груди получают лучевую терапию, особенно в случае с так называемыми органосохраняющими операциями облучения в большинстве случаев являются обязательными», — подчеркивает доктор Зайферт. Риск того, что заболевание может возникнуть снова, становится вполовину меньше благодаря облучению. Этот факт уже давно был доказан результатами большого количества очень крупных исследований. В любом случае, этой возможностью следует воспользоваться.
Хорошая переносимость
Сегодня большинство женщин получают лучевую терапию в соответствии с золотым стандартом. В данном контексте золотой стандарт означает, что отличающиеся от него методы лечения, как минимум, должны давать хорошие результаты, соответствующие стандарту, и ни в коем случае худшие результаты. В зависимости от того, насколько высоко оценивается риск рецидива, классическая форма облучения длится от пяти до шести недель и состоит из 25 — 32 разовых облучений. Из них 25 разовых сеансов лучевой терапии включают в себя низкодозное облучение всей груди. В случае с некоторыми пациентками могут проводиться от пяти до восьми прицельных разовых облучений, направленных исключительно на ложе опухоли. В таком случае специалисты говорят о так называемом «прицельном облучении ложа опухоли» (boost-облучение). Доза за один сеанс boost-терапии идентична дозе при облучении всей груди. В качестве нового золотого стандарта сегодня многим женщинам предлагается сокращенная лучевая терапия, которая включает в себя от 15 до 20 сеансов облучения. Специалисты называют такое облучение гипофракционированным.
В большинстве случаев лечение проводится в амбулаторном режиме
Терапия проводится в основном в амбулаторном режиме. «Тяжелые побочные эффекты, которые возникали ранее, уже давно остались в прошлом. Современные приборы для лучевой терапии можно направлять на поле облучение абсолютно прицельно», — говорит доктор Зайферт.
Также сегодня можно регулировать интенсивность излучения, так что расположенные за полем облучения ткани совсем не затрагиваются. «На момент окончания облучения кожа всегда немного раздраженная, поэтому пациенткам необходимо хорошо ухаживать за кожей, применяя лосьоны без ароматизаторов, носить легкую и свободную одежду, а также отказаться от плавания и солнечных ванн», — рассказывает доктор Зайферт.
В принципе считается, что кожа полностью восстанавливается приблизительно в течение от четырех до восьми недель. Против синдрома усталости, который скорее редко возникает при лучевой терапии, доктор Зайферт рекомендует физическую активность на свежем воздухе, легкую средиземноморскую кухню, а также интересные встречи с друзьями знакомыми.
Выше золотого стандарта
Во многих центрах радиологической онкологии будущее для лучевой терапии уже началось. При этом, в основном, развиваются четыре новых пути, направленных на улучшение эффективности уже имеющегося золотого стандарта или на повышение комфорта для пациенток без ограничения эффективности лучевой терапии. «Краеугольным камнем этих рассуждений является адаптация лучевой терапии в зависимости от индивидуальной ситуации пациентов», — говорит доктор Зайферт. «Мы называем это режимом и видами облучения, адаптированными к индивидуальным рискам. Таким образом, мы можем создать персонализированную лучевую терапию».
источник
Лучевая терапия при раке молочной железы – распространённый и результативный метод лечения. Радиотерапия осуществляется влиянием нейтронным, рентгеновским излучением на новообразования груди злокачественного характера. Благодаря данному излучению прекращается деление и распространение опухолевых клеток. Модернизация метода позволяет снизить побочные эффекты и осложнения. Лучевая радиотерапия способствует восстановлению дыхательных функций, снижает болевой синдром при онкологии. Также метод лечения укрепляет кости, защищая от появления переломов в случае проникновения метастазов в костные ткани.
Радиотерапия снижает риск открытия кровотечений при РМЖ, способствует возвращению женщины к полноценной жизни после операции. Проводится процедура под разным угловым наклоном по отношению к опухоли, что повышает результативность в борьбе с раком. Чаще к лечению подходят комплексно, применяя хирургическое вмешательство, радиотерапию и медикаментозный метод. Побочные эффекты после лучевой радиотерапии сводятся к повреждению здоровых клеток в тканях организма. Но повреждённые клетки самовосстанавливаются, устраняя болевые синдромы.
В зависимости от стадии рака, локализации опухоли и возраста женщины, применяются разные виды радиотерапии:
- Радикальная. Проводится путём мощного излучения, нацелена на полное устранение онкологии, раковых клеток из организма в целом. Применяется вместе с другими методиками лечения, до или после химиотерапии. Переносится болезненно, но результат – отступление рака. Последствия для организма болезненные и требуется время на восстановление.
- Паллиативная. Этот метод применяют при запущенных, завершающих стадиях онкологии, когда выздоровление невозможно. Цель паллиативной терапии – замедлить рост опухоли и затормозить распространение метастазов. С помощью облучения при лучевой терапии достигается ремиссия, устранение болезненных симптомов, продлевается жизнь пациентки.
- Симптоматическая. Применяется на четвёртой стадии рака, когда опухоль не операбельна. Облучение заглушает болевые симптомы, улучшает качество жизни женщины.
Лучевая радиотерапия также бывает наружной и внутренней. Наружная – когда источник излучения находится в специальном приборе. А внутренняя – когда вещество вводится непосредственно в очаг злокачественной опухоли. Происходит увеличение дозы вещества, влияющей на раковое новообразование. В этом случае соседние ткани и здоровые клетки не поражаются. Для облучения применяют комплексный подход, сочетание с другими способами лечения, но в отдельных случаях используют адъювантную монотерапию. Лучевое облучение проводят после операции или до хирургического вмешательства.
Лечащий врач назначает курс радиотерапии в лечении онкологических болезней. Показание к лучевой терапии следующее:
- Болезнь Педжета. Злокачественная опухоль сосково-альвеолярного участка, онкология при этом выбрасывает метастазы в лимфоузлы и здоровые участки.
- Изъязвлённая форма ракового заболевания.
- Отёчная, инфильтративная форма опухоли в онкологии.
- Карцинома, подобная маститу. Излучение проводится после курса химиотерапии.
Процедура лучевой терапии проводится перед операцией в случаях множественного поражения на молочных железах.
В зависимости от стадии развития рака груди, физического здоровья и особенностей организма пациентки, применяются разные схемы и подходы радиационной терапии. Степень агрессивности злокачественной опухоли также влияет на схему облучения, которая подбирается лечащим врачом отдельно для пациенток. Разрабатывая подходящее лечение и рассчитывая план, подбирается результативный метод с минимальным вредом для здоровых клеток организма. На поверхность груди доктором наносится разметка специальным маркером, для точного попадания лазерного луча. Применяются специальные рентгеновские аппараты, позволяющие использовать угол наклона.
Выбор необходимой схемы радиотерапии осуществляется по следующим критериям:
- Локализация злокачественной опухоли, скорость роста и агрессивность характера развития.
- Структура злокачественного новообразования, гистологические особенности.
- Стадия развития онкологии, степень распространения клеток, имеющих злокачественный характер, в здоровых тканях.
На первых, начальных стадиях развития опухоли лучевая радиотерапия применяется до операции, а также после удаления злокачественного новообразования. Принцип действия – уничтожение злокачественных клеток, предотвращение рецидива после лечения. Лучевая радиотерапия останавливает деление и распространение раковых образований и метастазов.
Наружная радиоактивная терапия длится до двух месяцев, с частотой сеансов до пяти раз в неделю. Процедура проходит в клинических, стационарных условиях, при помощи специального рентгеновского аппарата. Внутренняя лучевая терапия применяется реже, чем внешняя. Для данного вида процедуры применяют специальные имплантаты с радиоактивными веществами. Для введения катетеров в груди делают надрезы, через которые вводят имплантаты с лекарством.
Надрезы рассчитываются так, чтобы открывался доступ к очагу поражённого участка, злокачественного новообразования. Курс терапии длится до семи дней, с частотой сеансов ежедневно по семь минут. Если произошел выброс метастазов в организме, то лучи радиоактивной терапии направляются на все клетки и участки тела. После процедуры молочные железы постепенно восстанавливаются, возвращаются к выполнению своих функций. Количество курсов зависит от степени развития опухоли, стадии рака.
После проведённого хирургического вмешательства используют действие радиоактивных лучей, чтобы исключить рецидив, возвращение онкологии. При хирургии невозможно удалить все железы и ткани, поэтому злокачественная клетка может оставаться в организме. В этом случае применяются дополнительные терапевтические методы, усиливающие действие лучевой радиоактивной терапии.
Облучение классифицируется так:
- Послеоперационное. Проводят с промежутком от двух недель до месяца после мастэктомии – проведения хирургического вмешательства по удалению опухоли. Показание к проведению терапии – отсутствие результативности проведённой операции. Проводится профилактическое облучение лимфатических узлов, влияние радиоактивных лучей на ткани, которые не были поражены. Также уничтожаются злокачественные клетки, которые остались в поражённой онкологией зоне.
- Интраоперационное. Повод применения – при операциях, которые нацелены на сохранение грудных желёз и других поражённых органов. Радиоактивные лучи удаляют злокачественные раковые клетки, которые сохранились после процесса иссечения отдельных тканей.
- Самостоятельное. Применяется при завершающих стадиях рака, не поддающихся операции, а также в случаях, когда пациентка отказывается от операции по удалению грудных желёз. Также данный вид облучения применяют в случаях наличия противопоказаний к хирургическому вмешательству. Радиоактивные лучи данного вида нацелены на уничтожение злокачественных клеток, чтобы остановить раковый процесс роста опухоли. Устраняются болевые симптомы, достигается стойкая ремиссия, улучшающая качество жизни женщины.
Тип проводимой терапии устанавливает лечащий доктор, опираясь на локализацию опухоли, особенности организма пациентки, а также степень развития и агрессивность ракового новообразования. После радикальной мастэктомии разрабатывается специальная схема терапии радиоактивными лучами.
Каждый вид применяемой лучевой терапии сопровождается побочными действиями для организма. Влияние радиоактивных лучей сказывается на физическом состоянии, самочувствии пациентки, снижает защитные функции иммунитета. Повышается риск вирусных и бактериальных заболеваний, ощущается слабость и бессилие, сниженная работоспособность.
Реакции организма проявляются в различной локализации:
- Кожный покров. На коже образуется аллергическая реакция, схожая с солнечными ожогами. Наблюдаются явления: покраснение, зуд, крапивница, шелушение кожного покрова. Изменения оттенка кожи неравномерны, варьируются от ярко-красного до бледно-розового. Реакция на облучение проявляется не сразу, а постепенно, в процессе терапевтического лечения. Для снижения дискомфортных ощущений рекомендуется выбирать одежду, не ограничивающую движений, из тканей натурального происхождения. Следует выбирать верхнее бельё из хлопковых тканей, избегать синтетического материала.
- Грудь. Ощущается боль груди, подмышечных впадин. Швы после надрезов усиливают болевые ощущения. Наблюдается отёчность и онемение. Со временем болевые ощущения и дискомфорт проходят. Следует ограничить нагрузку на данный орган, избегать травм и ушибов. Важно подбирать правильную одежду, не раздражающую кожу. Доктор может назначить медикаментозные препараты в виде мазей, способствующие заживлению ран, снижению отёчности.
- Подмышечные впадины. Болевые ощущения связаны с проведённой операцией. В участках надрезов наблюдается отёк и покраснения, шелушение кожи. Облучение способствует усилению болевых симптомов, но со временем боль уходит.
- Внутренние органы и процессы. Радиоактивное облучение негативно сказывается на работе внутренних органов, нарушает работу желудочно-кишечного тракта. Ощущается тошнота, отвращение к пище. Также на лёгких образуются рубцы, которые сказываются на дыхании. Возможно появление болезненного, сухого кашля. В этом случае назначается прохождение рентгена, выписываются стероидные медикаменты.
- Мышечные ткани груди. Радиоактивная терапия раздражает мышечные ткани, нервные волокна. В результате этого ощущается резкая, стреляющая, колющая боль в грудных мышцах, схожая с действием электрического разряда. Для снижения болезненных, дискомфортных ощущений используют противовоспалительные медикаментозные препараты. Ткани восстанавливаются, дискомфорт исчезает в сроки, связанные с восстановлением. Степень боли зависит от лучевой терапии, мощности радиоактивного вещества.
- Боль в рёбрах. Действие радиоактивных волн способствует риску перелома ребер. После мастэктомии мышечный каркас отсутствует, поэтому костная ткань оказывается в зоне риска. Даже после установки имплантата риск перелома высок. Поэтому следует избегать травм и ушибов. Также следует употреблять в пищу продукты, содержащие кальций, укрепляющие кости, скелетную основу, чтобы восстановиться.
- Уплотнение мышц. После проведённой терапии радиоактивного облучения при РМЖ мышцы груди становятся твердыми, тугими. Это объясняется наличием образовавшихся рубцов под действием радиации. Это приводит к ограничению в движениях, малоподвижности. Чтобы устранить дискомфорт, назначают приём обезболивающих препаратов.
Для лучевой терапии нужна эмоциональная и физическая подготовка, готовность к побочным действиям, болевым синдромам, дискомфортным ощущениям. После проведения лечения нужна реабилитация. В отдельных случаях лучевая терапия бывает опасна, поэтому важно сотрудничать с лечащим врачом, соблюдать все рекомендации.
По окончании курса лучевой радиотерапии необходимо время для восстановления организма. Для этого важно предпринимать действия для укрепления иммунитета и здоровья организма. Степень полученных осложнений и побочных действий зависит от стадии развития злокачественной опухоли, мощности применяемых веществ при излучении. Лечащий врач рекомендует фитотерапию, чтобы ускорить процесс реабилитации организма. Это включает в себя следующие советы:
- Соблюдение правильного и здорового режима питания. Следует исключить из дневного рациона вредные продукты, содержащие красители, консерванты, синтетические вещества. Рекомендуется отдавать предпочтение свежим фруктам и овощам, которые содержат витамины и полезные микроэлементы. Также кисломолочные продукты будут способствовать укреплению костной ткани, насытят организм кальцием.
- Пить достаточное количество чистой воды. Обильное питье способствует выведению шлаков и токсинов из организма, ускорению метаболизма и обновлению клеток.
- Больше бывать на свежем воздухе. Это насытит клетки организма кислородом, ускорит процесс обновления и восстановления поражённых участков.
- Отказаться от курения и чрезмерного употребления алкоголя. Данные вредные привычки усугубят здоровье и могут спровоцировать рецидив онкологии.
- Поражённые участки тела нужно лечить только по схеме, установленной лечащим врачом. Нельзя применять народные средства лечения в виде примочек, растирок, согрева или массажа. Пострадавшие после лучевой терапии участки тела чувствительны, неправильное обращение может привести к осложнениям.
Соблюдение всех рекомендаций позволит сгладить неприятные последствия радиотерапии, а также ускорить реабилитацию.
источник
Лучевая терапия — важный компонент комплексного лечения локальных рецидивов (ЛР) рака молочной железы (РМЖ), включающего, как правило, хирургический этап, химио-, гормоно-, таргетную терапию.
Вопрос о необходимости и месте лучевого лечения при возникновении ЛР решается индивидуально в зависимости от клинических проявлений рецидивной опухоли (одиночный или множественные очаги, наличие или отсутствие инфильтративного роста и др.) и проведенного ранее лечения.
Для принятия решения об облучении рецидивной опухоли обязательно цитологическое или гистологическое подтверждение диагноза — рецидив РМЖ.
По данным ряда авторов, локальные рецидивы в 80-85% случаев располагаются в зоне первичной опухоли (табл. 18).
Мягкие ткани передней грудной стенки после радикальная мастэктомия (РМЭ) и оставшаяся часть молочной железы после органосохраняющих операций — зоны наибольшего риска рецидива болезни.
Таблица 18. Частота и локализация ЛР рака молочной железы
| Наблюдение, мес | Число больных | Частота рецидивов после органосохраняющих операций, % | ||
| без лучевой терапии | с лучевой терапией | |||
| NSABP B-06, 1984 | 248 | 1137 | 35 | 14 |
| Scotland, 1991 | 68 | 585 | 24 | 6 |
| Ontario, 1989 | 91 | 837 | 35 | 11 |
| Milan III, 1989 | 109 | 567 | 15 | 3 |
| M. Clarke и соавт., 2005 | 60 | 25 000 | 26 | 7 |
| J. Fodor и соавт., 2005 | 120 | 148 (моложе 40 лет) | 23 | 45 |
| РОНЦ им Н.Н. Блохина, 2007 | 69 | 387 | 21,6 | 5,4 |
Проведение послеоперационной терапии не только снижает частоту ЛР, но и улучшает показатели выживаемости.
По данным M.Clarke и соавт., адъювантная лучевая терапия после органосохраняющих операций снизила риск смерти от РМЖ в течение 15 лет на 5,4% (р=0,0002) и повысила показатели общей выживаемости на 5,3% (р=0,005).
Метаанализ 36 рандомизированных исследований (EBCTCG в 2002 и 2005 г.) показал, что у больных ранним раком молочной железы адъювантная лучевая терапия уменьшает частоту локальных рецидивов, улучшает показатели общей 15-летней выживаемости на 20% за счет уменьшения числа умерших больных от прогрессирования заболевания.
При возникновении ЛР в оставшейся части молочной железы после первичного лечения, включающего только органосохраняющую операцию, вариантами лечения могут быть РМЭ или иссечение местного рецидива опухоли с последующим облучением оставшейся части молочной железы и зон лимфооттока с профилактической целью.
По данным различных авторов, показатели 5-летней безрецидивной выживаемости у больных с изолированным ЛР после проведения радикальной мастэктомии колеблются от 60 до 75%, показатели общей выживаемости — от 80 до 85%.
Показаниями к щадящему методу лечения локальных рецидивов (ЛР) рака молочной железы (РМЖ) являются:
• отсутствие поражения регионарных лимфатических узлов,
• неинвазивный характер рецидивной опухоли,
• длительный срок между проведением первичного лечения и возникновением рецидива (более 2 лет),
• размер рецидивной опухоли не более 2 см и возможность ее иссечения с достижением хорошего косметического эффекта.
В исследовании D. McCready и соавт. из Women’s College Hospital (Канада) показано, что в случае только иссечения локальных рецидивов в оставшейся части молочной железы повторные локальные рецидивы возникли у 69% больных, а в случае дополнения операции лучевой терапией — у 11%.
Облучение оставшейся части молочной железы и зон лимфооттока проводится на гамма-терапевтических аппаратах или на низкоэнергетических линейных ускорителях электронов с использованием фотонного пучка энергией 6 МэВ методом классического фракционирования (разовая очаговая доза (РОД) 2 Гр 5 раз в неделю) в суммарной очаговой дозе (СОД) 50 Гр — на оставшуюся часть молочной железы, СОД на зоны регионарного метастазирования обычно составляет 46 Гр. При больших размерах молочных желез более выгодное дозное распределение достигается при использовании энергии 18 МэВ (рис. 20).
Рис. 20. Дозное распределение при облучении молочной железы с тангенциальных полей фотонами 6 МэВ.
Лечение локального рецидива в оставшейся части молочной железы после органосохраняющей операции и последующей лучевой терапии
Стандартом лечения рецидива в данном случае является выполнение мастэктомии.
Некоторые авторы при возникновении ЛР после проведенного ранее органосохраняющего лечения (органосохраняющая операция + лучевая терапия) в некоторых случаях (например, категорический отказ пациентки от выполнения мастэктомии) считают возможным выполнить только иссечение рецидивной опухоли, частота повторного локального рецидивав таких случаях достигает 20-30%.
B.Salvadori и соавт. приводят данные о лечении 191 больной с рецидивным рак молочной железы. РМЭ была выполнена 134 больным, различного объема иссечение опухоли — 57 больным, медиана прослеженности — 73 мес. Показатели актуриальной 5-летней общей и безрецидивной выживаемости достоверно не разичались. Повторные рецидивы возникли у 4% больных после радикальной мастэктомии и у 19% после реэксцизий.
Некоторые авторы дополняют иссечение рецидивной опухоли облучением даже в случаях проведенной ранее лучевой терапии. Но частота возникновения вторых рецидивов у этих больных сопоставима с показателями в группах больных после только иссечения рецидивной опухоли, а вероятность развития серьезных лучевых повреждений очень высока.
M.Deutsch и соавт. приводят результаты лечения 39 больных с ЛР, развившимися после проведенного ранее органосохраняющего лечения (органосохраняющая операция + лучевая терапия) в среднем через 63 мес (16-291 мес).
Лечение заключалось в иссечении рецидива и повторном облучении ложа удаленной опухоли электронным пучком различных энергий в суммарной очаговой дозе 50 Гр за 25 фракций. Авторы отмечают хорошую переносимость повторного курса облучения и отсутствие выраженных лучевых повреждений кожи при медиане наблюдения 51,5 мес. Повторные ЛР были зарегистрированы у 20,6% больных.
Необходимо помнить, что повторное облучение всегда необходимо проводить с большой осторожностью, при отсутствии признаков лучевых повреждений нормальных тканей, с точным учетом величины подведенных ранее доз, не превышая уровень толерантности нормальных тканей (сердце, легкое), с использованием объемного планирования (рис. 21).
Рис. 21. Локальное облучение ложа удаленной опухоли с 4 полей фотонами энергией 6 МэВ.
Частота возникновения локальных рецидивов на передней грудной стенке после радикальной мастэктомии менее 10%. Терапевтическая тактика в таких случаях должна состоять из хирургического удаления рецидивной опухоли с последующим облучением мягких тканей передней грудной стенки (электронами различных энергий, гамма-лучами, фотонным излучением РОД 2 Гр, СОД 50 Гр) и лимфатических коллекторов в суммарной очаговой дозе 44-46 Гр с профилактической целью.
По данным голландских онкологов L. Diepenmaat и соавт., при медиане наблюдения 7,2 года ЛР у больных инвазивным дольковым раком после проведенной РМЭ возникли в 8,7% случаев, при дополнении операции лучевой терапией — в 2,1% (р=0,002).
Как правило, лечение рецидивов в области передней грудной стенки является комплексным, включающим хирургический, лучевой и лекарственный методы. Обнадеживающие результаты лечения 145 больных с ЛР после проведенной ранее радикальной мастэктомии были показаны в исследовании немецких коллег J. Willner и соавт.
Лечение включало хирургическое удаление опухоли у 74%, мегавольтное облучение у 83%, гормональной терапии у 41% и химиотерапии у 12% пациентов, использовались различные комбинации. Местный контроль был достигнут у 86% больных (медиана наблюдения составила 8,9 года).
При возникновении рецидива на грудной стенке в случае проведения ранее лучевой терапии целесообразно хирургическое иссечение рецидива с последующим системным лечением. Облучение послеоперационного рубца нецелесообразно.
Лечение множественных рецидивных очагов в области передней грудной стенки с инфильтративным ростом при невозможности выполнения хирургического этапа лечения
Наиболее рациональным является широкое облучение грудной стенки с использованием классического фракционирования дозы. Суммарная доза определяется предшествующим лечением и остаточной толерантностью нормальных тканей.
Если ранее лучевая терапия не проводилась, то помимо послеоперационного рубца в зону облучения целесообразно включать и зоны регионарного метастазирования (шейно-надподключичную, подмышечную, парастернальную) на стороне поражения с профилактической целью в СОД 46 Гр. Для выравнивания поверхности тела, достижения равномерного дозного распределения используется тканеэквивалентный «болюс».
Одним из вариантов лечения является проведение облучения на фоне использования специальных салфеток с трансдермальным химиопрепаратом 5-фторурацил «Колетекс-5-фтур».
При развитии рецидива в регионарных лимфатических узлах целесообразно проведение комбинированного лечения, которое начинается с лекарственного этапа с последующим обсуждением использования лучевой терапии.
Перед началом любого вида терапии обязательна верификация диагноза, что особенно сложно при локализации процесса в подключичной зоне, в верхнеаксиллярных лимфатических узлах. В таких случаях большую помощь в диагностике оказывает проведение компьютерной томографии (КТ) с внутривенным введением контрастного вещества, магниторезонансная томография (МРТ).
При полной регрессии рецидивной опухоли после завершения лекарственного воздействия возможна тактика «наблюдай и жди», но чаще во втором этапе лечения используется лучевой метод.
Если область рецидива ранее не облучалась, то целесообразно на всю анатомическую область расположения рецидива (например, шейно-надподключичная; подмышечная с включением всех трех уровней аксиллярных лимфатических узлов) подвести методом классического фракционирования (разовая очаговая доза 2 Гр) суммарная очаговая доза 46-50 Гр, затем локально на определяемый рецидив подвести дополнительно 12-16 Гр.
Для точного определения зоны локального облучения целесообразно до начала комбинированного лечения провести «разметку» рецидива под контролем КТ или ультразвуковое исследование (УЗИ) с отметкой проекции пораженных лимфатических узлов на коже и определением глубины их залегания.
Если ранее лучевая терапия не проводилась, то в зону облучения целесообразно включать и переднюю грудную стенку на стороне поражения, РОД 2 Гр, СОД 46-50 Гр, и все лимфоколлекторы с профилактической целью, суммарной очаговой дозе 46 Гр.
Для снижения вероятности возникновения выраженных химиолучевых повреждений кожи, слизистых, сердечной и легочной ткани целесообразно лекарственный и лучевой этапы лечения проводить последовательно, а не одновременно.
Как правило, в объем облучения включаются вся молочная железа и передняя грудная стенка (при этом неизбежно в зону облучения попадает и небольшая часть прилежащего легкого).
Верхняя граница тангенциальных полей при облучении молочной железы должна отступать от пальпируемой ткани молочной железы на 2 см, обычно это уровень второго межреберья, в случае проведения лучевой терапии и на зоны лимфооттока верхней границей является нижний край ключицы; внутренняя — на 1 см кнаружи от срединной линии тела (по латеральному краю парастернального поля, если оно входит в зону облучения); наружная — по средней подмышечной линии или на 2 см кнаружи от пальпируемой ткани молочной железы; нижняя граница — на 2 см ниже маммарной складки; при локализации рецидивной опухоли в нижних квадрантах молочной железы эту границу опускают до 3 см, а при поражении маммарной складки — до 5 см.
Для адекватного включения в зону облучения всей ткани молочной железы и передней грудной стенки следует обращать внимание на положение коллиматора при лечении с тангенциальных полей. Особое внимание уделяется снижению дозы на легкое и сердце при равномерном облучении ткани молочной железы.
При облучении перелней грулной стенки верхней границей является нижний край ключицы, нижняя граница расположена на уровне переходной складки другой молочной железы.
При выборе парастернального поля исходят из того, что одноименные лимфатические узлы находятся вдоль a.mammaria interna, расположенной на 1 см кнаружи от края грудины. Кроме того, известно, что более чем в 80% случаев специфическое поражение выявляется в первых четырех межреберьях.
Вследствие этого парастернальная зона облучения должна охватывать верхние 6 межреберных промежутков; верхней ее границей является нижний край надключичного поля, нижней — мечевидный отросток, медиальной границей поля служит средняя линия тела; ширина парастернального поля составляет, как правило, 5-6 см. При определении СОД на парастернальные лимфатические узлы необходимо учитывать дозу, доставленную от облучения молочной железы или передней грудной стенки.
Границами надподключично-подмышечной зоны облучения являются: верхняя — граница средней и нижней трети сосудистого пучка шеи, нижняя — второе межреберье, медиальная — срединная линия тела, наружная — латеральнее всей аксиллярной области с включением части сосудистого пучка на плече.
В случае необходимости облучения только надподключичной зоны наружная граница поля находится у головки плечевой кости. На рис. 22 представлены границы полей при облучении молочной железы, зон лимфооттока.
Рис. 22. Границы полей при облучении молочной железы, зон лимфооттока.
Перед началом лучевого лечения проводится топометрическая подготовка на рентгеновских симуляторах для уточнения центров и границ облучения и объемов тканей, подлежащих блокированию защитными свинцовыми блоками. Для уточнения размеров и распространения первичной опухоли и регионарных метастазов, а также для изготовления топографо-анатомических срезов с отражением границ легочной ткани, органов средостения выполняется компьютерная томография.
Программа облучения должна выбираться индивидуально для каждой больной с учетом локализации, границ распространения опухолевого процесса и конституциональных особенностей женщины с помощью современных планирующих систем («ROCS», «СADPLAN», «HELAX», «Тонкий луч», «XIO» и др.).
Использование 3D-конформной лучевой терапии оптимизирует лучевое воздействие на грудную стенку и лимфоколлекторы, значительно сокращает лучевую нагрузку на сердце и легочную ткань. Для проведения 3D-конформной лучевой терапии больной выполняется 3D-планирование, на каждом КТ-срезе обозначаются органы риска, лечебные объемы (GTV, CTV, PTV), производятся 3D-реконструкция, расчет лечебных программ с выполнением дозно-объемных гистограмм (рис. 23).
Рис. 23. Пример ЗР-планирования
Проверку правильности размеров, конфигурации и взаимного расположения полей облучения в процессе проведения курса лучевого лечения следует проводить не менее двух-трех раз, используя рентгеновские симуляторы, гаммаграммы на дистанционном лучевом аппарате.
Лучевая терапия рецидивов рака молочной железы требует соблюдения дополнительных условий:
1. Адекватность кожной дозы (в отличие от раннего рака при распространенных и рецидивных опухолях часто имеется вовлечение в опухолевый процесс кожи и подкожной клетчатки). Для выравнивания поверхности тела, достижения равномерного дозного распределения используется тканеэквивалентный болюс.
Он помещается непосредственно на поверхность тела, результатом чего является увеличение дозы в коже и других поверхностных структурах непосредственно под ним. Для изготовления болюса используют парафин, влажную марлю, пластины из пластических полимеров. Клинические наблюдения показывают, что, исходя из толерантности кожи, использование болюса возможно на протяжении 40-60% курса облучения (или ежедневно, или через день).
2. Минимальное подведение дозы на легкое, на ткань другой молочной железы.
3. Точное соблюдение стыковки между нижней границей надподключичной области и верхней границей тангенциальных полей.
4. Предлучевая подготовка, симуляция и облучение проводятся на специальной подставке, позволяющей фиксировать положение тела пациентки (рис. 24).
Рис. 24. Специальное фиксирующее приспособление для проведения лечения больных с заболеванием молочной железы.
Таким образом, рациональное применение лучевой терапии не только способствует улучшению результатов лечения первичных проявлений рака молочной железы, но играет также важную роль в терапии различных клинических вариантов рецидивов заболевания.
И.В. Поддубная, Д.В. Комов, И.В. Колядина, О.П. Трофимова
источник