Анастрозол — инструкция по применению, отзывы, аналоги и формы выпуска (таблетки 1 мг Тева, ТЛ, Каби) лекарственного препарата для лечения рака молочной железы или груди у взрослых, детей и при беременности. Состав противоопухолевого средства
В данной статье можно ознакомиться с инструкцией по применению лекарственного препарата Анастрозол. Представлены отзывы посетителей сайта — потребителей данного лекарства, а также мнения врачей специалистов по использованию Анастрозола в своей практике. Большая просьба активнее добавлять свои отзывы о препарате: помогло или не помогло лекарство избавиться от заболевания, какие наблюдались осложнения и побочные эффекты, возможно не заявленные производителем в аннотации. Аналоги Анастрозола при наличии имеющихся структурных аналогов. Использование для лечения рака молочной железы или груди у взрослых, детей, а также при беременности и кормлении грудью. Состав препарата.
Анастрозол — противоопухолевый препарат, ингибитор синтеза эстрогенов.
Анастрозол является высокоселективным нестероидным ингибитором ароматазы — фермента, с помощью которого у женщин в постменопаузе андростендион в периферических тканях превращается в эстрон и далее в эстрадиол. Снижение концентрации циркулирующего эстрадиола у больных раком молочной железы оказывает терапевтический эффект. У женщин в постменопаузе анастрозол в суточной дозе 1 мг вызывает снижение концентрации эстрадиола на 80%.
Анастрозол не обладает прогестагенной, андрогенной и эстрогенной активностью. В суточных дозах до 10 мг не оказывает эффекта на секрецию кортизола и альдостерона, следовательно, при применении анастрозола не требуется заместительного введения кортикостероидов.
Анастрозол + вспомогательные вещества.
Фармакокинетика
После приема внутрь анастрозол быстро всасывается из ЖКТ. Пища незначительно уменьшает скорость всасывания, но не его степень и не приводит к клинически значимому влиянию на равновесную концентрацию препарата в плазме крови при однократном приеме суточной дозы анастрозола. Сведений о зависимости фармакокинетических параметров анастрозола от времени или дозы нет. Связь с белками плазмы крови — 40 %. Анастрозол экстенсивно метаболизируется у женщин в постменопаузе, при этом менее 10% экскретируется почками в неизмененном виде в течение 72 ч после приема препарата. Метаболизм анастрозола осуществляется N-деалкилированием, гидроксилированием и глюкуронидацией. Метаболиты анастрозола выводятся преимущественно почками. Основной метаболит анастрозола — триазол, определяемый в плазме крови, не обладает фармакологической активностью. Фармакокинетика анастрозола не зависит от возраста женщин в постменопаузе.
- адъювантная терапия раннего рака молочной железы, с положительными гормональными рецепторами у женщин в постменопаузе, в т.ч. после 2-3 летней адъювантной терапии тамоксифеном;
- первая линия терапии местно-распространенного или метастатического рака молочной железы, с положительными или неизвестными гормональными рецепторами у женщин в постменопаузе;
- вторая линия терапии распространенного рака молочной железы, прогрессирующего после лечения тамоксифеном.
Формы выпуска
Таблетки, покрытые оболочкой 1 мг.
Инструкция по применению и режим дозирования
Назначают по 1 мг 1 раз в сутки. Таблетку следует проглатывать целиком, запивая водой.
Рекомендуется принимать препарат в одно и то же время вне зависимости от приема пищи.
Продолжительность курса лечения зависит от формы и тяжести заболевания (при адъювантной терапии рекомендуемая продолжительность лечения — 5 лет). При появлении признаков прогрессирования заболевания прием препарата следует прекратить.
Побочное действие
- «приливы» крови к лицу;
- артралгия;
- триггерный палец;
- сухость слизистой оболочки влагалища;
- влагалищные кровотечения (в основном в течение первых недель после отмены или смены предшествующей гормональной терапии на анастрозол);
- кожная сыпь;
- истончение волос;
- алопеция;
- многоформная эритема (синдром Стивенса-Джонсона);
- тошнота, рвота;
- диарея;
- анорексия;
- повышение активности АЛТ, АСТ и ЩФ;
- повышение активности ГГТ и концентрации билирубина;
- гепатит;
- головная боль;
- повышенная сонливость;
- синдром запястного канала (в основном наблюдался у пациенток с факторами риска по данному заболеванию);
- гиперхолестеринемия;
- остеопороз и переломы костей;
- аллергические реакции;
- анафилактоидные реакции;
- ангионевротический отек;
- крапивница;
- анафилактический шок;
- астения.
Противопоказания
- пременопаузный период;
- выраженная печеночная недостаточность (безопасность и эффективность не установлена);
- сопутствующая терапия тамоксифеном или препаратами, содержащими эстрогены;
- беременность;
- период лактации (кормления грудью);
- детский возраст (безопасность и эффективность у детей не установлена);
- повышенная чувствительность к анастрозолу или другим компонентам препарата.
Применение при беременности и кормлении грудью
Противопоказано применение препарата Анастрозол при беременности и в период грудного вскармливания.
Применение у детей
Противопоказан детям и подросткам в возрасте до 18 лет. Безопасность и эффективность у детей не установлена.
Особые указания
В случае сомнений в гормональном статусе пациентки менопауза должна быть подтверждена определением концентрации половых гормонов в сыворотке крови.
В случае сохраняющегося маточного кровотечения на фоне приема анастрозола необходима консультация и наблюдение гинеколога.
Нет данных о применении препарата у пациенток с тяжелой степенью нарушений функции печени.
У пациенток с остеопорозом или с повышенным риском развития остеопороза, минеральную плотность костной ткани следует оценивать методом денситометрии, например, DEXA-сканированием (двухэнергетическая рентгеновская абсорбциометрия) в начале лечения и регулярно на его протяжении. При необходимости следует назначать лечение или профилактику остеопороза и тщательно наблюдать за состоянием пациентки.
Поскольку анастрозол снижает концентрацию циркулирующего эстрадиола, это может привести к снижению минеральной плотности костной ткани. На настоящий момент отсутствуют достаточные данные относительно положительного влияния бисфосфонатов на потерю минеральной плотности костной ткани, вызванной анастрозолом или их пользы при применении с целью профилактики.
Нет данных об одновременном применении анастрозола и препаратов — аналогов ГнРГ.
У женщин с рецептороотрицательной опухолью к эстрогенам эффективность анастрозола не была продемонстрирована, кроме тех случаев, когда имелся предшествующий положительный клинический ответ на тамоксифен.
Препараты, содержащие эстрогены, не должны назначаться одновременно с анастрозолом, т.к. эти препараты будут нивелировать его фармакологическое действие.
Эффективность и безопасность анастрозола и тамоксифена при их одновременном применении вне зависимости от статуса гормональных рецепторов сравнимы с таковыми при использовании одного тамоксифена. Точный механизм данного явления пока не известен.
Неизвестно, улучшает ли анастрозол результаты лечения при совместном использовании с химиотерапией.
Влияние на способность к вождению автотранспорта и управлению механизмами
Некоторые побочные эффекты анастрозола, такие как астения и сонливость, могут отрицательно влиять на способность выполнения работы, требующей повышенной концентрации внимания и быстроты психомоторных реакций. В связи с этим рекомендуется при появлении этих симптомов соблюдать осторожность при управлении транспортными средствами и механизмами.
Лекарственное взаимодействие
Исследования по лекарственному взаимодействию с феназоном и циметидином указывают на то, что совместное применение анастрозола с другими препаратами вряд ли приведет к клинически значимому лекарственному взаимодействию, опосредованному цитохромом Р450.
Клинически значимое лекарственное взаимодействие при приеме анастрозола одновременно с другими часто назначаемыми препаратами отсутствует.
На данный момент нет сведений о применении анастрозола в комбинации с другими противоопухолевыми препаратами.
Анастрозол снижает эффективность эстрогенов.
Не следует назначать тамоксифен одновременно с анастрозолом поскольку он может ослабить фармакологическое действие последнего.
Аналоги лекарственного препарата Анастрозол
Структурные аналоги по действующему веществу:
- Аксастрол;
- Анабрез;
- Анамастэн;
- Анастера;
- Анастрозол Каби;
- Анастрозол Тева;
- Анастрозол ТЛ;
- Анастрэкс;
- Аримидекс;
- Веро Анастрозол;
- Селана;
- Эгистразол.
Аналоги по лечебному эффекту (средства для лечения новообразований молочной железы):
- Абитаксел;
- Авастин;
- Алкеран;
- Аминоглутетимид;
- Аромазин;
- Билем;
- Бусерелин депо;
- Вепезид;
- Винельбин;
- Винкристин;
- Гемцитабин медак;
- Герцептин;
- Гормоплекс;
- Депостат;
- Доксолем;
- Доксорубифер;
- Доксорубицин;
- Зитазониум;
- Золадекс;
- Зомета;
- Икземпра;
- Интаксел;
- Кабецин;
- Карбоплатин;
- Келикс;
- Клобир;
- Кселода;
- Ледоксина;
- Лейкеран;
- Летрозол;
- Летротера;
- Ломустин;
- Люкрин депо;
- Маверекс;
- Мамомит;
- Метотрексат;
- Милтекс;
- Митоксантрон;
- Митотакс;
- Навельбин;
- Новантрон;
- Новофен;
- Нолвадекс;
- Омнадрен 250;
- Онкотрон;
- Ориметен;
- Паклитаксел;
- Паксен;
- Рубида;
- Тайверб;
- Таксол;
- Таксотер;
- Тамоксен;
- Тамоксифен;
- Таутакс;
- Тиотепа Тиоплекс;
- Фазлодекс;
- Фемара;
- Фторафур;
- Фторурацил;
- Халавен;
- Циклофосфан;
- Цитоксан;
- Экстраза;
- Элдезин;
- Эндоксан;
- Эписиндан
- Этопозид;
- Ютаксан.
источник
Анастрозол (аримидекс) — это препарат ингибиторов ароматазы и уже многие годы используется в лечении распространенного гормонально-позитивного рака молочных желез у пациенток в постменопаузе.
В октябре 2005 года управление по контролю за пищевыми продуктами и лекарственными препаратами США (FDA) одобрило применение анастрозола в качестве адъювантной терапии у пациенток с ранними стадиями рака молочной железы.
Исследование, которое называлось АТАС (Arimidex or Tamoxifen Alone or in Combination – сравнение аримидекса и тамоксифена по отдельности и в сочетании), началось в 1999 году и предположительно закончится в 2011 году.
Целью проводимого исследования является выяснение эффективности отдельного и сочетанного применения анастрозола и тамоксифена у пациенток с ранними стадиями гормонально-позитивного рака молочной железы.
В исследовании участвовало 9300 пациенток в постменопаузе с ранними стадиями гормонально-позитивного рака молочной железы, которые только что прошли первый этап лечения (операцию с или без химио- и радиотерапии).
Пациенткам назначался либо анастрозол, либо тамоксифен, либо оба препарата сразу. Исследователи наблюдали за пациентками в течение 5 лет. Они отмечали, какие побочные эффекты встречались в каждой группе пациенток и как часто наблюдался рецидив рака, метастазирование или летальный исход.
Исследователи продолжат наблюдать за этими пациентками еще 5 лет. Представим полученные результаты данного исследования.
При отдельном применении анастрозол оказался намного эффективнее, чем тамоксифен:
В снижении риска рецидива рака,
В снижении риска распространения рака (метастазирования),
В снижении риска развития нового рака в другой молочной железе.
В снижении риска летального исхода от рака.
Анастрозол при отдельном применении оказался намного эффективнее, чем сочетание аримидекса с тамоксифеном.
Улучшения отмечались у пациенток с различными типами гормонально-позитивного рака: эстроген-позитивного, прогестерон-позитивного и их сочетании. У пациенток, принимавших аримидекс, отмечалось меньше проявлений менопаузы и меньше случаев рака матки, тромбозов и инсультов. Однако при приеме аримидекса отмечалось большее число болей в суставах и переломов костей.
Так как проблемы с суставами и костной системой при применении анастрозола встречаются чаще, чем при приеме тамоксифена, рекомендуется проконсультироваться с врачом в плане исследования состояния костной ткани до начала лечения либо назначения препаратов, укрепляющих костную ткань.
Если у Вас постменопаузальный период и у Вас гормонально-позитивный рак молочной железы, Вы вполне можете принимать анастрозол. Однако, прежде всего, проконсультируйтесь с Вашим лечащим врачом.
Длительность приема анастразола — принимайте анастрозола до тех пор, пока Ваш врач не скажет Вам о прекращении необходимости его принимать. В исследовании АТАС, которое продолжается и сейчас, было показано преимущество анастрозола над тамоксифеном в снижении риска рецидива рака молочной железы у женщин в постменопаузе в течение 5 лет.
Анастрозол представляет собой таблетированный препарат и принимают его по одной таблетке в день. Рекомендуется принимать аримидекс в одно и то же время. Если Вы забыли принять таблетку, то примите ее сразу, как Вы вспомнили об этом, либо просто примите следующую дозу как обычно, но не пытайтесь принять две таблетки за один раз.
Побочные эффекты анастрозола
В клинических исследованиях было выявлено, что наиболее частыми побочными эффектами анастрозола были:
повышенное артериальное давление,
Кроме того, при приеме анастрозола чаще отмечались патологические переломы костей, чем при приеме тамоксифена (10 % и 7 % соответственно).
Анастрозол не следует применять в следующих ситуациях:
При аллергических реакциях на анастрозол и другие компоненты анастрозола.
При грудном вскармливании.
При беременности, либо если Вы возможно беременны или планируете беременность.
источник

Председатель Российского общества клинической онкологии,
заведующий отделением клинической фармакологии и химиотерапии,
заместитель директора по научной работе
ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России,
доктор медицинских наук, профессор,
Москва
Адъювантная гормональная терапия существенно изменила прогноз больных раком молочной железы с наличием рецепторов эстрогенов и прогестерона в опухоли. При назначении тамоксифена отмечается снижение на 50% частоты рецидива на фоне приема препарата и на 30% в следующие 5 лет после прекращения его приема. Это сопровождается снижением смертности на 30% в течение 15 лет с начала приема тамоксифена. Ингибиторы ароматазы в течение 5 лет обладают еще большим эффектом в сравнении с тамоксифеном, уменьшая риск прогрессирования на 30% за период приема и на 15% риск смерти в первые 10 лет. Однако накопленный опыт показывает, что после прекращения 5-летнего приема тамоксифена или ингибиторов ароматазы у больных сохраняется риск отсроченного прогрессирования. Это послужило основанием для проведения исследований по увеличению сроков адъювантной гормонотерапии.
Увеличение продолжительности приема тамоксифена было изучено в двух опубликованных на сегодняшний день исследованиях (таблица 1). В исследовании NSABP-14 увеличение продолжительности приема до 10 лет не привело к улучшению отдаленных результатов. В это исследование включались больные с N0, а значит с низким риском прогрессирования, что не позволило выявить потенциально возможную пользу длительного приема тамоксифена. В исследовании ATLAS увеличение продолжительности приема тамоксифена с 5 до 10 лет привело к достоверному снижению риска прогрессирования и смерти. При этом польза от длительного приема тамоксифена становится достоверной отсроченно, только после прекращения 10-летнего приема препарата. Причиной улучшения результатов лечения является уменьшение частоты локальных рецидивов заболевания, возникновения контрлатерального рака молочной железы (профилактический эффект) и незначительное снижение частоты отдаленных метастазов. В обоих исследованиях отмечено снижение частоты и выраженности ишемической болезни сердца, отсутствие увеличения частоты инсультов и тромбоэмболий и увеличение в 2 раза (с 2-3% до 4-5%) частоты возникновения рака эндометрия.
Таблица 1. Результаты рандомизированных исследований
по сравнению продленной и стандартной адъювантной гормонотерапии.
| Исследование | Число больных | Лечение | Срок наблюдения после рандомизации | БРВ | OВ |
|---|---|---|---|---|---|
| NSABP B-14 [1] | 1172 | Тамоксифен 5 лет Плацебо 5 лет | 7 лет | 78% 82% | 91% 94% |
| ATLAS [2] | 6846 | Тамоксифен 5 лет Плацебо 5 лет | 10 лет | 78,6%* 74,9% | 87,8%* 85% |
| MA.17 [3] | 1918 | Летрозол 5 лет Плацебо 5 лет | 5 лет | 95%* 91% | 93% 94% |
| NSABP B-42 [4] | 3966 | Летрозол 5 лет Плацебо 5 лет | 7 лет | 84,7% 81,3% | Н.Д. |
| IDEAL [5] | 1824 | Летрозол 5 лет Летрозол 2,5 года | 6,6 года | 82% 85,4% | Н.Д. |
| ABCSG-16 [6] | 3482 | Анастрозол 5 лет Анастрозол 2 года | 5 лет | 78% 78% | Н.Д. |
* – статистически достоверная разница;
Н.Д. – нет данных.
Ингибиторы ароматазы продемонстрировали большую эффективность в сравнении с тамоксифеном при проведении адъювантной гормонотерапии больным раком молочной железы с наличием рецепторов стероидных гормонов в опухоли. В связи с этим стало актуальным изучить клиническую эффективность увеличения продолжительности приема ингибиторов ароматазы по сравнению со стандартным 5-летним приемом. В таблице 1 приведены результаты исследования по изучению продленной терапии ингибиторами ароматазы. Следует отметить, что только одно исследование MA.17 опубликовано в полном виде, для всех остальных исследований известна только безрецидивная выживаемость и токсичность терапии. В исследовании MA.17 прием летрозола в течение 5 лет после окончания 5-летней терапии тамоксифеном (79% больных) или ингибиторами ароматазы (21%) привел к достоверному снижению безрецидивной выживаемости, не оказав влияния на общую. Отмечено, что основной причиной снижения безрецидивной выживаемости стало уменьшение частоты контрлатерального рака. В исследования NSABP B-42 10-летний прием летрозола не повлиял на частоту прогрессирования заболевания по сравнению с 5-летним приемом тамоксифена или ингибиторов ароматазы. Анализ токсичности демонстрирует увеличение риска развития сердечно-сосудистых заболеваний и костных переломов на фоне длительного приема препаратов. Риск развития переломов повышается после 7 лет приема ингибиторов ароматазы.
Два исследования посвящены определению оптимальной продолжительности проведения адъювантной гормонотерапии. Дополнительные 5 лет приема были выбраны эмпирически, и остается актуальным сокращение сроков проведения адъювантной терапии для удобства пациентов и уменьшения риска развития побочных эффектов. В исследовании IDEAL сравнивается дополнительное назначение летрозола в течение 2,5 и 5 лет после ранее проведенной стандартной 5-летней адъювантной терапии. При медиане наблюдения 6,6 года после рандомизации не отмечено разницы в показателях безрецидивной и общей выживаемости. Длительный прием летрозола сочетался со снижением частоты контрлатерального рака.
В исследовании ABCSG-16 больным раком молочной железы с наличием рецепторов стероидных гормонов в опухоли и отсутствием амплификации HER2, получавшим адъювантную терапию тамоксифеном или ингибиторами ароматазы в течение 5 лет, назначали дополнительный прием анастрозола в течение 2 или 5 лет. В исследование были включены 3484 больные без признаков болезни на момент рандомизации после 5 лет адъювантной терапии. Стратификация проводилась в зависимости от проводимой гормонотерапии в первые 5 лет (тамоксифен или ингибиторы ароматазы). Предварительные результаты, доложенные на прошедшем симпозиуме по раку молочной железы в Сан-Антонио (США) в декабре 2017 года, свидетельствуют, что частота развития прогрессирования заболевания была одинаковой в обеих группах, безрецидивная выживаемость составила 78% и не зависела от вида гормонотерапии в первые 5 лет. Не отмечено разницы в развитии контрлатерального рака молочной железы. В группе длительного приема анастрозола отмечается повышение частоты костных переломов после 3-го года приема. Авторы делают вывод, что увеличение продолжительности адъювантной терапии на 2 года (всего 7 лет) эффективно предотвращает прогрессирование рака молочной железы и предохраняет от развития побочных эффектов, обусловленных длительным приемом ингибиторов ароматазы. Добавление ингибиторов ароматазы в течение 5 лет не дает выигрыша в улучшении отдаленных результатов и сопровождается увеличением побочных эффектов.
Приведенные исследования показывают, что назначение тамоксифена или ингибиторов ароматазы в течение 7-10 лет может приводить к выигрышу в безрецидивной и общей выживаемости по сравнению с 5-летним их назначением. Очевидно, что выигрыш этот отмечается лишь у меньшинства пациенток, в то время как большинство напрасно получают потенциально токсичную терапию со снижением качества жизни. Поэтому важно при обсуждении увеличения продолжительности гормонотерапии оценивать риск дальнейшего прогрессирования после 5 лет адъювантной гормонотерапии у каждой конкретной больной. Этому было посвящено исследование Оксфордской группы EBCTCG (Early Breast Cancer Trialists Collaborative Group) [7].
Были обобщены 88 исследований по 5-летнему назначению адъювантной гормонотерапии и оценен риск прогрессирования и смерти в течение 15 (5-20) лет после прекращения приема в зависимости от различных прогностических факторов.
Результаты наблюдения за больными в последующие 15 лет после 5-летнего прекращения гормонотерапии демонстрируют увеличение кумулятивного риска прогрессирования и смерти от рака молочной железы. Риск прогрессирования и последующей смерти от рака молочной железы напрямую связан с наличием метастазов и их числом в подмышечных лимфоузлах (см. таблицу 2). В первые 5 лет приема гормональных препаратов наблюдается существенное отставание риска смерти от частоты развития прогрессирования заболевания. Однако при наблюдении в течение 20 лет частота смерти от рака молочной железы догоняет частоту рецидивирования и составляет в зависимости от метастатического поражения подмышечных лимфоузлов 15%, 28% и 49%.
Таблица 2. Риск прогрессирования и смерти при проведении гормонотерапии в течение 5 лет.
| Частота рецидивов | Частота смерти | |||
|---|---|---|---|---|
| 5-летняя | 20-летняя | 5-летняя | 20-летняя | |
| N0 | 6% | 22% | 3% | 15% |
| N1-3 | 10% | 31% | 5% | 28% |
| N4-9 | 22% | 52% | 12% | 49% |
Авторы изучили, какие клинические факторы в наибольшей степени определяют риск прогрессирования после прекращения приема гормонов за период 5-20 лет. Оказалось, что, несмотря на то, что на период 5 лет все больные не имели признаков прогрессирования заболевания, размер первичной опухоли и состояние подмышечных лимфоузлов в момент постановки диагноза в наибольшей степени предсказывали риск прогрессирования в последующие после прекращения приема гормональных препаратов годы. Минимальный ежегодный риск прогрессирования менее 1% и кумулятивный в 13% на период 20 лет отмечается у больных с T1N0. С увеличением размера первичной опухоли и числа метастазов в подмышечные лимфоузлы растет как ежегодный, так и кумулятивный риск прогрессирования, достигая максимальных значений 2,8% и 41% при T2N4-9. У больных с T1N0 на частоту прогрессирования оказывала влияние степень дифференцировки, увеличивая его с 10% при высокой степени до 17% при низкой.
Таким образом, проведенное исследование подтвердило, что после прекращения приема гормональных препаратов в течение 5 лет в последующие годы происходит увеличение риска прогрессирования, степень которого зависит от размера первичной опухоли, наличия и числа метастазов в подмышечных лимфоузлах. Все это оправдывает и объясняет целесообразность увеличения продолжительности приема тамоксифена или ингибиторов ароматазы у больных с высоким риском прогрессирования. При обсуждении необходимости продолжения гормонотерапии после 5 лет приема исследование EBCTCG помогает оценить риск прогрессирования и принять правильное решение.
Можно ли с большей точностью определить популяцию больных, которым показано проведение продленной адъювантной гормонотерапии? Возможно, использование генетических тестов (например, Oncotype DX или MammaPrint) с лучшей точностью в сравнении со стадией болезни позволит выявить пациентов с высоким риском прогрессирования после 5 лет адъювантной терапии. Но пока отсутствуют результаты таких исследований, практический интерес представляет исследование по изучению циркулирующих опухолевых клеток у больных после 5 лет адъювантной гормонотерапии [8]. В исследование, которое было представлено на конференции по раку молочной железы в Сан-Антонио в 2017 году, включались больные раком молочной железы II-III стадий с отсутствием экспрессии HER2, которым проводилась адъювантная химиотерапия с добавлением и без бевацизумаба (исследование E5103). Затем больным с наличием рецепторов стероидных гормонов назначали адъювантную гормонотерапию. У 546 больных без признаков прогрессирования выполняли определение наличия циркулирующих опухолевых клеток в крови методом CELLSEARCH CTC assay в период 4,5-7 лет с момента постановки диагноза.
Оказалось, что циркулирующие опухолевые клетки определяются у 4,8% больных: у больных с наличием рецепторов стероидных гормонов – 5,1%, при отрицательных рецепторах – 4,3%. При медиане наблюдения 1,6 года после выполнения теста наличие циркулирующих опухолевых клеток увеличивает риск прогрессирования в 20 раз у больных с положительными рецепторами и не влияет на частоту прогрессирования при отрицательных рецепторах. Было показано, что риск прогрессирования в ближайшие 2 года у больных с положительными рецепторами и наличием циркулирующих опухолевых клеток и без них составляет 35% и 2% соответственно. Авторы посчитали полученные результаты неожиданными. Первой неожиданностью было обнаружение циркулирующих опухолевых клеток у больных без признаков болезни после 5 лет интенсивной адъювантной химиогормонотерапии. Второй неожиданностью была высокая предсказывающая способность прогрессирования заболевания в случае обнаружения циркулирующих опухолевых клеток только у больных с наличием рецепторов стероидных гормонов в опухоли. И третья неожиданность – это быстрое прогрессирование болезни в этой группе больных после окончания адъювантной гормонотерапии.
Авторы делают вывод, что обнаружение циркулирующих опухолевых клеток у больных с наличием рецепторов стероидных гормонов в момент окончания 5-летнего приема адъювантной гормонотерапии является четким биомаркером быстрого прогрессирования заболевания в ближайшие годы после ее окончания. Можно предположить, что определение опухолевой ДНК в плазме крови больных после 5-летнего приема гормональной адъювантной терапии также может служить индикатором присутствия микрометастазов и высокого риска прогрессирования. Возможно, именно эти больные выигрывают от увеличения продолжительности адъювантной гормонотерапии, а тест на определение циркулирующих опухолевых клеток или опухолевой ДНК будет обязательным для определения оптимальной продолжительности гормонотерапии. Можно думать, что в группе больных с высоким риском прогрессирования будут найдены более эффективные методы лечения в сравнении с увеличением только продолжительности приема гормональных препаратов. Добавление ингибиторов циклинзависимых киназ приведет не только к повышению эффективности адъювантной гормонотерапии, но и к возможному сокращению сроков ее проведения. Интересным представляется назначение ингибиторов контрольных точек иммунного ответа у больных с микрометастазами рака молочной железы после проведения начального этапа гормонотерапии.
Исходя из полученных данных, можно сделать следующие выводы:
- Увеличение продолжительности адъювантной гормонотерапии обладает недостаточной эффективностью, улучшая показатели 10-летней безрецидивной выживаемости на 3-4%. Это обусловлено как резистентностью опухолевых клеток к проводимой более 5 лет гормонотерапии, так и отсутствием селекции больных, которые выигрывают в наибольшей степени от увеличения ее продолжительности.
- У больных с негативными факторами риска (в первую очередь по распространенности опухолевого процесса) можно рекомендовать следующие варианты продленной гормонотерапии:
- при первоначальном приеме тамоксифена 5 лет продление можно осуществить за счет дополнительного назначения тамоксифена еще на 5 лет или ингибиторов ароматазы на 2 года;
- при назначении ингибиторов ароматазы в качестве адъювантной гормонотерапии ее продолжительность должна составлять 5 лет. Проведенные исследования свидетельствуют о возможной пользе увеличения этого срока до 7 лет, что требует подтверждения в дополнительных исследованиях;
- при первоначальном приеме тамоксифена в течение 2-3 лет с последующим переходом на ингибиторы ароматазы в течение еще 2-3-лет можно рекомендовать продление приема ингибиторов до суммарной продолжительности их приема в течение 5 лет.
- Актуальным является поиск биомаркеров, предсказывающих высокий риск прогрессирования после 5 лет гормонотерапии. Именно в популяции больных с высоким риском прогрессирования следует определить как оптимальную продолжительность адъювантной терапии, так и препараты для ее проведения.
Ключевые слова: рак молочной железы, адъювантная гормонотерапия.
- Fisher B, Dignam J, Bryant J, et al. Five versus more than 5 years of tamoxifen for lymph node negative breast cancer: Updated findings from the National Surgical Adjuvant Breast and Bowel Project B-14 randomized trial. J. Natl. Cancer Inst. 2001; 93: 684-690.
- Davies C, Pan H, Godwin J, et al. Long-term effects of continuing adjuvant tamoxifen to 10 years versus stopping at 5 years after diagnosis of oestrogen.receptor-positive breast cancer: ATLAS, a randomised trial. Lancet. 2013; 381: 805-816.
- Goss P, Ingle J, Pritchard K, et al. Extending aromatase-inhibitor adjuvant therapy to 10 years. N. Engl. J. Med. 2016; 375: 209-219.
- Mamounas P, Bandos H, Lembersky C, et al. A randomized, double blinded, placebo-controlled clinical trial of extended adjuvant endocrine therapy with letrozole in postmenopausal women with hormone-receptor breast cancer who have completed previous adjuvant therapy with an aromatase inhibitor: results from NRG Oncology/NSABP B-42. 2016 San Antonio Breast Cancer Symposium. Abstract S1-05.
- Blok E, Kroep J, Meershoek-Klein E, et al. Optimal duration of extended adjuvant endocrine therapy for early breast cancer; results of the >Узнать больше о лечении рака молочной железы можно на
Большой конференции RUSSCO «Рак молочной железы»
(25-26 января 2018, Лотте Отель Москва)
Copyright © Российское общество клинической онкологии (RUSSCO)
Полное или частичное использование материалов возможно только с разрешения администрации портала.
источник
таблетки, покрытые пленочной оболочкой.
действующее вещество: анастрозол – 1 мг;
вспомогательные вещества – карбоксиметилкрахмал натрия (тип А), повидон К-25, кальция стеарат, натрия лаурилсульфат, лактозы моногидрат; опадрай II белый (85 F);
состав оболочки (опадрай II белый (85 F)): поливиниловый спирт, частично гидролизованный, макрогол (полиэтиленгликоль), тальк, титана диоксид.
таблетки, покрытые пленочной оболочкой, белого или почти белого цвета, круглые, двояковыпуклые. На поверхности таблеток допускается шероховатость пленочного покрытия.
противоопухолевое средство – эстрогенов синтеза ингибитор.
Фармакодинамика
Анастрозол – высокоселективный нестероидный ингибитор фермента ароматазы, который в организме женщин в постменопаузе превращает андростендион в периферических тканях в эстрон и далее в эстрадиол. Терапевтический эффект у больных раком молочной железы достигается за счет снижения уровня циркулирующего эстрадиола. У женщин в постменопаузе анастрозол в суточной дозе 1 мг вызывает снижение уровня эстрадиола на 80%.
He обладает прогестогенной, андрогенной и эстрогенной активностью. Суточная дола до 10 мг не оказывает воздействия на секрецию кортизола и альдостерона. Не требуется заместительное введение кортикостероидов. Анастрозол может вызывать снижение минеральной плотности костной ткани у пациенток с гормонпозитивным ранним раком молочной железы в постменопаузе. Анастрозол отдельно, а также в комбинации с бисфосфонатами не изменяет уровень липидов в плазме.
Фармакокинетика
Быстро всасывается, максимальная концентрация в плазме достигается в течение 2 часов после приема внутрь натощак. Пища незначительно снижает скорость всасывания. Степень снижения не имеет клинически значимого влияния на равновесную концентрацию препарата в плазме при однократном приеме суточной дозы. Приблизительно 90-95% равновесной концентрации анастрозола достигается после 7 дней приема препарата. Сведения о зависимости фармакокинетических параметров от времени и дозы отсутствуют. Возраст женщин в постменопаузе не влияет на фармакокинетику. Связь с белками плазмы – 40%.
Анастрозол выводится из организма медленно. Период полувыведения из плазмы составляет 40-50 часов. Экстенсивно метаболизируется у женщин в постменопаузе. В неизменном виде выделяется 10% дозы с мочой в течение 72 часов после приема. Метаболизируется путем N-деалкилирования, гидроксилирования и глюкуронизации. Основной метаболит триазол не обладает активностью. Выведение метаболитов происходит с мочой.
Цирроз печени или нарушение функции почек не изменяет клиренс анастрозола после перорального приема.
Фармакокинетика анастрозола у детей не изучалась.
- Адъювантная терапия раннего рака молочной железы, с положительными гормональными рецепторами у женщин в постменопаузе, в том числе, после адъютивной терапии тамоксифеном в течение 2-3 лет.
- Первая линия терапии местно-распространенного или метастатического рака молочной железы, с положительными или неизвестными гормональными рецепторами у женщин в постменопаузе.
- Вторая линия терапии распространенного рака молочной железы, прогрессирующего после лечения тамоксифеном, у женщин в постменопаузе.
- Повышенная чувствительность к анастрозолу или другим компонентам препарата.
- Беременность и период кормления грудью;
- Противопоказан женщинам в пременопаузе.
- Выраженная почечная недостаточность (клиренс креатинина менее 20 мл/мин).
- Умеренная или выраженная печеночная недостаточность (безопасность и эффективность не установлена).
- Сопутствующая терапия тамоксифеном или препаратами, содержащими эстрогены.
- Детский возраст (безопасность и эффективность у детей не установлена).
Остеопороз, гиперхолестеринемия, ишемическая болезнь сердца, нарушение функции печени, недостаточность лактазы, глюкозо-галактозная мальабсорбция.
Применение при беременности и в период грудного вскармливания противопоказано.
Внутрь, таблетка проглатывается целиком, запивая водой. Рекомендовано применение в одно и то же время.
Взрослые, включая пожилых: по 1 мг 1 раз в сутки, длительно. При появлении признаков прогрессирования заболевания прием препарата следует прекратить.
В качестве адъювантной терапии рекомендуемая продолжительность лечения составляет 5 лет.
При нарушении функции почек легкой и умеренной степени корректировки дозы не требуется.
При нарушении функции печени легкой степени корректировки дозы не требуется.
Частота развития побочных эффектов приведена в следующей градации: очень часто (≥1/10); часто (≥1/100,
источник
В большинстве случаев обследования больных с локализованными опухолями врач приходит к выводу, что болезнь носит преимущественно системный характер, и метастазы разовьются позже. Обнаружение многочисленных метастазов, часто спустя годы после проведения мастэктомии, а также в течение многолетнего наблюдения за больными подтверждает этот вывод.
По данным классических исследований Бринкли и Хейбитл, общая выживаемость больных раком молочной железы через 25 лет после лечения составляет только 20%. Даже среди пациенток, которым мастэктомия была сделана своевременно («ранние» операбельные случаи), выживаемость составляет лишь 30%.
Обычно появление метастазов приводит к смертельному исходу в пределах трех лет, хотя в случаях, когда лечение оказывается эффективным, пациентки могут жить дольше. Вероятность метастазирования опухоли сильно зависит от степени вовлечения подмышечных лимфатических узлов в патологический процесс, что определяется при гистологическом анализе образцов, взятых во время операции.
Существует взаимосвязь между количеством пораженных подмышечных лимфатических узлов и вероятностью распространения метастазов.
Со времени проведения первой операции терапевтической овариэктомии, проведенной Битсоном в 1896 г., стало очевидно, что при изменении гормонального статуса организма в случаях распространенного опухолевого процесса, по крайней мере для одной трети пациенток достигается симптоматический эффект.
Использовались различные методы: удаление яичников или их облучение (иногда называемое «создание искусственной менопаузы»), лечение эстрогенами, антиэстрогенами и антагонистами гонадотропин-рилизинг-гормона (например, гозерелином). Этот гормон регулирует секрецию лютеинизирующего гормона (LHRH).
Также применяли анаболические стероиды, глюкокортикоиды и прогестерон, проводили удаление надпочечников или гипофиза и назначали ингибиторы ароматазы (анастрозол или летрозол).
Стандартный подход основан на менструальном статусе пациентки. Для большинства больных с метастазирующими опухолями в пременопаузе и перименопаузе используется хирургическое удаление яичников или их облучение. Однако с появлением антагонистов гонадотропин-рилизинг-гормона эти процедуры стали применять реже.
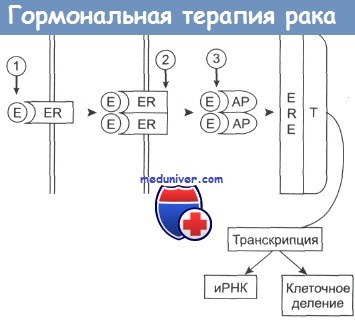
Комплекс приобретает активность (АР) и присоединяется к эстроген-зависимым структурам (ERE) клеточного ядра.
Происходит активация таких белков, участвующих в транскрипции (Т), как РНК-полимераза II, что приводит к синтезу белка и делению клетки.
Гозерелин вызывает снижение уровня эстрогенов в плазме крови (1); фульвестран (2) предотвращает процесс димеризации рецептора и его активацию; тамоксифен (3) связывается с активным комплексом, подавляя его способность инициировать транскрипцию.
Антагонисты обеспечивают стойкое снижение уровня эстрогенов и вызывают у пациентки состояние менопаузы, которое длится в продолжении примерно двух месяцев с начала применения гозерелина. Препарат назначается ежемесячно в виде внутримышечных инъекций. Вместе с тем в качестве альтернативы снова стал популярным такой хирургический метод, как лапароскопическое удаление яичников.
Это достаточно безопасная и несложная операция, после которой пациентка на одну ночь остается в стационаре. Следует отметить, что перед операцией больные проходят тщательный отбор по критерию гормональной чувствительности опухоли, и тем, для кого не предполагается проявление лечебного эффекта, операция не проводится.
Для пациенток с опухолью в постменопаузе широко применяется тамоксифен, поскольку он практически не проявляет побочных эффектов. Препарат действует как антиэстроген, но, вероятно, оказывает и прямой цитотоксический эффект. В течение почти 20 лет тамоксифен использовался в качестве стандартного препарата адъювантной терапии.
Тамоксифен назначается перорально в ежедневной стандартной дозе 20 мг. Он обладает медленным кумулятивным действием. Побочные эффекты редки, однако могут наблюдаться приливы, тошнота, гиперкальциемия, тромбоцитопения, удержание жидкости и расстройство менструального цикла. После приема препарата большинство пациенток прибавляют 1-2 фунта в весе и некоторые отмечают ухудшение состояния кожи, волос и ногтей.
Гораздо более существенный эффект получен при назначении гормонотерапии пациенткам с гормонально зависимыми опухолями, в то время как при лечении гормонально независимых опухолей благоприятный эффект наблюдался лишь в редких случаях. Прогноз в случаях гормонально зависимых и независимых опухолей отличается. Для больных с гормонально-зависимыми опухолями характерен более длительный безрецидивный период и большая выживаемость.
Совместное определение показателей ER и PR обеспечивает более точный прогноз в отношении чувствительности опухоли к гормонотерапии, чем это оказывается возможным при оперировании только показателем ER. Больные с PR-положительными опухолями также характеризуются более длительным безболезненным периодом.
На эффективность гормонотерапии сильно влияет характер распространения метастазов. Костные метастазы проявляют некоторую чувствительность к гормонам, хотя после лечения пациентки живут в среднем около 12-15 месяцев. Тем не менее некоторые больные с гормоночувствительными опухолями и с костными метастазами живут дольше, иногда несколько лет.
В большинстве случаев, при рецидиве опухоли, развившейся в пременопаузе, применяется гозерин (или его аналоги) или лапароскопическая овариэктомия (или облучение яичников). Эти меры эффективны для гормонально чувствительных опухолей. При опухолях в периоде постменопаузы обычно назначают тамоксифен, если пациентки раньше не получали этот препарат в качестве средства адъювантной терапии.
В любом случае можно ожидать, что выживаемость больных составит по крайней мере 30%. Экзогенные гормоны назначают до тех пор, пока не наступит эффект. В дальнейшем гормональную терапию продолжают только тем пациенткам, у которых проявился эффект первичного лечения. Предложены новые противоопухолевые препараты, относящиеся к группе ингибиторов ароматазы.
К числу их относится анастрозол, который блокирует биосинтез предшественников эстрогенов и их последующие превращения в тканях. Анастрозол действует при пероральном применении. Он хорошо переносится больными, так же как и другие родственные соединения, благодаря чему эти препараты быстро заняли место тамоксифена, который оказался неэффективным в лечении пациенток с гормонозависимыми опухолями, развивающимися в период постменопаузы. Рекомендуемая ежедневная доза препарата составляет 1 мг.
Если после первичного лечения возникает рецидив, то назначают другие препараты, например анаболические стероиды, прогестогены и глюкокортикоиды. Анаболические стероиды более эффективны у пациенток с опухолями, развившимися в постменопаузе, и, по-видимому, их особенно необходимо применять в случаях обнаружения костных метастазов.
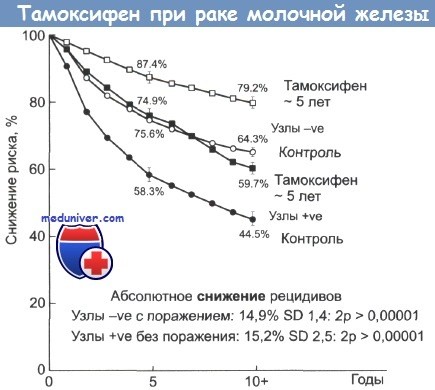
Светлые значки — пациентки без признаков поражения лимфатических узлов; затемненные значки — пациентки с признаками поражения лимфоузлов.
Благоприятный эффект достигается примерно у 20% пациенток, однако недостатком применения стероидов является вирилизация. Удобным для применения является нандролон деканоат (Deca-Durabolin), который назначается в виде внутримышечных инъекций в дозе 50-100 мг каждые 3-4 недели. Если гормонотерапия раньше давала положительные результаты, то можно применять прогестогены. Наиболее часто используется ацетат медроксипрогестерона (МРА, Provera), который обычно назначают перорально в дозе 100 мг три раза в день.
Однако его применение ограничено из-за развития побочного эффекта — прибавления в весе. Такой же эффективностью обладает другое производное прогестерона — мегестрол-ацетат (Megace).
Широко обсуждается вопрос выбора метода лечения первого рецидива опухоли. Следует в этом случае использовать гормональный метод или же химиотерапию с использованием цитотостатиков? Если принимать во внимание количественные показатели, то выбирать надо между гормонотерапией (эффективна в 30% случаев) и комбинационной химиотерапией (эффективность которой в два раза выше). Однако это упрощенное решение вопроса, ответить на который на самом деле сложно.
Реакция опухоли на гормоны обычно носит более продолжительный характер, и у пациентки наблюдаются минимальные токсические проявления. При химиотерапии развивается более кратковременный эффект, который сопровождается токсическими и психологическими осложнениями. Большинство клиницистов в Великобритании в качестве средства первичного лечения предпочитают использовать гормональную терапию. Выбор облегчается все более широким применением метода анализа состояния рецепторов эстрогенов: гормональная терапия должна проводиться только среди пациенток с ER-положительными опухолями. Недавно предложен препарат фульвестрант (Faslodex), подавляющий функции рецепторов эстрогенов. Он может применяться у пациенток с гормоноустойчивыми опухолями, которые развились в постменопаузе. Одним из основных преимуществ этого препарата, по сравнению с агонистом эстрогенов, тамоксифеном, является отсутствие побочных эффектов. Он также не опустошает пул эстрогенов в женском организме, что происходит при применении ингибиторов ароматазы.
источник
таблетки, покрытые пленочной оболочкой.
действующее вещество: анастрозол – 1 мг;
вспомогательные вещества – карбоксиметилкрахмал натрия (тип А), повидон К-25, кальция стеарат, натрия лаурилсульфат, лактозы моногидрат; опадрай II белый (85 F);
состав оболочки (опадрай II белый (85 F)): поливиниловый спирт, частично гидролизованный, макрогол (полиэтиленгликоль), тальк, титана диоксид.
таблетки, покрытые пленочной оболочкой, белого или почти белого цвета, круглые, двояковыпуклые. На поверхности таблеток допускается шероховатость пленочного покрытия.
противоопухолевое средство – эстрогенов синтеза ингибитор.
Фармакодинамика
Анастрозол – высокоселективный нестероидный ингибитор фермента ароматазы, который в организме женщин в постменопаузе превращает андростендион в периферических тканях в эстрон и далее в эстрадиол. Терапевтический эффект у больных раком молочной железы достигается за счет снижения уровня циркулирующего эстрадиола. У женщин в постменопаузе анастрозол в суточной дозе 1 мг вызывает снижение уровня эстрадиола на 80%.
He обладает прогестогенной, андрогенной и эстрогенной активностью. Суточная дола до 10 мг не оказывает воздействия на секрецию кортизола и альдостерона. Не требуется заместительное введение кортикостероидов. Анастрозол может вызывать снижение минеральной плотности костной ткани у пациенток с гормонпозитивным ранним раком молочной железы в постменопаузе. Анастрозол отдельно, а также в комбинации с бисфосфонатами не изменяет уровень липидов в плазме.
Фармакокинетика
Быстро всасывается, максимальная концентрация в плазме достигается в течение 2 часов после приема внутрь натощак. Пища незначительно снижает скорость всасывания. Степень снижения не имеет клинически значимого влияния на равновесную концентрацию препарата в плазме при однократном приеме суточной дозы. Приблизительно 90-95% равновесной концентрации анастрозола достигается после 7 дней приема препарата. Сведения о зависимости фармакокинетических параметров от времени и дозы отсутствуют. Возраст женщин в постменопаузе не влияет на фармакокинетику. Связь с белками плазмы – 40%.
Анастрозол выводится из организма медленно. Период полувыведения из плазмы составляет 40-50 часов. Экстенсивно метаболизируется у женщин в постменопаузе. В неизменном виде выделяется 10% дозы с мочой в течение 72 часов после приема. Метаболизируется путем N-деалкилирования, гидроксилирования и глюкуронизации. Основной метаболит триазол не обладает активностью. Выведение метаболитов происходит с мочой.
Цирроз печени или нарушение функции почек не изменяет клиренс анастрозола после перорального приема.
Фармакокинетика анастрозола у детей не изучалась.
- Адъювантная терапия раннего рака молочной железы, с положительными гормональными рецепторами у женщин в постменопаузе, в том числе, после адъютивной терапии тамоксифеном в течение 2-3 лет.
- Первая линия терапии местно-распространенного или метастатического рака молочной железы, с положительными или неизвестными гормональными рецепторами у женщин в постменопаузе.
- Вторая линия терапии распространенного рака молочной железы, прогрессирующего после лечения тамоксифеном, у женщин в постменопаузе.
- Повышенная чувствительность к анастрозолу или другим компонентам препарата.
- Беременность и период кормления грудью;
- Противопоказан женщинам в пременопаузе.
- Выраженная почечная недостаточность (клиренс креатинина менее 20 мл/мин).
- Умеренная или выраженная печеночная недостаточность (безопасность и эффективность не установлена).
- Сопутствующая терапия тамоксифеном или препаратами, содержащими эстрогены.
- Детский возраст (безопасность и эффективность у детей не установлена).
Остеопороз, гиперхолестеринемия, ишемическая болезнь сердца, нарушение функции печени, недостаточность лактазы, глюкозо-галактозная мальабсорбция.
Применение при беременности и в период грудного вскармливания противопоказано.
Внутрь, таблетка проглатывается целиком, запивая водой. Рекомендовано применение в одно и то же время.
Взрослые, включая пожилых: по 1 мг 1 раз в сутки, длительно. При появлении признаков прогрессирования заболевания прием препарата следует прекратить.
В качестве адъювантной терапии рекомендуемая продолжительность лечения составляет 5 лет.
При нарушении функции почек легкой и умеренной степени корректировки дозы не требуется.
При нарушении функции печени легкой степени корректировки дозы не требуется.
Частота развития побочных эффектов приведена в следующей градации: очень часто (≥1/10); часто (≥1/100,
источник
Противоопухолевое средство, селективный нестероидный ингибитор ароматазы.
Белый кристаллический порошок. Растворимость в воде 0,25 мг/мл (при 25 °C), не зависит от pH в физиологическом диапазоне. Очень легко растворим в метаноле, этаноле, ацетоне, тетрагидрофуране. Легко растворим в ацетонитриле. Молекулярная масса 293,4.
Проявляет активность в отношении эстрогенозависимых опухолей молочной железы у женщин в постменопаузном периоде. Андростендион — основной источник циркулирующих эстрогенов у женщин в постменопаузе, в периферических тканях превращается в эстрон, и затем в эстрадиол, этот процесс происходит при участии фермента ароматазы. Механизм действия анастрозола связан с ингибированием ароматазы (селективный нестероидный ингибитор) в периферических тканях, в т.ч. жировой, что приводит к уменьшению количества эстрадиола. При лечении анастрозолом в рекомендованной дозе — 1 мг в сутки — уровень эстрадиола снижается на 70% в течение 24 ч, на 80% — после 14 дней. Супрессия уровня сывороточного эстрадиола поддерживается в течение 6 дней после прекращения ежедневного приема по 1 г анастрозола. Снижение уровня циркулирующего эстрадиола оказывает терапевтический эффект при опухолях молочной железы у женщин в постменопаузе. При ежедневном приеме в дозах 3, 5 и 10 мг анастрозол не оказывал эффекта на секрецию кортизола и альдостерона. Анастрозол не проявлял прямой прогестогенной, андрогенной и эстрогенной активности у животных, но изменял уровни циркулирующих прогестерона, андрогенов и эстрогенов.
После приема внутрь всасывается 83–85% дозы, прием пищи влияет на абсорбцию (уменьшает всасывание). Cmax достигается через 2 ч (натощак). В крови с белками плазмы связывается до 40%. Равновесная концентрация в крови при ежедневном приеме достигается примерно через 7 дней, величина ее в 3–4 раза выше, чем при однократном приеме. Анастрозол экстенсивно метаболизируется у женщин в постменопаузе, менее 10% экскретируется с мочой в неизмененном виде в течение 72 ч после приема, 60% выводится в виде метаболитов. Биотрансформация в печени осуществляется путем N-деалкилирования, гидроксилирования и глюкуронизации с образованием неактивных метаболитов, основной из которых — триазол. Терминальный T1/2 составляет примерно 50 ч. Фармакокинетика анастрозола не зависит от возраста женщин в диапазоне 50–80 лет.
Острая токсичность у животных. В исследованиях острой токсичности на грызунах (крысы) показано, что при однократном пероральном приеме летальная доза анастрозола превышала 100 мг/кг/сут (примерно в 800 раз выше рекомендованной дозы для человека, в мг/м 2 ) и ассоциировалась с сильным раздражением желудка (некроз, гастрит, изъязвление, геморрагия). При пероральном введении собакам медиана летальной дозы превышала 45 мг/кг/сут.
Мутагенность. Анастрозол не проявлял мутагенных и кластогенных свойств в ряде тестов in vitro и in vivo , в т.ч. в тесте Эймса, тесте на хромосомные аберрации на лимфоцитах человека, в микроядерном тесте у крыс.
Репродуктивная токсикология. Пероральное введение анастрозола самкам крыс (с момента 2 нед перед скрещиванием и до 7 дня беременности) вызывало значимое повышение бесплодия и снижение числа благополучных беременностей при дозе 1 мг/кг/сут (примерно в 10 раз превышает МРДЧ в мг/м 2 и в 9 раз превышает AUC0–24 женщин-волонтеров, находящихся в постменопаузе, при приеме в рекомендованных дозах). При дозах ≥0,02 мг/кг/сут (примерно 1/5 МРДЧ в мг/м 2 ) отмечались предимплантационные потери яйцеклеток или потеря плода. После 3-недельного приема восстановление фертильности наблюдалось через 5 нед после отмены ЛС . Неизвестно, указывают ли отмеченные эффекты нарушения фертильности у крыс на возможность нарушения фертильности у человека.
Канцерогенность. Двухгодичные исследования у крыс при пероральном введении животным анастрозола в дозах от 1,0 до 25 мг/кг/сут (в 10–243 раза превышают МРДЧ в мг/м 2 ) выявили повышение частоты гепатоцеллюлярной аденомы и карциномы, а также стромальных полипов матки у самок, аденомы щитовидной железы у самцов в случае введения препарата в высоких дозах (25 мг/кг/сут). Отмечалось дозозависимое повышение частоты гиперплазии яичников и матки у самок. При дозе 25 мг/кг/сут плазменные уровни AUC0–24 у крыс были в 110–125 раз выше, чем эти же показатели у женщин-волонтеров, находящихся в постменопаузе, при приеме терапевтических доз ЛС .
В двухгодичных исследованиях у мышей при пероральном приеме анастрозола в дозах от 5 до 50 мг/кг/сут (примерно в 24–243 раза превышают МРДЧ в мг/м 2 ) обнаружено увеличение частоты возникновения доброкачественных опухолей (стромальных, эпителиальных, гранулярных) яичника при всех исследованных дозах. Также отмечалась дозозависимая гиперплазия яичников у самок мышей. Эти изменения в яичниках расцениваются как специфическое следствие ингибирования ароматазы в организме грызунов и не рассматриваются как клинически значимые для человека. Частота обнаружения лимфосарком была повышена у самок и самцов мышей при высоких дозах. При дозе 50 мг/кг/сут плазменные уровни AUC0–24 у мышей были в 35–40 раз выше, чем таковые у женщин-волонтеров, находящихся в постменопаузе, при приеме ЛС в терапевтических дозах.
Адъювантная терапия раннего гормоноположительного рака молочной железы у женщин в постменопаузе, лечение распространенного рака молочной железы у женщин в постменопаузе, адъювантная терапия раннего гормоноположительного рака молочной железы у женщин в постменопаузе после терапии тамоксифеном в течение 2–3 лет.
Гиперчувствительность, пременопаузный период, сопутствующая терапия тамоксифеном или препаратами, содержащими эстрогены; выраженная почечная недостаточность (клиренс креатинина ИБС .
Категория действия на плод по FDA — X.
Со стороны нервной системы и органов чувств: астенический синдром, инсомния, сонливость, тревожность, депрессия, головная боль, головокружение, парестезия.
Со стороны сердечно-сосудистой системы и крови (кроветворение, гемостаз): анемия, гипертензия (сильное головокружение, длительно продолжающаяся головная боль), лейкопения с/без инфекции, тромбофлебит, тромбоэмболия.
Со стороны респираторной системы: диспноэ, синусит, ринит, бронхит, фарингит.
Со стороны органов ЖКТ : снижение аппетита, тошнота, рвота, запор/диарея, сухость во рту.
Аллергические реакции: в т.ч. сыпь, зуд, полиморфная эритема, синдром Стивенса-Джонсона.
Прочие: приливы, сухость влагалища, вагинальное кровотечение, миалгия, артралгия, боль в груди, боль в спине, уменьшение подвижности суставов, потливость, гриппоподобный синдром, периферические отеки, истончение волос и алопеция, гиперхолестеринемия, повышение уровней ЩФ , АСТ и АЛТ (у больных с метастазами в печень), повышение массы тела.
Препараты, содержащие эстрогены, уменьшают фармакологическое действие анастрозола, в связи с чем они не должны назначаться одновременно с анастрозолом.
Не следует назначать тамоксифен одновременно с анастрозолом, поскольку он может ослабить фармакологическое действие последнего. При совместном применении анастрозола и тамоксифена у пациенток с раком молочной железы плазменная концентрация анастрозола снижалась на 27% по сравнению с таковой при приеме только анастрозола, при этом совместный прием не влиял на фармакокинетику тамоксифена и N-дезметилтамоксифена.
Не выявлено клинически значимого эффекта анастрозола на фармакокинетику и антикоагулянтную активность варфарина. В исследовании у 16 добровольцев-мужчин анастрозол не влиял на экспозицию (оцененную по Сmax и AUC) и антикоагулянтную активность (измеренную по ПВ , АЧТВ и тромбиновому времени) варфарина.
Описаны единичные клинические случаи передозировки анастрозола. Разовая доза, которая могла бы привести к симптомам, угрожающим жизни, не установлена.
Лечение: индукция рвоты (если больной находится в сознании), симптоматическая терапия, наблюдение за больным и контроль жизненно важных органов и систем. Возможен диализ. Специфический антидот не найден.
У женщин с рецептороотрицательной опухолью к эстрогенам эффективность анастрозола не была продемонстрирована, кроме тех случаев, когда имелся предшествующий положительный клинический ответ на тамоксифен. Эффективность и безопасность анастрозола и тамоксифена при их одновременном применении вне зависимости от статуса гормональных рецепторов сравнимы с таковыми при использовании одного тамоксифена (точный механизм данного явления пока не известен).
В случае сомнений в гормональном статусе пациентки менопауза должна быть подтверждена определением половых гормонов в сыворотке крови.
В случае сохраняющегося маточного кровотечения на фоне приема анастрозола необходима консультация и наблюдение гинеколога.
Препараты, содержащие эстрогены, не должны назначаться одновременно с анастрозолом, т.к. эти препараты будут нивелировать его фармакологическое действие.
Снижая уровень циркулирующего эстрадиола, анастрозол может вызывать снижение минеральной плотности костной ткани. У пациенток, страдающих остеопорозом или имеющих риск развития остеопороза, минеральная плотность костной ткани должна оцениваться методом денситометрии (например DEXA-сканированием) в начале лечения и в динамике. При необходимости должны быть начаты лечение или профилактика остеопороза под тщательным наблюдением врача.
Нет данных об одновременном применении анастрозола и препаратов-аналогов ЛГРГ (рилизинг гормон лютеинизирующего гормона).
Неизвестно, улучшает ли анастрозол результаты лечения при совместном использовании с химиотерапией.
Некоторые побочные действия анастрозола, такие как астения и сонливость, могут отрицательно влиять на способность к выполнению потенциально опасных видов деятельности, требующих повышенной концентрации внимания и быстроты психомоторных реакций. В этой связи рекомендуется при появлении этих симптомов соблюдать осторожность при управлении транспортными средствами и механизмами.
источник