Лечение рака груди всегда состоит из комплекса нескольких способов: гормонотерапии, химиотерапии, хирургической операции и радиотерапии. Гормональный метод необходимо отличать от заместительной гормональной терапии. Он применяется для уничтожения оставшихся после применения других методов лечения раковых клеток, а также для снижения риска рецидива заболевания. Основная цель – уменьшение воздействия эстрогенов на онкогенное образование.
Схему гормонотерапии подбирает специалист. Он учитывает стадию, на которой было обнаружено заболевание, менопаузальный статус женщины и факторы риска повторного появления опухоли. Важно грамотно сочетать терапию злокачественной патологии с другими сопутствующими заболеваниями, если они имеются, ведь это может усиливать побочные эффекты.
Операция по вырезанию одного или двух яичников применяется только у женщин со сбережённой менструальной функцией или при преждевременном климаксе. В постменопаузе хороший результат показывают препараты, понижающие выработку эстрогенов, в репродуктивном возрасте применяют рилизинг-гормоны.
После забора биопсии часть опухоли обследуют. Если патологическое образование – гормонозависимое, то гормональное лечение рака молочной железы успешно почти в 70% случаев.
Основные показания для назначения лечения при гормонозависимых опухолях:
- наследственный фактор;
- значительные размеры онкообразования;
- нулевая стадия патологического процесса;
- появление метастаз;
- рак 4 стадии;
- метастатический рак;
- для предупреждения повторного формирования опухоли после первичного комплексного лечения карциномы.
Различают 3 вида гормонотерапии:
- адъювантная – выполняется для снижения риска повторного появления карциномы. Такое лечение длится 5-10 лет;
- неоадъювантная – назначается перед операцией, если новообразование более 2 см и затронуты лимфоузлы. Терапия обычно растягивается на 3-6 месяцев;
- лечебная – применяется для уменьшения или устранения имеющихся очагов рака, а также при неоперабельных состояниях.
Выбор варианта терапии во многом зависит от менструального статуса женщины: пременопаузы или постменопаузы. Гормональные средства подбираются доктором и применяются разнообразными способами: отдельно, в комбинации или последовательно одно за другим. Если злокачественный процесс обнаружен на этапе, когда оперативное вмешательство выполнить уже невозможно, то гормонотерапия при раке молочной железы необходима для продления жизни женщины.
Гормональная терапия при раке молочной железы имеет два направления: замедление или блокировка выработки эстрогенов и применение антиэстрогенных препаратов.
Выделяют 5 основных типов гормонального лечения. Каждый из них имеет определённый механизм действия: понижение эстрогена в крови, уменьшение или прекращение его выработки:
- Ингибиторы ароматазы. Они влияют на концентрацию эстрогенов. Ингибиторы ароматазы блокируют эстрогеновые рецепторы, не дают клеткам делиться и размножаться. Они назначаются пациенткам после наступления климакса. Выделяют 3 вида ингибиторов ароматазы при раке молочной железы: Аромазин, Аримидекс, Фемара. Препараты часто становятся причиной повышенной хрупкости костей. Доктор должен регулярно проводить обследования костной ткани, и при необходимости, на фоне применения ингибиторов ароматазы прописать, для предотвращения остеопороза, приём кальция с витамином D.
- Модуляторы рецепторов к эстрогенам. Это такие препараты как Тамоксифен и Кломифен. Они прекращают выработку эстрогенов.
- Блокаторы эстрогеновых рецепторов. Самым известным из них является Фаслодекс и Фулвестрант. Их цель – предотвращение воздействия на клетки онкообразования.
- Прогестины. Снижают выделение определённых гормонов гипофиза, ответственных за выработку андрогенов и эстрогенов.
- Воздействие на яичники. Существуют 3 способа:
- медикаментозный: Золадекс и Люпрон рекомендуются инъекционно 1 раз в месяц для уменьшения производства яичниками эстрогена;
- овариальная абляция – облучение яичников, применяется редко;
- операция овариэктомия – вырезание одного или двух яичников. После выполнения их резекции – для уменьшения риска рецидива заболевания рекомендуют: андрогены – чтобы гипофиз не стимулировал появление новых фолликулов; кортикостероиды и эстрогены – для отключения выработки эстрогенов надпочечниками и яичниками.
В пременопаузе чаще всего используют овариэктомию, облучение яичников или медикаментозный способ с последующим назначением Тамоксифена. В постменопаузе самый применяемый вариант лечения – употребление антиэстрогенов около 5 лет.
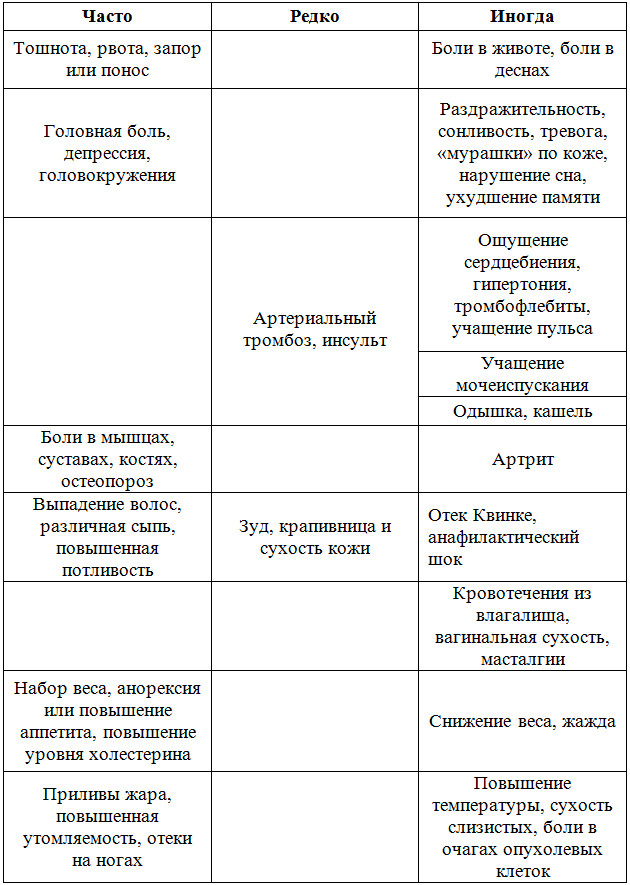
Количество, длительность, а также характер побочных эффектов после терапии рака зависят от множества факторов: возраста, общего состояния женского здоровья, стадии, на которой было получено лечение, а также назначенной специалистом схемы. Самые распространённые общие последствия гормонотерапии:
- увеличение массы тела;
- преждевременный климакс;
- приливы жара;
- отёчность ног;
- нарушение сна;
- запор или понос;
- боли в дёснах;
- учащение мочеиспускания;
- одышка;
- алопеция;
- тошнота, рвота;
- усиленная потливость;
- ухудшение памяти;
- сухость влагалища;
- депрессия.
Все они в основном имеют кратковременное течение и исчезают спустя несколько недель после завершения гормонотерапии, реже на это необходимы месяцы. Некоторые из необходимых для лечения медикаментов обладают сильными побочными эффектами.
Тамоксифен повышает возможность тромбообразования и развития катаракты, а также гепатита, является одним из факторов риска при возникновении рака матки и диагностировании бесплодия.
Ингибиторы ароматазы – провоцируют остеопороз, увеличивают риск язвенных поражений системы ЖКТ, повышают холестерин в крови, массу тела, а также приводят к алопеции.
После приёма Фаслодекса могут появиться нарушения в работе мочевыделительной системы – цистит, уретрит, а также расстройство стула и кожные высыпания.
Золадекс и Люпрон провоцируют приливы жара, депрессию, понижение или повышение давления, артралгию.
Побочными явлениями при применении гормонов после удаления яичников становятся нарушения водно-солевого обмена, развитие алкалоза, увеличение уровня сахара в крови, появление невроза с бессонницей. Возможно диагностирование синдрома Кушинга, а также язвенных поражений системы ЖКТ.
Последствия приёма прогестинов – прибавление массы тела, облысение, тромбоэмболические осложнения.
Гормонотерапия при раке молочной железы – один из способов лечения гормоночувствительных опухолей груди, который при условии грамотного назначения и правильного проведения очень эффективен.
Если оба рецептора (прогестероновые и эстрогеновые) обнаружены в злокачественных клетках опухоли, то терапия даёт хорошие результаты в 70% ситуаций, если выявлен один их тип – то лишь примерно в 30% случаев. При других видах карциномы груди эффективность лечения может быть лишь около 10%.
источник
Гормональная терапия является эффективным методом лечения гормональнозависимых опухолей молочной железы. Иногда ее называют антиэстрогеновой терапией, так как она направлена на предотвращение воздействия эстрогена на онкологические клетки.
В Москве на онкологических болезнях (в том числе и на раке молочной железы) специализируются врачи Юсуповской больницы. Это одно из лучших учреждений по оснащенности, высококвалифицированным врачам, ценовой политике, качеству оказываемых услуг и сервису, в котором процент положительного исхода лечения один из самых высоких в стране.
В большинстве случаев гормональная терапия оказывает эффективное действие, так как 75% всех опухолей, расположенных в молочных железах, имеют гормонзависимую природу. В зависимости от общего состояния пациентки, стадии заболевания, характера течения, распространенности, менопаузального статуса доктор подбирает оптимальную схему лечения. Ее нужно строго придерживаться, ведь только так можно достичь положительного результата.
Показаниями к назначению гормональной терапии являются:
- снижение вероятности возникновения рака у женщин, которые не страдают этим заболеванием, но находятся в зоне высокого риска;
- снижение риска рецидивов при неинвазивном раке;
- снижение вероятности рецидива или появления новых опухолей после оперативного вмешательства, химиотерапии и лучевой терапии;
- уменьшение размеров опухоли при инвазивном раке;
- метастатический рак.
Гормонотерапию часто называют «страховкой» после применения других методов лечения рака, так как операция, лучевая терапия и химиотерапия не могут дать 100% гарантию, что пациентка не заболеет вновь. Препараты гормонотерапии оказывают влияние на весь организм, подавляя действие эстрогена, и назначаются только в случаях гормонозависимых опухолей.
В Юсуповской больнице применяется только лучшее диагностическое оборудование от производителей с мировым именем, полный перечень лекарственных препаратов (антибиотики, химиопрепараты, гормональные таблетки и инъекции).
- адъювантная (профилактическая);
- неоадъювантная;
- лечебная.
Применяется как дополнительная терапия после оперативного вмешательства, химического облучения и лучевой терапии с целью профилактики рецидивов. Обычно такая терапия длится от 5 до 10 лет, при этом доктор назначает препараты ингибиторов ароматазы или тамоксифен.
Неоадъювантная терапия представляет собой комплексное лечение перед проведением оперативного вмешательства или лучевой терапией. Она применяется в следующих случаях:
- для уменьшения размеров опухоли и ее метастазов;
- для уменьшения объема хирургического вмешательства;
- для увеличения безрецидивной и общей выживаемости;
- для определения чувствительности опухоли к цитостатикам;
- для оценки новых способов лечения.
Такая терапия длится от 3 до 6 месяцев, хотя при положительном результате лечение продлевается.
Назначается пациенткам с неоперабельным раком и при генерализации. Также лечебную терапию назначают молодым женщинам с метастазами в печень или легкие, а также в период ремиссии.
Выбор лечения рака молочной железы зависит от многих факторов, среди которых:
- гормональный статус обнаруженной опухоли;
- менопаузальный статус женщины;
- стадия заболевания;
- применяемые ранее способы лечения;
- наличие сопутствующих соматических болезней;
- риск развития рецидива.
После применения неоадъювантной терапии у 80% пациенток опухоль уменьшается в размерах, а у 15% — отмечена полная морфологическая ремиссия.
Все виды терапии применяются в Юсуповской больнице. Врач, учитывая состояние пациентки, природу опухоли и стадию заболевания, подберет оптимальную схему лечения, которая поможет в эффективном лечении.
Гормонотерапию при раке молочной железы подбирают в зависимости от того, сохранен ли у женщины менструальный цикл. Так, пациенткам в пременопаузе (менструальный цикл постоянный) назначают:
- тамоксифен сроком на 5 лет (на ранних стадиях заболевания);
- операцию по удалению яичников;
- после удаления яичников или подавления их функции с помощью медикаментов назначают ингибиторы ароматазы.
Женщинам в период менопаузы (пациентка находится в климактерическом или постклимактерическом состоянии):
- назначают ингибиторы ароматазы после хирургического вмешательства, химической и лучевой терапии;
- если пациентка до менопаузы принимала тамоксифен, то его заменяют ингибиторами ароматазы;
- если женщина принимала тамоксифен на протяжении последних 5 лет, то его заменяют фемарой;
- если при лечении тамоксифеном была выявлена новая опухоль или рецидив, то вместо него назначают ингибиторы ароматазы;
- если в период приема ингибитора ароматазы выявлен рецидив, то его заменяют на тамоксифен, фаслодекс или назначают другой ингибитор ароматазы.
Опухоли по своей природе могут быть доброкачественными и злокачественными. Если опухоль доброкачественная, при этом существует риск ее перехода в рак, то единственным препаратом, который назначается таким пациенткам, является тамоксифен. Также он применяется при обнаружении протоковой карциномы in situ.
Женщинам с HER2-позитивным раком предпочтительнее назначать ингибиторы ароматазы. Также они назначаются, если тамоксифен оказался нерезультативным.
Относится к группе антиэстрогенов и препятствует соединению эстрогенов с раковыми клетками, что, соответственно, не дает последним увеличиваться. Его назначают женщинам на ранних стадиях заболевания и в период предменопаузы.
Одно из торговых названий этого препарата – Тамоксифен-Нолвадекс (в таблетках). У некоторых пациенток при их приеме отмечается сухость влагалища или, наоборот, чрезмерные выделения, усиленное потоотделение, покраснение кожи, увеличение веса.
Эти препараты блокируют выработку эстрогенов в организме женщины и назначаются пациенткам уже после наступления менопаузы. Как показывает практика, многим женщинам удалось преодолеть рак молочной железы благодаря приему одного из этой группы препаратов (аримидекс, фемара, аромазин). Каждый препарат назначается в определенных случаях:
- аримидекс – на ранних стадиях заболевания сразу после удаления опухоли;
- аромазин – на ранних стадиях рака тем женщинам, которые ранее несколько лет принимали тамоксифен;
- фемара – на ранних стадиях болезни после оперативного вмешательства пациенткам, которые принимали тамоксифен 5 и более лет.
У большинства женщин прием этих препаратов не вызывает никаких негативных симптомов, но некоторые отмечают тошноту, сухость во влагалище и боль в суставах. Также длительный прием ингибиторов ароматазы может стать причиной хрупкости костей, поэтому вместе с данными препаратами параллельно назначают кальций и витамин Д.
Этот препарат является аналогом природного ЛГРГ и применяется для подавления работы гипофиза. Он снижает количество гормонов, которые вырабатывают эстрогены, но при прекращении его приема гипофиз начинает работать в усиленном режиме. Поэтому врачи после нескольких месяцев приема золадекса рекомендуют операцию по удалению яичников (овариоэктомию) хирургическим способом или путем облучения.
Побочное действие препарата заключается в снижении полового влечения, покраснении, сильном потоотделении, головных болях, перепадах настроения. Золадекс вводят внутримышечно в нижнюю часть брюшной стенки 1 раз в месяц.
Несмотря не огромную пользу, гормонотерапия имеет ряд негативных последствий. Примерно половина женщин, которым назначается гормонотерапия при раке молочной железы, отмечают:
- увеличение массы тела;
- потливость;
- отечность;
- сухость влагалища;
- преждевременное наступление менопаузы;
- перепады настроения, депрессия.
Широко используемый препарат тамоксифен может стать причиной образования тромбов, рака матки и бесплодия. Препараты, которые направлены на снижение уровня эстрогенов (ингибиторы ароматазы), в некоторых случаях приводят к остеопорозу, повышению холестерина, заболеваниям ЖКТ. При появлении вышеперечисленных симптомов следует немедленно обратиться к доктору. Он сможет подобрать другие оптимальные лекарства.
С момента обнаружения опухоли в молочной железе женщине нужно пересмотреть свой рацион. Правильно подобранная диета позволит значительно улучшить общее самочувствие и снизить риск дальнейшего развития заболевания.
Питание при раке должно быть максимально сбалансированным, с большим количеством витаминов и микроэлементов. Кушать необходимо часто, но маленькими порциями, при этом придерживаться принципа раздельного питания.
Врачи Юсуповской больницы считают, что питание при гормонотерапии рака молочной железы должно быть именно таким:
- употреблять много ярко окрашенных овощей и фруктов (морковь, тыква, томаты, капуста, клюква, чеснок) и злаков (коричневый рис, пророщенная пшеница, отруби);
- калорийность рациона должна зависеть от веса пациентки: женщинам с лишним весом с помощью диеты нужно попытаться избавиться от лишних килограммов;
- уменьшить количество животных жиров в рационе и увеличить количество растительных;
- употреблять пищу, богатую кальцием и витамином Д;
- отказаться от продуктов, в состав которых входят фитоэстрогены;
- полностью исключить копченую, жареную, соленую, острую пищу и продукты с консервантами;
- ограничить количество сахара (в том числе и напитков с его содержанием);
- полностью отказаться от алкоголя, курения и наркотических средств;
- как можно меньше кушать красное мясо;
- обязательно добавить в рацион морскую рыбу, морепродукты, морскую капусту;
- ежедневно употреблять 1-2 порции молочных продуктов;
- пить как можно больше сырой воды (не менее 2-2,5 л в день), зеленого чая и отваров из травяных сборов.
В Юсуповской больнице есть все необходимое оборудование для диагностики и лечения заболевания, а при выявлении образования в молочной железе в лаборатории можно сделать анализ на определение его природы.
Важно заметить, что каждая женщина в возрасте после 35 лет должна раз в год посещать маммолога чтобы исключить вероятность патологических образований в груди. Это можно сделать в Юсуповской больнице, которая находится по адресу: 117186, г. Москва, ул. Нагорная, д.17, корп.6, предварительно записавшись на прием.
источник
Молочная железа – гормонально-зависимый орган: на рост и деление ее клеток оказывают влияние эстрогены, прогестерон и пролактин, причем каждый это делает по-разному. Рак груди – это участок, в котором клетки мутировали, то есть видоизменились (и чем сильнее, тем более злокачественна опухоль), приобрели способность быстро делиться, вытесняя нормальные клетки.
Причины такого явления до сих пор до конца не изучены. Одни ученые считают «виновниками» вирусы, другие – наличием определенных генов, третьи – продуктами жизнедеятельности живущих в организме паразитов. Тем не менее, если в таких мутировавших клетках сохранились рецепторы к половым гормонам, воздействие на них гормональными средствами будет уничтожать раковую опухоль. Такое воздействие является гормонотерапией при раке молочной железы.
Лекарства, используемые с терапевтической целью – это не гормоны, но вещества, блокирующие их действие на опухоль, таким образом не дающие ей расти. Они не используются сами по себе, но эффективны в сочетании с хирургическим удалением ракового новообразования, лучевой терапией и химиотерапией.
Лекарства, блокирующие гормональные рецепторы, дают хорошие результаты не исключительно в терапии маммарной карциномы, но и эффективно предупреждают развитие рецидивов и метастазов данной злокачественного образования.
Гормонотерапия, в случае рака груди, и заместительная гормонотерапия после лечения рака молочной железы – абсолютно разные понятия. В первом случае опухолевые клетки уничтожаются препаратами, включающимися в процесс синтеза половых гормонов, в результате чего выключается стимулирующее действие эстрогенов на рост опухоли. Заместительная же гормонотерапия после лечения патологии – это введение в организм женщины синтетических гормонов, которые будут замещать те, которые исчезли в результате лечения раковой опухоли (особенно если для подавления роста образования было применено хирургическое удаление яичников).
У женщины в крови постоянно имеются гормоны:
p, blockquote 9,0,0,0,0 —>
- 5 видов эстрогенов;
- 3 вида прогестеронов.
Их уровень различен в разные дни цикла, а при климаксе объем данных гормонов значительно снижается, так как яичники – основной «производитель» этих веществ – «отключается» по физиологическим причинам, остаются только эстрогены, синтезируемые надпочечниками и жировой тканью.
Женские гормоны связываются как «ключ с замком» со специальными структурами, рецепторами, на поверхности нужных клеток. «Замок» отворяется, пуская гормон внутрь, а дальше он вступает в реакцию с ядром клетки, и так регулирует ее размножение, рост и гибель. Максимальное число рецепторов находится в жировой ткани, яичниках и молочной железе.
Раковая опухоль, появляясь в молочной железе, строится из клеток, которые должны были быть нормальными, но видоизменились в процессе деления и не были уничтожены иммунной системой. Многие из них трансформировались не полностью, и рецепторы к эстрогенам и прогестеронам в них сохранились. Попадая к таким клеткам, обычные женские гормоны вызывают их усиленное деление с последующим попаданием в лимфу и кровь (метастазирование).
Таким образом, если у женщины обнаружен рак груди, и эта опухоль имеет рецепторы к половым гормонам (что чаще всего наблюдается после менопаузы), у врачей появляется дополнительный путь воздействия на нее: отключив механизм доставки гормона к опухолевым клеткам, подавить ее рост. Это не химиотерапия и не облучение злокачественного новообразования, которое может воздействовать только на делящуюся клетку. Здесь – другой путь: отключить возможность делиться у всех раковых клеток.
Гормональная терапия при раке молочной железы показана в том случае, если патологическое образование будет чувствительно к гормонам. Для определения чувствительности проводится иммуногистохимическое исследование клеток биопсийного материала, взятого у пациентки при биопсии. По результатам исследования в 65-75% паталогические клетки чувствительны как к эстрогенам, так и к прогестеронам, в 10% — только к прогестеронам.
Понять, что здесь нужна гормональная терапия, можно по заключению, выданному иммуногистохимической лабораторией:
p, blockquote 17,0,0,0,0 —>
- если написано «ER+/ PR +», это значит, что есть и эстрогеновые, и прогестероновые рецепторы, и назначенное гормональное лечение рака молочной железы располагает 70% шансом победить опухоль;
- «ER+/ PR -» или «ER-/ PR+», то есть наличие только одного типа рецепторов прогнозирует успех только в 33% случаев;
- когда написано, что «гормональный статус не известен», это означает, что на пути от забора клеточного материала из опухоли до лаборатории произошло его повреждение, нарушение правил транспортировки или хранения. Такие же слова лаборант напишет, если клеток слишком мало для проведения с ними иммуногистохимических реакций;
- заключение «гормоно-негативная» (оно обычно бывает в 25% случаев) означает, что в раковой опухоли рецепторов слишком мало.
В последних двух случаях гормонотерапия не проводится, так как ее прогнозируемая эффективность крайне низкая.
Обнаружение эстроген- или прогестин-позитивности в раковой опухоли – означает, что после ее хирургического удаления, чтобы возможно оставшиеся раковые клетки перестали делиться и через время отмерли, нужно применить гормонотерапию. Также подобное лечение можно применить и до вмешательства – чтобы снизить размер патологии и профилактировать ее метастазирования. Если злокачественное новообразование груди обнаружено на той стадии, когда операцию провести уже нельзя, гормонотерапия нужна для продления жизни пациентам.
Данный вид лечения используется при эстроген-положительных раках молочной железы в случаях:
p, blockquote 21,0,0,0,0 —>
- если у близких родственников отмечались злокачественные образования груди, а теперь и у женщины самой выявлен дефектный рост клеток органа;
- большие размеры опухоли;
- 0 стадия рака;
- рак имеет тенденцию к прорастанию в соседние ткани, нервы и сосуды;
- имеются метастазы;
- после лечения химио или лучевой терапией, а также после оперативного вмешательства – для профилактики рецидива.
Узнайте больше о раке молочной железы, его видах и методах лечения, перейдя по ссылке.
В зависимости от целей назначения, гормонотерапия может быть:
p, blockquote 25,0,0,0,0 —>
- Адъювантной. Она применяется по окончании операции, для профилактирования рецидива и метастазирования.
- Неоадъювантной. Проводится перед операцией, в основном, при 3 фазе рака и когда есть метастазы в лимфоузлы. Большинство пациенток, которым проводят такую терапию, находится в постменопаузе.
- Лечебной. Она применяется у неоперабельных пациенток, чтобы, остановив рост новообразования, продлить жизнь.
Препараты подбираются в зависимости от нескольких факторов:
p, blockquote 26,0,0,0,0 —>
- стадии раковой опухоли;
- того, находится женщина в менопаузе или нет;
- есть ли сопутствующие заболевания, которые усугубятся при снижении уровня (или блокаде) эстрогенов: остеопороз, артрит, тромбоз.
Сколько будет длиться гормонотерапия, зависит от вида выбранного препарата, его эффективности и переносимости.
Если блокаторы действия эстрогенов и прогестинов вызывают значительные побочные эффекты, в некоторых случаях может проводиться удаление яичников – хирургическое или лучевое. Это останавливает рост ракового новообразования за счет уменьшения выработки половых гормонов. После резекции яичников – для предупреждения рецидива рака молочной железы – назначаются уже не блокаторы эстрогенов или прогестеронов, а гормоны:
p, blockquote 28,0,0,0,0 —>
- андрогены (мужские гормоны) – чтобы гипофиз не стимулировал появление новых фолликулов в несуществующих уже яичниках;
- кортикостероиды (дексаметазон, преднизолон) – для выключения выработки эстрогенов надпочечниками;
- эстрогены – чтобы выключить функцию яичников и подавить выделение гипофизом тех веществ, которые направлены на стимуляцию яичников;
- эстрогены совместно с кортикостероидами нужны для угнетения надпочечниковой и гипофизарной стимуляции яичников, которые уже удалены.
По механизму действия, лекарства подразделяются на:
p, blockquote 31,0,0,0,0 —>
- Снижающие уровень в организме эстрогена.
- Останавливающие соединение женских гормонов с рецепторами клеток опухоли.
Модуляторы рецепторов к эстрогенам
До 2005 года гормонотерапию проводили только модулятором эстрогеновых рецепторов – Тамоксифеном. Этот препарат прочно связывается с рецепторами к эстрогену, не давая гормону попасть к ним. Он очень хорошо изучен, и именно этим объясняются описанные побочные эффекты гормонотерапии при раке молочной железы. Получается, другие антиэстрогеновые средства могут переноситься не лучше, просто они еще не так глубоко исследованы.
Другие препараты этой группы – Ралоксифен и Торемифен. Они также широко используются, к тому же не повышают риска формирования рака печени или карциномы эндометрия, как Тамоксифен.
Блокаторы эстрогеновых рецепторов
Препараты данной группы, например, Фаслодекс, разрушает эстррогеновые рецепторы опухоли.
Ингибиторы ароматазы
В основном, в постменопаузе, эстрогены образуются в жировой, мышечной, печеночной и надпочечниковой тканях из мужских гормонов. Происходят эти реакции под действием фермента ароматазы. Соответственно, если этот фермент «отключить», андрогены прекратят трансформироваться в эстрогены, а рак груди перестанет получать стимуляцию расти и делиться.
Эти средства сейчас признаны наиболее эффективными для лечения рака молочной железы на любых стадиях. К тому же, у них меньше побочных симптомов, чем у блокаторов эстрогенов.
Препаратом этой группы последнего поколения является Летрозол. Он связывается с геном одной из субъединиц ароматазы, которая превращает андрогенов в эстрогены, также ингибируя синтез эстрогенов в тканях.
Если препараты первых трех групп неэффективны, для проведения гормонотерапии назначаются прогестины. Они уменьшают секрецию тех гормонов гипофиза, которые «командуют» выработкой андрогенов и эстрогенов. Также прогестагены блокируют превращение эстрогенов из андрогенов внутри печеночной ткани.
Данные препараты обладают побочными эффектами: повышение давления, синдром Кушинга, кровотечения из влагалища.
Можно отметить такие основные последствия гормонотерапии при раке молочной железы:
p, blockquote 46,0,0,0,0 —> p, blockquote 47,0,0,0,1 —>
Несмотря на возможные осложнения, назначенное лечение принимать обязательно – оно продлевает жизнь.
источник
Гормонотерапия при раке молочной железыотносится к одним из вариантов лечения этой патологии. Ее целью является уменьшение стимулирующего воздействия женских половых гормонов (эстрогенов) на рост опухоли.
Новообразование в молочной железе состоит из перерожденных атипичных клеток. Многие из них сохранили рецепторы к эстрогенам и прогестерону. Это половые гормоны, вырабатываемые в норме в организме женщины. Они способствуют усиленному делению патологических клеток, проникновению их в кровь и попаданию в другие органы и ткани (метастазирование).
Показаниями для проведения гормонотерапии при раке молочной железыявляются:
- Наследственность. Если у близких родственников были подобные случаи заболевания, то применение гормонов будет достаточно эффективно.
- Большие размеры новообразования.
- 4-я стадия онкологического процесса и наличие метастазов. В этом случае гормональная терапия проводится в качестве паллиативного лечения.
- Для предупреждения повторного развития опухоли после проведенной операции.
- Противопоказания для проведения химиотерапии или облучения.
Таким образом, применяя гормоны, которые уменьшают образование эстрогена и прогестерона, можно уменьшить рост опухоли. Гормональная терапия показана только в том случае, если злокачественное образование чувствительно к гормонам. Для определения этого проводится биопсия с последующим иммуногистохимическим исследованием клеток.
Лаборатория выдает заключение, в котором может быть указано несколько вариантов:
- ER+/ PR +. Такой показатель значит, что опухоль содержит рецепторы к эстрогену и прогестерону. В этом случае гормонотерапия помогает уменьшить опухоль у 80 % больных.
- ER+/ PR -» или «ER-/ PR+». Это обозначает, что имеются только эстрогеновые или только прогестероновые рецепторы.
- Гормононегативная опухоль. Такое заключение выносится, когда рецепторы отсутствуют или их крайне мало. В этом случае гормонотерапия не эффективна.
- Неизвестный гормональный статус. Бывает при неправильном заборе биопсии, когда в биоптат не попадают атипичные клетки.
После хирургического вмешательства гормонотерапия необходима для того, чтобы оставшиеся раковые клетки потеряли способность к размножению.
Выделяют три вида гормонотерапии:
- Адъювантная.
- Неоадъювантная.
- Лечебная. Применяется при неоперабельных состояниях.
В зависимости от возраста женщины, пред или постменопаузы, гормонального статуса опухоли выбирают необходимый вариант терапии.
Адъювантная (дополнительная) гормонотерапия при раке молочной железы проводится после других способов лечения (хирургическое вмешательство, лучевая или химиотерапия). Она направлена на уменьшение риска повторных рецидивов онкологии грудии уничтожение метастазов опухоли за пределами первичного очага.
У молодых женщин в период перед менопаузой, при опухолях, содержащих большое количество эстрогеновых рецепторов, адъювантная системная терапия может быть ограничена только применением гормонов. Таким пациенткам назначаются препараты, которые приводят к подавлению функции яичников. Лечение длится в течение 5 – 10 дней.
У больных, находящихся в периоде менопаузы, в первую очередь назначаются ингибиторы ароматазы в качестве начальной терапии. Их прием снижает риск развития рака эндометрия и тромбоэмболических осложнений. Однако повышается вероятность возникновения остеопороза, суставных болей и переломов.
Такое лечение назначается перед хирургическим лечением, обычно длится от 3-х месяцев до полугода.
Целью метода является уменьшение размеров новообразования для снижения объема оперативного вмешательства. В этом случае возможно выполнение органосохраняющей операции.
Этот вид гормонотерапии является методом выбора для лечения первичного операбельного рака молочной железы и позволяет увеличить период безрецидивной ремиссии.

Благоприятными отдаленными результатами такого лечения является исчезновение атипично измененной ткани молочной железы и подмышечных групп лимфоузлов.
До начала проведения неоадъюватной терапии проводят обследование, при котором определяют биологическую характеристику опухоли, наличие рецепторов к прогестерону и эстрогену.
Этот метод лечения эффективен у пожилых женщин в постменопаузе. Такая методика позволяет не прибегать к проведению системной полихимиотерапии.
Применяется при неоперабельной опухоли для уменьшения новообразований, которые имеют размеры больше 5 см. Используется для того, чтобы замедлить рост опухоли и облегчить общее состояние больной.
Таким образом удается несколько улучшить качество жизни и ее продолжительность.
В некоторых случаях дополнительно применяют облучение яичников (лучевую кастрацию) или их удаление. Это также позволяет уменьшить выработку эстрогенов и прогестерона.
Для проведения гормонотерапии используются несколько групп препаратов.
Антиэстрогены.«Золотым стандартом» лечения новообразований молочных желез считается применение тамоксифена (фарестон, фазлодекс, нольвадекс).
При гормональных опухолях ржмв качестве первой линии гормонотерапии при ракеназначают именно этот препарат.
Его терапевтическое действие основано на селективной способности блокировать рецепторы эстрогенов. Он избирательно действует только на те рецепторы, которые находятся в клетках опухоли. Тамоксифен подавляет стимулирующие эффекты эстрогенов и уменьшает размеры новообразования.
Также он может блокировать эстрогеновые рецепторы в здоровых тканях молочной железы. Это позволяет предупредить дальнейшее распространение атипичных клеток.
Препарат назначают внутрь от 20 до 30 мг в сутки. Длительность курса лечения может составлять несколько лет. Его применяют женщинам при нормальном менструальном цикле, при менопаузе и в постменопаузальный период.
Ингибиторы ароматазы. В основном эстрогены синтезируются в организме женщины яичниками. Однако жировая и мышечная ткани, печень, надпочечники содержат особый фермент (ароматазу), которая способствует превращению андрогенов в эстрогены.
Такие препараты нельзя назначать женщинам в период менструации, потому что снижение эстрогенов в тканях и внутренних органах приведет к повышению их образования в работающих яичниках.
Ингибиторы ароматазы делятся на стероидные и нестероидные лекарственные средства.
К стероидным относится аминоглютетимид (ориметен, мамомит). Он вызывает обратимую блокировку ароматазы.

К нестероидными ингибиторам относятся фадразол, фемара, аримидекс. Эти препараты хорошо переносятся больными, имеют большой период полувыведения, редко приводят к развитию побочных эффектов.
Прогестины. Промегестон, дроспиренон, мегестрол уменьшают количество эстрогеновых рецепторов, снижают внутрипеченочное образование эстрогенов из андрогенов.
Эти препараты применяют парентерально или перорально. Прием лекарственного средства прекращают, если возникают побочные действия (рвота, головокружения, головные боли) или при отсутствии эффекта на онкологический процесс. Применение прогестинов не рекомендуется сочетать с одновременным употреблением других гормональных средств.
Андрогены. Угнетают фолликулостимулирующую функцию гипофиза, тем самым создавая неблагоприятные условия для роста опухоли.
Их рекомендуется назначать женщинам фертильного возраста и пациенткам, находящимся в менопаузе менее 10 лет. Наибольший эффект применения этих препаратов достигается после удаления яичников.
У женщин при сохранении менструального цикла используется следующая схема лечения:
- Длительное применение тамоксифена.
- Удаление или облучение яичников и наступление медикаментозной или лучевой менопаузы.
- Применение стероидных или нестероидных ингибиторов ароматазы.
У больных в период климакса (менопаузе) применяют:
- Проведение операции с последующей химио или лучевой терапией.
- Прием фемары или фазлодекса сроком не менее 5 лет.
Гормонотерапия является более щадящим методом, чем химиотерапевтическое лечение. Она легче переносится, у нее нет выраженного токсического эффекта. В этот период всем пациенткам рекомендуется длительный прием препаратов кальция.
Длительное применение андрогенов в качестве гормонотерапии при раке молочной железы может привести к неприятным последствиям.Наблюдается маскулинизация женщины: развивается облысение по мужскому типу, появляется увеличение клитора, грубеет голос, возникают прыщи на лице.
Ингибиторы ароматазы также имеют множество побочных эффектов: синдром Иценко -Кушинга, увеличение массы тела, судороги, головокружение, сонливость, отеки.
Прием антиэстрогенов может способствовать развитию гиперплазии эндометрия и частым маточным кровотечениям. Со стороны органов зрения часто наблюдается ретинопатия, катаракта.
К общим побочным эффектам гормонотерапии при раке молочной железы относятся:
- Депрессия и раздражительность.
- Ощущение «приливов».
- Сухость во влагалище.
- Бессонница.
- Алопеция.
- Повышенное тромбообразование.
- Высокий риск развития язвенных поражений желудочно – кишечного тракта.
- Бесплодие и злокачественные образования матки.
- Увеличение холестерина, образование атеросклеротических бляшек в сосудах.

Все эти симптомы носят кратковременный характер и проходят через несколько недель после завершения лечения.
Эффективность гормонотерапии при раке молочной железы зависит от размеров опухоли, стадии онкологического процесса, возраста женщины и наличия сопутствующих заболеваний. При гормонально – позитивной опухоли положительный эффект в лечении развивается у 70 – 80% больных.
При гормонально – неактивных опухолях такой вид лечения применять нецелесообразно.
источник
*Импакт фактор за 2017 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.
Российский онкологический научный центр им. Н.Н. Блохина РАМН
Х имиотерапия и гормонотерапия играют существенную роль в комплексном лечении рака молочной железы практически при всех стадиях заболевания. Это объясняется особенностями данной опухоли – даже на ранних стадиях заболевания велик риск существования отдаленных микрометастазов, особенно при наличии факторов риска (поражении подмышечных лимфоузлов, отрицательных рецепторах эстрадиола и прогестерона, гиперэкспрессии Неr–2/neu и т.д.). Применение адъювантной химио– и гормонотерапии значительно улучшило результаты лечения операбельного рака молочной железы. При запущенном раке молочной железы химиотерапия и гормонотерапия являются основными методами лечения, позволяющими значительно продлить жизнь больного и улучшить ее качество. У 10–25% женщин с диссеминированным раком молочной железы возможно достижение полной регрессии опухоли с длительным безрецидивным периодом.
Адъювантная терапия рака молочной железы сегодня представляет собой систему стандартов, эффективность которых доказана в большом числе клинических исследований [1].
До настоящего времени остается четыре независимых прогностических фактора при резектабельном раке молочной железы: поражение регионарных лимфатических узлов, размер первичной опухоли, степень дифференцировки и содержание рецепторов к стероидным гормонам (к эстрогенам – РЭ и к прогестерону – РП).
Стандартами химиотерапии и эндокринной терапии являются: 4 цикла химиотерапии в режиме АЦ (адриамицин + циклофосфан) или АЦФ (адриамицин + циклофосфан + фторурацил) или 6 циклов химиотерапии по схеме ЦМФ (циклофосфан + метотрексат + фторурацил), а также тамоксифен 20 мг в день в течение 5 лет.
Первый фактор, положенный в основу назначения адъювантной терапии – поражение регионарных лимфатических узлов, разделяет всех больных на две группы.
Рак молочной железы без метастазов в регионарные лимфоузлы
Для назначения адъювантной терапии в этой группе необходимо определение групп повышенного риска. Граница для назначения адъювантной лекарственной терапии, что означает группу повышенного риска – снижение пятилетней выживаемости до 95% и менее (табл. 1).
Только в группе низкого риска пятилетняя выживаемость больных составляет более 95%. Во всех остальных группах проведение адъювантной лекарственной терапии улучшает результаты хирургического лечения.
Больным в пременопаузе с умеренным или высоким риском и положительным уровнем эстрогенных рецепторов показана химиотерапия с последующим назначением тамоксифена. При гормононезависимых опухолях показано назначение только химиотерапии.
Больным в постменопаузе с умеренным или высоким риском и положительным уровнем эстрогеновых рецепторов показан прием тамоксифена, а в группе высокого риска – комбинация химиотерапии с тамоксифеном. При отрицательном уровне рецепторов к эстрогенам показано применение только химиотерапии.
Всем пожилым больным (старше 70 лет) показан прием тамоксифена, а в группе высокого риска возможно дополнительное назначение химиотерапии. С уче– том возраста больных дополнительное назначение химиотерапии должно быть индивидуально обоснованным.
Рак молочной железы с метастазами в регионарные лимфоузлы
У всех больных раком молочной железы с метастазами в регионарные лимфатические узлы применение адъювантной лекарственной терапии улучшает результаты лечения.
При положительном уровне рецепторов к эстрогенам вне зависимости от менструальной функции показана комбинированная адъювантная терапия – химиотерапия и эндокринная терапия тамоксифеном.
При гормононезависимых опухолях показано применение только химиотерапии.
Всем пожилым больным (старше 70 лет) показан прием тамоксифена вне зависимости от уровня эстрогеновых рецепторов. Если уровень рецепторов к эстрогенам отрицательный, возможно дополнительное назначение химиотерапии. С учетом возраста больных дополнительное назначение химиотерапии должно быть индивидуальным.
При всей внешней простоте и схематичности назначения адъювантного лечения лишь методы, доказавшие свою эффективность в результате длительных клинических исследований, применяются для лечения больных. Оптимальная тактика адъювантной терапии постоянно совершенствуется. Совсем недавно химиотерапия рекомендовалась только больным в пременопаузе с метастазами в регионарные лимфатические узлы. В настоящее время только больным с низким риском и пожилым больным с положительными эстрогеновыми рецепторами не показано проведение химиотерапии.
При проведении адъювантной химиотерапии необходимо строго придерживаться оптимального режима (стандартных доз и интервалов между циклами). Неоправданные модификации режимов химиотерапии, несомненно, ухудшают результаты лечения.
Сегодня продолжаются исследования роли выключения функции яичников и рутинное применение данного метода адъювантного лечения нецелесообразно.
Появились данные об эффективности таксанов, как дополнительной химиотерапии к антрациклин–содержащим комбинациям у больных с неблагоприятным про– гнозом.
В связи с широкими исследованиями роли гиперэкспрессии рецептора Her2/neu наметились новые тенденции в оценке прогноза и лечения больных. Однако пока необходимо дополнительное число исследований для изменения практических рекомендаций.
Исследования по адъювантной терапии рака молочной железы интенсивно продолжаются, и можно надеяться, что в ближайшее время все больше и больше женщин будут излечиваться от рака молочной железы.
Неоадъювантная терапия – системное лечение, которое проводится до начала локального лечения (хирургического вмешательства или лучевой терапии).
Задачи неоадъювантной терапии:
- уменьшение размеров первичной опухоли и регионарных метастазов
- уменьшение объема оперативного вмешательства (радикальная резекция вместо радикальной мастэктомии)
- определение чувствительности опухоли к цитостатикам, выявление резистентных случаев с целью использования альтернативных режимов для адъювант– ной химиотерапии
- увеличение общей и безрецидивной выживаемости
- оценка новых режимов лечения по частоте полной клинической и морфологической ремиссии.
Стандартом неоадъювантной химиотерапии по результатам многоцентрового исследования NSABP B–18 признана схема АЦ, при применении которой объективный эффект составил 80%, полная морфологическая ремиссия отмечена у 15% больных.
Предполагалось, что раннее воздействие противоопухолевых лекарств на микрометастазы приведет к увеличению общей и безрецидивной выживаемости. Однако анализ 7 крупных рандомизированных исследований, в том числе NSABP B–18, включившего 1500 женщин с операбельным раком молочной железы, проведенный Wolff [2], не подтвердил эту гипотезу. Продолжительность жизни может быть увеличена только за счет рационального подхода к лечению – использования альтернативных режимов для адъювантной химиотерапии в случае низкой эффективности неоадъювантного лечения.
Продолжается поиск наиболее эффективного режима неоадъювантной химиотерапии. Особенно важным показателем является достижение полной морфологической регрессии опухоли, так как именно этот показатель статистически достоверно коррелирует с ростом общей выживаемости. С этой целью исследуются комбинации, включающие наиболее эффективные препараты, входящие в режимы неоадъювантной химиотерапии в последние годы – цисплатин, навельбин, таксаны. Некоторые авторы показали преимущество комбинаций антрациклинов и таксанов по сравнению со стандартным режимом АС. Разрабатываются новые режимы, включающие препараты, недавно вошедшие в практику химиотерапии, например, кселода и герцептин. Исследуются интенсивные режимы химиотерапии, однако пока не получено достоверных доказательств влияния интенсификации неоадъювантной химиотерапии на отдаленные результаты лечения.
Обсуждается количество курсов неоадъювантной химиотерапии. Признано, что эффект химиотерапии и частота полных регрессий опухоли зависят от количест– ва курсов лечения. Поэтому целесообразно проводить не менее 4 курсов, что безопасно для больных при условии регулярного контроля за динамикой заболевания.
У больных в менопаузе с положительными РЭ и/или РП применяется неоадъювантная гормонотерапия. Объективный эффект гормонотерапии достигает 50–70%. Для неоадъювантной гормонотерапии могут быть рекомендованы тамоксифен, анастразол, летрозол, экземестан.
Диссеминированный рак молочной железы
Для выбора метода лечения перед началом терапии необходимо оценить ряд прогностических факторов, определяющих возможный ответ заболевания на проводимое лечение. Длительный период, прошедший после лечения первичной опухоли до появления отдаленных метастазов, поражение только мягких тканей и костной системы или единичные отграниченные очаги в легких, медленный рост опухоли, удовлетворительное общее состояние больной, пожилой возраст и постменопауза, положительный уровень рецептов эстрадиола и/или прогестерона свидетельствуют о вероятно высокой чувствительности опухоли к гормонотерапии. В случае раннего появления отдаленных метастазов после лечения первичной опухоли, быстрого прогрессирования заболевания, молодого возраста больной, при множественных висцеральных метастазах, наличии лимфангоита кожи или легких лечение необходимо начинать с химиотерапии.
Эффективность гормонотерапии при положительном уровне РЭ и РП достигает 50–70%, снижается при положительных рецепторах одного вида (33%). При отрицательных РЭ и РП существует небольшой процент больных (5–10%), отвечающих на гормонотерапию. Традиционными препаратами, рекомендованными для первой линии гормонотерапии у больных в менопаузе, являются антиэстрогены – тамоксифен и торемифен. В настоящее время в I линии эндокринотерапии альтернативой тамоксифену являются антиароматазные препараты – анастрозол и летрозол. Во II линии эндокринотерапии больных раком молочной железы в менопаузе (при использовании тамоксифена в I линии) в настоящее время вместо прогестинов используются антиароматазные препараты (анастрозол, летрозол, экземестан). Применять прогестины во II линии гормонотерапии считается неэтичным.
У больных в пременопаузе гормонотерапию можно начинать с выключения функции яичников с помощью агониста гонадотропин–рилизинг гормона гипофиза – гозерелина (золадекса), а также хирургическим или лучевым методами.
Эффект гормонотерапии оценивается через 6–8 нед после начала лечения. Положительным ответом считается не только полная или частичная регрессия опухоли, но и длительная стабилизация заболевания (>=6 месяцев). Лечение продолжается до прогрессирования болезни. В случае быстрого прогрессирования болезни после гормонотерапии первой линии следует начать химиотерапию. При прогрессировании после длительного положительного эффекта на фоне первой линии гормонотерапии, а также кратковременной полной или частичной регрессии опухоли начинают гормонотерапию второй линии – ингибиторы (инактиваторы) ароматазы.
Наиболее известные ингибиторы ароматазы – аминоглютетемид (ориметен, мамомит), ингибитор ароматазы первого поколения, стероидный инактиватор ароматазы – экземестан (аромазин) и препараты третьего поколения – летрозол (фемара), анастрозол (аримидекс). Экземестан, летрозол и анастрозол менее токсичны и не требуют заместительной кортикостероидной терапии. Они эффективны и у больных, принимавших ранее аминоглютетемид: если лечение аминоглютетемидом было эффективным, частота ответа составляет 25–33%, если неэффективным – 6–12%. У пременопаузальных больных ингибиторы ароматазы назначаются только после выключения функции яичников, чтобы избежать активизации синтеза эстрогенов в функционирующих яичниках по принципу «обратной связи».
Третья линия гормонотерапии – прогестины – медроксипрогестерона ацетат (фарлутал, провера) и мегестрола ацетат (мегейс). Достаточно редко в наше время в III линии гормонотерапии используются андрогены и у женщин в постменопаузе – эстрогены.
Стандартами I линии химиотерапии рака молочной железы являются схемы: ЦМФ (циклофосфан 100 мг/м 2 внутрь ежедневно дни 1–14, метотрексат 40 мг/м 2 в/в дни 1,8, фторурацил 600 мг/м 2 в/в дни 1,8, интервал 4 нед), ЦАФ (циклофосфан 100 мг/м 2 внутрь ежедневно дни 1–14, доксорубицин 30 мг/м 2 в/в дни 1,8, фторурацил 500 мг/м 2 в/в дни 1, 8, интервал 4 недели), АЦФ (фторура– цил 500 мг/м 2 , доксорубицин 50 мг/м 2 , циклофосфан 500 мг/м 2 каждые 3 нед), ЕЦФ (фторурацил 500 мг/м 2 , эпирубицин 100 мг/м 2 , циклофосфан 500 мг/м 2 каждые 3 нед), АЦ (доксорубицин 60 мг/м 2 , циклофосфан 600 мг/м 2 каждые 3 нед).
Большинство исследователей отдают предпочтение антрациклиновым комбинациям, учитывая более высокий противоопухолевый эффект этих комбинаций по сравнению с ЦMФ. Комбинация ЦМФ чаще используется у пожилых больных, при противопоказаниях к применению антрациклинов.
Высокую эффективность показали комбинации антрациклинов и таксанов – АТ (доксорубицин 50–60 мг/м 2 , паклитаксел 175 мг/м 2 , интервал 3 нед), ЕД (эпирубицин 100 мг/м 2 , доцетаксел 75 мг/м 2 , интервал 3 нед).
Длительность химиотерапии обычно определяется ответом опухоли: после достижения максимального эффекта проводится дополнительно 2 курса ПХТ. Затем предпочтение может быть отдано наблюдению за больным до прогрессирования. При продолжении лечения до прогрессирования увеличивается время до прогресси– рования, однако общая выживаемость не меняется, при этом снижается качество жизни больных.
Ведется поиск эффективных комбинаций для первой линии лечения диссеминированного рака молочной железы, включающих новые препараты, в частности, капецитабин (кселода). Показано, что капецитабин имеет лечебную активность, сходную с ЦМФ.
У больных, имевших прогрессирование после химиотерапии антрациклинсодержащими комбинациями, стандартом дальнейшего лечения являются таксаны (паклитаксел 175 мг/м 2 в/в со стандартной премедикацией 1 раз в 3 нед, доцетаксел 100 мг/м 2 в/в со стандартной премедикацией 1 раз в 3 нед). В монотерапии у резистентных к антрациклинам больных объективный эффект составляет 41%. В последнее время все более популярным становится еженедельное введение таксанов, при этом увеличивается интенсивность лечения без увеличения токсичности. Эффективны комбинации таксанов с другими препаратами: навельбин 20 мг/м 2 в/в дни 1, 5-й + доцетаксел 75 мг/м 2 в/в со стандартной премедикацией день 1-й, интервал 3 нед; паклитаксел 175 мг/м 2 в/в со стандартной премедикацией день 1-й + фторурацил 1 г/м 2 /день в/в кап. 72–часовая инфузия дни 1, 2, 3-й, интервал 3 нед; кселода 1650 мг/м 2 дни 1–14 + паклитаксел 175 мг/м 2 (или доцетаксел 75 мг/м 2 )1 раз в 3 нед; гемцитабин 1 г/м 2 дни 1, 15-й + паклитаксел 135 мг/м 2 дни 1, 15-й, интервал 4 нед.
Для третьей и последующих линий лечения четких стандартов не разработано. Применяются комбинации препаратов, включающие навельбин, препараты платины (цисплатин, оксалиплатин), антиметаболиты (длительные инфузии фторурацила, гемцитабин, томудекс, кселода). Следует отметить высокую эффективность кселоды у больных во II (объективный ответ у 36% больных) и III (20%) линиях химиотерапии. Препарат может быть рекомендован, как альтернатива таксанам во II линии химиотерапии.
Некоторые режимы, эффективные во II–III линии лечения диссеминированного рака молочной железы: МММ – митомицин 8 мг/м 2 в/в день 1 + митоксантрон 8 мг/м 2 в/в день 1 + метотрексат 30 мг/м 2 в/в день 1; МЕП – митомицин 10 мг/м 2 в/в день 1 + цисплатин 40 мг/м 2 в/в дни 2, 7 + вепезид 100 мг/м 2 в/в дни 3 ,4, 5, интервал 4 нед; цисплатин 80 мг/м 2 в/в день 1 + кселода 2000 мг/м 2 внутрь ежедневно дни 1–14; навельбин 25 мг/м 2 в/в дни 1, 8 + митомицин 7 мг/м 2 в/в день 1, интервал 4 недели; навельбин 20 мг/м 2 в/в дни 1, 15 + цисплатин 80 мг/м 2 в/в день 1, интервал 4 нед; циклофосфан 600 мг/м 2 в/в день 1 + лейковорин 500 мг/м 2 в/в кап. в течение 2 часов + фторурацил 1,5 г/м 2 в/в постоянная 24–часовая инфузия, дни 1, 15, интервал 4 нед; навельбин 25 мг/м 2 в/в дни 1, 8 + томудекс 1 мг/м 2 в/в дни 1, 8, интервал 3 нед.
В 25–30% случаев в опухоли молочной железы отмечается гиперэкспрессия Неr–2/neu, коррелирующая с плохим прогнозом заболевания. У таких больных эф– фективен Герцептин – препарат принципиально нового механизма действия – рекомбинантные гуманизированные моноклональные антитела, связывающиеся с рецептором Неr–2/neu. Герцептин применяется еженедельно, первое введение – 4 мг/кг в/в, последующие – 2 мг/кг. Лечение продолжается до прогрессирования заболевания. Герцептин рекомендуется к применению у больных с гиперэкспрессией Неr–2/neu в комбинации с гормонотерапией и химиотерапией. Добавление герцептина к комбинации АС повысило частоту объективных эффектов с 42 до 60%. При резистентности к антрациклинам комбинация герцептина с таксолом была эффективна у 49% больных (при монотерапии таксолом эффект составил 17%). Изучаются комбинации герцептина с другими цитостатиками, например, с кселодой, навельбином [5].
1. Материалы шестой конференции по адъювантной терапии рака молочной железы, Сан–Галлен Швейцария, 1998 год.
2. A.C.Wolff, N.E. Davidson: Primary systemic therapy in operable breast cancer. J Clin Oncol 18:1558–1569, 2000.
3. C.А. Тюляндин: Химиотерапия диссеминированного рака молочной железы. Практическая онкология, 2, 2000.
источник
Рак молочной железы относят к гормонозависимым опухолям, поэтому очень действенным считается проведение гормонотерапии при раке молочной железы.
Гормонотерапия это один из способов терапии онкологии молочной железы, среди которых химиотерапия, радиотерапия и хирургический способ лечения. Гормонотерапия преследует своей целью уменьшить воздействие гормона эстрогена на раковое новообразование.
Метод лечения гормонами составляет специалист, он учитывает стадию заболевания, статус менопаузы женщины, риск рецидивного возникновения раковой опухоли. Очень важно сочетать лечение онкологии груди с другими заболеваниями, так их присутствие может усилить побочные эффекты.
При лечении такого вида рака применяются различные виды лечения, в постменопаузе отличный результат выдают лекарственные препараты, которые понижают выработку гормона эстрогена, а в репродуктивном возрасте применяют релизинг-гормоны.
Назначение гормональной терапии показано, если биопсия показала, что рак является гормонозависимым и это делает лечение в 70% случаев успешным.
Гормонозависимая опухоль груди появляется, если повышается гормон эстроген, а его повышение возможно при использовании его при лечении:
- поликистоза яичников;
- нарушений месячных;
- миомы матки.
К группе риска можно отнести женщин, которые:
- имеют сбои в работе яичников;
- сделали аборт;
- имели угрозу выкидыша;
- перенесли замершую беременность.
Симптомами гормонозависимой опухоли груди считаются:
- увеличение лимфоузлов;
- боли в месте новообразований;
- появление уплотнений.
Показателями для рекомендации лечения гормонотерапией при гормонозависимых опухолях являются:
- наследственный фактор;
- внушительные размеры опухоли;
- рак на последней стадии;
- метастатический рак;
- для предотвращения рецидива после лечения карциномы;
- возникновение метастаз.
Уменьшение уровня эстрогенов и прогестерона в крови проявляет, в общем, положительное воздействие на здоровье женщины, это снижает вероятность рецидива гормонозависимого заболевания.
Гормонотерапию целесообразнее проводить в сочетании с прочими способами лечения. Назначение лечения гормональными препаратами проводят при:
- Вероятности появления метастазов;
- Различных уплотнениях после проведения операции;
- Раке, не поддающегося химиотерапии;
- Росте новообразования в отсутствии роста онкоклеток.
Запомните! Терапия рака молочной железы при помощи гормонотерапии разрешает одновременно несколько проблем, каждая из которых требует использование определенного препарата.
Выбор метода воздействия зависит от некоторых факторов:
- Предыдущих способов лечения;
- Гормонального статуса раковой опухоли;
- Стадии онкологического заболевания;
- Непереносимости препаратов;
- Сопутствующих диагнозов (некоторые болезни ухудшают прогнозы основного заболевания);
- Периода жизни пациента – пре- и постменопауза.
Так же при назначении лечения требуется знать, присутствуют ли в опухоли рецепторы к гормонам, и к которым именно. От гормонального статуса заболевания зависит и назначение лечения. Наиболее благоприятный прогноз, когда есть рецепторы одновременно к прогестерону и эстрогену, также бывают случаи:
- Негативности ко всем гормонам;
- Неизвестного гормонального статуса;
- Чувствительности только к эстрогену (прогестерону), когда рецептор эстрогена (прогестерона) позитивный.
Гормонотерапия рака молочной железы (РМЖ) подразделяется на три вида:
- Адъювантная гормонотерапия может длиться около 5-10 лет, она выполняется для уменьшения риска рецидива карциномы;
- Неоадъювантная гормонотерапия проводится в промежутке 3-6 месяцев, ее назначают перед операцией, когда опухоль более 2 см и в процесс втянуты лимфоузлы;
- Лечебная гормонотерапия применяется при неоперабельных опухолях или для уменьшения и устранения раковых очагов (больше 2 стадии (2а)).
* Только при условии получения данных о заболевании пациента, представитель клиники сможет рассчитать точную цену на лечение.
Можно выделить несколько ведущих видов гормонального лечения, любой из которых имеет отдельный механизм воздействия: понижение уровня эстрогена в крови, прекращение его выработки или ее уменьшение:
- Ингибиторы ароматазы. Они оказывают влияние на концентрацию эстрогенов, блокируя рецепторы и не давая клеткам размножаться и делиться. Такие ингибиторы прописываются больным после наступления менопаузы. Можно выделить 3 вида ингибиторов ароматазы при онкологии груди: Фемара, Аримидекс, Аромазин. Но эти препараты могут привести к повышению хрупкости костей. При приеме подобных препаратов назначается кальций с витамином D, для предотвращения остеопороза;
- Блокираторы эстрогеновых рецепторов, при эстрогенозависимых опухолях. Эти препараты предотвращают воздействие на клетки раковой опухоли. К таким препаратам можно отнести: Фулвестрант, Фазлодекс;
- Модуляторы рецепторов к эстрогенам, которые останавливают выработку эстрогенов. Это антиэстрогенные препараты в таблетках: Кломифен, Тамоксифен;
- Прогестины, которые уменьшают выработку определенных гормонов гипофиза, которые ответственны за появление андрогенов и эстрогенов;
- Воздействие на яичники — еще один способ гормонотерапии. Таких способов три: медикаментозный (инъекции Золадексом или Люпроном), хирургический (удаление яичников — овариэктомия), радиационное облучение.
При лечении возможны побочные эффекты, появление которых зависит от множества факторов: стадии онкологического заболевания молочной железы, когда было получено лечение, возрастной категории пациентки, общего состояния здоровья, схемы назначенного лечения. Самыми частыми побочными эффектами являются:
- Преждевременный климакс и сопутствующие ему симптомы – приливы, увеличение веса и т.д.;
- Отечность ног;
- Проблемы со сном;
- Нарушение пищеварения (запоры или поносы);
- Боли в деснах;
- Сухость влагалища;
- Тошнота или рвота;
- Алопеция;
- Усиленная потливость;
- Депрессия;
- Ухудшение памяти.
В основном, эти симптомы через непродолжительное время проходят (спустя несколько недель по завершению лечения гормонами), иногда может продолжаться до 2 месяцев.
Ингибиторы ароматазы могут спровоцировать возникновения остеопороза, повышают холестерин в крови, могут вызвать проблемы с ЖКТ и приводят к алопеции.
Тамоксифен повышает риск тромбообразования, гепатита, является фактором риска для возникновения рака матки и проблем бесплодия.
Золадекс и Люпрон вызывают скачки давления, артралгию, депрессию.
После хирургического удаления яичников может нарушаться водно-солевой обмен, может развиться алкалоз, поднятие уровня сахара в крови, также может диагностироваться синдром Кушинга и язвенные поражения органов ЖКТ.
При приеме прогестинов возможно прибавление веса, выпадение волос, тромбоэмболические осложнения.
Диета при лечении гормонотерапией может понизить вероятность появления рецидива заболевания. В питании предпочтение надо отдавать отварным или тушеным блюдам, исключив полностью жареное. Также ограничения касаются употребления сахара, солений, жиров животного происхождения. Полностью исключить требуется:
- Консерванты;
- Кофе;
- Сою;
- Фастфуд;
- Продукты с пищевыми добавками;
- Алкоголь.
Из мясных блюд желательно употреблять нежирные сорта мяса, рекомендуется добавлять в пищу лук и чеснок. Пить побольше жидкости, простой воды. В рационе должны присутствовать следующие продукты:
- Морепродукты;
- Крупы;
- Фрукты;
- Растительные жиры;
- Жирная морская рыба;
- Морская капуста;
- Яйца;
- Овощи;
- Молочные продукты.
Эффективность гормонотерапии при онкологии молочной железы зависит от размера опухоли, также играет немаловажную роль наличие сопутствующих заболеваний и иммунитет пациентки.
Эффективность лечения гормонотерапией довольно высока, но требуется соблюдение всех рекомендаций врача, в том числе относительно питания.
Прогнозы гормонотерапии довольно оптимистичны, особенно, если гормонозависимая опухоль имеет рецепторы, и прогестерона, и эстрогена, тогда эффективность лечения составляет – 70 % случаев, при нахождении в опухоли, хотя бы одного из гормонов – эффективность составляет 30%. При прочих видах карциномы груди эффективность терапии составляет всего лишь 10%. При опухоли, которая считается негормонозависимой, такой тип лечения применять нецелесообразно.
Нужна ли гормонотерапия после мастэктомии?
Для предотвращения появления метастаз гормонотерапию могут назначить после хирургического вмешательства.
источник