Рак молочной железы – одно из самых распространенных «женских» онкологических заболеваний. Риск заболеть для среднестатистической женщины в течение жизни составляет 6%. В этой статье Сергей Михайлович Портной — онколог-маммолог Европейской клиники, доктор медицинских наук, — рассказывает о том, почему в молочной железе возникают злокачественные опухоли, какие существуют факторы риска и методы профилактики.
В 2016 году в России рак молочной железы был диагностирован у 68547 женщин и у 548 мужчин. Этот тип рака относится к опухолям видимой локализации: если регулярно осматривать и ощупывать молочные железы, его можно самостоятельно обнаружить на ранних стадиях. Тем не менее, на момент обращения к врачу в 26,3% случаях заболевание диагностируется на III и IV стадиях, когда его уже считают запущенным.
Заболеваемость раком молочной железы с каждым годом растет примерно на 2% — не только в России, но и в других развитых странах. Но смертность ежегодно снижается — тоже на 2%.
Ученые называют две основные причины развития рака молочной железы:
Мутации в генах. Они бывают наследственными, и в этом случае передаются от родителей детям.
Но чаще всего генетические дефекты, из-за которых возникает рак молочной железы, являются приобретенными, то есть возникают в течение жизни и не передаются потомству.
Гормональные нарушения.
Многие опухоли молочной железы являются гормонально-позитивными.
Размножение раковых клеток стимулируют высокие уровни женских половых гормонов — эстрогенов.
В 1936 году ученые провели интересный эксперимент. Они вывели две группы лабораторных мышей: у одних риск рака молочной железы был обычным, а у других искусственно повышен — вероятность развития опухоли составляла 88%.
Далее ученые взяли детенышей мышек с повышенным риском и отдали на вскармливание животным из первой группы. Молоко приемных мам оказалось «целебным»: среди этих мышат и их потомства резко снизилась распространенность рака молочной железы, хотя у них и была изначально «плохая наследственность».
Оказалось, что в молоке мышей, склонных к развитию рака, присутствует вирус MMTV (mouse mammary tumor virus). Он же был обнаружен и у женщин. Но исследователи пока не спешат переносить результаты «мышиных экспериментов» на человека. Вирусная теория пока остается недоказанной.
С развитием злокачественных опухолей связаны две разновидности генов: условно их называют протоонкогенами и генами-супрессорами.
Протоонкогены кодируют белки, которые отвечают за нормальное размножение клеток. Если в таком гене происходит мутация, или появляется очень много его копий, он превращается в онкоген. Соответствующий белок становится слишком активным, и клетка начинает бесконтрольно размножаться.
Гены-супрессоры предотвращают развитие злокачественных опухолей. Они подавляют размножение клеток, «ремонтируют» поврежденную ДНК и вызывают апоптоз — запрограммированную клеточную смерть. Если в гене-супрессоре происходит мутация, то белок, который он кодирует, больше не может нормально выполнять свои функции.
Протоонкогены и гены-супрессоры можно сравнить с педалями «газ» и «тормоз» в автомобиле. В опухолевых клетках «водитель» постоянно давит на «газ», либо отказывают «тормоза». При раке молочной железы чаще всего происходит второе: перестают нормально работать гены-супрессоры.
Наследственные опухоли молочной железы встречаются в 5–15% случаев.
За последние десятилетия ученые обнаружили десятки разных генов, которые, так или иначе, способствуют развитию рака груди. В таблице представлены самые распространенные:
- Гены BRCA1 и BRCA2 участвуют в репарации ДНК, играют важную роль в развитии эмбриона. Риск РМЖ при мутациях — 65% и 45% соответственно.
- Ген ATM участвует в восстановлении поврежденной ДНК, а если она не может быть восстановлена — способствует гибели клетки. Риск РМЖ при мутации — 52%.
- Ген BLM rодирует белок из группы геликаз — «опекунов генома». Участвует в копировании и восстановлении ДНК. Риск РМЖ при мутации повышается в 6,28 раз.
- Ген BRIP1 участвует в репарации ДНК. Риск РМЖ при мутации повышается в 2-7,7 раз.
- Ген CDH1 кодирует Е-кадгерин, который регулирует дифференцировку (созревание) клеток и нужен для межклеточного соединения. При мутации CDH1 развивается наследственный диффузный рак желудка. Риск РМЖ при мутации — 42% (повышается к 80 годам).
- Ген CHEK2 участвует в репарации ДНК. Риск РМЖ при мутации — 28% — 44%.
- Ген LKB1 кодирует фермент серин/треонинкиназу 11, которая помогает клеткам правильно ориентироваться в тканях, регулирует использование клетками энергии, способствует запуску апоптоза. Риск РМЖ при мутации — 29%.
- Гены NBS1 и MLH1 участвуют в восстановлении ДНК. Риск РМЖ при мутации повышается в 3,1 и 3,41 раза соответственно.
- Ген PALB2 кодирует белок, который взаимодействует с продуктом гена BRCA2 и участвует в восстановлении ДНК. Риск РМЖ при мутации — 33% — 58%.
- Ген PTEN регулирует рост клеток. Мутация в этом гене приводит к синдрому Коудена. Риск РМЖ при мутации — 85.2%.
- При мутации в гене RECQL риск РМЖ повышается в 33,5 раза.
- Ген TP53 кодирует белок р53 — «страж генома», который активируется при повреждении ДНК, останавливает размножение клетки и вызывает апоптоз. Риск РМЖ при мутации — 45%.
Приобретенные мутации возникают в течение жизни и не передаются по наследству. Некоторые из них безобидны и не влияют на работу клеток, а некоторые приводят к раку. В настоящее время известны далеко не все приобретенные мутации, которые связаны с раком молочной железы.
Примерно в каждом пятом случае в опухоли повышено количество HER2 — белка-рецептора, который находится на поверхности клеток и стимулирует их размножение. Такой рак называется HER2-позитивным. Существуют таргетные препараты, способные ингибировать этот белок.
Главный и самый очевидный фактор риска рака молочной железы — принадлежность к женскому полу. Хотя у мужчин заболевание тоже встречается, женщины болеют в 100 раз чаще.
Далее, говоря о факторах риска рака молочной железы, мы поделим их на две группы: те, на которые нельзя повлиять, и те, которые связаны с образом жизни.
Факторы риска, на которые вы не можете повлиять:
- Возраст. Со временем во всех клетках организма накапливаются мутации. «Ошибки» при копировании ДНК во время деления клеток неизбежны. Рак молочной железы чаще всего встречается после 55 лет. В современных развитых странах население «стареет», и это одна из причин роста распространенности рака молочной железы.
- Наследственность. Если у женщины есть одна близкая родственница, у которой диагностирован рак молочной железы, ее риски повышаются примерно вдвое, если две такие близкие родственницы — втрое. «Примерно 15% женщин, страдающих раком груди, имеют близких родственниц, у которых тоже установлен этот диагноз.
- Раннее менархе. Научные исследования показали, что риск напрямую зависит от того, в каком возрасте были первые месячные. Чем раньше, тем больше вероятность получить диагноз «рак молочной железы» в будущем.
- Поздняя менопауза. Здесь снова есть прямая связь: чем раньше наступила менопауза, тем ниже риск. Если условно считать, что при прекращении месячных в 50–54 года вероятность заболеть равна 1, то при менархе после 55 лет она составит 1,12, а до 40 лет — лишь 0,67.
- Радиация. Когда изучили судьбу 77 752 жителей Японии, перенесших атомную бомбардировку Хиросимы и Нагасаки, оказалось, что к 2002 году у 14 048 из них были диагностированы злокачественные опухоли, в том числе 970 случаев рака молочной железы. Риски повышаются и после курсов лучевой терапии. Например, у женщин, которые в 25–30 лет перенесли облучение по поводу болезни Ходжкина, риск заболеть раком груди к 40–45 годам составил 13%, в то время как среди всех женщин в целом этот показатель составляет лишь 1%.
- Плотность ткани молочной железы. Ее определяют с помощью рентгенографии, и если она повышена, риск рака груди увеличивается примерно в полтора раза. Плотность ткани молочной железы зависит от соотношения в ней железистой, фиброзной и жировой ткани. Ее повышение может быть связано с физиологическими изменениями или фиброзно-кистозной мастопатией.
Факторы риска, связанные с образом жизни, на которые можно повлиять:
- Отсутствие родов. Каждые последующие роды, по данным некоторых исследований, снижают риск примерно на 7%.
- Поздние роды. У женщин, родивших первого ребенка в 30–34 года риск повышен в 2,2 раза по сравнению с теми, кто родили до 25 лет, а при первых родах после 35 лет — в 3,3 раза.
- Отсутствие грудного вскармливания. Проанализировав данные 150 000 женщин, ученые обнаружили, что каждые 12 месяцев кормления грудью снижают риск на 4,3%.
- Гормональные контрацептивы. Риск постепенно снижается после того как женщина перестает принимать препараты и опускается до среднестатистических показателей через 10 лет. Внутриматочные средства и вагинальные кольца с гормонами также повышают вероятность заболевания.
- Заместительная гормональная терапия (ЗГТ) во время менопаузы. Опыт США показал, что сокращение применения ЗГТ помогает снизить заболеваемость раком молочной железы. Гормональные препараты для лечения симптомов менопаузы нужно назначать с осторожностью, врач должен взвесить все за и против, рассказать женщине о возможных рисках.
- Избыточная масса тела и ожирение. Этот фактор приобретает особое значение в постменопаузе. Жировая ткань вырабатывает эстрогены, при избыточной массе повышается уровень инсулина, и это способствует развитию рака молочной железы. Но здесь не всё так просто и однозначно. Например, у женщин-европеек в репродуктивном возрасте с увеличением массы тела риски, напротив, снижаются, а у азиаток — растут. Большое значение имеет распределение подкожного жира — опаснее всего, когда он откладывается преимущественно в области талии.
- Алкоголь. При ежедневном употреблении более 28 граммов этилового спирта (700 мл 5% пива, или 300 мл 12% вина, или 90 мл водки) риск рака молочной железы повышается на 20% по сравнению с непьющими.
Из разряда мифологии: какие факторы не повышают вероятность развития рака груди?
- Аборты: ни спонтанное, ни искусственное прерывание беременности не повысят ваши риски. Это было доказано после анализа данных 83 000 женщин из 16 стран мира.
- Антиперспиранты по слухам нарушают отток лимфы, способствуют образованию токсичных веществ и развитию онкологических заболеваний. Но этому нет никаких научных подтверждений.
- Бюстгальтеры одно время незаслуженно обвиняли в том, что они способствуют развитию рака, потому что сдавливают молочные железы и препятствуют нормальному кровообращению, оттоку лимфы. Этот миф опровергло исследование 2014 года, в котором приняло участие 1500 женщин.
Защитить себя от рака молочной железы на 100% невозможно, но некоторые меры помогают снизить риск.
Для того чтобы понять, какие виды профилактики нужны в конкретном случае, нужно определить индивидуальные риски женщины. Это делают с помощью специальной таблицы по модели Гейла, разработанной Национальным институтом рака США и центром биостатистики исследовательской группы NSABP.
Факторы риска, которые учитываются по модели Гейла:
- Раннее начало менструаций (до 11-12 лет) — риск повышен в 1,07-1,19 раз.
- Поздние роды (после 20-30 лет) — в 1,2-1,9 раз.
- Менопауза в 55 лет и старше — в 1,12 раз.
- Применение гормональных контрацептивов — в 1,21 раза.
- Применение заместительной гормонотерапии — в 1,14-1,47 раза.
- Избыточный вес — в 1,08-1,6 раз.
- Высокая рентгенологическая плотность молочных желёз — в 1.52-1.53 раз.
- Кисты — в 1,55 раз.
- Аденоз — в 2 раза.
- Фиброаденома — в 1,41 раза.
- Папиллома — в 2,06 раза.
- Мутация гена NBS1 — в 3,1 раза.
- Мутация в гене MLH1 — в 3,41 раза.
- Атипическая протоковая гиперплазия — в 3,28 раза.
- Атипическая дольковая гиперплазия — в 3,92 раза.
- Атипическая гиперплазия — риск составляет 35,5%-46,6%.
- Дольковый рак in situ — 24,3%-26%.
- Лучевая терапия в СОД 40 Гр, включающая молочные железы в возрасте до 30 лет — 26–29%.
- Мутация гена BRCA1 — в 14-33 раза.
- Мутация гена BRCA2 — в 9,9-19 раз.
- Мутация гена ATM — в 3,2 раза.
- Мутация гена BLM — в 6,28 раза.
- Мутация гена BRIP1 — в 2-7,7 раз.
- Мутация гена CDH1 — риск 42%.
- Мутация гена CHEK2 — в 3,25-101,34 раза.
- Мутация гена LKB1 — в 13,9 раз.
- Мутация гена PALB2 — в 5-9 раз.
- Мутация гена PTEN — в 25,4 раза.
- Мутация гена RECQL — в 33,5 раза.
- Мутация гена TP53 — в 105 раз.
Если вероятность развития рака молочной железы в течение жизни составляет менее 15%, женщину не относят к группе повышенного риска. Достаточно «бытовых» мер профилактики, связанных с образом жизни:
- Физическая активность. Исследования показывают, что женщины, которые регулярно выполняют физические упражнения, реже страдают раком молочной железы. Как часто нужно заниматься спортом? Эксперты из Американского Онкологического Сообщества (American Cancer Society) рекомендуют как минимум 150 минут умеренной или 75 минут интенсивной физической активности в неделю.
- Ранние роды. Если у женщины нет близких родственниц, страдающих раком молочной железы, то рождение первого ребенка до 20 лет помогает снизить риски. А если есть две или более больных близких родственниц (скорее всего, женщины в этой семье являются носительницами дефектных генов), ситуация прямо противоположная: ранние роды повышают риск.
- Поддержание нормального веса. Всем женщинам в течение всей жизни рекомендуется поддерживать здоровую массу тела. В этом помогут физические упражнения и правильное питание. Купите напольные весы, научитесь рассчитывать свой индекс массы тела (ИМТ). Если справиться с лишними килограммами не получается самостоятельно, стоит обратиться за помощью к диетологу, эндокринологу.
- Ограничение алкоголя. Эксперты Американского Онкологического Сообщества рекомендуют женщинам употреблять не более 350 мл 5% пива, или 150 мл 12% вина, или 45 мл водки в день.
Если риск заболеть раком молочной железы в течение жизни составляет 16% и более, стоит рассмотреть дополнительные меры профилактики. Врач может назначить некоторые препараты:
- Тамоксифен блокирует эффекты эстрогена в тканях молочной железы. Его можно использовать как у женщин репродуктивного возраста, так и в постменопаузе.
- Ралоксифен обладает аналогичным действием, но его можно использовать только в постменопаузе. В настоящее время он не применяется на территории России.
- Ингибиторы ароматазы подавляют производство эстрогенов за пределами яичников. Эти препараты применяют в постменопаузе.
Все гормональные препараты имеют серьезные побочные эффекты, поэтому применять их нужно осторожно. Например, тамоксифен действует в матке как слабый эстроген и может вызывать гиперплазию, полипы, и даже рак эндометрия.
Все три знаменитости перенесли профилактическую двойную мастэктомию.
У Анджелины Джоли от рака груди умерли некоторые близкие родственницы. Это заставило актрису проверить свои гены. Врачи обнаружили у Джоли мутантный ген BRCA1. В 2013 году у нее были удалены обе молочные железы. В 2015 Анджелина решилась на вторую операцию — удаление яичников. Это тоже было сделано, чтобы предотвратить рак.
У Шэрон Осборн тоже был обнаружен «неправильный» ген, который повышает риск рака молочной железы. На тот момент женщина уже хорошо знала, что значит побывать в шкуре онкологического больного: в 2002 году врачи диагностировали у нее рак прямой кишки, который успел распространиться на лимфатические узлы. Шэрон смогла победить болезнь. Для того чтобы не пережить этот кошмар снова, в 2012 году она решила удалить обе молочные железы.
«Это было нелегко. Я не хотела прожить всю оставшуюся жизнь с этой тенью, нависшей надо мной». Из интервью Шэрон Осборн журналу Hello!
У Кристины Эпплгейт в 2008 году был диагностирован рак молочной железы — к счастью, на ранней стадии. Врачи сказали, что можно обойтись резекцией с последующим курсом лучевой терапии и сохранить грудь. Но актриса выбрала радикальное решение — двойную мастэктомию. Генетический анализ показал, что Кристина является носителем мутантного гена BRCA1. В 2017 году она в профилактических целях удалила фаллопиевы трубы и яичники.
Мастэктомия — это еще один метод профилактики рака молочной железы у женщин с высоким риском, например, у носительниц мутантных генов. Некоторые женщины, у которых был обнаружен рак в одной груди, предпочитают выполнить профилактическую контралатеральную мастэктомию — удалить вторую грудь. Это помогает предотвратить в ней рак в будущем.
Окончательное решение о том, какими мерами профилактики воспользоваться, принимает сама женщина. Задача врача — донести до пациентки подробную и достоверную информацию, рассказать о доступных вариантах.
Меры профилактики не обеспечивают стопроцентную защиту от рака молочной железы, поэтому важна ранняя диагностика.
Самая простая мера — самообследование молочных желез. Его стоит проводить раз в месяц, в один и тот же день, лучше всего в первые несколько дней после окончания месячных. Начинать можно с 18–20 лет.
Мы подготовили наглядную инструкцию, из которой вы узнаете, как правильно проводить самообследование молочных желез:
По некоторым данным, до 50% всех опухолей молочной железы женщины выявляют самостоятельно.
Каждой женщине в любом возрасте нужно ежегодно посещать маммолога. И не стоит забывать о скрининге:
- Женщинам старше 40–50 лет рекомендуется раз в год проходить маммографию — рентгенографическое исследование молочных желез.
- У более молодых женщин маммография не так информативна из-за более высокой плотности тканей молочных желез. Рекомендуется ежегодно проходить УЗИ.
Если стали беспокоить симптомы, нужно немедленно посетить врача:
Не стоит сразу паниковать. Лишь у 3–5% женщин, обратившихся с этими жалобами к врачу, выявляют рак. Но провериться нужно обязательно.
Итак, во время УЗИ, маммографии или МРТ-маммографии был обнаружен какой-то узел. Что дальше? Нужно выяснить, что это за образование, является ли оно доброкачественным, или это рак. Для оценки снимков удобнее всего пользоваться системой, разработанной специалистами Американского колледжа радиологов (ACR, American College of Radiology). Врач должен отнести узел к одной из категорий, в зависимости от этого определяют дальнейший план действий:
- Категории 1 и 2 — норма и доброкачественные изменения соответственно. Показано наблюдение.
- Категория 3 — вероятно доброкачественные изменения. Необходимо более активное наблюдение или проведение биопсии.
- Категории 4A-4C — легкое, умеренное или серьезное подозрение на злокачественную опухоль.
- Категория 5 — узел, который очень похож на злокачественную опухоль. Нужно провести биопсию.
- Категория 6 — это злокачественная опухоль, которая подтверждена по результатам биопсии. Начинают лечение онкологического заболевания по протоколам.
После того как получено заключение по итогам биопсии, врач должен оценить прогноз (каков риск, что злокачественная опухоль возникнет в будущем?) и принять решение, нужно ли удалять узел:
- Аденоз повышает риск рака в 2 раза. Если узел выглядит подозрительно, и врач не уверен полностью в достоверности результата биопсии, проводят операцию.
- Фибраденома редко перерождается в рак. Ее можно не удалять, если она не растет, и диагноз подтвержден гистологически.
- Папиллома или атипическая протоковая гиперплазия повышают риск рака в 2–3 раза. Их нужно удалять. Внутри таких новообразований могут оказаться раковые клетки, которые не были обнаружены с помощью биопсии.
- Атипическая дольковая гиперплазия повышает риск рака почти в 4 раза, причем, риск тем выше, чем больше в молочной железе очагов. Но не обязательно удалять весь узел, если врач уверен, что в нем нет раковых клеток.
- Дольковый «рак на месте» (in situ) требует эксцизионной биопсии: нужно удалить узел и провести его гистологическое исследование.
Ранняя диагностика и своевременное лечение помогают сохранить жизнь. Если рак молочной железы удалось обнаружить на 0 или I стадии, пятилетняя выживаемость составляет почти 100%. На II стадии — 93%. На III стадии этот показатель снижается до 72%, а на IV — до 22%.
источник
Регулярный осмотр является первым шагом профилактики рака молочной железы. Онкология груди диагностируется у каждой 8 женщины после 35 лет. Выявить первые признаки развития патологического процесса можно самостоятельно, проводя каждый месяц самоосмотр и посещая гинеколога.
План мероприятий по профилактике рака молочной железы выделяет категории женщин, которые должны в первую очередь обращать внимания на изменения в груди:
- возраст после 35 лет;
- травмы и повреждения тканей груди;
- доброкачественные новообразования груди в анамнезе;
- ежедневные стрессы;
- поздний климактерический период;
- хронические заболевания органов в области малого таза;
- поздние роды (после 30–35 лет);
- искусственное вскармливание малыша.
Факторы риска, провоцирующие рак молочной железы, которые можно исключить:
- при первых родах не отказывайтесь от грудного вскармливания;
- любое заболевание лечите вовремя, не допускайте хронизации процесса;
- при обнаружении уплотнения или деформации срочно посетите маммолога.
При выполнении профилактического самоосмотра можно обнаружить изменения, которые указывают на начало развития патологического процесса:
- уплотненное образование;
- изменение формы железы;
- западение соска;
- кожа вокруг соска похожа на корочку цитрусовых;
- незначительные выделения из соска.
При обнаружении одного из симптомов, обратитесь к гинекологу или маммологу. Вовремя предпринятые меры профилактики рака молочной железы помогают сохранить здоровье и красоту груди.
Цель первичной профилактики рака молочной железы – предупреждение развития болезни. К мероприятиям относится грамотное использование контрацептивов на гормональной основе и отказ от абортов. Пациенткам из группы риска рекомендуется пересмотреть образ жизни и ежемесячно выполнять самоосмотр на 5–7 день менструального цикла.
- осмотреть форму, отсутствие асимметрии, изменения кожных покровов;
- прощупать грудь на наличие уплотнений;
- обследовать область подмышек и ключицы на наличие увеличенных лимфоузлов.
Ранняя диагностика рака молочной железы увеличивает шансы на выздоровление в три раза.
Цель вторичной профилактики – своевременное выявление и лечение новообразования. Дифференциация процесса проходит с помощью маммографии, которая позволяет обнаружить изменения в тканях молочной железы. Ежегодное прохождение процедуры после 45 лет является обязательным пунктом первичной и вторичной профилактики рака молочной железы.
С помощью УЗИ груди специалист может обнаружить новообразование небольшого размера (4–6 мм). Исследование назначается на 6–8 день после начала менструации. По показаниям проводится мастэктомия – процедура направлена на диагностику и профилактику рака молочной железы.
Цель третичной профилактики рака молочной железы – устранение процесса образования вторичных очагов опухолевого роста у пациенток, которые прошли курс химиотерапии по данному заболеванию. Профилактика метастазов и рецидивов рака молочной железы осуществляется с помощью нескольких методов:
- ежегодная маммография;
- УЗ-исследование молочных желез;
- анализы на онкомаркеры;
- диагностическая пункция тканей груди.
На этом этапе методы профилактики рака молочной железы проводятся по рекомендации врача.
Лекарства для профилактики рака молочной железы снижают активность опухолевого роста и препятствуют связыванию рецепторов с эстрогеном:
- Тамоксифен – является противоопухолевым и антиэтсрогенным препаратом. Назначается при третичной профилактике.
- Метотрексат – средство с составом, аналогичным фолиевой кислоте. Обладает противоопухолевым и иммуностимулирующим действием.
- Кселода – аналог пиримидина. Оказывает выраженное противоопухолевое действие.
- Экземестан – снижает вероятность развития рака груди на 65%.
- Ралоксивен – помогает предотвратить рак МЖ в климактерический период и укрепляет кости.
К препаратам для профилактики рака молочной железы относят БАД «Индинол». Биологически активная добавка при регулярном приеме нормализует функции груди. Действующим веществом является индол-3-карбинол, который получают их крестоцветных растений – цветная капуста, редька, брокколи и т. д. «Индинол» помогает для профилактики рака молочной железы путем регуляции уровня гормона. При регулярном приеме БАД снимает отечность и убирает симптом «нагрубания желез».
Употребление специальных продуктов помогает закрепить эффект при проведении профилактики рака молочной железы у женщин:
- Продукты, содержащие бета-каротин. При употреблении жирорастворимого витамина риск развития рака снижается на 17%. Содержится в моркови, хурме, тыкве, персиках. Ежедневная норма – 200 гр. сырого овоща.
- Брокколи (спаржевая капуста) – содержит в составе большое количество сульфорафана, который обладает противораковым и антибактериальным действием. Рекомендуемое количество приема – 50 гр. ежедневно. Можно отварить или стушить.
- Капуста белокочанная – регулярный прием снижает риск появления новообразований на 75%. В продукте содержится тирозиназ и глюкозинолат, которые обладают противораковым эффектом. В неделю нужно принимать не менее 500 гр. сырого овоща.
- Помидор – содержит ликопин, который является антиоксидантом и способствует выведению свободных радикалов из организма. Употреблять этот продукт для профилактики рака молочной железы можно в любом виде, минимум три раза в неделю.
- Чеснок – уничтожает раковые клетки, очищает организм от токсинов. В профилактических целях рекомендуется съедать по зубчику чеснока 2–4 раза в неделю.
- Свежие шампиньоны – уменьшают размеры раковых опухолей, останавливают выработку женских половых гормонов. Еженедельный прием должен быть не менее 200 гр., приготовленных любым видом.
- Плоды черники – повышают иммунные силы организма и выводят свободные радикалы из организма. Съедать нужно 200 гр. два раза в неделю.
Рекомендуется выбирать аэробные упражнения для профилактики рака молочной железы, которые повышают выносливость организма и насыщают ткани кислородом. Начинать тренировки нужно с 3 раз в неделю, затем увеличить до 5 раз. Время одного занятия – 30–50 минут. К подходящим видам спорта для женщин относят:
- Бег трусцой – упражнение помогает справиться с лишним весом, улучшает циркуляцию крови в организме. Длительные тренировки повышают выносливость организма.
- Плавание – занятия укрепляют мышцы туловища и снимают боли при заболеваниях костно-мышечного аппарата. При регулярном выполнении наблюдаются улучшения в работе сердечно-сосудистой системе.
- Езда на велосипеде (или велотренажер) – эффективным является при выполнении на большой скорости. Занятия помогают справиться с лишними килограммами и улучшают тонус мышц ног, ягодиц и пресса.
- Аквааэробика – занятия разрешены и в период беременности. Тренировка способствует расслаблению мышц и снятию усталости.
Профилактика рака молочной железы народными средствами заключается в приеме средств, приготовленных на натуральных компонентах:
- Измельчить 500 гр. корней лопуха, отжать из смеси сок. К жидкости добавить 10 ст. л. свежего меда и три измельченных лимона. Принимать 12 дней, по десертоной ложке перед сном.
- Вишневые веточки (5 ст. л.) залить козьим молоком (2 литра). Проварить на медленном огне 6 часов. Процедить и принимать по половине стакана три раза в день. Профилактический курс составляет 3 месяца с перерывом через каждые 4 недели.
- Растопить килограмм сливочного масла, к нему добавить очищенный и измельченный прополис (150 гр.). Варить 5 минут, постоянно помешивая. В целях профилактики принимать по 1 десертной ложке, растворяя в стакане молока.
Для профилактики рецидивов рака молочной железы подойдут нетрадиционные методы терапии:
- Компресс с овсом. 200 гр. овсяных хлопьев (или трухи) залить кипятком и настаивать 10 минут. Завернуть смесь в марлю, приложить к груди и накрыть целлофаном. Оставить компресс на час. Отвар не выливать, а выпить место чая.
- Примочки с толчеными ягодами калины. В смесь (200 гр.) добавить миндальное масло и отвар коры дуба. Примочки проводить с помощью ватного диска, перед сном.
15 октября – всемирный день профилактики рака молочной железы. В этот день в медицинских учреждениях проводятся профилактические беседы и бесплатные осмотры всех желающих. Больным оказывается паллиативная помощь, а его родственникам предлагается пройти обучающие курсы, чтобы облегчить уход за пациентом. По окончании осмотра выдается памятка профилактики рака молочной железы, где указан алгоритм самообследования и контакты центров, в которые следует обратиться при обнаружении изменений.
Роль медсестры в профилактике рака молочной железы заключается в проведении санитарно-просветительских работ. Участковый медицинский сотрудник раз в неделю проводит беседы, на которых можно узнать:
- основы профилактики;
- новые методики терапии;
- основы здорового образа жизни;
- алгоритм первой помощи.
По желанию родственников медицинская сестра помогает ухаживать за тяжелыми больными, объясняет этапы профилактики пролежней и других осложнений.
источник
В регионах Республики Казахстан с 15 по 24 октября2018 года будет проводится Национальная программа «Предупредить проще, чем исправить» приуроченная к Всемирному Дню осведомленности о раке молочной железы.
Основной целью и задачей Национальной программы является предупреждение развития болезни развития болезни путем формирования здоровье сберегающего поведения и своевременного прохождения скирининговых исследований.
- Как часто нужно проходить скрининговое исследование на рак молочной железы? И как оно проходит?
В рамках гарантированного объема бесплатной медицинской помощи проводится скрининг рака молочной железы, маммографическое исследование, среди женщин в возрасте 40-70 лет. Периодичность — один раз в два года. Как и любое другое рентгеновское обследование, оно входит в компетенцию специалистов-рентгенологов. Для каждой груди делается по два рентгеновских снимка. Каждую грудь зажимают на короткое время между двумя пластинами. Это может вызвать неприятные, иногда даже болезненные ощущения. Однако сдавливание необходимо, потому что только в этом случае могут быть сделаны качественные снимки, а облучение может быть сведено до минимума.
- Как и когда проводить самообследование груди?
Ответ: Каждая женщина должна знать о том, что один раз в месяц она должна проводить самообследование груди: это лучший способ раннего выявления каких-либо изменений в состоянии тканей молочных желез.
Процедуру следует проводить следующим образом:
- Осмотреть бюстгальтер в тех местах, в которых он соприкасается с сосками, и убедиться в отсутствии каких либо пятен.
- Осмотреть соски и ареолу, убедившись в отсутствии изменений: покраснений, втяжений, шелушений, высыпаний или изъязвлений.
- Встать перед зеркалом, поднять руки за голову и обратить внимание на форму груди и наличие каких либо неровностей, выпячиваний или вдавленных участков в отдельных частях груди.
- Осмотреть кожу груди на наличие изменений ее оттенка или изменений в виде «лимонной корки».
- Провести поочередное прощупывание молочных желез. Для этого необходимо прилечь на кровать и под лопатку (со стороны осматриваемой железы) подложить валик или небольшую подушку таким образом, чтобы грудная клетка была несколько приподнята, а молочная железа наиболее распластана. Правая молочная железа прощупывается подушечками пальцев трех-четырех пальцев левой руки. Пальцы следует расположить плашмя и передвигать их по кругу (от соска к внешнему краю железы), перемещая на сантиметры и ощупывая всю область железы. Таким же образом (только правой рукой) ощупывается левая грудь.
Помните о том, что выявление любых уплотнений, шишечек или болезненных участков всегда должно становиться поводом для безотлагательного обращения к маммологу. И не откладывайте визит к врачу «на потом», т. к. злокачественные опухоли молочных желез могут быть быстро прогрессирующими и чрезвычайно агрессивными, и вы можете упустить свой шанс на выздоровление.
- Какие основные первичные признаки рака молочной железы?
Ответ: Основными симптомами рака молочной железы, которые женщина может обнаружить сама, являются:
кровянистые выделения из соска;
уплотнение или втяжение участка кожи над опухолью;
увеличение лимфатических узлов в подмышечной, подключичной и надключичной областях.
- Как своевременно диагностировать рак молочной железы?
Ответ: Методом маммографии можно диагностировать опухоли, даже если они малы и незначительны. В начальной стадии существует возможность относительно легко поддающегося лечения, поэтому важно, чтобы рак был обнаружен на ранней стадии.
- Что может вызвать возникновение рака молочной железы?
Ответ: Основными факторами риска являются человеческие качества и привычки, которые делают их более склонными к болезням, чем других:
- Пол – у женщин рак молочной железы диагностируется чаще, чем у мужчин.
- Возраст – чем старше становится женщина, тем больше риск заболевания раком груди.
- История семьи – если у ближайших родственников был рак молочной железы.
- Беременность — у женщин, у которых не наступила беременность до 30 лет, или у тех, которые вообще не были беременны, риск заболевания раком молочной железы намного выше.
- Алкоголь – исследования показывают, что употребление алкоголя немного увеличивает риск заболевания раком груди.
- Курение – исследования доказывают, что курение и рак молочной железы связаны – чем дольше женщина курит, тем больше риск заболевания.
Лишний вес – исследования свидетельствуют, что лишний вес увеличивает риск заболевания раком груди, особенно у женщин после менопаузы. Это объясняется тем, что в жировых клетках увеличивается уровень эстрогена, а высокий уровень эстрогена увеличивает риск заболевания раком груди.
ШҚО денсаулық басқармасының «Семей қаласының жедел шұғыл медициналық жәрдем станциясы» шаруашылық жүргізу құқығындағы коммуналдық мемлекеттік кәсіпорынның
КГП «Станция скорой медицинской помощи г. Семей» Управления здравоохранения ВКО
источник
Рак молочной железы – одно из самых распространенных заболеваний у женщин. Шансы на успешное лечение резко повышаются в том случае, если заболевание диагностируют на ранней стадии.
Уровень заболеваемости раком молочной железы в России растет пугающими темпами – на 64% за последние 20 лет. Смертельно опасная опухоль, еще недавно занимавшая по частоте четвертое место, сейчас вышла на первое. Раннее обнаружение метастазов позволяет провести своевременное лечение и повысить его эффективность. Для этого специалисты настоятельно рекомендуют придерживаться простой системы:
1. Периодический осмотр у врача
Заболеваниями молочной железы занимаются врачи самых разных специальностей – маммологи, гинекологи, хирурги, рентгенологи, онкологи. Осмотр можно пройти в поликлинике, женской консультации, рентгеномаммографическом кабинете общего назначения. Специалист должен тщательно осмотреть молочные железы, подмышечные впадины. Следующий этап – беседа. Сразу же расскажите ему обо всех симптомах, которые возникали в последнее время. Наиболее частым симптоматическим явлением являются уплотнения и узлы в районе молочной железы. Также могут произойти небольшие изменения формы груди, соска, поверхности кожи. Большинство из них со временем исчезают, поэтому некоторые пациентки не придают им значения в разговоре с врачом. Но нужно помнить, что рак молочной железы часто развивается и бессимптомно! От вашей информации зависит ваше же здоровье – помните об этом!
2. Маммографическое обследование 
Если при осмотре будут выявлены какие-либо отклонения – врач выдаст вам направление на рентгеновскую маммографию. Она является несомненным лидером в выявлении тех форм рака, которые невозможно обнаружить при пальпации. В чем заключается процедура? В течение нескольких секунд женщина испытывает компрессию молочных желез. Это необходимо для получения высококачественных снимков. Снимки – маммограммы – делаются для каждой молочной железы в двух проекциях: прямой и косой. Всего, как вы уже догадались, 4 снимка. Когда делать обследование? Лучше всего идти на маммографию в начале менструального цикла с 5 по 12 день. С ее помощью можно не только выявить самые первые признаки болезни, но и оценить степень распространения процесса и характер роста опухоли. Это крайне важно для выбора дальнейшего способа лечения!
3. Самообследование 
источник
Профилактика рака молочной железы очень важна особенно для молодых женщин во избежание осложнений заболевания. Своевременная профилактика рака молочной железы избавит от многих проблем в зрелом возрасте.
Профилактика рака молочной железы включает в себя несколько мер.
Во-первых, эффективной мерой профилактики является регулярная сексуальная жизнь и роды до двадцати восьми лет.
Следующая мера профилактики рака молочной железы – это кормление ребенка грудью. Есть мнение, что грудное вскармливание особенно эффективно в плане предупреждения онкологии груди при длительном периоде лактации – не менее полутора лет. Тем не менее, есть и другая точка зрения, что связи между раком груди и грудным вскармливанием не существует. Обусловливается последнее мнение тем, что и беременность, и период лактации отодвигают начало менструального цикла после родов. А такое положение вещей может, напротив, спровоцировать развитие рака молочных желез. Однако доказано, что если у женщины имеется более двух детей, которых она долго кормила грудью, то риск заболевания раком у нее ниже на 50%.
Другая мера профилактики рака молочной железы – активный образ жизни. Занятия спортом, прогулки на свежем воздухе не только продлевают молодость, но и защищают от онкологии.
Конечно, профилактика рака предполагает отказ от сигарет и ограничение спиртного.
Для профилактики рака груди необходимо избавляться от ожирения, лечить диабет и патологии тканей печени.
Стрессы также могут стать провоцирующим условием для рака груди.
Основа профилактики рака молочной железы – регулярное посещение маммолога. Здоровая женщина должна не реже раза в год проходить тщательное обследование молочных желез. Если такое условие не соблюдается, то после тридцати пяти следует непременно показаться маммологу.
Женщинам, имеющим крайне высокий риск развития рака груди, в отдельных случаях проводят профилактическое устранение молочных желез. Задача подобного рода оперативного вмешательства состоит в предельно эффективном сокращении риска заболевания до проявления первых симптомов рака.
Помимо этого, каждая женщина должна помнить, что в процессе операции устраняется практически вся ткань груди, но небольшое ее количество тем не менее сохраняется. И, несмотря на то, что вмешательство предельно сокращает риск развития заболевания, рак может начать распространяться в оставшейся после хирургии ткани.
Разумеется, перед назначением пациентке удаления груди проводится масса различных исследований, так как для выполнения такой операции требуются очень веские показания. Только после получения результатов всех анализов и исследований и после обсуждения с 
Кроме всего прочего, женщины с назначением на профилактическое удаление груди часто имеют очень высокий риск рака яичников, по причине чего им рекомендуется удалить и эти органы по завершению детородного периода.
Общепринятая программа профилактики рака молочной железы:
— от 20 до сорока лет: ежемесячное самостоятельное ощупывание груди, ежегодное посещение маммолога и гинеколога;
— от 40 до 50 лет: ежемесячное самостоятельное обследование груди, ежегодное посещение специалиста, ежегодное прохождение маммографии;
— от 50 до 60 лет: ежемесячное самостоятельное исследование молочных желез на предмет наличия уплотнений и узлов, ежегодное обследование у маммолога, ежегодное прохождение процедуры маммографии;
— после шестидесяти лет: ежегодное самостоятельное обследование груди, прохождение процедуры маммографии и посещение гинеколога и маммолога.
Женщинам, входящим в группу риска развития рака молочных желез, необходимо проходить указанные обследования один раз в полгода.
источник
*Импакт фактор за 2017 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.
В статье рассматривается проблема мастопатии и риска рака молочной железы (РМЖ) с позиции трех специалистов: акушера-гинеколога, гинеколога-эндокринолога и онколога.
Представлены данные об эпидемиологии мастопатии и РМЖ, популяционные риски развития РМЖ, причины, предрасполагающие к мастопатии, и факторы риска РМЖ. Обсуждаются понятия мастопатии и масталгии. Подробно описаны клиническая симптоматика, методы физикального осмотра пациенток с нераковыми заболеваниями молочных желез (МЖ), включающие пальпацию МЖ и регионарных лимфоузлов. Представлены правила маммологического скрининга, предложенные Международной ассоциацией специалистов репродуктивной медицины. Среди инструментальных методов диагностики используются маммография, УЗИ, пункции узловых образований и подозрительных участков и цитологическое исследование пунктата.
Особое внимание уделено нарушениям гормонального баланса, поскольку МЖ является не только органом-мишенью для большого количества гормонов (в первую очередь половых) и факторов роста, но и местом локального биосинтеза и метаболизма половых гормонов.
В статье объяснена важность морфологического исследования ткани МЖ у женщин с подозрением на РМЖ и приведены примеры гистологических картин предраковых состояний. Описаны механизмы действия патогенетической терапии с приведением в качестве примеров некоторых лекарственных препаратов.
Ключевые слова: мастопатия, рак молочной железы, постменопауза, гиперэстрогенемия, Мамоклам.
Для цитирования: Керчелаева С.Б., Сметник А.А., Беспалов В.Г. Мастопатия и профилактика рака молочной железы как междисциплинарная проблема // РМЖ. 2016. № 15. С. 1018–1025.
Для цитирования: Керчелаева С.Б., Сметник А.А., Беспалов В.Г. Мастопатия и профилактика рака молочной железы как междисциплинарная проблема // РМЖ. Мать и дитя. 2016. №15. С. 1018-1025
Mastopathy and breast cancer prevention as interdisciplinary problem
Kerchelaeva S.B. 1 , Smetnik A.A. 2 , Bespalov V.G. 3
1 Pirogov Russian National Research Medical University, Moscow
2 Scientific Center for Obstetrics, Gynecology and Perinatology named after academician V.I. Kulakov, Moscow
3 Research Institute of Oncology named after N.N. Petrov, St.-Petersburg
The paper addresses the problem of mastopathy and the risk of breast cancer (BC) from the position of three specialists: obstetrician and gynecologist, endocrinologist and oncologist.
The data on mastopathy and BC epidemiology; population risks for BC; causes, predisposing to mastopathy and BC, and risk factors for BA is provided. The concept of mastopathy and mastalgia is discussed. Clinical symptoms, methods of physical examination for non-cancerous (benign) breast conditions , including palpation of breast and regional lymph nodes, are provided. The paper presents breast screening program proposed by International Federation of Fertility Societies. Instrumental diagnostic methods include mammography, ultrasound, puncture of nodules and suspicious sites, punctate cytology.
Special attention is paid to hormonal imbalance, since breast is not just the target organ for a large number of hormones (especially sex hormones) and growth factors, but a local place for sex hormones’ biosynthesis and metabolism.
The paper explains the importance of morphological examination of breast tissue in women with suspected BC and gives examples of precancerous conditions’ histology. Mechanisms of action of pathogenic therapy are discussed with focus on some drugs.
Key words: mastopathy, breast cancer, postmenopause, hyperestrogenemia, Mamoklam.
For citation: Kerchelaeva S.B., Smetnik A.A., Bespalov V.G. Mastopathy and breast cancer prevention as interdisciplinary problem // RMJ. 2016. № 15. P. 1018–1025.
В статье освещена междисциплинарная проблема мастопатии и профилактики рака молочной железы

Диагностика нераковых заболеваний молочных желез – профилактика рака молочной железы
Профессор С.Б. Керчелаева
ГБОУ ВО «РНИМУ им. Н.И. Пирогова» МЗ РФ, Москва
Эпидемиология. Известно, что в разных странах популяционные риски развития РМЖ неодинаковы. В России в 2013 г. заболеваемость РМЖ составила 320 на 100 тыс. населения, т. е. примерно 0,008% женской популяции ежегодно. Из 741 пациентки, жительниц Ганы, обратившихся за маммологической помощью, масталгия была основным симптомом в 50,2% случаев. РМЖ был диагностирован у 7,8% пациенток, рецидивирующий рак – у 0,8% пациенток. В остальных случаях (около 88%) масталгия не была ассоциирована со злокачественной трансформацией тканей МЖ [1, 2]. В ходе изучения связи между циклической масталгией и РМЖ с участием 5463 женщин 28% (1529 пациенток) сообщили о боли в груди. При этом у 15,8% был диагностирован РМЖ [3]. Таким образом, надо понимать, что масталгия не является маркером раковой трансформации, но ее следует признать значимым фактором риска.
В общей популяции фиброзно-кистозная болезнь встречается у 60–80% женщин, причем пациентки репродуктивного возраста с гинекологическими заболеваниями в анамнезе обеспечивают самый высокий процент. Клинические проявления мастопатии не только ухудшают качество жизни пациенток, но и повышают риск развития РМЖ в десятки раз [4]. Со стороны акушеров-гинекологов незаслуженно мало внимания уделяется доброкачественным заболеваниям МЖ. Клинические симптомы мастопатии приравнивают к норме, хотя это, как правило, свидетельствует о патологическом процессе.
Несмотря на то, что МЖ относится к визуальным локализациям и легко доступна для исследования, РМЖ в 1 и 2 стадии диагностируется лишь у 57,6% пациенток, причем летальность на первом году жизни с момента установления диагноза составляет около 12,6% случаев. Больные с запущенными формами РМЖ составляют высокий процент наблюдений. Анализ причин запущенности заболевания показал, что в значительной степени запущенность связана с низкой медицинской культурой населения: 42% пациенток откладывали свой визит к врачу, мотивируя это занятостью, неблагоприятной ситуацией на работе, семейными обстоятельствами и т. д., у 10,9% пациенток причиной была боязнь идти к врачу, в 6,5% случаев женщины занимались самолечением, что приводило к резкому прогрессированию заболевания. Однако в 32,5% случаев запущенность заболевания лежит на совести врачей общей лечебной сети ввиду их низкой онкологической грамотности и отсутствия онкологической настороженности. У 51,7% больных от момента появления клинических признаков РМЖ до постановки диагноза проходило от 1 до 6 мес. [5].
В любом современном государстве основу профилактики составляют скрининговые программы, причисленные по значимости к государственным программам, а борьба с раковыми опухолями на мировом уровне включена в глобальные задачи человечества.
С 2009 г. на основании приказа № 808 МЗ РФ выявление и терапия заболеваний МЖ входят в сферу ответственности акушеров-гинекологов, тогда как ранее этими вопросами занимались исключительно маммологи и хирурги.
В 2012 г. Минздрав России издал новое руководство к действию – приказ № 572н, регламентирующий, как и приказ № 808, что медицинскую помощь женщинам с целью выявления заболеваний МЖ оказывает врач акушер-гинеколог. Кроме того, в действующем приказе в пункте 85 написано, что женщин с выраженными кистозными узловыми изменениями МЖ направляют в онкологический диспансер для верификации диагноза.
Анатомия и физиология. МЖ – это гормонозависимые органы, входящие в репродуктивную систему женщины, которые развиваются и начинают функционировать под влиянием целого комплекса гормонов: рилизинг-факторов гипоталамуса, гонадотропных гормонов гипофиза (фолликулостимулирующего и лютеинизирующего), хорионического гонадотропина, пролактина, тиреотропного гормона, кортикостероидов, инсулина, эстрогенов, прогестерона, андрогенов. МЖ в своем развитии проходят несколько этапов. После рождения МЖ представляют собой рудиментарные образования. В период полового созревания, когда у девочек начинают функционировать яичники, МЖ начинают увеличиваться в объеме, и с наступлением менструальной функции ткань МЖ подвергается ежемесячным циклическим изменениям в соответствии с фазами менструального цикла. С прекращением менструальной функции ткань МЖ подвергается инволютивным изменениям, а именно жировому перерождению. Паренхима МЖ представлена сложными альвеолотрубчатыми железами, собранными в мелкие дольки, из которых формируются крупные доли. В МЖ имеется от 6 до 24 долей. Каждая из них имеет свой выводной проток, некоторые протоки могут сливаться перед выходом на поверхность соска.
Кровоснабжение МЖ осуществляется за счет внутренней грудной и подмышечной артерий и ветвей межреберных артерий. Вены МЖ сопровождают артерии и широко анастамозируют с венами окружающих областей.
С онкологических позиций большое значение имеет строение лимфатической системы МЖ. Выделяют внутриорганную и внеорганную лимфатическую систему МЖ. Различают следующие пути оттока лимфы от МЖ: подмышечный, подключичный, парастернальный, ретростернальный, межреберный, перекрестный и путь Героты.
Патогенез. По определению ВОЗ, мастопатия – это фиброзно-кистозная болезнь с нарушением соотношения эпителиального и соединительнотканного компонента, с разнообразными пролиферативными и регрессивными изменениями в тканях МЖ. У термина «мастопатия» имеется множество синонимов, наиболее часто используют такие как «фиброзно-кистозная болезнь», «доброкачественная дисплазия молочных желез», однако обобщающим считают термин «нераковые заболевания молочных желез».
В России для диагностики нераковых заболеваний МЖ применяют клинико-рентгенологическую классификацию мастопатии Н.И. Рожковой [6], согласно которой выделяют 5 форм диффузной мастопатии:
с преобладанием:
– железистого компонента;
– фиброзного компонента;
– кистозного компонента;
– смешанную форму диффузной фиброзно-кистозной мастопатии;
– склерозирующий аденоз.
Кроме того, по результатам биопсии устанавливают диагноз в соответствии с гистологической классификацией опухолей МЖ (ВОЗ, 1995).
Различают морфологически непролиферативную и пролиферативную формы доброкачественной дисплазии. При этом риск малигнизации при непролиферативной форме составляет 0,86%, при умеренной пролиферации – 2,34%, при резко выраженной пролиферации – 31,4% наблюдений. По данным гистологических исследований операционного материала, РМЖ сочетается с фиброзно-кистозной болезнью в 46% случаев [7].
Отмечается четкая связь между заболеваемостью РМЖ и детородной функцией. Женщина, родившая впервые в 18 лет, имеет втрое меньший риск заболеть РМЖ, чем впервые родившая в 35 лет. Ранняя первая беременность способствует резкому увеличению продукции одного из 3–х эстрогенов – эстриола, который является продуктом метаболизма эстрадиола и эстрона и тормозит канцерогенное воздействие последних. С другой стороны, поздние роды (после 30–40 лет) приводят к резкому повышению уровня эстрадиола, что может способствовать развитию РМЖ. Также к причинам, предрасполагающим к мастопатии, относят следующие факторы: неблагоприятный репродуктивный анамнез, гинекологические заболевания, гиперпролактинемию, факторы сексуального характера, эндокринные нарушения, повседневные фрустрирующие ситуации, заболевания печени, генетическую отягощенность [8]. Чрезвычайно важными являются факторы риска РМЖ: выделения из соска вне лактации, обнаружение мутации генов семейства BRCA в крови, в перименопаузальном периоде – наличие уплотнения ткани молочной железы по результатам маммографического скрининга.
Из вышеизложенного следует, что в противораковой борьбе большое значение имеют своевременное выявление и лечение нераковых заболеваний МЖ.
Диагностика заболеваний молочной железы основывается на осмотре МЖ, их пальпации, что должно проводиться с особой тщательностью и онкологической настороженностью. Физикальное обследование включает пальпацию МЖ, регионарных лимфоузлов (подключичных, надключичных, подмышечных).
Из дополнительных методов используются маммография, УЗИ, пункции узловых образований и подозрительных участков и цитологическое исследование пунктата. Кроме того, необходимо руководствоваться приказом № 572н, который регламентирует обязательное скрининговое обследование женщин старше 35 лет.
Международная ассоциация специалистов репродуктивной медицины, Российская ассоциация маммологов предложила Правила маммологического скрининга для акушера-гинеколога: каждую женщину моложе 35 лет необходимо опрашивать для выявления прогностических факторов РМЖ (разница между ростом в сантиметрах и массой тела в килограммах более 110, возраст начала менструации – до 13 лет, гинекологические заболевания в анамнезе (миома матки, полип матки, эндометриоз, кисты яичников, дисфункция яичников, бесплодие и др.), отсутствие родов, первые роды в возрасте старше 30 лет, стрессовые ситуации, ушибы, маститы, операции на МЖ, онкологические заболевания у близких родственников). Мануальное обследование проводить всем; при наличии факторов риска РМЖ, но при отсутствии изменений молочных желез направлять на УЗИ. При наличии пальпаторных изменений направлять не только на УЗИ, но и на маммографию.
Каждую женщину старше 35 лет направлять на маммографию с периодичностью 1 раз в 2 года при отсутствии изменений. При наличии рака в семье – направлять на ДНК-исследование крови с целью выявления мутаций генов BRCA-1 и -2. При обнаружении мутаций направлять на консультацию онколога для выработки плана наблюдения или лечения.
Главная цель первичных диагностических мероприятий – определить характер процесса. При обнаружении узлового очага пациентку нужно направить к рентгеномаммологу, который выполнит биопсию с цитологическим и гистологическим исследованием пунктата. С учетом результата пациентка будет направлена к маммологу-онкологу, который будет заниматься ее лечением. При диффузном процессе пациенткой должен заниматься акушер-гинеколог, который проведет полное обследование, в т. ч. и гормонального статуса, для дальнейшего консервативного лечения и мониторинга. При обнаружении галактореи (вне беременности и лактации) необходимо определить концентрацию гормона пролактина и тиреотропного гормона, а также взять отпечаток-мазок отделяемого для цитологического исследования. В зависимости от его результатов решается вопрос о дальнейшем ведении пациентки. Гиперпролактинемия – одна из причин эстроген-прогестеронового дисбаланса, именно пролактин стимулирует рост числа эстрогеновых рецепторов в тканях МЖ, повышает чувствительность клеток к действию эстрадиола и ускоряет пролиферацию эпителиальных клеток.
Профилактика заболеваний молочной железы. Основная задача акушера-гинеколога – вести среди женского населения пропаганду против абортов, проводить своевременное лечение воспалительных заболеваний органов малого таза, коррекцию нарушений менструального цикла на всех этапах жизни женщины, коррекцию хронической ановуляции, лечение эндометриоза, миомы матки, полипов матки, опухоли яичников. Перечисленные состояния характеризуются гормональным дисбалансом и дефицитом прогестерона, все это приводит к отеку и гипертрофии внутридольковой соединительной ткани, пролиферации протокового эпителия, что является причиной обтурации протоков и образования кист. Гиперэстрогенизм вследствие недостаточной лютеиновой фазы цикла обусловливает развитие дисгормональных дисплазий МЖ у женщин репродуктивного возраста.
Негормональная базовая терапия диффузной формы нераковых заболеваний МЖ включает: коррекцию диеты, психологическую коррекцию, нормализацию функционального состояния печени, желудочно-кишечного тракта, использование мочегонных средств, препаратов, улучшающих кровоснабжение, использование арсенала фитотерапии.
Многие специалисты сегодня задаются вопросом: есть ли возможности прогнозирования РМЖ? На основании исследовательских работ результаты экспериментов показали, что большая часть канцерогенного влияния эстрогенов связана с образованием агонистических метаболитов эстрогенов, преимущественно 16-гидроксиэстрогена (16-ОНЕı). Другие метаболиты, такие как 2-гидроксиэстрон (2-ОНЕı) и 2-гидроксиэстрадиол, обеспечивают протективное действие, выступая как антагонисты 16-гидроксиэстрогена [9, 10]. Установлено, что при нормальном соотношении стероидных гормонов в организме женщины концентрация метаболита 2-ОНЕı превышает концентрацию 16-ОНЕı не менее чем в 2 раза. Уменьшение этого соотношения признано фактором риска РМЖ. Таким образом, соотношение 2-ОНЕı к 16-ОНЕı менее 2,0 можно считать адекватным универсальным биомаркером и надежным диагностическим критерием для определения риска и прогноза развития эстрогензависимых опухолей [8, 11].
Заключение. Долгое время считали, что мастопатия – это не заболевание, поскольку очаги фиброза и кисты в МЖ очень распространены, а потому не требуют лечения. Однако сегодня, изучая данную проблему, мы пришли к выводу, что указанные изменения нельзя считать вариантом нормы. Сегодня нераковые заболевания МЖ следует рассматривать как маркер гормонального и тканевого неблагополучия МЖ, а также как фактор онкологической настороженности. Нераковые заболевания МЖ необходимо активно выявлять и лечить, тем самым обеспечить женщине приемлемое качество жизни и проведение онкопрофилактики.
Риск рака молочной железы и половые гормоны
К.м.н. А.А. Сметник
ФГБУ «Научный центр акушерства, гинекологии и перинатологии им. акад. В.И. Кулакова» МЗ РФ, Москва
Молочная железа является органом-мишенью для большого количества гормонов и факторов роста, среди которых одну из ведущих ролей играют половые гормоны и экспрессия соответствующих рецепторов [12].
Клетки МЖ, экспрессирующие эстрогеновые рецепторы (ЭР), пролиферируют медленно, в отличие от ЭР-негативных клеток, которые митотически активны. Пролиферация здорового эпителия, не содержащего ЭР или прогестероновые рецепторы (ПР), происходит за счет паракринных эффектов от рядом расположенных покоящихся ЭР-позитивных клеток. В отличие от этого в опухолевых рецептор-позитивных клетках митозы регулируются аутокринными механизмами. В менструальном цикле в МЖ происходят последовательные волнообразные процессы пролиферации и апоптоза. Эндогенный прогестерон в синергизме с эстрадиолом способны стимулировать процессы пролиферации и апоптоза в МЖ, васкуляризацию, выработку протеогликанов, аккумуляцию жидкости в ткани МЖ, что приводит к субъективным ощущениям нагрубания МЖ и повышению маммографической плотности в лютеиновую фазу менструального цикла [13]. Именно в лютеиновую фазу в МЖ наблюдается максимальная частота митозов [14].
МЖ является местом локального биосинтеза и метаболизма половых гормонов. К ферментам, участвующим в локальном синтезе и метаболизме эстрогенов, относятся ароматаза (переход андрогенов в эстрогены), сульфатаза (переход неактивных сульфатных форм эстрогенов в активные), 17-дигидрогеназа I и II (из эстрона в эстрадиол и наоборот), сульфотрансфераза (образование сульфатных форм) [15]. Возможно, высокая распространенность гормонально зависимого рака в период низкой продукции половых гормонов яичниками (в постменопаузе) обусловлена отчасти ролью данных ферментных систем. Активность эстронсульфатазы в опухолевой ткани МЖ в 10–500 раз выше активности ароматазы. Также важную роль играют гидроксиметаболиты эстрогенов и ряд метаболитов прогестерона, которые оказывают пролиферативные либо антипролиферативные эффекты [16].
Клинические и экспериментальные данные о роли гормонов в развитии мастопатии зачастую противоречивы. Тем не менее, мастопатия является гормонозависимым заболеванием, обусловленным дисбалансом в гипоталамо-гипофизарно-яичниковой системе.
Если говорить о развитии РМЖ, то переход в гормонозависимой регуляции с паракринного на аутокринный механизм – важная часть опухолевого процесса [12, 17]. Андрогеновые рецепторы присутствуют в 70–80% случаев РМЖ (экспрессируются чаще, чем ЭР или ПР). В случае коэкспрессии андрогеновых рецепторов при ЭР-позитивных раках прогноз обычно лучше. Однако при ЭР-негативном раке андрогеновые рецепторы часто служат компенсаторным механизмом для роста опухоли [18]. Факторы риска РМЖ приведены в таблице 1 [19].
На приеме гинеколога-эндокринолога одним из самых частых вопросов со стороны пациенток является вопрос о возможности назначения им, в зависимости от возраста, комбинированных оральных контрацептивов (КОК) или менопаузальной гормонотерапии (МГТ). Врачу же приходится оценивать безопасность гормональной терапии в каждом конкретном случае, в т. ч. с позиций возможного влияния на риск РМЖ. Общепринятым является положение о том, что изменения синтеза и метаболизма эстрогенов и прогестерона имеют фундаментальное значение для риска развития РМЖ [21].
В случае сочетания мастопатии с гинекологическими заболеваниями, требующими гормональной коррекции, назначение последней возможно.
Метаанализ 13 проспективных когортных исследований КОК не выявил значимого повышения риска РМЖ. Однако различные типы гестагенов в составе КОК также по-разному влияют на различные прогестероновые рецепторы [22]. Например, согласно данным Ruan X. et al. (2012), следующие гестагены, входящие в состав КОК, повышали пролиферацию в культуре клеток РМЖ (MCF-7) при высоких концентрациях: дроспиренон, левоноргестрел, дезогестрел. В отличие от этого, пролиферативный эффект отсутствовал в случае хлормадинона ацетата и номегестрола ацетата [23].
В постменопаузе в опухолевой ткани МЖ концентрация локального эстрадиола в 20–50 раз выше, чем в плазме (результат локальной конверсии из андрогенов, эстрона и эстрона сульфата). При этом не наблюдаются значимые различия в концентрациях эстрадиола: в крови при РМЖ и в норме; в самой МЖ при раке в репродуктивном возрасте и постменопаузе; локально при РМЖ в постменопаузе на фоне приема МГТ и без МГТ. Таким образом, опухолевая концентрация эстрадиола не зависит от уровня в плазме [24].
Согласно рекомендациям Всемирной ассоциации по менопаузе (International Menopause Society) от 2016 г., возможное повышение риска РМЖ, связанное с МГТ, невелико и оценивается менее чем в 0,1% в год, или менее 1,0 случая на 1000 женщин на год использования [25]. Этот уровень схож или ниже, чем повышение риска, связанное с такими частыми факторами образа жизни, как сниженная физическая активность, ожирение и употребление алкоголя. Данные, полученные в исследовании WHI (Women’s Health Initiative – «Инициатива во имя здоровья женщин»), не показали повышения риска РМЖ у женщин, впервые применяющих МГТ в течение 5–7 лет после начала терапии [20]. Исследование WHI также показало, что монотерапия конъюгированными эквин-эстрогенами в течение 7,1 года снижала риск диагностирования РМЖ и смертности у женщин с удаленной маткой [26].
В 3-х исследованиях было высказано предположение, что микронизированный прогестерон или дидрогестерон могут быть связаны с более низким риском, чем синтетический прогестаген [27–29]. Доступные в настоящее время данные не позволяют предположить различия в риске между пероральным и трансдермальным путями применения эстрадиола [30]. Тем не менее в настоящее время недостаточно данных клинических исследований адекватной мощности для полной оценки возможной разницы в частоте развития РМЖ при использовании разных типов, доз и путей введения эстрогенов, типа прогестагена и применения андрогенов.
На сегодняшний день в мировую практику лечения расстройств, связанных с менопаузой, активно внедряется комбинация селективного модулятора эстрогеновых рецепторов – базедоксифена (который блокирует эстрогеновые рецепторы в МЖ и эндометрии) и конъюгированных эквин-эстрогенов [31]. Данный препарат способствует уменьшению плотности МЖ, но требуются дополнительные данные для подтверждения ее влияния на заболеваемость РМЖ [32].
Таким образом, можно сделать вывод, что с точки зрения любого увеличения риска РМЖ более значим именно прогестагенный компонент МГТ и КОК, а не эстроген. Риск может быть ниже при применении микронизированного прогестерона или дидрогестерона, чем при использовании синтетического прогестагена в составе МГТ. Риск РМЖ, связанный с применением МГТ, невелик, зависит от ее длительности и неуклонно снижается после ее прекращения. Имеющихся в настоящее время данных о безопасности недостаточно для поддержки назначения МГТ женщинам, перенесшим РМЖ. До назначения МГТ следует оценить соответствующий риск. Возможное увеличение риска РМЖ, связанное с МГТ, может быть частично снижено путем отбора женщин с исходно более низким индивидуальным риском, включая низкую плотность МЖ, а также путем образования по вопросам превентивных мер, направленных на коррекцию образа жизни (снижение массы тела, приема алкоголя и увеличение физической активности). У женщин, принимающих МГТ, следует проводить ежегодную маммографию [25]. Современные прогестагены, натуральный прогестерон и селективный модулятор эстрогеновых рецепторов оптимизируют влияние гормонотерапии на МЖ. Эти данные следует учитывать гинекологам-эндокринологам при ведении пациенток с мастопатией.
Мастопатия как фактор риска РМЖ: вопросы этиопатогенеза и лечения
Д.м.н. В.Г. Беспалов
ФГБУ «НИИ онкологии им. Н.Н. Петрова» МЗ РФ, Санкт-Петербург
Мастопатия (фиброзно-кистозная болезнь) – распространенная патология, ее частота в женской популяции составляет до 50% [33]. В целом мастопатия не является предраком или стадией онкологического процесса в МЖ. Однако нельзя недооценивать роль мастопатии в развитии РМЖ. Рост заболеваемости РМЖ в XX в. во многих странах сопровождался параллельным ростом частоты мастопатии. В 2014 г. в России зарегистрировано 65 088 новых случаев РМЖ, 21,2% (1-е место) в структуре заболеваемости женщин раком; за 10 лет стандартизованный показатель заболеваемости вырос на 19,79%, рост на 1,78% в год [34]. При этом мастопатия имеется у 50–60% российских женщин [35]. Выделяют более 50 доброкачественных заболеваний МЖ или форм мастопатии, среди которых многие существенно повышают риск РМЖ.
Взаимосвязь этиологии и патогенеза мастопатии и РМЖ
Существует 4 группы доказательств связи мастопатии с РМЖ: 1) у мастопатии и РМЖ общие факторы риска; 2) патогенез мастопатии и РМЖ имеет общие черты, ключевую роль играет относительная или абсолютная хроническая гиперэстрогения; 3) при мастэктомии в связи с РМЖ в тканях МЖ часто обнаруживают морфологические проявления мастопатии и предраковые изменения; 4) у больных РМЖ чаще была предшествующая мастопатия [36].
РМЖ – полиэтиологическое заболевание, идентифицировано более 80 факторов риска РМЖ, которые можно разделить на 5 групп: половые и возрастные, генетические, репродуктивные, гормональные и обменные, внешней среды и стиля жизни. Мастопатия – также полиэтиологическое заболевание, а основные факторы риска РМЖ и мастопатии совпадают [37]. Если РМЖ в большинстве случаев развивается в постменопаузальном возрасте, то пик заболеваемости мастопатии приходится на возраст 30–50 лет, т. е. данная патология предшествует развитию РМЖ. Кровные родственники, больные РМЖ; носительство мутантных генов, отвечающих за репарацию ДНК и биосинтез половых гормонов, являются одновременно факторами риска и РМЖ, и мастопатии. Большинство репродуктивных факторов риска одинаковы для РМЖ и мастопатии: раннее менархе, низкая частота родов, поздние первые роды, отсутствие или короткий период грудного вскармливания, искусственные аборты, высокая рентгеновская плотность маммограмм в позднем репродуктивном возрасте. Гормональные и обменные факторы риска в большинстве одинаковы для РМЖ и мастопатии: гиперэстрогения, гиперпролактинемия, гипотиреоз; гиперпластические заболевания гениталий и гинекологические заболевания, связанные с нарушениями гормонального баланса; ожирение, сахарный диабет, болезни печени. Из факторов внешней среды и стиля жизни одинаковы для РМЖ и мастопатии нарушения питания в виде избытка жиров, калорий, животных белков, алкоголя, недостатка овощей и фруктов, пищевых волокон, витаминов и минералов; депрессия, нарушения сна, работа в ночные смены; сниженная физическая активность.
Мастопатию можно считать биомаркером гормонального неблагополучия на уровне организма и локального неблагополучия в ткани МЖ. Множественные факторы риска нарушают гормональный баланс в организме женщины, вызывают гиперэстрогению и гиперпролиферацию эпителия в ткани МЖ, что приводит к развитию мастопатии, а при наличии врожденных или приобретенных повреждений генов – РМЖ.
Риск РМЖ у больных мастопатией
Мастопатия является и самостоятельным фактором риска РМЖ. В эпидемиологических когортных исследованиях при сроках наблюдения за женщинами от 6 до 20 лет установлено, что относительный риск РМЖ (в сравнении с частотой РМЖ в общей популяции, с женщинами без мастопатии, с непролиферативной мастопатией) при мастопатии без пролиферации эпителия статистически недостоверно, но в некоторых исследованиях и статистически достоверно, повышается в 1,27–2,23 раза; при мастопатии с гиперплазией без атипии достоверно повышается в 1,53–3,58 раза; при мастопатии с атипичной гиперплазией достоверно повышается в 2,03–10,35 раза [38]. Dyrstad S.W. et al. провели метаанализ 32 эпидемиологических ретроспективных и проспективных исследований о связи мастопатии с риском РМЖ; относительный риск РМЖ при непролиферативных формах мастопатии статистически недостоверно повышался до 1,17, при пролиферативных формах без атипии – достоверно повышался до 1,76, при пролиферативных формах с атипией – до 3,93 [39].
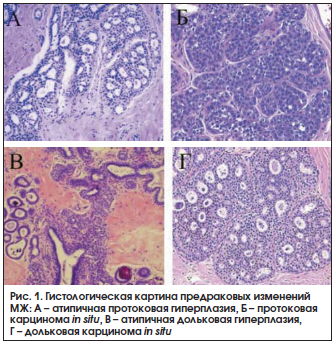
К предраковым изменениям МЖ относят протоковую атипичную гиперплазию и карциному in situ, дольковую атипичную гиперплазию и карциному in situ, склерозирующий аденоз, радиальный рубец [40]. Основные формы предрака МЖ приведены на рисунке 1.
В таблице 2 указывается степень риска РМЖ при мастопатии по данным R.J. Santen и R. Mansel [40].
Коллегия американских патологов рекомендовала подразделять женщин с мастопатией на 3 категории в зависимости от выявленных при биопсии МЖ морфологических изменений: 1) непролиферативная – риск РМЖ не повышен и равен популяционному; 2) пролиферативная без атипии – риск РМЖ повышен в 1,5–2 раза по сравнению с популяцией; 3) пролиферативная с атипией – риск РМЖ повышен в 4–5 раз по сравнению с популяцией [41]. При биопсии МЖ и морфологическом обследовании примерно у 5% женщин с мастопатией выявляется атипическая гиперплазия [42].
Лечение мастопатии и профилактика РМЖ
Стандартов лечения мастопатии на сегодняшний день нет. К общим недостаткам большинства применяемых сегодня средств можно отнести невысокую эффективность, побочное и токсическое действие, необходимость применения в виде комплекса с другими средствами, нацеленность только на облегчение патологической симптоматики, а не на более серьезную задачу – профилактику РМЖ. Поэтому актуальной является проблема создания специальных лекарственных средств для лечения мастопатии. С учетом характера данной патологии такие средства должны быть эффективными, безопасными, пригодными для длительного применения, направленными на профилактику РМЖ. Патогенетическое лечение мастопатии относят к первичной и вторичной профилактике РМЖ [43, 44].
В настоящее время для патогенетического лечения мастопатии существуют лишь единичные препараты. Например, лекарственный препарат Мамоклам, который производят из липидной фракции бурой морской водоросли Laminaria; действующими веществами Мамоклама являются органический йод, полиненасыщенные жирные кислоты омега-3 типа, хлорофилл. Мамоклам разрешен для медицинского применения в качестве лекарственного средства для лечения мастопатии. В эпидемиологических исследованиях показано, что все 3 действующих вещества Мамоклама снижают риск развития РМЖ. В клинических исследованиях доказано, что Мамоклам вызывает регрессию масталгии, ослабляет предменструальное нагрубание МЖ, вызывает регрессию уплотнений и кист в МЖ, снижает маммографическую плотность, нормализует процессы пролиферации эпителия МЖ, нормализует менструальный цикл и баланс тиреоидных и половых гормонов [45–47].
Патогенетическое лечение мастопатии должно быть направлено на нормализацию гормонального баланса в организме женщины, прежде всего баланса половых гормонов; на уменьшение гиперэстрогении как на системном уровне, так и на уровне рецепторного аппарата клеток в ткани МЖ; на подавление процессов гиперпролиферации железистого эпителия МЖ. Основным действующим веществом Мамоклама является йод в органически связанной форме (в составе аминокислот). При поступлении в организм в дозах, превышающих суточную потребность, йод накапливается в тканях МЖ и оказывает прямое действие на патогенетические пути развития мастопатии: подавляет пролиферацию эпителия, индуцирует апоптоз и дифференцировку клеток, снижает чувствительность ткани МЖ к эстрогенам; в щитовидной железе формируются йодолипиды, которые оказывают антиоксидантное действие и контролируют клеточную пролиферацию в МЖ; йод также опосредованно влияет на состояние МЖ, нормализуя баланс тиреоидных и половых гормонов, уменьшая местную гиперэстрогению в тканях МЖ [48–50]. Показано, что при лечении мастопатии йодом в дозах, превышающих суточную потребность, нормализуется архитектоника тканей МЖ [51]. Длительный прием йода в дозах, превышающих суточную потребность, возможен только для органического йода, который содержится в Мамокламе. Другой компонент Мамоклама – полиненасыщенные жирные кислоты омега-3 типа также влияют на патогенетические пути развития мастопатии: формируют структуру и определяют вязкость клеточных мембран, регулируют клеточные сигналы, нормализуют баланс эстрогенов, в результате чего уменьшают гиперэстрогению и ослабляют пролиферацию клеток в ткани МЖ [52].
Выводы
1. К группе повышенного онкологического риска женщины, страдающие мастопатией, могут быть отнесены после оценки всех индивидуальных факторов риска и морфологического анализа тканей МЖ.
2. Решающим в оценке степени риска развития РМЖ у больных мастопатией является морфологическое исследование ткани МЖ, полученной при биопсии. Риск РМЖ не повышается или является минимальным при непролиферативных формах мастопатии, при пролиферативной форме без атипии риск возрастает в 2 раза, при пролиферативной с атипией – в 4 раза и достигает наиболее высоких цифр (до 12 раз) при протоковой или дольковой карциноме in situ.
3. Своевременная диагностика и патогенетическое лечение мастопатии не только улучшают качество жизни, но и должны быть направлены на профилактику РМЖ. Мамоклам – эффективный и безопасный лекарственный препарат для патогенетического лечения мастопатии, при длительном применении Мамоклам снижает риск РМЖ.
источник