Метастазирование в кости это тяжелое раковое осложнение с сильными болевыми симптомами, означающее переход рака в 3, 4 стадию. Прогноз лечения и продолжительность жизни при этом значительно снижаются, сколько живут с метастазами в костях зависит от применяемой терапии и агрессивности первичного очага
Процесс метастазирования это страшное осложнение, которое всегда происходит при раке, если болезнь вовремя не выявлена и не начато ее лечение. Обычно метастазы образуются в мягких тканях, органах, но иногда ими поражаются и кости. Метастазу в костных структурах следует рассматривать как еще один эпизод рака, когда аномальные клетки из первичной опухоли, перемещаясь по организму, осаждаются в элементах скелета.
Метастазы в костях появляются на поздних стадиях развития патологии, в 4-х из пяти случаев первичные опухоли это рак молочной железы для женщин и простаты у мужчин. Такая ситуация не имеет хорошего прогноза, пациент страдает от симптомов сильных болей, ослабленные кости переламываются даже при незначительном воздействии. Первичное онкологическое поражение почек и щитовидной железы, ведет к метастазированию в структурах черепа.
Кроме перечисленных видов рака от метастазирования в костные ткани страдают при злокачественных опухолях легких, почек, яичников у женщин, саркоме, лимфоме и поражении органов желудочно-кишечного тракта. В резких случаях бывает миграция атипичных клеток и из других охваченных болезнью органов.
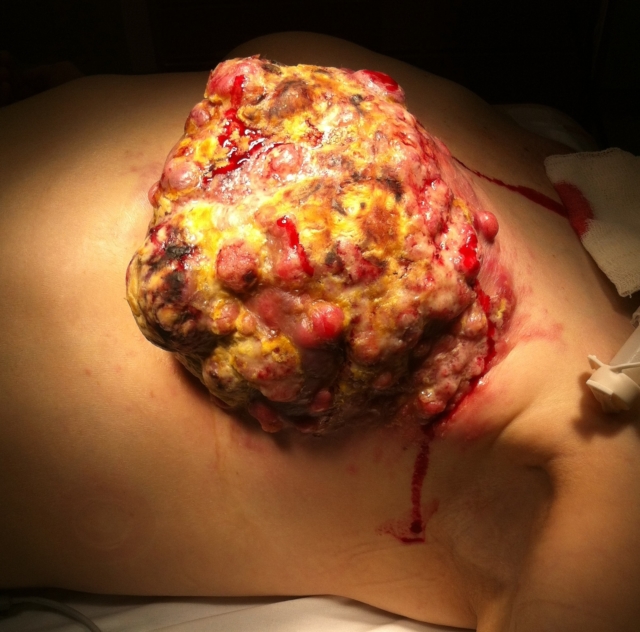
Фото 1. Разрушение метастазой костной ткани
Появление тяжелых признаков и симптомов болезни связано с нарушением постоянного обновления тканей костей, существующее у здорового человека. Нормальное клеточное взаимодействие, элементами которого выступает резорбция, ремоделирование и костеобразование, нарушается, так как остеобласты и остеокласты, отвечающие за указанный функционал, блокируются раком. В итоге, в кости наблюдается вытеснение здоровых и полезных тканей, место которых занимает метастаза.
Рак молочной железы частая причина костного метастазирования. При таком женском заболевании злокачественные структуры посредствам лимфогенного или гематогенного перемещения, перемещаются и накапливаются в костях, преимущественно таза и груди.
Течение недуга сопровождается интенсивными болями, свою лепту в которые вносят регулярные переломы. Обычно это означает 4 степень рака, продолжительность жизни и выживаемость при которой небольшая.
Исходя из разновидности активизации онкологии, выделяется несколько их типов:
- Остеопластическими называют ситуацию образования плотных участков, внедренных в кость.
- К остеолитическим относят процесс разрушения костной ткани.
Любой случай заболевания это комбинация из двух указанных патологических процессов. Наиболее часто метастазы случаются в костях, активно питаемых кровью, они образуются в:
- Плечевой зоне
- Тазу
- Ребрах
- Черепе, элементах позвоночника
На ранних стадиях образования не имеют никаких признаков, позже появляются симптомы боли и другие проявления.
Ранняя степень метастазирования протекает бессимптомно, но по мере роста, воздействие онкологии на кость становится более явным, и появляются первые признаки:
- Гиперкальциемия. Так именуют последствие метастазы в кости, встречающееся в более чем трети больных. Патология вызывает повышенную активность остеокластов, из-за чего резко повышается кальций в крови. Это ведет к повышенной нагрузке на почки, что грозит нарушением обратной всасываемости и чрезмерному выделению мочи.
- Патологические переломы.
- Спинномозговая компрессия при опухоли в позвоночнике.
В результате гиперкальцемии и пережатия спинномозговых каналов у человека появляются следующие симптомы:
- Со стороны нервной системы онкобольной с метастазами в костях страдает от заторможенности, неуравновешенной психики, спутанного сознания, аффективных нарушений.
- Сердце и сосуды начинают неправильно функционировать, что заканчивается аритмией, пониженным артериальным давлением, низкой частотой сердечных сокращений. Все это граничит с сердечной недостаточностью и мгновенной смертью.
- Вероятна почечная недостаточность из-за интенсивной нагрузки на них
- Желудочно-кишечный тракт страдает от расстройства, больного часто подташнивает, отсутствует аппетит, запор переходит ведет к кишечной непроходимости и т.д.
В условиях, когда метастазы в костных тканях разрушают больше 50% кортикального слоя, резко возрастает вероятность переломов. От этого страдают кости позвоночного столба в пояснице или грудном отделе и бедра. Незначительное превышение нагрузки заканчивается переломов кости и симптомами сильнейшей боли.
По причине метастазов в костях они настолько ослабевают, что нередко ломаются вообще сами по себе. При этом из-за относительного смещения в месте слома, функционал конечности или костного элемента полностью теряется. Не успев срастись, происходит еще один слом и так далее. В итоге человек практически обездвижен и ему грозит инвалидность с необходимостью постоянного обезболивания.
Дальнейший рост злокачественной опухоли ведет к сдавливанию сломанными костями мягких тканей, располагающихся рядом. Это грозит постоянными сильнейшими болями, слабостью мышц, нарушенной чувствительностью. Продолжительность жизни при таких осложнениях очень мала, терминальная стадия ведет к параличу и отказу органов таза.
В таких условиях жизнь с метастазами в костях становится серьезным испытанием. Речи об излечении уже не идет, задача медиков состоит в улучшении условий существования.
При метастазировании костей позвоночника существует риск спинномозгового пережатия. Часто это явление наблюдается при локализации в грудной части позвоночного столба. Симптомы формируются последовательно, по мере усиления давления на спинной мозг, проходящий в специальном позвоночном канале. Резкое появление признаков происходит при переломе позвоночного элемента.
Если вовремя заметить и начать лечить спинномозговое пережатие, то его последствия обратимы, на поздних стадиях признаки паралича будут становиться все более явными, несмотря лечение.
Статистика говорит, что лишь каждый десятый онкопациент способен к самостоятельному перемещению после развития паралича.
Надежное и информативное диагностирование костного метастазирования возможно при помощи скелетной сцинтиграфии. Метод позволяет понять, насколько распространено образование, и на какой степени оно находится.
Данной процедурой находят метастазы в любых костях человеческого туловища и конечностей. Эффективно выявляются даже начальные стадии недуга, когда симптомы еще не проявлены. Итогом лечения на данном этапе будет значительное улучшение прогноза и продолжительности жизни.
Фото 2. Вид тазовых костей на рентгене
Более доступный и бесконтактный метод это рентген. Однако он выявляет лишь зрелую вторичную метастазу, когда разрушению уже подвергся значительный объем кости. Преимущество рентгенологии заключается возможности дифференцирования вторичного новообразования, исходя из его типа. Разная окраска пятен на фото, будет говорить о различной их природе.
На более поздних этапах диагностики для уточнения диагноза и метода лечения применяют:
- КТ и МРТ
- Радиоизотопное диагностирование
- Остеосцинтиграфию
- Анализы мочи и крови
При обнаружении опухоли в черепе, проводятся дополнительные обследования для исключения поражения соседних органов.
То, чем и как лечить метастазы в костях будет зависеть от локализации патологии, степени ее развития и параметров исходного рака. Перечислим основные методы лечения:
- Операции применяются в рамках паллиативной помощи, когда улучшение прогноза выздоровления невозможно и больной уже неизлечим, но нужно максимально продлить срок жизни и улучшить ее качество. Благодаря хирургической удалению опухолей удается уменьшить сдавливание нервных окончаний спинного мозга, уменьшить вероятность сломов костей. Все это значительно снижает болевой синдром и частично возвращает потерянные анатомический функционал.
- Применение лучевой и химиотерапии используется для подготовки пациента к операции, либо после нее, а также как самостоятельное лечение. Путем химического или лучевого уничтожения онкоклеток удается остановить рост метастаз в костях.
- Прием бисфосфонатов. Это специальные препараты, тормозящие разрушение костной ткани.
- При некоторых видах рака эффективно использование радиофармпрепаратов.
- Активизация иммунной системы позволяет продлить продолжительность жизни человека. За счет активизации собственных сил организм лучше начинает бороться со злокачественным распространением, изнутри помогая внешнему лучению.
Так называют лекарства, защищающие костные структуры от разрушения. Они показаны при остеокластной патологии для компенсации вредного действия метастаз.
Благодаря поглощению басфосфоната в месте, где произошло метастазирование, негативная деятельность замедляется или совсем прекращается. В дополнение препарат тормозит выработку остеокластов, которые быстро погибают или самостоятельно разрушаются. Механика действия состоит в накапливании активного вещества вокруг образования. При наборе необходимой массы начинается позитивное воздействие по угнетению разрушающей функции.
Бывает два вида бисфосфонатов. Первые состоят из азотистых соединений и более действенны в отношении метастаз в костях. Вторая группа лишена таких соединений и лечение с ее помощью менее эффективно. Что конкретно назначить будет зависеть от финансовых возможностей больного и стадии развития новообразования.
Сколько конкретно живут пациенты с метастазированием в костях невозможно. Примерно это сделать можно увидев историю болезни. Для точного прогноза выживаемости врачу надо проанализировать много информации о метастазе и других раковых новообразованиях.
Приведем цифры сколько живут люди с метастазами в костной ткани в зависимости от первичной онкологии:
- Метастазирование рака легкого и меланомы дает продолжительность жизни около 6 месяцев.
- Простата – 1-3 года
- Рак молочных желез – 18-24 месяца
- Почки с костным метастазированием дают человеку до 12 месяцев жизни
- Самый лучший прогноз при злокачественном поражении щитовидной железы. С рассматриваемыми в статье осложнениями люди живут еще до 4-х лет.
Автор: редактор сайта, дата 25 января 2018
источник
Если диагностированы метастазы в костях при раке молочной железы сколько живут зависит от адекватного и своевременного лечения. Появление метастазов в костях считается очень опасным осложнением распространения рака. Чаще всего, при появлении метастазов, врачи говорят о 4 стадии рака. Они отмечают, что, если болезнь активно развивается и метастазы поразили костную ткань, то продолжительность жизни пациента составляет всего пару месяцев.
Появление метастазов в костной ткани негативно сказывается на общем здоровье пациента.
Медики отмечают, что метастазы образуются у больного при развитии рака:
Важно отметить, что метастазы могут появиться и при развитии рака иных органов: ребер, позвоночника, черепа, бедра, плеча и в костях тазового дна.
Их образование связано со способностью человеческого организма постоянно костеобразовываться. Этот процесс возникает под влиянием двух групп клеток:
- Остеокласт. Они регулируют процесс разрушения и поглощения костных клеток.
- Остеобласт. Они осуществляют выработку новой костной ткани.
В том случае, если здоровье пациента находится на нормальном уровне, то данный процесс осуществляется 1 раз в 10 лет. Если же данный процесс нарушен, то происходит аномальная выработка данных клеток.
Медики разделяют два вида рака в зависимости от поражения клеток:
- Остеолитический рак заключается в поражение остеокласт. Благодаря этому осуществляется истончение костной ткани, человек часто ломает конечности.
- Остеобластический рак заключается в нарушении структуры остеобластов. Благодаря этому происходит увеличение костной ткани, образование наростов и иных новообразований.
Медики отмечают, что на ранних стадиях рак не проявляется никакими симптомами. В результате этого его трудно выявить. При переходе болезни в более тяжелую стадию пациента могут беспокоить следующие симптомы:
- сильная головная боль;
- появление болевых ощущений в конечностях. Обычно это связано с оказанием чрезмерного давления на нервные окончания;
- резкое увеличение внутрикостного давления и нарушение двигательной активности;
- частые переломы конечностей. Это связано с чрезмерным истончением костной ткани;
- появление опухоли или уплотнения в проблемной области.
- увеличение количества кальция в крови. Это является очень опасным для человека, так как кальций оказывает негативное воздействие на работу сердечной системы и вызывает развитие почечной недостаточности;
- появление поражений в нервной системе, оказание чрезмерного давления на спинной мозг и нервные корешки. В запущенных случаях они ведут к развитию паралича.
- интоксикация организма. Обычно об этом свидетельствует появление апатии, депрессии, вялости, хронической усталости, слабости, тошноты, потери аппетита.
Важно отметить, что развитие в организме метастазов может выявить только специалист. Для этого им могут быть применены дополнительные методы исследования:
- использование рентгенографии. Является очень информативным методом, но не позволяет выявить рак на ранней стадии.
- применение компьютерной томографии. С ее помощью специалист может выявить степень развития рака, а также изучить внутренние ткани на наличие в них повреждений.
- использование МРТ диагностики. Она позволяется выявить масштаб метастазированной области и дать наиболее полную картину болезни.
- применение сцинтиграфии. С ее помощью можно выявить степень накопления раковыми клетками специальных лучей. Также данный метод позволяет наиболее точно определить зону появления метастазов.
Помимо этого, пациенту будет назначена сдача биохимического анализа крови и биопсия.
Важно отметить, что метод лечения зависит от степени развития болезни и особенностей самого пациента.
Медики отмечают, что в настоящее время разработано несколько методик избавления от метастазов. К ним следует отнести:
- Использование химиотерапии . Внедрение специальных препаратов оказывает негативное воздействие на процесс распространения раковых клеток. Медики отмечают, что данный способ имеет огромное количество различных побочных эффектов.
- Применение лучевой терапии. Она основана на оказании воздействия на раковые клетки с помощью специальных рентгеновских лучей. Многие пациенты отмечают, что данный способ является одним из самых действенных при избавлении от раковой опухоли. Недостатком данной терапии является длительный период реабилитации больного.
- Проведение медикаментозной терапии. Обычно, если метастазы поразили кости, то применяются такие препараты как биосфосфаты. Они помогают быстрее восстановить костную ткань.
Для достижения большого эффекта медиками проводиться комплексная терапия. Помимо этого, больному назначается прием обезболивающих средств и иммунномодуляторов.
Важно отметить, что при поражении метастазами костей специалисты дают не очень положительный прогноз на выживаемость. Обычно такие метастазы свидетельствуют о переходе болезни в тяжелую стадию.
Таким образом, при раке молочной железы с метастазами в кости обычно пациенты живут от 3 месяцев до 1 года. В некоторых случаях отмечается, что пациенты могут жить около 2 лет.
В данном случае выживаемость зависит от следующих факторов:
- от того, какие лечебные мероприятия проводились в первое время при лечении начальной стадии рака;
- от конечной степени развития болезни;
- от особенностей течения заболевания и способности организма противостоять болезни.
Таким образом, метастазы, особенно в костях, являются очень опасным осложнением грудной онкологии, но чем ранее пациенту был поставлен диагноз и проведено грамотное лечение, тем выше шанс на продолжение жизни у пациента и быстрое избавление от болезни.
источник
Метастазы в кость ─ это наиболее часто встречаемая локализация поражения при распространенном раке молочной железы (РМЖ). Нарушение скелетной анатомии и функциональности происходит за счет ростовых факторов опухолевых клеток. Ростовые факторы стимулируют активность остеокластов (многоядерные клетки огромных размеров, которые разрушают костную ткань). Частота костных метастазов при раке грудной железы достигает 65 – 75%.
Этапы метастазирования опухоли при прогрессировании заболевания:
- Прогрессирование первичной опухоли ─ раковые клетки взаимодействуют с микроокружением, образуются удаленные преметастатические ниши.
- Диссеминация (рассеивание и распространение) опухолевых клеток ─ раковые клетки мигрируют, агрессивно поражают ткани и выходят в кровяное русло.
- Оседание в костной ткани ─ случайное и беспорядочное их попадание и оседание в костной ткани, уклонение от иммунитета.
- Выживание раковой клетки ─ миграция атипичных клеток в специфичные ниши.
- Распространение опухоли и ангиогенез (образование новых кровеносных сосудов, питающих опухоль) ─ раковые клетки подчиняют клетки микроокружения и формируют собственную сосудистую систему.
- Прогрессия метастаза и прогрессирование заболевания в целом ─ опухоль становятся независимой от микроокружения.
Моделирование костной ткани осуществляется остеобластами и остеокластами (костные клетки). Опухоль стимулирует разрушение костной ткани остеокластами. Ростовые факторы усиливают развитие раковых клеток. Происходит дисбаланс физиологического процесса моделирования костей. Другие виды клеток, которые находятся в окружении, также могут влиять на развитие опухоли.
Ростовые факторы выделяются атипичными клетками. Они принимают участие и обуславливают все процессы образования опухоли:
- Факторы, образованные в костной ткани, стимулируют рост и миграцию опухоли.
- Факторы, образованные в самой опухоли, организовывают разрушение кости.
- Факторы, препятствующие образованию здоровой костной ткани.
- Факторы экспрессии молекул раковых клеток, которые способствуют обширному метастазированию.
Чаще поражаются «несущие» части скелета ─ бедренные и тазовые кости, позвоночник. Переломы приводят пациента к длительной инвалидности. Восстановление очень медленное. Продолжительный и устойчивый болевой синдром.
Важно! Угроза патологического перелома сохраняется даже в случае эффективной противоопухолевой терапии.
К клиническим проявлениям метастатической болезни относятся:
- деформация костей;
- гиперкальциемия ─ много кальция в крови;
- боль;
- нарушение опорной функции;
- патологические переломы;
- неврологические нарушения.
Рак молочной железы с метастазами в кости ─ это тяжелое состояние больных, сопровождаемое переломами. Дисфункциями систем и органов, вызванными гиперкальциемией фиксируется в 65% случаев.
Высокий кальций встречается в 7 – 15% случаев. Сопровождается такими симптомами, как сухость во рту, постоянная жажда, запоры, рвота, полиурия (увеличение суточной нормы выделяемой мочи). В тяжелых случаях наблюдается развитие острой почечной недостаточности, потеря сознания.
Сверхсильные боли ─ частое осложнение при распространенных опухолях (42 – 95% случаев). Причины болевого синдрома:
- Раковые клетки выделяют химические вещества, которые стимулируют болевые рецепторы.
- За счет увеличения опухолевой массы повышается внутрикостное давление.
- Растяжение надкостницы и микропереломы.
- Реактивное мышечное сокращение.
- Проникновение раковых клеток в нервные окончания.
- Сдавление нервов.
Боль бывает острая и хроническая. Острая или «прорывная» боль характеризуется внезапным приступом. Хроническая ─ постоянная, пульсирующая, изнуряющая, усиливается при прогрессировании.
Еще одно осложнение ─ это декомпрессия спинного мозга, встречается в 3% случаев.
Можно ли полностью излечить заболевание с метастазами?
Цель лечения ─ это подавление опухоли, предотвращение осложнений (компрессия тканей, переломы), восстановление утраченных функций, улучшение качества жизни.
Терапия РМЖ с метастазами в кость направлена на системное лечение основного заболевания. А также на замедление разрушения костной ткани и ускорение ее восстановления. По показаниям назначается:
- лучевая терапия;
- хирургическое вмешательство;
- ортопедическое лечение;
- наркотические препараты для снятия боли.
Бисфосфонаты являются стандартом лечения при РМЖ. Они останавливают развитие метастазов в кость, оказывают профилактическое и терапевтическое действие на остеопороз, который является следствием онкологического заболевания.
Применение бисфосфонатов значительно:
- увеличивает время до первого костного осложнения;
- снижает риск развития гиперкальциемии;
- уменьшает количество используемых наркотических анальгетиков;
- сокращение показаний к проведению лучевой терапии костей;
- улучшает результаты комплексного лечения и выживаемость.
Женская онкология имеет тенденцию к омоложению. Заболевание встречается у женщин в возрасте от 30 лет. Если есть метастазы в костях при раке молочной железы, вопрос, сколько живут, становится актуальным.
Насколько качественно будут жить пациенты, их активность и жизнедеятельность зависят от течения заболевания и адекватной терапии. Значительно затрудняют специфическое лечение и негативно влияют на выживаемость осложнения. Пятилетняя выживаемость отмечается у 20%. Медиана (усредненный показатель) составляет 24 месяца.
источник
4 стадия рака молочной железы (РМЖ) – терминальная. Она характеризуется выраженной симптоматикой. Женщина не сомневается в наличии онкологической патологии – настолько интенсивно проявляется боль. Состояние ослаблено и сопровождается всесторонней дисфункцией. Нарушена деятельность внутренних органов. У 90% пациенток подавлено психоэмоциональное состояние. Это связано с осознанием степени тяжести заболевания, изнурительным лечением и симптоматикой, в составе которой преобладает боль. Чтобы минимизировать уровень стресса, важна помощь и поддержка близких.
РМЖ терминальной стадии развития характеризуется прогрессированием злокачественного процесса в обеих молочных железах и распадом опухоли. Средний размер новообразования достигает 5 см в диаметре. Опухоль поражает всю толщу железистой ткани, преодолевает её предел; отличается массивностью. Вызывает высокую степень болезненности. Направляет метастазы в печень, кости таза и рёбер, лёгкие, головной мозг. Наблюдается интенсивное поражение лимфатических узлов – подмышечных, подключичных, ключичных, реже – подчелюстных.
На фоне и вследствие опухолевого процесса возникает 2 основные проблемы – ослабление защитных свойств организма и метастазы. Рак груди опасен риском её ампутации; высокой вероятностью развития различных заболеваний, что связано со снижением иммунитета.
Из-за ослабления иммунитета женщина подвержена инфекционно-вирусным патологиям.
Метастазы, присутствующие в печени, лимфатических узлах, лёгких и головном мозге, проявляются болью. Это вызывает бессонницу, снижение двигательной активности.
Мастэктомия приравнивается к значительному стрессу, влияет на самооценку, становится причиной депрессии.
На терминальной стадии опухолевого процесса груди наблюдаются следующие признаки:
- Поражённая молочная железа деформируется, её размер уменьшается или увеличивается.
- Пациентка испытывает сильную боль, которую приходится регулярно купировать анальгетиками.
- Кожа молочной железы сморщена, достаточно интенсивно шелушится.
- Контур ареолы изменяется, оттенок её ткани становится насыщеннее, сосок темнеет.
- Из груди почти постоянно выделяется гнойная секреция, которая сменяется кровотечением.
Поскольку на терминальной стадии рака груди присутствуют метастазы, возникает дополнительная симптоматика (зависит от поражённого органа). Наблюдается пожелтение кожи, боль в рёбрах и костях таза, цефалгия. Злокачественный процесс характеризуется астеновегетативными явлениями. К ним относится слабость, апатия, потемнение перед глазами вследствие снижения показателей давления, головокружение. При наличии метастазов в лёгких происходит нарушение дыхания, боль в спине и груди, проблемы с принятием удобного, безболезненного положения тела.
В онкологии прогрессирование рака молочной железы связывают с развитием анемии, кахексии (истощения), мигрени, гиповитаминоза, печёночной недостаточности. Перечисленные заболевания предварительно устанавливают благодаря клиническому и биохимическому анализу крови; УЗИ органов, дисфункцию которых предполагает врач. Снижение концентрации витаминов в организме и уровня гемоглобина компенсируют нормализацией питания. Дополнительно пациентке внутривенно-капельно вводят витамины в чистом виде и препараты железа внутримышечно.
Состояние и функциональную активность печени корректируют гепатопротекторами, приступы мигрени угнетают обезболивающими средствами.
Кахексия – тяжёлое состояние, которое устраняют путём улучшения качества питания и посредством внутривенно-капельного введения растворов. Применяют глюкозу и её аналоги. Поскольку во время прогрессирования опухолевого процесса у пациентки отсутствует аппетит – назначают парентеральное питание.
Рак грудной железы на терминальной стадии развития хорошо поддаётся диагностике. Поскольку опухоль на этом этапе разрастается до крупного размера, врач без труда определяет её при пальпации. Другие виды диагностики:
- Маммография (показана женщинам старше 40 лет).
- УЗИ молочных желез (выявляет все виды изменений в груди).
- Дуктография. Метод предполагает использование контрастного вещества. Оно заполняет млечные протоки и железистую часть груди. Это позволяет в полной мере визуализировать их структуру.
- КТ, МРТ – это методы сложной лучевой визуализации. Они предоставляют информацию о размере опухоли, её границах, степени сращения с окружающими тканями. Также благодаря указанным видам диагностики определяют структуру и особенности кровоснабжения новообразования.
- Рентгенологическое исследование рёбер и костей таза. Позволяет выявить присутствие метастазов. Проводят сразу после уточнения параметров новообразования.
- Флюорография (если врач предполагает наличие метастазов в лёгких).
- УЗИ органов брюшной полости с акцентом на состоянии печени.
- КТ головного мозга (при подозрении на наличие атипичных клеток в нём).
Для подтверждения злокачественного происхождения опухоли проводят биопсию молочной железы. Метод предполагает взятие небольшой частицы ткани, затем образец направляют в лабораторию для изучения под микроскопом. Исследование определяется как гистологический анализ. Благодаря этому виду диагностики с точностью определяют, какого характера опухоль – доброкачественного или злокачественного.
Лабораторные исследования (анализ крови, мочи) позволяют установить:
- концентрацию билирубина (прямого, непрямого), АСТ, АЛТ (перечислены печёночные пробы);
- уровень гемоглобина;
- показатели онкомаркеров.
При опухолевых очагах в печени, лимфатических узлах или других органах также показана их биопсия с дальнейшим гистологическим анализом.
Терминальная стадия рака молочной железы тяжело поддаётся лечению. Причина – наличие метастазов и неконтролируемое деление атипичных клеток. На этом этапе опухолевого процесса операцию проводят не всегда, поскольку общее состояние пациентки ослаблено. Наличие очагов атипичных клеток внутри лёгких отягощает процесс дыхания во время наркоза. Это исключает возможность адекватного обезболивания во время хирургического вмешательства.
Операция на 4 стадии развития злокачественного процесса не предполагает секторальный или сегментарный метод. Эти виды хирургического вмешательства сводятся к удалению опухоли и лишь незначительной части окружающих тканей. Оптимальная схема лечения при терминальной фазе рака груди – мастэктомия (ампутация молочной железы), сопровождаемая иссечением лимфатических узлов. Причина такого выбора операции – на 4 стадии РМЖ новообразование имеет достаточно крупный размер.
Если операция не противопоказана, её успешность закрепляют курсом химиотерапии. В совокупности такой подход продлевает жизнеспособность.
Также химиотерапию при раке молочной железы 4 стадии проводят в качестве отдельного вида лечения. Назначают сочетание из таких сильнодействующих препаратов, как Винбластин, Доксорубицин, Таксол. Каждое из перечисленных лекарственных средств вводят внутривенно.
Рак молочной железы 4 степени ассоциируется с необратимым процессом и обречённостью. Главная задача родственников – обеспечить максимально комфортные условия пребывания в семье. Это относится не только к медикаментозному обеспечению и вопросу нормализации питания, но и к психологической обстановке.
Чтобы улучшить условия жизни родственницы, страдающей раком груди 4 стадии, следует:
- Составлять рацион с учётом потребностей человека с онкологической болезнью.
- С пониманием относиться к тому, что двигательные и физические возможности женщины – ограничены.
- Поддерживать, не вступать в споры – нецелесообразно пытаться переубеждать человека со столь тяжёлым заболеванием.
- По возможности обеспечить пациентке необходимый набор лекарственных препаратов.
- Корректно реагировать на спонтанные перемены настроения, при необходимости – обеспечить консультацию психолога.
- По возможности установить круглосуточный пост, чтобы регулярно приносить питьё, отводить в туалет или оказывать иную помощь.
- Обеспечить психологический покой (не создавать конфликтных ситуаций при женщине с онкологической болезнью).
Не нужно забывать, что женщина нуждается в ежедневном пребывании на свежем воздухе. Если двигательные возможности ограничены, следует воспользоваться специальной коляской для транспортировки недееспособных людей. Немаловажная часть ухода – гигиенические процедуры, в выполнении которых женщине нужно помогать.
Одна из ошибок врачей – общение с пациенткой исключительно профессиональной терминологией. Это вызывает непонимание и может испугать. Не следует обнадёживать, предоставлять искажённые сведения о состоянии здоровья, прогнозе. Задача врачей – максимально корректно, понятным языком сообщить пациентке действительную клиническую ситуацию.
Для подавления боли, степень которой при раке 4 стадии – очень высока, вводят наркотические анальгетики. Нестероидные противовоспалительные препараты применяют несколько реже. Из числа таковых назначают Ибупрофен, Диклофенак, Вольтарен. Перечисленные лекарственные средства оказывают более высокий анальгезирующий эффект при внутримышечном введении. Из наркотических анальгетиков применяют Трамадол, Кодеин, Промедол. Чтобы не вызвать привыкание организма, применять любой из перечисленных препаратов следует не чаще 1 раза в 4 часа.
При раке молочной железы 4 стадии с метастазами показатели выживаемости – достаточно низкие. Это связано с необратимыми процессами рассматриваемого этапа опухолевого процесса. Даже комплексное, правильно составленное лечение не может существенно продлить выживаемость, если опухоль обнаружена уже в фазе распада. При выявлении рака на 4 стадии, но отсутствии лечения длительность жизни не превышает полугода (при условии регулярного проведения обезболивания).
Если лечение всё же проведено – выживаемость может достигнуть 2-2,5 лет, при мастэктомии с последующим удалением подмышечных лимфоузлов – до 5 лет.
Также определяющее значение имеет локализация метастазов. Независимо от характера проводимого лечения, в онкологии сделали следующее наблюдение:
- При наличии метастазов в головном мозге длительность жизни не превышает 2-3 недель.
- При развитии опухолевых очагов в лёгких выживаемость не превышает 3 лет.
- Если метастазы присутствуют в печени, средняя продолжительность жизни – полгода.
На выживаемость влияет возраст пациента, состояние его иммунитета, наличие сопутствующих заболеваний, психоэмоциональное самочувствие.
Возможность продления жизни при терминальной стадии РМЖ зависит от ухода, питания, обезболивания и санации органов, подверженных поражению метастазами.
Введение анальгетиков положительно отражается на общем самочувствии, помогает восстановиться за время сна. Питание компенсирует недостаток полезных веществ. Уход за женщиной – это содействие реализации её потребностей, обеспечение психологической поддержки. Санация органов, подверженных метастазированию, позволит на раннем этапе выявить опухолевые очаги и устранить их.
4 стадия рака молочной железы сопровождается интенсивной болью и ухудшением общего самочувствия. Женщина страдает бессонницей, выраженным дискомфортом в костях, дисфункцией внутренних органов, изменением активности головного мозга. Высокий уровень болевого синдрома предполагает регулярное введение анальгетиков, в том числе, наркотического типа. Со стороны родственников требуется внимание, уход, забота, содействие своевременному посещению врача.
источник
Прежде всего немного опишем само понятие рак груди. Под раком молочной железы подразумевают злокачественную опухоль молочной железы, а именное ее железистой ткани.
По статистике, данное заболевание стоит на первом месте среди заболеваний у женщин. Больше страдают заболеванием женщины после 65 лет, чем до 65. Для развития заболевания могут служить множество факторов:
- нерожавшая женщина;
- курение;
- начало ранней менструации до 12 лет;
- поздний климакс, который начался после 55 лет;
- наследственность;
- ожирение;
- сахарный диабет;
- гипертоническая болезнь;
- алкоголь (злоупотребление);
- непрерывное употребление гормональных средств (более 8 лет).
- Т — первичная опухоль,
- N — региональные лимфатические узлы,
- M — отдельные метастазы.
Типы рака молочной железы:
- внутрипротоковый рак;
- дольковый;
- инвазивный протоковый;
- инвазивный дольковый;
- рак с признаками воспаления;
- тубулярная карцинома;
- медуллярный;
- коллоидный;
- папиллярный;
- метапластический;
- рак с остеокластоподобными клетками;
- аденоид — кистозный рак;
- секреторная карцинома (ювенильный);
- кистозная гипертсекреторная карционома;
- апокринный;
- рак с признаками эндокринного новообразования;
- криброзный.
Существуют четыре стадии рака груди:
- 1 стадия — неинвазивная — иногда её называют нулевой. Этот вид опухоли характерен тем, что носит непроникающий характер, размер опухоли менее 2 см.
- 2 стадия — подразделяется на подгруппы:
- 2а — новообразование размером менее 2 см, которое задевает лимфатические узлы в подмышечной впадине.
- 2б — новообразование размером от 2 см до 6 см, которая задевает лимфатические узлы в подмышечной впадине.
- 3 стадия — подразделяется на подгруппы:
- 3а — патологические клетки начинают прорастать в кожу, лимфатические узлы в области подмышек.
- 3в — новообразование заметно увеличивается, образуются спайки на лимфатических узлах.
- 3с — происходит деформация соска, опухолевые клетки все больше и больше прорастают на лимфатическую систему, которая находится не только в области подмышек, но и в области ключицы.
- 4 стадия — считается критичной. Характеризуется заметным увеличением первоначального объема патологической ткани. Происходит образование метастаз, которые проникают как во внутренние органы, так и в головной мозг.
Четвертая стадия заболевания характеризуется последней стадией рака. Часто данную стадию называет вторичным раком молочной железы. Для данной стадии характерно распространения раковых клеток за пределы первичного поражения (на другие органы). Развитие данной степени обычно происходит быстро. Зависит от:
- внешних факторов,
- психологического состояния,
- формы рака,
- своевременного лечения.
Данная степень очень опасна, к сожалению, зачастую онкологи не в силах помочь женщине, которая первично обратилась с раком 4 стадии.
Но не стоит забывать, что при своевременном обращении к онкологу и правильном лечении, 4 стадия рака — это не безнадежный диагноз.
Как показывает практика, рак 4 стадии очень распространен у женщин в возрасте от 30 до 40 лет, и женщин, у которых наступил климакс.
- неивазивная — не проникающая;
- гипотиреодная (у женщин в возрасте от 10 лет до 30 лет);
- яичниковая (у женщин средних лет);
- гипертензивная (женщины, у которых уже наступил климакс);
- гипофизарная (женщины старше 65 лет).
Ранние признаки рака 4 стадии молочной железы могут начаться через некоторое время после установленного диагноза рака груди. Реже, рак 4 степени диагностируется как первичный диагноз. К ранним симптомам относятся:
- заметное ухудшение общего состояния;
- общая слабость, частое головокружение;
- поднятие температуры тела, которая не связана с воспалительными процессами;
- гиперемия ткани груди;
- отек молочной железы;
- заметная деформация соска;
- изменение строения кожи в области патологических клеток, часто называют «гусиная кожа»;
- наличие «сосков» вытянутой кожи в области ореола;
- заметное увеличение пораженной груди;
- выделение из соска жидкости с примесью гноя.
Когда наступает последняя стадия рака молочной железы, то клинически можно увидеть:
- патологические клетки во всей области молочной железы;
- первичное новообразование достигло своих размеров — более 5 см;
- имеются метастазы на лимфатических узлах (часто легкие, печень, головной мозг, желудок).
- снижение аппетита;
- заметная общая слабость, быстрая утомляемость;
- постоянная тошнота;
- мигрень;
- боль в суставах, костях , которое не проходят;
- потеря веса;
- одышка, кашель (как следствие метастаз в легких);
- боль в области диафрагмы;
- заметное увеличение живота.
Первоначальными исследованиями считают:
- осмотр и пальпация врачом;
- ультрозвуковое исследование молочной железы;
- онкомаркеры.
Для распознавания наличие метастаз и более точного развития заболевания проводится полное обследование. Оно заключается в:
- ОАК;
- ОАМ;
- рентген легких;
- ультрозвуковое исследование органов брюшной полости;
- МРТ молочной железы (при необходимости брюшной полости);
- МРТ головного мозга;
- остеосцинтиграфия;
- биопсия молочной железы.
Дополнительные исследования по показаниям могут быть: плевральная пункция, биопсия необходимого органа, КТ, ПЭТ).
К сожалению, при постановке диагноза рака 4 стадии речь о полном выздоровлении не идет. Лечение направленно на улучшение качество жизни, на продлении жизни, облегчение симптомов. Лечение помогает замедлить рост патологических клеток. Тактика проведение лечения зависит от:
- расположение метастаз, их количества;
- от возраста пациентки;
- от лечения назначенного ранее;
- от общего состояния женщины.
После этого применяется один из видов лечения. Виды лечения:
- Хирургическое: удаление молочной железы или желез.
- Химиотерапия: комплекс лекарственных средств, которые имеют свойство разрушать опухоль. Данный метод может очень тяжело переноситься и часто приводит к: слабости, тошноте, выпадению волос, нарушению со стороны ЖКТ.
- Лучевая терапия — излучениями ионами. Часто назначается в комплексе с хирургическим видом лечения и другими лекарствами. Различают несколько видов:
- радикальная — полностью убирает патологические клетки;
- паллиативная — способствует продлить жизнь, не дает полного удаления клеток;
- частичная — снимает болевой синдром.
- Гормональная терапия: половой гормон (эстроген) дает возможность клеткам восстанавливаться. Все онкологические новообразования зависят от гормонов в крови. При отсутствии метастаз, данное лечение может способствовать уменьшению патологических клеток и препятствовать их развитию.
- Бисфосфонаты: лекарственные средства, которые способствуют торможению разрушения костей, также являются защитой от раковых клеток.
Ранняя диагностика и выполнение всех требований лечения, может помочь Вам на долго продлить жизнь.
Обезболивающие средства несут огромную роль в жизни онкологических больных. В особенности при раке 4 стадии обезболивание просто необходимо.
Препараты, которые используются при не сильно выраженной боли при раке 4 стадии:
- Противовоспалительные: Аспирин, Диклофенак — работают в комплексе с более сильными препаратами.
- Стероиды: Преднизолон и др. — снимают отек, устраняют боль при давлении опухоли на органы.
- Бисфосфонаты: устраняют боль при раке молочной железы (при опухоли, которая распространяется на кости).
- Ингибиторы селективной циклооксигеназы 2 типа: новое поколение препаратов, которые обезболивают и также имеют противоопухолевое действие.
Умеренные препараты при раке 4 стадии:
- Кодеин может назначаться с парацетамолом.
- Трамадол может применяться каждые 12 часов. Максимальная доза 400 мг в сутки.
Средства часто применяемые в практике:
- Морфий: дает возможность на долго обезболить.
- Фентанил Альфентанил: таблетки под язык, раствор для иньекций.
- Бупренорфин: сильное действие, накапливается в течении суток.
- Оксикодон: хорошо помогает при болях (метастазах) кости, нервной ткани.
- Гидроморфон: более эффективен в инъекциях.
- Метадон: хорошо влияет на подавление боли в нервной ткани.
В настоящее время лечение может значительно продлить жизнь. Сказать сколько вы можете прожить с данным диагнозом не возможно. Все, конечно, строго индивидуально и зависит от того какой вид опухоли, когда вы обратились к доктору и начали лечения, от вашего организма. 4 стадия онкологии считается самой опасной и в большинстве случает не излечимой. В среднем, как показывает статистика, продолжительность жизни не превышает 6 лет в 12% случаев. Тем самым получается, что из 100% на течение 5 лет: 12% — живут, 82% — умирают.
Самое главное — это не опускать руки. Найдите хорошего квалифицированного врача онколога-маммолога. При необходимости организуйте группу поддержки.
Помните, что данный диагноз — это не приговор. В первую очередь, мы вам советует окружить себя только положительными эмоциями. Очень помогают родные и близкие люди. Помните, что важную роль играет самовнушение. Самовнушение о плохом исходе может усугубить картину и исход в целом. И главное, вы должны понимать, что каждый день ученые разрабатывают все более инновационные техники лечения, апробируют новые препараты.
источник
Первое место среди онкопатологии у женщин — рак груди. Симптомы, диагностика, лечение и прогноз 4 стадии болезни
Рак грудной железы находится на первом месте среди онкологических патологий у представителей женского пола. Чаще всего заболеванию подвержены женщины, возраст которых превышает 65 лет. Некоторые виды раковой опухоли сложно диагностировать на первых порах заболевания из-за быстрого роста опухолевых клеток и метастазов.
Рак грудных желез делится на 4 стадии, как и любые иные злокачественные опухоли.
Четвертая степень раковой опухоли — критичная. Эта степень обладает выраженными и отчетливыми характерными признаками:
- деформация одной или двух пораженных желез;
- гиперемия и язвы на коже в месте злокачественного новообразования;
- локальное воспаление, мастит;
- сильная общая интоксикация организма;
- повышенный титр онкомаркеров;
- выраженная анемия;
- увеличение метастазов в других областях тела;
- сильно выраженный болевой синдром;
- ухудшение иммунитета;
- энергетическое истощение.
Скорость развития опухолевых клеток зависит от:
- окружающих факторов;
- состояния психики;
- своевременно начатого лечения.
Для заболевания характерны различные формы:
- неинвазивная или «нулевая» — не проникающая, с опухолевым размером менее 2 см;
- гипотиреоидная или «рак молодых» — в возрасте от десяти до тридцати лет;
- яичниковая — у женщин от тридцати до пятидесяти лет;
- гипертензивная — в возрасте 50-65 лет;
- гипофизарная — у женщин старше 65 лет.
Факторы, провоцирующие патологию:
- отсутствие родов;
- табакокурение;
- раннее наступление месячных — до двенадцати лет;
- позднее наступление менопаузы — после 55 лет;
- наследственное заболевание;
- болезненная полнота;
- сахарный диабет;
- гипертония;
- чрезмерное употребление спиртных напитков;
- беспрерывное применение гормональных препаратов дольше восьми лет.
Ознакомьтесь с фото молочной железы с 4 степенью злокачественного новообразования.
Заболевание можно заметить по следующим ранним признакам:
- выделение гнойной жидкости из соска;
- «соски» из вытянутого кожного покрова в локации ареолы;
- заметное изменение формы соска;
- сильное покраснения тканей груди из-за переполнения кровью сосудов в этой области;
- опухание грудных желез;
- повышение температуры тела без видимых причин;
- гусиная кожа в локации новообразований;
- ощущение упадка сил и частые головокружения;
- видимое увеличение пострадавшей груди;
- ухудшение самочувствия.
Поздние признаки заболевания заключаются в следующем:
- рост живота;
- головные боли;
- гнойники и опухоли лимфатических узлов: легкие, печень, желудок, головной мозг;
- постоянный болевой синдром в суставах и костях;
- частая тошнота;
- снижение или отсутствие аппетита;
- резкое снижение веса;
- при опухолевых клетках в легких — одышка, кашель;
- потеря сил и быстрая утомляемость, которые усиливаются пропорционально увеличению новообразований, т.к. на деление атипичных клеток организм тратит большое количество энергии;
- раковые клетки по всей области грудной железы;
- болевые ощущения в области диафрагмы, которые отмечаются еще в третьей степени и становятся со временем интенсивней;
- размер опухоли больше 5 см.
При обращении к врачу пациент проходит несколько этапов диагностики:
- медосмотр и прощупывание;
- УЗИ груди;
- онкомаркеры;
- общий анализ крови и мочи;
- УЗИ органов брюшной полости;
- МРТ молочной железы, брюшной полости (при необходимости), головного мозга;
- остеосцинтиграфия;
- биопсия молочной железы.
Доктор может назначить вспомогательные исследования:
- плевральная пункция;
- биопсия необходимого органа;
- компьютерная томография;
- позитронно-эмиссионная томография.
Применяют следующие виды лечения:
- Химиотерапия: цель терапии — формирование регресса метастазов и ракового процесса. Препараты назначаются наименее токсичные противоопухолевые цитостатические и антиметаболические: Трастузумаб, Метотрексат, Эпирубицин, Адриабластин, Циклофосфан.
- Гормональная терапия: во время гормонотерапии применяются селективные модуляторы рецепторов эстрогена (например, Тамоксифен) и деструкторы рецепторов эстрогена (например, Фаслодекс).
- Таргетная терапия: применяются препараты из группы моноклональных антител. Обычно применяется Трастузумаб, выборочно ингибирующий клетки с активным геном HER2.
- Паллиативное лечение: применяется в случае отрицательного результата при других видах терапии. Этот вид направлен на улучшение общего самочувствия пациента, снижение болевых ощущений и депрессивных состояний. Терапия не влияет на течение и результат заболевания, но обеспечивает жизнедеятельность, приближенную к нормальной.
На терминальных стадиях назначают обезболивающие из разных групп:
- нестероидные антифлогистические средства;
- слабые и сильные опиаты;
- блокады нервных стволов.
Часто рак сопровождается второстепенными заболеваниями:
- анемия;
- раковое истощение;
- интоксикация организма и другие.
На четвертой стадии рака рассматривается вопрос — до какого момента есть смысл проводить терапию. Разумно будет проводить терапию до тех пор, пока польза лечения превышает его вредные воздействия.

Обычно 4 стадию рака молочной железы сопровождает паллиативное лечение, направленное на:
- снятие боли и улучшение общего состояния больного;
- продление жизни;
- снижение распространения опухолевого процесса.
- сильное истощение организма;
- снижение иммунитета;
- сильный болевой синдром.
Уход за больным состоит не столько в действиях, направленных на выздоровление, сколько на обеспечение его комфортного дожития:
- Задача врачей состоит в том, чтобы подобрать обезболивающие препараты, обеспечить процедуры детоксикации, провести необходимые виды терапии.
- Задача родственников — в обеспечении положительного эмоционального фона, уберечь пациента от простуд, инфекций, истощения. Стоит помнить, что продолжительность жизни напрямую зависит от веса пациента, поэтому нельзя допускать его потери.
- Правильное питание не вылечит того, кто находится на 4 степени заболевания, но улучшит качество жизни, поможет избежать негативных последствий проводимой терапии: гастрит, язва, проблемы с кишечником, рвота, тошнота и другие.
Диета при онкологии простая:
- следует отказаться от жирной и жареной пищи;
- потреблять больше клетчатки, цельнозерновых и бобовых;
- отказаться от употребления спиртных напитков;
- употреблять больше продуктов с высоким содержанием кальция;
- исключить из рациона сою и продукты с иммуномодулирующим эффектом;
- снизить количество сахара в рационе;
- регулярно принимать поливитаминные комплексы.
Рак молочной железы — наиболее часто встречающееся заболевание среди других онкологических проявлений. Заболеть могут и мужчины, но чаще раку груди подвержены женщины.
Вылечить заболевание полностью пока считается невозможным, но лечение поможет облегчить боль, улучшить качество жизни человека и даже продлить ее срок. Один из важнейших факторов — эмоциональное состояние. Поэтому, важно запастись позитивом и терпением.
Предлагаем посмотреть интересное видео про признаки рака груди и способы диагностики заболевания:
источник
Метастазы рака молочной железы в кость. Многие считают рак молочной железы заболеванием, поражающим только женщин. Однако в редких случаях он может развиваться и у мужчин.
Статья на конкурс «био/мол/текст»: Диагностирование рака молочной железы с метастазами в костях — это событие, которое меняет жизнь пациента. Как правило, такую патологию невозможно вылечить, но можно контролировать с помощью постоянного лечения. Что же происходит с костями при метастазировании? Какие методы терапии использует современная медицина?
Эта работа опубликована в номинации «Свободная тема» конкурса «био/мол/текст»-2018.
Генеральный спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.
Спонсором приза зрительских симпатий выступил медико-генетический центр Genotek.
В 1889 году британский врач Стивен Педжет описал концепцию «семена и почва». Согласно его теории, опухолевые клетки распространяются по организму не случайным образом, а требуют взаимодействия с микросредой органа-хозяина. Злокачественные клетки, или «семена», атакуют только подходящие для роста органы, то есть «почву». Таким образом, очаги роста опухоли в новых органах (метастазы) будут развиваться только тогда, когда определенные «семена» будут высажены на пригодную для них «почву».
Педжет обнаружил, что у женщин с раком молочной железы (РМЖ) метастазы развивались с гораздо большей вероятностью в костях, чем в любых других органах [1].
Наш обзор посвящен метастазам РМЖ в кость, изменениям, которые вызывают опухолевые клетки в кости, а также современной терапии таких метастазов.
Рак молочной железы — злокачественная опухоль железистой ткани молочной железы. Это наиболее распространенная злокачественная опухоль у женщин, а по числу заболевших среди мужского и женского населения она занимает второе место после рака легких. В 2018 году было зарегистрировано более двух миллионов новых случаев [6].
Рисунок 1. Очаги возникновения вторичной опухоли при РМЖ. Первоначально опухоль развивается в груди. Однако по мере роста опухоли раковые клетки отрываются и распространяются по соседним тканям или отправляются в отдаленные органы, такие как легкие. Однажды в другой ткани они могут образовать вторичную опухоль.
Современная медицина разработала эффективные способы лечения РМЖ 1–3 стадии, что значительно увеличило выживаемость пациентов [7]. Однако 9 из 10 смертей от РМЖ обусловлены нарушением функций различных органов, вызванным распространением раковых клеток по организму, то есть метастазированием. Как правило, РМЖ может распространяться на кости, головной мозг, легкие, печень и лимфатические узлы (рис. 1). Согласно статистическим исследованиям, самой частой областью метастазирования является кость [8]. Она — преобладающее место развития метастазов люминального и Her2-позитивного типов РМЖ, при этом существенно менее предпочитаемое метастазами трижды негативного типа РМЖ [9].
На ранних стадиях метастазы РМЖ в костях бессимптомны, в результате их трудно выявить. Однако всем пациентам с РМЖ раз в несколько месяцев проводят биохимический анализ крови и биопсию для обнаружения рецидива заболевания. Для диагностирования метастазов в кости необходимо пройти рентгенографию, компьютерную томографию, магнитно-резонансную томографию, сцинтиграфию [8].
Кость — это динамическая ткань, играющая центральную роль в поддержании гомеостаза всего организма. Основными элементами кости считаются остеобласты, которые участвуют в создании и минерализации кости, остеокласты, обеспечивающие разрушение (резорбцию) костной ткани, и остеоциты, поддерживающие структуру (рис. 2). Все эти клетки костной ткани ответственны за «строительные работы»: поглощение старых клеток кости и порождение новых. Они существуют в равновесии и регулируют работу друг друга, что помогает обеспечить гомеостаз кости. Сбалансированный цикл образования и разрушения костной ткани называют добродетельным циклом (от англ. virtuous cycle) ремоделирования костей [10].
Рисунок 2. Костные клетки. В костной ткани обнаружены четыре типа клеток. Недифференцированные остеогенные клетки могут развиться в остеобласты. Когда остеобласты попадают в кальцинированную матрицу, их структура и функции меняются, и они становятся остеоцитами. Остеокласты по внешнему виду отличаются от других клеток костной ткани.
Кость также содержит красные клетки костного мозга и эндотелиальные клетки, которые образуют капилляры сосудистой системы кости [11].
Все типы клеток разделяют один «дом», следовательно, они взаимодействуют между собой и регулируют функции друг друга. Однако сосудистая система кости направляет метастазирование раковых клеток в эту микросреду [12].
Одиночные клетки могут оторваться от исходной опухоли в груди и распространиться по организму двумя способами: гематогенным (по кровеносным сосудам) и лимфогенным (по лимфатическим сосудам). Лимфогенные метастазы поражают соседние и отдаленные лимфатические узлы, а гематогенные чаще появляются в костном мозге и костях (рис. 3). Более подробно об образовании гематогенных метастазов рассказывает статья «Обнаружены организаторы побега раковых клеток из первичного очага» [13].
Рисунок 3. Схематическое изображение распространения раковых клеток по кровеносной системе.
Как только клетки РМЖ достигают кости, они создают перекрестные помехи в слаженной работе костных клеток. Раковые клетки врываются в добродетельный цикл и приводят к дисбалансу в сторону резорбции кости. В результате возникает порочный цикл (от англ. vicious cycle).
При определенных условиях раковые клетки отделяются от опухоли и становятся мигрирующими. Они интравазируют в соседние кровеносные сосуды и распространяются по организму, в кровотоке клетки могут попасть в ловушку и экстравазировать. При их выходе в подходящую ткань начинается рост вторичной опухоли.
Даже на ранних этапах РМЖ опухолевые клетки могут мигрировать в костный мозг. Они могут бездействовать долгое время и вызвать рецидив спустя годы .
Процесс ремоделирования костной ткани состоит из пяти основных этапов: покоя, активации, резорбции, реверсии, формирования (рис. 4). В каждом этапе участвуют разные типы клеток кости [15].
Рисунок 4. Ремоделирование кости. Состоит из пяти фаз: 1) фаза покоя — остеоциты неподвижны; 2) фаза активации — дифференцировка остеокластов из преостеокластов; 3) фаза резорбции — разрушение кости остеокластами; 4) фаза реверсии — дифференцировка остеобластов; 5) фаза формирования — остеобласты создают и минерализуют кость.
Межклеточный матрикс на 85–90% состоит из коллагеновых волокон, которые обеспечивают структурную поддержку минерализации кости. Остальная часть — это протеогликаны, карбоксилированные белки, клеточные адгезивные белки и факторы роста.
Остеобласты образуются из мезенхимных стволовых клеток. Во время своей работы они выделяют в костный матрикс смесь факторов роста и белков, образуя специфическую микросреду. Затем они подвергаются запланированной клеточной гибели или дифференцируются в остеоциты (рис. 5).
Рисунок 5. Схема дифференцировки остеобластов, остеоцитов. Остеобласты начинают дифференцироваться из мезенхимных стволовых клеток в костном мозге.
Остеобласты выделяют факторы роста кости, включая трансформирующий фактор роста β (TGF-β), инсулиноподобные факторы роста (IGF), факторы роста фибробластов (FGF), интерлейкины, тромбоцитарный фактор роста (PDFG). Эти факторы остаются внутри костного матрикса и высвобождаются после деградации кости. Этот процесс обеспечивает обратную связь между формированием и резорбцией кости [11].
Остеокласты — фагоциты для кости — дифференцируются из линии моноцитов/макрофагов (рис. 6). Активированные остеокласты собираются на поверхности кости и присоединяются к ней через специальные рецепторы. Они подкисляют микроокружение на границе кость—остеокласт и секретируют ферменты, участвующие в деградации: протеазы, коллагеназу и щелочную фосфатазу.
Рисунок 6. Схема дифференцировки остеокластов. Остеокласты — гигантские многоядерные клетки, дифференцируются из гемопоэтических стволовых клеток линии моноцитов/макрофагов костном мозге.
Развитие зрелых остеокластов — это многоступенчатый процесс, который регулируется сложной системой цитокинов и взаимодействием внутри стромы кости. Соседние стромальные клетки и остеобласты продуцируют колониестимулирующий фактор макрофагов (M-CSF), который действует через рецептор колониестимулирующего фактора 1 (c-FMS) на многоядерных предшественниках, и активируют экспрессию рецептора RANK (рис. 7). Его лиганд, RANKL, так же, как M-CSF, синтезируется остеобластами и стромальными клетками в ответ на действие паратиреоидного гормона (PTH). RANKL — цитокин из семейства факторов некроза опухоли. Связываясь со своим рецептором, он активирует ряд важных факторов, которые регулируют экспрессию генов остеокластов. Это создает условия для финальной дифференцировки, слияния предшественников и функционирования возникших многоядерных остеокластов. Активированные остеокласты разрушают кость и высвобождают TGF-β и другие факторы роста кости, усиливающие пролиферацию остеобластов [11].
Рисунок 7. Модель нормального костного ремоделирования. Кость постоянно реконструируется. Этот процесс требует взаимодействия костеобразующих остеобластов и костеразрушающих остеокластов. Подробности в тексте.
Остеобласты продуцируют остеопротегерин (OPG) — цитокин из семейства факторов некроза опухоли. Он связывается с RANKL, ингибируя взаимодействие RANK—RANKL, и, следовательно, подавляет остеокластогенез и резорбцию кости. Взаимодействие RANK—RANKL—OPG помогает поддерживать добродетельный цикл.
Переключение между добродетельным и порочным циклами связано с деятельностью раковых клеток. Они нарушают баланс костного микроокружения несколькими способами: стимулируют рост и устраняют физический барьер, то есть минерализованную костную матрицу (рис. 8).
Рисунок 8. Порочный цикл костного метастаза РМЖ. В костях клетки РМЖ секретируют факторы (фиолетовые стрелки), которые нарушают дифференцировку и активность остеобластов, увеличивают продукцию RANKL, усиливая образование остеокластов. На остеокласты они влияют и непосредственно. Зрелые остеокласты разрушают в кость, тем самым высвобождая внедренные в костный матрикс факторы роста. Они, попадая в опухолевое микроокружение, способствуют росту опухоли (красная стрелка). Тот же эффект дают факторы, выделяемые остеобластами и остеоцитами (синяя стрелка).
Традиционно костные метастазы делят на две категории: остеолитические и остеобластные. Остеолитические поражения чаще всего встречаются при РМЖ и характеризуются чрезмерной активацией остеокластов. При этом доминирующий процесс в кости — разрушение. Остеобластные поражения чаще встречаются при раке предстательной железы и характеризуются чрезмерной активацией остеобластов.
Однако в последние годы стало ясно, что разделение костных метастазов на чисто остеолитические или остеобластные неправильно, так как примерно у 20% пациентов с метастазами в кости, возникающими из опухолей молочной железы, поражение смешанное [18].
В этом обзоре мы более подробно рассмотрим механизм остеолитического поражения костной ткани.
В резорбции костной ткани участвуют остеокласты, деятельность которых находится под контролем целого ряда клеток костного мозга. Опухолевым клеткам необходимо препятствовать такому контролю и продуцировать собственные факторы, регулирующие активность остеокластов. Ключевым участником является TGF-β, который активирует рост опухоли и подавляет иммунную систему. TGF-β индуцирует синтез белка, связанного с паратиреоидным гормоном (PTHrP), и интерлейкина 11, которые стимулируют активацию остеокластов. В случае с PTHrP это обусловлено его способностью связываться с рецептором РТН и изменять соотношение RANKL/OPG в пользу RANKL [16].
Опухолевые клетки также продуцируют факторы, ингибирующие дифференцировку остеобластов, а значит, подавляют формирование костей [19].
Таким образом, при метастазировании РМЖ опухолевые клетки усиливают резорбцию кости путем прямого секретирования RANKL, что приводит к высвобождению биоактивных молекул. Эти продукты деградации вовлечены в регуляцию добродетельного цикла и стимулируют рост опухоли в случае развития метастаза в кости. Например, кальций — это первый продукт, выделяющийся при разрушении костного матрикса. Опухолевые клетки экспрессируют на своей поверхности кальций-чувствительные рецепторы, которые реагируют на повышение уровня кальция и стимулируют рост опухоли [20].
При метастазах РМЖ костная ткань резорбируется преимущественно собственными нормальными клетками. Прямая деградация костной ткани опухолью встречается редко. Метастатические клетки РМЖ способны продуцировать коллагеназу и другие ферменты, разрушающие кость [21], [22].
Остеобласты проходят сложный многоступенчатый процесс дифференцировки. Все клетки на разных стадиях дифференцировки играют определенную роль в добродетельном/порочном циклах.
Первый этап дифференцировки представлен преостеобластами, которые находятся в стенках гаверсовых и фолькмановских каналов. Для незрелых остеобластов характерна высокая производительность RANKL. При костных метастазах они могут стимулировать остеолиз [20], [21]. Некоторые источники сообщают, что RANKL может стимулировать пролиферацию вторичной опухоли РМЖ в кости [23], [24].
В присутствии раковых клеток преостеобласты усиливают производство провоспалительных цитокинов, таких как интерлейкин-6, моноцитарный хемотаксический белок, фактор некроза опухоли α, макрофагальный воспалительный белок 2 и др. Эти молекулы помогают поддерживать опухолевые клетки и также являются остеокластогенными.
Зрелые остеобласты, в отличие от преостеобластов, расположены на поверхности эндотелия. Во время формирования кости они выделяют биологически активные вещества, которые проявляют свою функцию только после высвобождения из разрушающейся костной матрицы. Среди этих молекул есть факторы, которые стимулируют рост опухоли и неоангиогенез — формирование новых микрососудов для питания опухоли [11]. В конце концов остеобласты дифференцируются в остеоциты или подвергаются апоптозу .
Гибель остеобластов — это не случайное событие, а строго регулируемый процесс, необходимый для обеспечения определенного размера и архитектуры кости. Метастазирующая опухоль РМЖ способна вызывать апоптоз остеобластов, продуцируя индукторы апоптоза [11]. Однако влияние апоптотических остеобластов на добродетельный и порочный циклы описано плохо.
Опухолевые клетки также могут выделять вещества, активирующие остеобласты. В настоящее время факторы, ответственные за этот процесс, не совсем ясны. Основная роль отводится эндотелину-1 (ЕТ-1). Этот фактор секретируется клетками РМЖ и рака предстательной железы и стимулирует возникновение остеобластных метастазов. В результате может начаться процесс ненормального костеобразования [26]. Кости быстро растут, становятся утолщенными, жесткими, негибкими.
Последний этап дифференцировки остеобластов представлен остеоцитами. Они локализованы в костном матриксе, что делает их идеальными регуляторами ремоделирования кости. Однако это же преимущество становится недостатком при развитии костных метастазов, поскольку они способны подпитывать порочный цикл.
Остеоциты — важные продуценты RANKL. Также они могут контролировать метастатический рост, секретируя факторы, некоторые из которых активируют пролиферацию раковых клеток молочной железы [16].
Пациент с костными метастазами испытывает мучительную сильную боль, у него повышается риск переломов, качество жизни катастрофически снижается. Терапия метастазов РМЖ в кости включает в себя различные методы, которые могут влиять как на саму опухоль, так и на ее микроокружение [11].
Чаще всего метастатический РМЖ возникает через несколько месяцев или лет после завершения лечения раннего рака. Риск возникновения вторичной опухоли после лечения РМЖ варьирует от человека к человеку. Но это сильно зависит от характеристики раковых клеток, стадии первичной опухоли, способов лечения. Например, в течение 15 лет вторичная опухоль в кости возникает у примерно 30% пациентов с HER2-позитивным и у 15% — с трижды негативным РМЖ [9].
Наиболее агрессивной вторичной опухолью считается метастатический трижды негативный РМЖ. Он часто поражает пациенток молодого возраста. С таким типом метастазов продолжительность жизни пациентов может не превысить и 6 месяцев [27].
В настоящее время метастатический РМЖ нельзя излечить. Однако это не означает, что его нельзя лечить. Терапия метастазов РМЖ в кости направлена на увеличение продолжительности и качества жизни. Современные методы лечения в США позволяют продлить жизнь 35% таких пациентов по меньшей мере на пять лет, а некоторые пациенты могут прожить 10 и более лет после постановки диагноза [27].
До начала лечения врач объясняет, какие поправки нужно внести в диету и образ жизни пациента. Во-первых, необходимо принимать достаточное количество кальция и витамина D, во-вторых, регулярно выполнять физические упражнения. Соблюдение этих правил позволит пациенту сохранить кости крепкими и минимизировать проявления остеопороза [28].
Тактику лечения врач определяет индивидуально для каждого пациента в зависимости от:
- типа и локализации первичной опухоли;
- количества и расположения вторичных опухолей в кости;
- наличия метастазов в других органах;
- возраста и общего состояния больного;
- предыдущего лечения;
- побочных эффектов.
В лечении костных метастазов можно выделить два основных подхода:
- системную терапию, которая направлена на лечение первичной опухоли;
- местную терапию, которая должна облегчить боли пациентов и уничтожить вторичную опухоль [27].
Системная терапия включает в себя гормональную терапию, химиотерапию и таргетную терапию.
Гормональная, или эндокринная, терапия — основной способ лечения пациентов с метастатическим РМЖ, положительным по эстрогеновым/прогестероновым рецепторам. Такой способ лечения подразумевает, что лекарственный препарат блокирует действие эстрогена или прогестерона либо снижает их концентрацию в организме. Это может замедлить рост и деление опухолевых клеток.
Существуют различные факторы, позволяющие определить, какой вид гормональной терапии подходит пациенту. К ним относится эффективность и безопасность доступных видов лечения, предшествующая терапия (в том числе гормональная), но в первую очередь — нахождение пациентки в пременопаузе или постменопаузе. Для женщин в пременопаузе гормональная терапия начинается с подавления функции яичников, чтобы остановить производство гормонов. В постменопаузе яичники уже не функционируют, и эстроген производится в жировой ткани и надпочечниках; в этом случае используют ингибиторы ароматаз [27].
Если первый препарат гормональной терапии перестает работать, то назначают второй, и т.д. В какой-то момент — может, через несколько месяцев или лет — гормональная терапия перестает вызывать ответ, и тогда рекомендуют переключиться на химиотерапию.
Побочные эффекты эндокринной терапии зависят от вида лечения и могут включать в себя мышечные боли, чувство усталости, легкую тошноту. К серьезным побочным эффектам относят повышение риска инсульта, рак матки, потерю прочности костей [29].
Химиотерапия — это первый этап лечения метастазов РМЖ, если первичная опухоль HER2-положительная и не имеет рецепторов к эстрогену/прогестерону. К химиотерапии обращаются и когда гормональная терапия перестает действовать [27].
Химиотерапевтические препараты, например 5-фторурацил, капецитабин или метотрексат, попадая в кровоток, разносятся по всему организму, уничтожая любые быстрорастущие клетки, в том числе и здоровые.
На выбор вида химиотерапии влияют агрессивность и быстрота роста раковых клеток, предшествующие варианты химиотерапии, побочные эффекты и т.д. [28].
Как и при гормональной терапии, если первый препарат или комбинация препаратов перестали действовать, и опухоль начинает расти, переходят на второй, третий и т.д. препараты. С каждым таким переходом шансов на уменьшение размеров опухоли становится всё меньше.
Побочные эффекты зависят от вида лекарства. К наиболее частым относят усталость, анемию, выпадение волос, тошноту и рвоту, а к самым серьезным — поражения сердца, легких, почек, вероятность возникновения другого вида рака. Пациентам могут назначать лекарственные средства, которые предотвращают или уменьшают выраженность побочных эффектов. Например, некоторые химиотерапевтические препараты повреждают ДНК, и для ее репарации и снижения вероятности возникновения устойчивости к химиотерапии назначают поли(AДФ-рибоза)-полимеразы (PARP) [28].
Таргетная, или молекулярно-таргетная, терапия — активно развивающееся направление лечения рака. Она блокирует рост раковых клеток за счет вмешательства в конкретный молекулярный механизм канцерогенеза.
Таргетная терапия используется как системный подход для лечения костных метастазов РМЖ. Она применяется либо в виде монотерапии, либо в сочетании с гормональной или химиотерапией.
Для лечения положительных по эстрогеновым/прогестероновым рецепторам и HER2-негативных метастазов РМЖ используют ингибиторы киназ CDK4 и CDK6. Ингибиторы CDK4/6 предназначены для прерывания роста опухолевых клеток. FDA одобрило три препарата на их основе: рибоциклиб, палбоциклиб, абемациклиб. Первый из них в начале 2018 года одобрил и Минздрав России.
Для увеличения эффективности эндокринной терапии положительных по гормональным рецепторам и HER2-негативных метастатических опухолей используют ингибиторы mTOR [27].
Для лечения HER2-позитивного метастатического рака активно применяют ингибиторы тирозинкиназы, такие как лапатиниб [27].
Многие таргетные методы лечения относятся к иммунотерапии. Иммунотерапия — это новейший, действенный и перспективный метод лечения многих форм рака. В последнее время ее применяют и для лечения костных метастазов.
Есть два способа действия: усиление иммунной системы, чтобы организм сам боролся с раком, и использование белков, уничтожающих раковые клетки. Иммунотерапия рака предполагает введение в организм противоопухолевых биопрепаратов: цитокинов, моноклональных антител или опухолевых вакцин. Ее используют и в системном, и в местном лечении вторичных опухолей при РМЖ.
Иммунотерапия в качестве системного подхода применяется в лечении HER2-позитивного РМЖ. Опухолевые клетки этого типа выставляют на своей поверхности большое количество рецепторного белка HER2, который важен для их роста. И для лечения используют антитела, которые блокируют внутриклеточные сигналы синтеза этого белка или вмешиваются в его работу. К таким моноклональным антителам относятся трастузумаб и пертузумаб [27].
Побочные эффекты таргетной терапии зависят от вида лекарственного средства. Однако для всех них типичны тошнота, рвота, диарея и слабость. К серьезным побочным эффектам можно отнести снижение сердечной функции и заболевания печени, например гепатит [28].
Местную, костно-таргетную терапию в сочетании с системной рекомендуют всем пациентам с костными метастазами РМЖ. К ней относят использование бисфосфонатов и деноcумаба, лучевую терапию и хирургические вмешательства. Выбор между этими видами лечения зависит от размера метастазов, осложнений, предпочтений пациента.
Бисфосфонаты — это стандартная терапия, используемая для уменьшения боли в костях, снижения темпов метастазирования, предотвращения потери костной массы и значительного улучшения качества жизни пациентов.
Рисунок 9. Формула бисфосфоната
Бисфосфонаты представляют собой молекулы, состоящие из двух фосфонатных групп, соединенных атомом углерода (рис. 9). Такая химическая конфигурация позволяет им с высокой степенью сродства связываться с гидроксиапатитной составляющей кости. Дополнительные функциональные группы, присоединенные к центральному атому углерода, придают бисфофонатам различные фармакологические свойства [7].
Бисфосфонаты вводят в организм перорально или путем инфузий. Основной механизм их действия заключается в ингибировании резорбции кости, поскольку после эндоцитоза они стимулируют апоптоз остеокластов. Это разрывает порочный круг сигналов между остеокластами и раковыми клетками в кости [16].
Применение бисфосфонатов может сопровождаться гриппоподобными симптомами и гипокальциемией. Эти препараты обладают выраженной нефротоксичностью и противопоказаны при низком клиренсе креатинина. Их применение, в особенности золедроновой кислоты, повышает риск остеонекроза челюстей.
У пациентов с метастатическим РМЖ радиотерапию используют как способ облегчения боли и профилактики осложнений [33].
Машина фокусирует ионизирующее излучение на метастазах в кости. Облучение, длящееся всего несколько минут, уничтожает раковые клетки.
Побочные эффекты зависят от облучаемого места. К наиболее распространенным последствиям лучевой терапии относятся раздражение кожи и чрезмерная утомляемость [28].
Для радиотерапии могут использоваться и так называемые радиофармацевтические препараты. Обычно это радиоизотопы щелочно-земельных металлов (стронций-89, самарий-153). Их можно избирательно доставлять прямо к метастазу. Во-первых, они могут самостоятельно накапливаться в зонах повреждения кости (как «имитаторы» кальция). Во-вторых, радиоизотопы можно конъюгировать с лигандами, обеспечивающими их направленную доставку в кость [29], [34]. В области костных метастазов исходящее от препарата излучение «убивает» рак.
Препарат усиливает местный эффект лучевой терапии, облегчает боль, иногда сокращает потребность в дальнейшей радиационной терапии.
К основным недостаткам использования радиоизотопов относится уменьшение содержания в крови тромбоцитов и лейкоцитов [28].
Хирургическое вмешательство у пациентов с метастазами в кости проводится редко. Основное показание для него — патологический перелом [7]. С помощью хирургии также можно стабилизировать слабую кость путем вставки винтов, стержней и т.д.
Рисунок 10. Механизм действия деносумаба. Высокоаффинное связывание деносумаба с RANKL ингибирует созревание и активность остеокластов, предотвращая взаимодействие RANKL с рецептором RANK на зрелых и незрелых остеокластах.
Иммунотерапией при местном лечении костных метастазов РМЖ можно назвать применение деноcумаба.
Деноcумаб — человеческое моноклональное антитело (IgG2), которое специфично связывается с RANKL. В результате не образуется связи RANKL—RANK (рис. 10). Лечение денозумабом предотвращает производство остеокластов и, следовательно, останавливает резорбцию кости [7].
На фоне применения деносумаба часто развиваются суставные и мышечные боли, гипокальциемия, инфекционные заболевания [35].
Сейчас ведется разработка средств для лечения метастатического рака молочной железы, нацеленных на новые мишени. Мишенями могут стать катепсин К, TGF-β, PTHrP, хемокиновые рецепторы и т.д. [30], [34]. Эти молекулы играют важную роль в порочном цикле, следовательно, воздействие на них может остановить рост вторичной опухоли или разрушение кости. Перспективным препаратом остается и деносумаб. Показано, что он улучшает минеральную плотность костей [20]. Однако из-за сложности механизмов костного метастазирования возникает необходимость комбинирования лекарственных препаратов, нацеленных на разные мишени.
Следующая задача состоит в том, чтобы разработать для каждого пациента индивидуальное лечение, предсказывая возможный клинический исход. Геномное и протеомное профилирование имеет прогностический потенциал, коррелирующий с прогрессированием заболевания. Такое профилирование может прогнозировать и исход лечения тем или иным препаратом. В будущем подобные технологии помогут отбирать пациентов, находящихся в группе риска возникновения метастатического РМЖ, и исключать ненужное лечение [20], [21].
Таким образом, РМЖ с метастазами в костях — это уже не приговор. Но, к сожалению, лечение такого рака — сложный, выматывающий процесс. Разумеется, говорить о 100% излечении пока невозможно. Однако использование стандартных терапевтических методов совместно с новыми подходами способно продлить жизнь пациентам и улучшить их состояние, то есть игра всё же стόит свеч.
Важно запомнить, что рак — это не паразит, который колонизирует и разрушает здоровые ткани. Это «умная» группа клеток, которая взаимодействует с нормальными клетками хозяина и использует важные тканевые сигналы ради собственного благополучия.
источник