Гормональная терапия является эффективным методом лечения гормональнозависимых опухолей молочной железы. Иногда ее называют антиэстрогеновой терапией, так как она направлена на предотвращение воздействия эстрогена на онкологические клетки.
В Москве на онкологических болезнях (в том числе и на раке молочной железы) специализируются врачи Юсуповской больницы. Это одно из лучших учреждений по оснащенности, высококвалифицированным врачам, ценовой политике, качеству оказываемых услуг и сервису, в котором процент положительного исхода лечения один из самых высоких в стране.
В большинстве случаев гормональная терапия оказывает эффективное действие, так как 75% всех опухолей, расположенных в молочных железах, имеют гормонзависимую природу. В зависимости от общего состояния пациентки, стадии заболевания, характера течения, распространенности, менопаузального статуса доктор подбирает оптимальную схему лечения. Ее нужно строго придерживаться, ведь только так можно достичь положительного результата.
Показаниями к назначению гормональной терапии являются:
- снижение вероятности возникновения рака у женщин, которые не страдают этим заболеванием, но находятся в зоне высокого риска;
- снижение риска рецидивов при неинвазивном раке;
- снижение вероятности рецидива или появления новых опухолей после оперативного вмешательства, химиотерапии и лучевой терапии;
- уменьшение размеров опухоли при инвазивном раке;
- метастатический рак.
Гормонотерапию часто называют «страховкой» после применения других методов лечения рака, так как операция, лучевая терапия и химиотерапия не могут дать 100% гарантию, что пациентка не заболеет вновь. Препараты гормонотерапии оказывают влияние на весь организм, подавляя действие эстрогена, и назначаются только в случаях гормонозависимых опухолей.
В Юсуповской больнице применяется только лучшее диагностическое оборудование от производителей с мировым именем, полный перечень лекарственных препаратов (антибиотики, химиопрепараты, гормональные таблетки и инъекции).
- адъювантная (профилактическая);
- неоадъювантная;
- лечебная.
Применяется как дополнительная терапия после оперативного вмешательства, химического облучения и лучевой терапии с целью профилактики рецидивов. Обычно такая терапия длится от 5 до 10 лет, при этом доктор назначает препараты ингибиторов ароматазы или тамоксифен.
Неоадъювантная терапия представляет собой комплексное лечение перед проведением оперативного вмешательства или лучевой терапией. Она применяется в следующих случаях:
- для уменьшения размеров опухоли и ее метастазов;
- для уменьшения объема хирургического вмешательства;
- для увеличения безрецидивной и общей выживаемости;
- для определения чувствительности опухоли к цитостатикам;
- для оценки новых способов лечения.
Такая терапия длится от 3 до 6 месяцев, хотя при положительном результате лечение продлевается.
Назначается пациенткам с неоперабельным раком и при генерализации. Также лечебную терапию назначают молодым женщинам с метастазами в печень или легкие, а также в период ремиссии.
Выбор лечения рака молочной железы зависит от многих факторов, среди которых:
- гормональный статус обнаруженной опухоли;
- менопаузальный статус женщины;
- стадия заболевания;
- применяемые ранее способы лечения;
- наличие сопутствующих соматических болезней;
- риск развития рецидива.
После применения неоадъювантной терапии у 80% пациенток опухоль уменьшается в размерах, а у 15% — отмечена полная морфологическая ремиссия.
Все виды терапии применяются в Юсуповской больнице. Врач, учитывая состояние пациентки, природу опухоли и стадию заболевания, подберет оптимальную схему лечения, которая поможет в эффективном лечении.
Гормонотерапию при раке молочной железы подбирают в зависимости от того, сохранен ли у женщины менструальный цикл. Так, пациенткам в пременопаузе (менструальный цикл постоянный) назначают:
- тамоксифен сроком на 5 лет (на ранних стадиях заболевания);
- операцию по удалению яичников;
- после удаления яичников или подавления их функции с помощью медикаментов назначают ингибиторы ароматазы.
Женщинам в период менопаузы (пациентка находится в климактерическом или постклимактерическом состоянии):
- назначают ингибиторы ароматазы после хирургического вмешательства, химической и лучевой терапии;
- если пациентка до менопаузы принимала тамоксифен, то его заменяют ингибиторами ароматазы;
- если женщина принимала тамоксифен на протяжении последних 5 лет, то его заменяют фемарой;
- если при лечении тамоксифеном была выявлена новая опухоль или рецидив, то вместо него назначают ингибиторы ароматазы;
- если в период приема ингибитора ароматазы выявлен рецидив, то его заменяют на тамоксифен, фаслодекс или назначают другой ингибитор ароматазы.
Опухоли по своей природе могут быть доброкачественными и злокачественными. Если опухоль доброкачественная, при этом существует риск ее перехода в рак, то единственным препаратом, который назначается таким пациенткам, является тамоксифен. Также он применяется при обнаружении протоковой карциномы in situ.
Женщинам с HER2-позитивным раком предпочтительнее назначать ингибиторы ароматазы. Также они назначаются, если тамоксифен оказался нерезультативным.
Относится к группе антиэстрогенов и препятствует соединению эстрогенов с раковыми клетками, что, соответственно, не дает последним увеличиваться. Его назначают женщинам на ранних стадиях заболевания и в период предменопаузы.
Одно из торговых названий этого препарата – Тамоксифен-Нолвадекс (в таблетках). У некоторых пациенток при их приеме отмечается сухость влагалища или, наоборот, чрезмерные выделения, усиленное потоотделение, покраснение кожи, увеличение веса.
Эти препараты блокируют выработку эстрогенов в организме женщины и назначаются пациенткам уже после наступления менопаузы. Как показывает практика, многим женщинам удалось преодолеть рак молочной железы благодаря приему одного из этой группы препаратов (аримидекс, фемара, аромазин). Каждый препарат назначается в определенных случаях:
- аримидекс – на ранних стадиях заболевания сразу после удаления опухоли;
- аромазин – на ранних стадиях рака тем женщинам, которые ранее несколько лет принимали тамоксифен;
- фемара – на ранних стадиях болезни после оперативного вмешательства пациенткам, которые принимали тамоксифен 5 и более лет.
У большинства женщин прием этих препаратов не вызывает никаких негативных симптомов, но некоторые отмечают тошноту, сухость во влагалище и боль в суставах. Также длительный прием ингибиторов ароматазы может стать причиной хрупкости костей, поэтому вместе с данными препаратами параллельно назначают кальций и витамин Д.
Этот препарат является аналогом природного ЛГРГ и применяется для подавления работы гипофиза. Он снижает количество гормонов, которые вырабатывают эстрогены, но при прекращении его приема гипофиз начинает работать в усиленном режиме. Поэтому врачи после нескольких месяцев приема золадекса рекомендуют операцию по удалению яичников (овариоэктомию) хирургическим способом или путем облучения.
Побочное действие препарата заключается в снижении полового влечения, покраснении, сильном потоотделении, головных болях, перепадах настроения. Золадекс вводят внутримышечно в нижнюю часть брюшной стенки 1 раз в месяц.
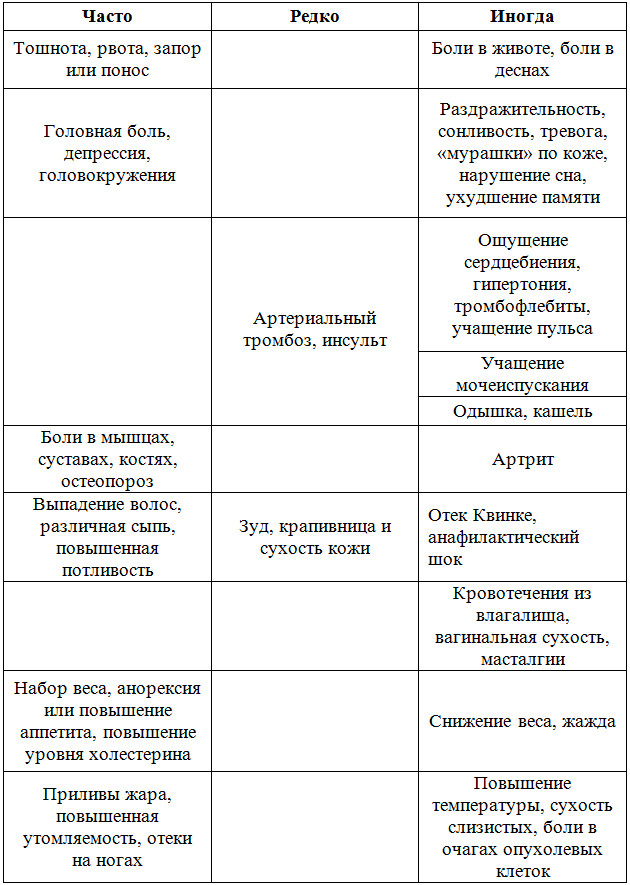
Несмотря не огромную пользу, гормонотерапия имеет ряд негативных последствий. Примерно половина женщин, которым назначается гормонотерапия при раке молочной железы, отмечают:
- увеличение массы тела;
- потливость;
- отечность;
- сухость влагалища;
- преждевременное наступление менопаузы;
- перепады настроения, депрессия.
Широко используемый препарат тамоксифен может стать причиной образования тромбов, рака матки и бесплодия. Препараты, которые направлены на снижение уровня эстрогенов (ингибиторы ароматазы), в некоторых случаях приводят к остеопорозу, повышению холестерина, заболеваниям ЖКТ. При появлении вышеперечисленных симптомов следует немедленно обратиться к доктору. Он сможет подобрать другие оптимальные лекарства.
С момента обнаружения опухоли в молочной железе женщине нужно пересмотреть свой рацион. Правильно подобранная диета позволит значительно улучшить общее самочувствие и снизить риск дальнейшего развития заболевания.
Питание при раке должно быть максимально сбалансированным, с большим количеством витаминов и микроэлементов. Кушать необходимо часто, но маленькими порциями, при этом придерживаться принципа раздельного питания.
Врачи Юсуповской больницы считают, что питание при гормонотерапии рака молочной железы должно быть именно таким:
- употреблять много ярко окрашенных овощей и фруктов (морковь, тыква, томаты, капуста, клюква, чеснок) и злаков (коричневый рис, пророщенная пшеница, отруби);
- калорийность рациона должна зависеть от веса пациентки: женщинам с лишним весом с помощью диеты нужно попытаться избавиться от лишних килограммов;
- уменьшить количество животных жиров в рационе и увеличить количество растительных;
- употреблять пищу, богатую кальцием и витамином Д;
- отказаться от продуктов, в состав которых входят фитоэстрогены;
- полностью исключить копченую, жареную, соленую, острую пищу и продукты с консервантами;
- ограничить количество сахара (в том числе и напитков с его содержанием);
- полностью отказаться от алкоголя, курения и наркотических средств;
- как можно меньше кушать красное мясо;
- обязательно добавить в рацион морскую рыбу, морепродукты, морскую капусту;
- ежедневно употреблять 1-2 порции молочных продуктов;
- пить как можно больше сырой воды (не менее 2-2,5 л в день), зеленого чая и отваров из травяных сборов.
В Юсуповской больнице есть все необходимое оборудование для диагностики и лечения заболевания, а при выявлении образования в молочной железе в лаборатории можно сделать анализ на определение его природы.
Важно заметить, что каждая женщина в возрасте после 35 лет должна раз в год посещать маммолога чтобы исключить вероятность патологических образований в груди. Это можно сделать в Юсуповской больнице, которая находится по адресу: 117186, г. Москва, ул. Нагорная, д.17, корп.6, предварительно записавшись на прием.
источник
Под химиотерапией (ХТ) предполагается применение лекарственных средств, непосредственно убивающих раковые клетки, это разные виды цитостатиков, преимущественно вводимых инъекционно — внутривенно. Эти лекарства обладают высокой токсичностью, поскольку уничтожают любые клетки, но в первую очередь, злокачественные.
Гормонотерапия (ГТ) базируется на прекращении поступления в раковую клетку необходимых ей гормональных средств, в результате чего нарушаются процессы роста и деления, что приводит к её гибели. Гормональное воздействие значительно менее агрессивное, но требует постоянного многолетнего приёма таблеток для создания определённого гормонального фона, не позволяющего роста и размножения раковых клеток.
Выбор лекарственного лечения при раке молочной железы зависит:
- от распространения опухоли на время выявления, то есть размера новообразования в молочной железе и количества раковых лимфатических узлов в подмышечной области, а также наличия метастазов в других органах;
- чувствительности опухолевых клеток к гормональным препаратам, что определяется по наличию рецепторов гормонов, положительными считаются клетки от 1% рецепторов;
- маркёра чувствительности рака к лекарственным препаратам, что показывает ген множественной лекарственной резистентности HER2, которого много — гиперэкспрессия или в геноме встроено множество его копий — амплификация.
Есть дополнительные факторы, показывающую высокую агрессивность рака — Ki67 и определение 21 гена, но они не используются для выбора вида лекарственного лечения: химиопрепаратов или антигормонов. Если в раковых клетках нет рецепторов гормонов, то гормональное воздействие будет безрезультатным, поэтому для терапии выбираются химиотерапевтические препараты.
Недавно стали выделять четыре биологических подтипа рака.
Если клетки содержат гормональные рецепторы, то это люминальный подтип. Вариант «А» наиболее благоприятный, при нём уровень эстрогеновых (ЭР) и прогестиновых рецепторов (ПР) достаточно высокий, при варианте «В» прогестероновых рецепторов нет. Считается, что ПР говорят о чувствительности ЭР, то есть предполагают хорошую реакцию на антигормональное воздействие. Как правило, при люминальном варианте гена HER2 не определяется, что тоже говорит об ожидаемой пользе лекарств.
К базальному подтипу относят новообразования без рецепторов и HER2, его иногда именуют трижды негативный, такой вариант однозначно не реагирует на гормональные средства, поэтому применяются цитостатики.
Биологический подтип рака без гормональных рецепторов, но с наличием гена лекарственной устойчивости HER2 относят к нелюминальному или с гиперэкспрессией HER2. Он плохо реагирует на лекарства, поэтому к химиотерапии добавляется специальный препарат, подавляющий ген HER2.
- Практически при всех стадиях рака молочной железы, кроме самой минимальной, для уменьшения вероятности возврата болезни предполагается дополнительное послеоперационное лечение — адъювантная лекарственная терапия.
- При значительном поражении молочной железы для улучшения результатов операции применяется дооперационное лекарственное — неоадъювантное воздействие, что позволяет уменьшить раковый узел, выявить чувствительность клеточной популяции к конкретным лекарствам и даже избежать послеоперационной профилактики.
- При неоперабельной — генерализованной стадии процесса на первом этапе химиотерапевтическое воздействие неизбежно.
Цитостатические препараты назначаются при высокой агрессивности РМЖ и незначительной зависимости клеток от гормонов. Формально, уже 1% ЭР и ПР предполагает реакцию на эндокринное воздействие, но особо выраженного результата от ГТ ждать не приходится.
При люминальном подтипе преимущества на стороне воздействия гормонами, но при высоком пролиферативном потенциале — Ki67 больше 20% и высоком риске рецидива по анализу 21 гена, что встречается при люминальном В, показана и химиотерапия. Базальный и нелюминальный молекулярные варианта лечатся цитостатиками.
Клинический пример:
Пациентка 54 года, работает профессором высшей математики и теоретической механики в столичном ВУЗе. Во время плановой маммографии было выявлена одиночная опухоль диаметром 2,5 см. Заподозрен рак молочной железы. После биопсии диагноз был уточнен: «Тройной негативный рак молочной железы, стадия 2». Существует несколько научных школ: европейская — «давайте сначала прооперируем, потом будем проводить химиотерапию»; альтернативное мнение американской школы онкологии со ссылкой на американские guidelines «давайте сделаем химиотерапию, а потом решим оперировать ли и в каком объеме». В результате попыток на протяжении 3 месяцев самостоятельно проанализировать рекомендации клинической онкологии, посещения еще врачей, и неоднократные обследования, в результате развития опухолевого процесса рак из стадии 2 перешел в стадию 4: при сцинтиграфии выявлено поражение костей, одиночные метастазы в печень.
Комментарий и рекомендации врача-онколога, маммолога к.м.н. Д.А.Шаповалова:
Пациентка обошла в течение 3 месяцев врачей, чтобы сделать правильный выбор. Но выбора она себе не оставила. Потеряны годы жизни. Ее прогноз крайне неутешительный. Предполагаемая продолжительность жизни согласно статистическим данным — менее 2 лет, вместо 10-15, которые были бы при начале активной терапии в момент первичной диагностики.
Во всех случаях, когда предполагается использовании ХТ и гормонотерапии, начинают с цитостатиков и вместе с гормонами их не используют, поскольку эндокринное воздействие снижает чувствительность клеток к лекарствам. Лучевая терапия тоже проводится после завершения ХТ, не противопоказан параллельный прием гормональных лекарств.
Курсы лечения начинаются через 3–4 недели после операции, но при хорошем заживлении раны можно начинать ХТ и раньше, а отсрочка может неблагоприятно сказаться в дальнейшем.
Стандартно проводится не менее 4 курсов ХТ, если требуется препарат, подавляющие ген HER2, то его вводят каждые три недели целый год или 17 раз.
Дооперационное лекарственное воздействие возможно тогда, когда нет сомнений в проведении и обязательности профилактики рецидива рака, то есть при всех стадиях, кроме I и не операбельного рака молочной железы IV стадии — с метастазами.
Лечение лекарствами до операции выявит истинную чувствительность рака к выбранным лекарствам, что невозможно при адъювантном лечении. При стандартной профилактике опухоли уже нет, хоть лекарственная комбинация выбирается из оптимальных по сочетанию результата и осложнений, но индивидуальная реакция не прогнозируема. Соответственно, нечувствительность рака к лекарствам до операции позволит отказаться от лекарственной профилактики после хирургического этапа.
Если неоадъювантные циклы приведут к регрессии новообразования, то можно отказаться от мастэктомии в пользу сохраняющей молочную железу операции.
При люминальном, А варианте РМЖ неоадъювантная химиотерапия мало изменяет благоприятный прогноз болезни, поэтому не практикуется. При всех остальных подтипах уменьшение ракового узла, тем более полное его исчезновение, позитивно сказывается на дальнейшем течении заболевания.
Клинический пример:
Пациентка М., 40 лет, работает воспитателем в детском дошкольном учреждении. За неделю до обращения в клинику самостоятельно обнаружила уплотнение в молочной железы, с измененной кожей над уплотнением в виде «лимонной корки». На основе отзывов и рекомендаций записалась на прием к Шаповалову Д.А., хирургу онкологу, к.м.н., заведующему хирургическим отделением клиники «Медицина 24/7». На основании данных анамнеза и первичной диагностики, пациентке было рекомендовано проведение полихимиотерапии после проведения core-биопсии с иммуногистохимическим исследованием. Пациентка была удивлена, что врач отказал в первичном проведении операции.
Комментарий и рекомендации врача-онколога, Д.А.Шаповалова:
В данном случае имеется классический вариант отечно-инфильтративной формы рака молочной железы IIIа/b/c стадии, что согласно рекомендаций NCCN, ESMO и ASCO требует на первом этапе ОБЯЗАТЕЛЬНОГО (!) проведения лекарственного противоопухолевого лечения — комбинации полихимиотерапии и таргетной терапии. При наиболее частой форме, собственно выявленной у пациентки, люминальном B-варианте были назначены согласно «золотого стандарта» по схеме Dose-Dance препараты AC-T в количестве 4+4 курсов. Невзирая на настоятельные требования пациентки начать лечение в день обращения, начало лечение было отложено до получения результатов определения Ki67 (5 рабочих дней), составивших 75% (агрессивная быстро делящаяся опухоль). От схемы СAF отказались, учитывая молодой возраст пациентки.
Через 2 курса от начала лечения была произведена клиническая оценка результата — отечность уменьшилась, опухолевый узел уменьшился по данным УЗИ. Лечение было продолжено.
Перед операцией используются аналогичные профилактическим комбинации, при положительном гене HER2 лечение обязательно, причём не менее 9 введений.
Если из 4 стандартных курсов провели только 2, то оставшиеся 2 надо доделать после удаления железы. После операции проводится столько курсов, сколько не удалось сделать до «полного счёта».
Рак молочной железы III стадии радикально сомнительно удалим даже с мастэктомией, его считают местно-распространенным, подлежащим комбинированному подходу, то есть с участием всех методов противоопухолевого лечения: лекарственного, лучевого и хирургического. Главная задача ХТ — уменьшить размер раковых узлов.
Разумеется, в этом случае химиотерапия до операции — неизбежность, а дальнейшее зависит от результата полноценной цикловой ХТ с соблюдением межкурсовых интервалов и доз лекарств.
Уменьшение узла в молочной железе в результате стандартного числа курсов приводит к операции и облучению.
Когда новообразование не среагировало на ХТ, меняется комбинация цитостатиков и при хорошем эффекте после завершения прибегают к удалению с последующим облучением.
Если после замены лекарств результата нет, проводится лучевая и только после неё операция.
Нужна ли профилактическая ХТ после удаления молочной железы, определяется индивидуально.
источник
Молочная железа – гормонально-зависимый орган: на рост и деление ее клеток оказывают влияние эстрогены, прогестерон и пролактин, причем каждый это делает по-разному. Рак груди – это участок, в котором клетки мутировали, то есть видоизменились (и чем сильнее, тем более злокачественна опухоль), приобрели способность быстро делиться, вытесняя нормальные клетки.
Причины такого явления до сих пор до конца не изучены. Одни ученые считают «виновниками» вирусы, другие – наличием определенных генов, третьи – продуктами жизнедеятельности живущих в организме паразитов. Тем не менее, если в таких мутировавших клетках сохранились рецепторы к половым гормонам, воздействие на них гормональными средствами будет уничтожать раковую опухоль. Такое воздействие является гормонотерапией при раке молочной железы.
Лекарства, используемые с терапевтической целью – это не гормоны, но вещества, блокирующие их действие на опухоль, таким образом не дающие ей расти. Они не используются сами по себе, но эффективны в сочетании с хирургическим удалением ракового новообразования, лучевой терапией и химиотерапией.
Лекарства, блокирующие гормональные рецепторы, дают хорошие результаты не исключительно в терапии маммарной карциномы, но и эффективно предупреждают развитие рецидивов и метастазов данной злокачественного образования.
Гормонотерапия, в случае рака груди, и заместительная гормонотерапия после лечения рака молочной железы – абсолютно разные понятия. В первом случае опухолевые клетки уничтожаются препаратами, включающимися в процесс синтеза половых гормонов, в результате чего выключается стимулирующее действие эстрогенов на рост опухоли. Заместительная же гормонотерапия после лечения патологии – это введение в организм женщины синтетических гормонов, которые будут замещать те, которые исчезли в результате лечения раковой опухоли (особенно если для подавления роста образования было применено хирургическое удаление яичников).
У женщины в крови постоянно имеются гормоны:
p, blockquote 9,0,0,0,0 —>
- 5 видов эстрогенов;
- 3 вида прогестеронов.
Их уровень различен в разные дни цикла, а при климаксе объем данных гормонов значительно снижается, так как яичники – основной «производитель» этих веществ – «отключается» по физиологическим причинам, остаются только эстрогены, синтезируемые надпочечниками и жировой тканью.
Женские гормоны связываются как «ключ с замком» со специальными структурами, рецепторами, на поверхности нужных клеток. «Замок» отворяется, пуская гормон внутрь, а дальше он вступает в реакцию с ядром клетки, и так регулирует ее размножение, рост и гибель. Максимальное число рецепторов находится в жировой ткани, яичниках и молочной железе.
Раковая опухоль, появляясь в молочной железе, строится из клеток, которые должны были быть нормальными, но видоизменились в процессе деления и не были уничтожены иммунной системой. Многие из них трансформировались не полностью, и рецепторы к эстрогенам и прогестеронам в них сохранились. Попадая к таким клеткам, обычные женские гормоны вызывают их усиленное деление с последующим попаданием в лимфу и кровь (метастазирование).
Таким образом, если у женщины обнаружен рак груди, и эта опухоль имеет рецепторы к половым гормонам (что чаще всего наблюдается после менопаузы), у врачей появляется дополнительный путь воздействия на нее: отключив механизм доставки гормона к опухолевым клеткам, подавить ее рост. Это не химиотерапия и не облучение злокачественного новообразования, которое может воздействовать только на делящуюся клетку. Здесь – другой путь: отключить возможность делиться у всех раковых клеток.
Гормональная терапия при раке молочной железы показана в том случае, если патологическое образование будет чувствительно к гормонам. Для определения чувствительности проводится иммуногистохимическое исследование клеток биопсийного материала, взятого у пациентки при биопсии. По результатам исследования в 65-75% паталогические клетки чувствительны как к эстрогенам, так и к прогестеронам, в 10% — только к прогестеронам.
Понять, что здесь нужна гормональная терапия, можно по заключению, выданному иммуногистохимической лабораторией:
p, blockquote 17,0,0,0,0 —>
- если написано «ER+/ PR +», это значит, что есть и эстрогеновые, и прогестероновые рецепторы, и назначенное гормональное лечение рака молочной железы располагает 70% шансом победить опухоль;
- «ER+/ PR -» или «ER-/ PR+», то есть наличие только одного типа рецепторов прогнозирует успех только в 33% случаев;
- когда написано, что «гормональный статус не известен», это означает, что на пути от забора клеточного материала из опухоли до лаборатории произошло его повреждение, нарушение правил транспортировки или хранения. Такие же слова лаборант напишет, если клеток слишком мало для проведения с ними иммуногистохимических реакций;
- заключение «гормоно-негативная» (оно обычно бывает в 25% случаев) означает, что в раковой опухоли рецепторов слишком мало.
В последних двух случаях гормонотерапия не проводится, так как ее прогнозируемая эффективность крайне низкая.
Обнаружение эстроген- или прогестин-позитивности в раковой опухоли – означает, что после ее хирургического удаления, чтобы возможно оставшиеся раковые клетки перестали делиться и через время отмерли, нужно применить гормонотерапию. Также подобное лечение можно применить и до вмешательства – чтобы снизить размер патологии и профилактировать ее метастазирования. Если злокачественное новообразование груди обнаружено на той стадии, когда операцию провести уже нельзя, гормонотерапия нужна для продления жизни пациентам.
Данный вид лечения используется при эстроген-положительных раках молочной железы в случаях:
p, blockquote 21,0,0,0,0 —>
- если у близких родственников отмечались злокачественные образования груди, а теперь и у женщины самой выявлен дефектный рост клеток органа;
- большие размеры опухоли;
- 0 стадия рака;
- рак имеет тенденцию к прорастанию в соседние ткани, нервы и сосуды;
- имеются метастазы;
- после лечения химио или лучевой терапией, а также после оперативного вмешательства – для профилактики рецидива.
Узнайте больше о раке молочной железы, его видах и методах лечения, перейдя по ссылке.
В зависимости от целей назначения, гормонотерапия может быть:
p, blockquote 25,0,0,0,0 —>
- Адъювантной. Она применяется по окончании операции, для профилактирования рецидива и метастазирования.
- Неоадъювантной. Проводится перед операцией, в основном, при 3 фазе рака и когда есть метастазы в лимфоузлы. Большинство пациенток, которым проводят такую терапию, находится в постменопаузе.
- Лечебной. Она применяется у неоперабельных пациенток, чтобы, остановив рост новообразования, продлить жизнь.
Препараты подбираются в зависимости от нескольких факторов:
p, blockquote 26,0,0,0,0 —>
- стадии раковой опухоли;
- того, находится женщина в менопаузе или нет;
- есть ли сопутствующие заболевания, которые усугубятся при снижении уровня (или блокаде) эстрогенов: остеопороз, артрит, тромбоз.
Сколько будет длиться гормонотерапия, зависит от вида выбранного препарата, его эффективности и переносимости.
Если блокаторы действия эстрогенов и прогестинов вызывают значительные побочные эффекты, в некоторых случаях может проводиться удаление яичников – хирургическое или лучевое. Это останавливает рост ракового новообразования за счет уменьшения выработки половых гормонов. После резекции яичников – для предупреждения рецидива рака молочной железы – назначаются уже не блокаторы эстрогенов или прогестеронов, а гормоны:
p, blockquote 28,0,0,0,0 —>
- андрогены (мужские гормоны) – чтобы гипофиз не стимулировал появление новых фолликулов в несуществующих уже яичниках;
- кортикостероиды (дексаметазон, преднизолон) – для выключения выработки эстрогенов надпочечниками;
- эстрогены – чтобы выключить функцию яичников и подавить выделение гипофизом тех веществ, которые направлены на стимуляцию яичников;
- эстрогены совместно с кортикостероидами нужны для угнетения надпочечниковой и гипофизарной стимуляции яичников, которые уже удалены.
По механизму действия, лекарства подразделяются на:
p, blockquote 31,0,0,0,0 —>
- Снижающие уровень в организме эстрогена.
- Останавливающие соединение женских гормонов с рецепторами клеток опухоли.
Модуляторы рецепторов к эстрогенам
До 2005 года гормонотерапию проводили только модулятором эстрогеновых рецепторов – Тамоксифеном. Этот препарат прочно связывается с рецепторами к эстрогену, не давая гормону попасть к ним. Он очень хорошо изучен, и именно этим объясняются описанные побочные эффекты гормонотерапии при раке молочной железы. Получается, другие антиэстрогеновые средства могут переноситься не лучше, просто они еще не так глубоко исследованы.
Другие препараты этой группы – Ралоксифен и Торемифен. Они также широко используются, к тому же не повышают риска формирования рака печени или карциномы эндометрия, как Тамоксифен.
Блокаторы эстрогеновых рецепторов
Препараты данной группы, например, Фаслодекс, разрушает эстррогеновые рецепторы опухоли.
Ингибиторы ароматазы
В основном, в постменопаузе, эстрогены образуются в жировой, мышечной, печеночной и надпочечниковой тканях из мужских гормонов. Происходят эти реакции под действием фермента ароматазы. Соответственно, если этот фермент «отключить», андрогены прекратят трансформироваться в эстрогены, а рак груди перестанет получать стимуляцию расти и делиться.
Эти средства сейчас признаны наиболее эффективными для лечения рака молочной железы на любых стадиях. К тому же, у них меньше побочных симптомов, чем у блокаторов эстрогенов.
Препаратом этой группы последнего поколения является Летрозол. Он связывается с геном одной из субъединиц ароматазы, которая превращает андрогенов в эстрогены, также ингибируя синтез эстрогенов в тканях.
Если препараты первых трех групп неэффективны, для проведения гормонотерапии назначаются прогестины. Они уменьшают секрецию тех гормонов гипофиза, которые «командуют» выработкой андрогенов и эстрогенов. Также прогестагены блокируют превращение эстрогенов из андрогенов внутри печеночной ткани.
Данные препараты обладают побочными эффектами: повышение давления, синдром Кушинга, кровотечения из влагалища.
Можно отметить такие основные последствия гормонотерапии при раке молочной железы:
p, blockquote 46,0,0,0,0 —> p, blockquote 47,0,0,0,1 —>
Несмотря на возможные осложнения, назначенное лечение принимать обязательно – оно продлевает жизнь.
источник
Как правильно подобрать схему химиотерапии при онкологии молочной железы? Где лучше проводить химиотерапию — в России или за рубежом? Каков порядок прохождения лечения в Европейской клинике?
Химиотерапевтическое лечение рака молочной железы — один из методов комплексного лечения. Его суть состоит в назначении пациентам цитостатических препаратов, тормозящих развитие опухоли и разрушающих опухолевые клетки в молочной железе. Химиотерапия при раке молочной железы может использоваться как самостоятельный метод, а также как перед хирургической операцией, так и после операции. В этих случаях химиотерапия преследует различные цели.
При использовании химиотерапии в ходе подготовки к хирургическому лечению рака молочной железы цитостатические препараты способствуют уменьшению опухоли, что позволяет максимально сохранить здоровые ткани молочной железы. Послеоперационная химиотерапия помогает остановить метастазирование и предотвратить рецидив заболевания.
Протоколы химиотерапии при различных вариантах течения рака молочной железы разработаны и утверждены в качестве стандартов ведущими научными онкологическими сообществами — NCCN, ESMO, ASCO.
Молекулярный анализ опухоли молочной железы — новый этап в современном лечении особо агрессивных опухолей. Мы предоставляем возможность проведения анализа опухоли на чувствительность к препаратам химиотерапии. На основании отчета о проведенном исследовании мы получаем очень эффективный план борьбы с опухолью, дающий максимально благоприятный шанс на выздоровление.
Химиотерапия рака молочной железы в Европейской клинике выполняется с использованием различных схем лекарственной терапии, в том числе рекомендованных пациентам во время их консультаций или первичного лечения в странах Западной Европы, преимущественно Германии, Швейцарии и Италии, а также Израиля.
Рак молочной железы чувствителен ко многим препаратам: герцептин, авастин, метотрексат, адрибластин, 5-фторурацил, циклофосфан, доцетаксел, паклитаксел, кселода и ряд других. В соответствии с протоколами, нами используются следующие схемы лечения рака молочной железы: CMF (Циклофосфан, Метотрексат, Фторурацил), FAC (Фторурацил, Адриабластин, Циклофосфан), CAF (Циклофосфан, Адриабластин, Фторурацил), а также схемы с таксанами (Доцетаксел, Паклитаксел).
Химиотерапия имеет целью убийство клеток злокачественной опухоли не только груди, но и любого другого органа. Конечный результат лекарственного воздействия — запрограммированная клеточная смерть или апоптоз, достигается он несколькими способами и при разной исходной чувствительности опухоли к лекарству. В большинстве случаев рак молочной железы весьма чувствителен к большинству специальных лекарств — цитостатиков. В клинической практике используется несколько групп лекарственных препаратов, потому что каждый цитостатик своим путем приводит раковую клетку к смерти.
Представители группы антиметаболитов нарушают нормальную клеточную жизнь, подменяя участвующие в биохимических реакциях естественные вещества их синтетическим подобием. В схемах химиотерапии при раке молочной железы используются антиметаболиты метотрексат и фторурацил. Часто употребляемые при онкологии груди алкилирующие цитостатики портят ДНК, образуя поперечные сшивки между её цепочками. В большинство схем ХТ вводят один из самых старых препаратов циклофосфан.
Противоопухолевые антибиотики не лечат воспаление, как и алкилирующие, они манипулируют с клеточной ДНК, но несколько по-другому повреждая её. Один самых результативных при раке молочной железы препаратов — доксорубицин пациентки часто называют «красной химиотерапией». Ещё один представитель «красных» — противоопухолевый антибиотик эпирубицин, меньше повреждающий сердечную мышцу, входит во множество комбинаций. Когда-то выделенные из растений, а теперь химически синтезируемые, растительные алкалоиды мешают сборке клеточных структур, что вынуждает к включению механизма апоптоза. Сегодня паклитаксел, доцетаксел и винорельбин считаются лидерами противоракового воздействия.
В некоторых клинических ситуациях для повышения эффективности химиопрепараты сочетают с таргетными средствами, например, с герцептином или бевацизумабом. Но вместе с гормональными препаратами не используют, так как результат лечения ухудшается. Схема ХТ составляется из лекарств разнонаправленного механизма из нескольких групп, но стараются не комбинировать цитостатики с одинаковым побочным действием. В последнее время редко одновременно применяется более одного двух лекарств, потому что эффективность, в отличие от токсичности, не увеличивается.
Предлагаем ознакомиться с нашим материалом, рассказывающим о влиянии химиотерапии на беременность
Ключевых факторов в успехе химиотерапии рака молочной железы два. Во-первых, максимально раннее выявление патологических изменений, поскольку упустить время при раке молочной железы из-за его быстрого прогрессирования очень легко. Во-вторых, обязательное проведение тестов на чувствительность опухоли к гормональным препаратам (наличие рецепторов к эстрогенам и прогестерону), включая FISH-тест.
Правильно подобранная схема химиотерапии позволяет в большинстве случаев существенно улучшить качество жизни даже в запущенных ситуациях, и у многих пациентов продлить жизнь, а при сочетании с хирургическим лечением и лучевой терапией даже добиться длительного излечения рака молочной железы.
Злокачественные новообразования разного строения по-разному реагируют на лекарства, рак груди довольно чувствителен к цитостатикам, а саркома неважно реагирует на химиотерапию. В клинических исследованиях нашли достоверные критерии ответа злокачественной опухоли на цитостатическую терапию. Главные показатели чувствительности к ХТ — уровень гормональных рецепторов в опухоли и наличие гена HER2, манифестирующего устойчивость к лекарствам. А размер новообразования не указывает на чувствительность рака к лекарствам, правда, при большой опухоли курсов сделают больше.
Рак одной морфологической структуры имеет ещё и индивидуальные характеристики, которые не научились распознавать, но зато можно определить чувствительность клеток рака к конкретному лекарственному препарату. Генетическое картирование опухоли позволит избежать бесполезной для женщины ХТ.
Европейская клиника использует общепринятый в Европе формат химиотерапевтического лечения при раке молочной железы. Это лечение в условиях дневного стационара, когда пациентка может приехать в клинику на 2-3 часа перед работой или в конце рабочего дня и пройти сеанс химиотерапии. Эта процедура проводится в большом зале химиотерапии или в специальной одноместной палате под наблюдением дежурного врача реаниматолога и специально обученной медицинской сестры.
Если лечение не осложняется отсроченной рвотой, развивающейся после окончания действия введённых перед ХТ противорвотных средств, то амбулаторное лечение разумно. Обычно отсроченная рвота начинается поздним вечером, и в этой ситуации не способны помочь родственники, не владеющие методикой внутривенных инъекций, а приём таблеток физически невозможен. После первого эпизода мучений женщина начинает бояться лечения, что приводит к развитию психогенной рвотной реакции, когда от одной мысли в любое время начинается тошнота. Кратковременная госпитализация, буквально на сутки двое, позволит вводить противорвотные профилактически — до появления неприятных симптомов, а капельные вливания специальных растворов и индивидуальная нутритивная поддержка уменьшат негативные реакции на цитостатики.
При использовании ряда схем может потребоваться суточная госпитализация или контролируемое введение препарата в течение 46 часов. В этом случае мы предлагаем размещение в условиях комфортабельного стационара в одно- и двухместных палатах.
В палатах имеются электрические функциональные кровати с противопролежневыми матрацами, установлены телевизоры со спутниковым телевидением и DVD, имеются все необходимые индивидуальные санитарные удобства. Во всех палатах установлены палатная сигнализация с кнопками вызова дежурной медицинской сестры у кровати пациента и в санузле. В палаты подается специально очищенный с помощью антибактериальных фильтров воздух.
В клинике имеется собственная библиотека и фильмотека. Пациенты обеспечиваются 3-х-5-ти разовым индивидуальным питанием. Все это в сочетании с профессионализмом врачей и и круглосуточным медицинским сестринским уходом способствуют комфорту и спокойствию пациентов.
Сама процедура введения химиотерапевтических препаратов может проводиться как с использованием классических систем для переливания, так и с применением электронных дозаторов — инфузоматов и перфузоров. Они позволяют максимально точно контролировать скорость и продолжительность введения препаратов химиотерапии.
Индивидуальный подбор схемы лечения проводится врачом онкологом химиотерапевтом на основании результатов комплексного обследования. При наличии медицинских показаний к проведению нескольких курсов химиотерапии, мы настоятельно рекомендуем пациенткам постановку специальных систем для введения химиопрепаратов, так называемых портов.
В Европейской клинике качество препаратов, их дозировка, последовательность введения, строго соответствует Европейским протоколам химиотерапии. В протоколы лечения включены только оригинальные лекарственные препараты производства ведущих западных фармацевтических компаний. Так называемые дженерики в нашей практике практически не используются.
В нашей клинике проводится комплексное химиотерапевтическое лечение под контролем параметров гомеостаза и показателей крови, что позволяет точно контролировать продолжительность и скорость введения препарата, а также общую длительность и число курсов лечения. При необходимости мы проводим переливание крови соответствующей группы и препаратов крови – плазмы, тромбоконцентрата и других
Принципиально выделяют 2 вида химиотерапии рака молочной железы — адъювантную (и неоадъювантную) при оперативных вмешательствах и лечебную химиотерапию при генерализованных формах. Кроме того, часто используется термин «индукционная химиотерапия».
Химиотерапия может назначаться до операции – неоадъювантная химиотерапия. Химиотерапия после удаления молочной железы или её части по поводу рака называется адъювантной, синоним вспомогательная (дополнительная или профилактическая химиотерапия) проводится при операбельном раке молочной железы.
Весомым преимуществом неоадъювантной химиотерапии является уменьшением размеров удаляемого злокачественного образования и формирование четкой границы опухолевой и здоровой ткани за счет частичной гибели опухолевых клеток на фоне химиотерапии. Кроме того, целью неоадъювантной химиотерапии является уничтожение микро метастазов, что в большинстве случаев улучшает условия операбельности опухоли и увеличивает выживаемость пациенток. Одним из преимуществ неоадъювантной химиотерапии является возможность на основе реакции опухоли (её уменьшения в размерах) распознать, правильно ли выбран применяемый для данной опухоли курс химиотерапии.
Недостатком неоадъювантной химиотерапии является затягивание оперативного вмешательства, трудности при определении гистологического типа опухоли, сложности при определении рецепторов к эстрогенам и прогестерону после проведения нескольких курсов химиотерапии.
Стандарты предписывают обязательную химиотерапию при раке молочной железы после операции или длительное гормональное воздействие, избежать этого можно только при благоприятном варианте крошечного рака. Этот вид ХТ называется адъювантной или профилактической, он направлен на уничтожение микроскопических очагов рака в зоне операции и циркулирующих в крови и лимфе злокачественных клеток. Клинические исследования показали, что после такого лекарственного воздействия вероятность развития метастазов ниже, а продолжительность жизни выше.
Лечебная химиотерапия проводится в случае генерализованного рака молочной железы (при наличии отдаленных метастазов, выраженного местного распространения). Целью этого вида химиотерапии является уменьшение размеров метастатических опухолей и повышения качества жизни и увеличение продолжительности предстоящей жизни.
Индукционная химиотерапия проводится при местно-распространенном раке молочной железы, который не является операбельным из-за больших размеров образования и отсутствия четкой границы со здоровыми тканями. Цель индукционной химиотерапии — уменьшение опухоли до размеров, когда можно будет выполнить оперативное вмешательство.
«Красная» химиотерапия получила свое название из-за того, что растворы химиопрепаратов, которые применяются в данном случае (доксорубицин, эпирубицин), имеют красный цвет. Этот вид лечения отличается наиболее выраженными побочными, токсичными эффектами. Еще химиотерапия бывает «желтой», «голубой» и «белой».
Один из примеров «красной» химиотерапии — это химиотерапия при РМЖ по схеме AC. Аббревиатура образована первыми буквами названий двух препаратов:
- Доксорубицин (Адриамицин — Adriamycin).
- Цитоксан (Циклофосфамид — Cyclophosphamide).
Такая схема химиотерапии применяется при раке молочной железы 2 и 3 стадии, когда опухолевые клетки распространились на лимфатические узлы.
Отзывы о химиотерапии по схеме AC от женщин в Интернете рассказывают о таких побочных эффектах, как тошнота и рвота, снижение количества клеток крови, выпадение волос, анорексия, бесплодие. В Европейской клинике курсы химиотерапии проводятся под прикрытием поддерживающей терапии, что позволяет перенести лечение максимально комфортно.
Ниже представлены некоторые отзывы о химиотерапии при раке молочной железы от пациенток Европейской клиники:
У моей бабушки в своё время был рак молочной железы. Поэтому я можно сказать была готова к этому диагнозу. Но всё равно очень страшно и я не ожидала что так рано. Так как я регулярно проверялась, опухоль обнаружили на начальной стадии. Ещё без метастазов. Так как размер был очень небольшой, сразу прооперировали, а потом начали химиотерапию. Сейчас курс закончился. Чувствую себя хорошо, окружающие говорят, что и выгляжу не хуже чем до операции) Спасибо за моё здоровье. Думаю, что скоро пациентам не понадобится никаких «чудесных» новых лекарств. Достаточно и того что есть. Просто надо делать всё ВОВРЕМЯ и ПРАВИЛЬНО. Как в этой клинике.
Эти два метода нельзя сравнивать по эффективности, поскольку оба имеют вполне определенные показания и определенные результаты, зависящие от особенностей опухолей и возраста больных. В случае чувствительности опухоли к химиотерапии эффективность будет такой же, как при чувствительности опухоли к гормонотерапии. Нередко бывают ситуации, когда химиотерапия неэффективна, но эффективна гормонотерапия и наоборот. Очевидным преимуществом химиотерапии является быстрый эффект. После 1-2 курсов можно узнать о результате лечения. Очевидным недостатком химиотерапии являют побочные эффекты — поражение крови, выпадение волос, тошнота и рвота и ряд других, которые отсутствуют при гормональной терапии рака молочной железы.
Степень чувствительности к гормональному воздействию предсказывают по количеству рецепторов эстрогенов и прогестерона в цитоплазме раковой клетки, чем их больше, тем выше вероятность ответа на антигормоны. Чувствительность рака к химиотерапии предсказывается по наличию специфического гена HER-2. Обнаружение его говорит, что опухоль может не реагировать на присутствие лекарства-убийцы, сегодня для его подавления используются таргетные препараты герцептин и пертузумаб. Опухоль может реагировать и на цитостатики, и на гормоны, тогда гормональное воздействие начинается после завершения циклов ХТ и продолжается многие годы.
 Предлагаем ознакомиться с информационными материалами для пациентов, проходящих химиотерапию в Европейской клинике. Читайте о том, как справиться с последствиями и побочными эффектами химиотерапии Предлагаем ознакомиться с информационными материалами для пациентов, проходящих химиотерапию в Европейской клинике. Читайте о том, как справиться с последствиями и побочными эффектами химиотерапии |
Часто пациенток пугает необходимость получения химиотерапии, поскольку она может сопровождаться побочными явлениями: тошнотой, рвотой, развитием лейкопении (уменьшение числа лейкоцитов в крови), тромбоцитопении (уменьшения числа тромбоцитов в крови), снижения уровня гемоглобина, алопецией (выпадением волос). Однако следует понимать, что на одной чаше весов находится выздоровление, а на другой — возможные побочные эффекты, которые являются хоть и неприятными, но временными.
Химиотерапия «славится» большим числом неприятных реакций, потому что цитостатики не отличают раковую клетку от нормальной. Выносливость тканей организма определяется численностью в ней делящихся клеток, поэтому быстрорастущие клетки крови, половых желёз, волосяных фолликулов, слизистых оболочек погибают вместе с раковыми, но в значительно меньшем количестве. Массовая клеточная гибель и токсическое действие метаболитов химиопрепаратов — это и есть осложнения, приносящие физические страдания.
Некоторые группы препаратов имеют избирательное действие на определённые ткани: какие-то убивают преимущественно форменные элементы крови, какие-то — почечных канальцев, какие-то — нервные волокна, какие-то — слизистые. Для каждого цитостатика определен список возможных осложнений, но индивидуальны их интенсивность и спектр. Иногда тяжелые осложнения ставят вопрос о снижении дозы препарата, что может ухудшить общий результат лечения.
В Европейской клинике в протоколы химиотерапии обязательно включены противорвотные препараты, которые уменьшают выраженность побочных эффектов и позволяют практически не менять привычного рациона питания и образа жизни. Клиника имеет лицензию на переливание препаратов крови и кровекомпонентов, что позволяет компенсировать предшествующие или развивающиеся на фоне химиотерапии изменения в крови.
При проведении химиотерапии в случае запущенных состояний, требующих также массивного обезболивания, мы применяем международно-признанную трехступенчатую систему, включающую применение ненаркотических и наркотических обезболивающих средств.
Собственно лучевая терапия при раке молочной железы в Европейской клинике не проводится. При наличии необходимости в таком вмешательстве мы направляем пациента в дружественное лечебное учреждение. Суть эффективности лучевой терапии при раке молочной железы заключается в подавлении опухоли или зон возможного метастазирования, как правило, с помощью линейных ускорителей. Убивая опухолевые клетки или снижая их жизнеспособность, лучевая терапия создает более благоприятные условия для оперативного вмешательства, значительно повышает его надежность и радикализм.
В настоящее время лучевая терапия при раке молочных желез проводится в основном в послеоперационном периоде. Такое вмешательство показано у больных раком молочной железы с повышенным риском местного рецидива заболевания.
Мы также рекомендуем проведение лучевой терапии, подвергать органосохраняющим операциям, с целью снижения угрозы местного рецидива рака молочной железы в оставшейся части молочной железы на 50-60%. Проведение лучевой терапии на современных линейных ускорителях, как правило, не сопровождается осложнениями или побочными явлениями, требующими приостановки или прекращения лечения.
— Проводится ли в Европейской клинике восстановление молочной железы после ее полного удаления при лечении рака молочной железы?
Решение вопроса о реконструктивной операции после мастэктомии принимается совместно оперирующим хирургом и пациенткой до первичного хирургического лечения. Примерно половина женщин моложе 50 лет, которые планируют мастэктомию, решаются также на проведение реконструктивной операции, позволяющей с помощью собственных тканей или эндопротеза восстановить молочную железу. Большая часть пациенток старше 55 лет предпочитает в чашечке бюстгальтера носить протез молочной железы.
Тщательная забота об организме и уход за ним, чрезвычайно важны перед, во время и после противоопухолевого лечения. Сюда относится правильное питание и максимально активный образ жизни. Для сохранения нормального веса необходимо получать достаточное количество калорий. Кроме этого, для поддержания сил важно получать достаточно белка. Иногда, особенно во время и вскоре после окончания лечения, аппетит пропадает. Вы можете чувствовать себя неуютно или уставшей. Вам может казаться, что изменился вкус привычных блюд и продуктов. Кроме этого, хорошему питанию противодействуют побочные эффекты лечения (снижение аппетита, тошнота, рвота, язвочки в ротовой полости). С другой стороны, некоторые женщины, которые проходят лечение рака молочной железы, с трудом справляются с избыточным весом.
Для удовлетворения ваших потребностей в питании спросите совета у лечащего врача. В случае необходимости мы приглашаем врача диетолога, имеющего опыт работы с онкологическими пациентами.
После завершения лечения рака молочной железы рекомендуется регулярно проходить профилактические осмотры. Осмотры выявят любые изменения со стороны здоровья. Если между регулярными консультациями появились какие-то отклонения в состоянии здоровья, незамедлительно свяжитесь с лечащим врачом. Врач должен провести проверку на предмет рецидива рака и метастазов во внутренние органы. Кроме этого, профилактические осмотры позволяют выявить нарушения, вызванные противоопухолевым лечением.
О любых изменениях в зоне операции или в другой молочной железе следует немедленно сообщать врачу. Расскажите доктору о любых отклонениях, таких как боль, снижение аппетита или веса, изменения менструального цикла, необычные выделения из влагалища или нечеткость зрения. Кроме этого, поговорите с врачом, если у вас возникают головные боли, головокружение, одышка, кашель или охриплость голоса, боли в спине или нарушения пищеварения, которые кажутся вам необычными или не проходят со временем. Подобные нарушения могут появиться спустя месяцы, и даже годы после лечения. Профилактический осмотр обычно включает клиническое обследование шеи, подмышечных областей, грудной клетки и молочных желез.
Так как возможно появление новой опухоли, следует регулярно проходить маммографию. Лечащий врач также может назначить другое инструментальное обследование или анализы (УЗИ послеоперационного рубца, УЗИ брюшной полости и малого таза, рентгенографическое обследование органов грудной клетки, сцинтиграфию, анализы крови), а при реконструкции молочной железы и МРТ (магнитно резонансная томография).
Рак молочной железы — общая информация для пациентов о заболевании.
Рак молочной железы 4 стадии — информация о поздних стадиях рака молочной железы.
Лечение рака молочной железы — общая информация о возможностях его лечения.
Реконструкция груди после операции — онкопластическая хирургия. Фотографии результатов пластических операций пациенток с РМЖ.
Таргетная терапия опухолей — таргетное лечение рака молочной железы.
источник
В развитых странах в структуре онкологической заболеваемости женщин рак молочной железы (РМЖ) занимает 1-е место (26% всех случаев рака).
По данным ВОЗ, в мире ежегодно умирает от РМЖ 590 000 женщин.
В 2006 г. в России рак молочной железы составил 17,8% всех злокачественных опухолей у женщин.
Показатель заболеваемости в 2006 г. составил 65,5 случая на 100 000 населения, абсолютное число заболевших — 48 821. Смертность в 2006 г. равнялась 29,5 случая на 100 000 женского населения, 1-летняя летальность — 11,5%. Мутация генов BRCA1 и BRCA2 увеличивает риск РМЖ.
Выбор метода лечения больных раком молочной железы зависит от стадии заболевания и от биологической характеристики опухоли (степень злокачественности, рецепторный статус, экспрессия HER2).
Ниже приводится классификация РМЖ по системе TNM и группировка по стадиям (табл. 9.17).
ТХ — недостаточно данных для оценки первичной опухоли.
Т0 — признаков первичной опухоли нет.
Tis — рак in situ.
Tis (DCIS) — протоковый рак in situ.
Tis (LCIS) — дольковый рак in situ.
Tis (Paget’s) — рак Педжета соска при отсутствии опухоли в паренхиме железы. При этом рак Педжета в сочетании с опухолью паренхимы оценивают в соответствии с размерами последней.
Т1 — опухоль не более 2 см в наибольшем измерении.
T1mic — микроинвазивный рак размером 0,1 см и менее в наибольшем измерении.
Т1а — опухоль более 0,1 см, но не более 0,5 см.
T1b — опухоль более 0,5 см, но не более 1 см.
T1c — опухоль более 1 см, но не более 2 см.
Т2 — опухоль более 2 см, но не более 5 см в наибольшем измерении.
Т3 — опухоль более 5 см в наибольшем измерении.
Т4 — опухоль любого размера с непосредственным распространением на а) грудную стенку, б) кожу с учетом описанных ниже принципов:
Т4а — опухоль поражает грудную стенку;
Т4b — отек (включая симптом лимонной корки), изъязвление кожи или метастазы в
коже той же молочной железы;
Т4с — сочетание признаков Т4а и Т4b;
T4d — диффузный рак.
NX — недостаточно данных для оценки регионарных лимфоузлов (например, они были ранее удалены).
N0 — регионарные лимфоузлы не пальпируются.
N1 — пальпируются подвижные подмышечные лимфоузлы с той же стороны.
N2 — пальпируются подмышечные лимфоузлы с той же стороны, спаянные друг с другом или окружающими тканями, либо имеются клинические признаки метастазов в окологрудинных лимфоузлах той же стороны при отсутствии таких признаков для подмышечных лимфоузлов.
N2a — подмышечные лимфоузлы на стороне опухоли спаяны друг с другом или окружающими тканями.
N2b — клинические признаки метастазов в окологрудинных лимфоузлах той же стороны при отсутствии таких признаков для подмышечных лимфоузлов.
N3 — пальпируются подключичные лимфоузлы (лимфоузел) вне зависимости от состояния подмышечных лимфоузлов, либо имеются клинические признаки метастазов в окологрудинных и подмышечных лимфоузлах, либо имеются метастазы в надключичных лимфоузлах, необязательно в сочетании с метастазами в подмышечных или окологрудинных лимфоузлах.
MX — недостаточно данных для оценки отдаленных метастазов.
М0 — отдаленных метастазов нет.
M1 — отдаленные метастазы имеются.
Таблица 9.17. Группировка рака молочной железы по стадиям (6-е издание, 2002)
Своеобразное течение РМЖ и биологические особенности этой опухоли обусловливают использование на определенных этапах заболевания всех существующих методов лечения — хирургического, лучевого, гормонального, химиотерапевтического, включая таргетную терапию; однако оптимальная последовательность их применения до настоящего времени остается предметом активных клинических исследований.
По современным представлениям, для выбора оптимальной терапии больной раком молочной железы необходимо иметь сведения о содержании в опухоли рецепторов стероидных гормонов (рецепторов эстрогена (РЭ), рецепторов прогестерона (РП)), экспрессии HER2 и степени злокачественности опухоли, определяемой по степени ее дифференцировки.
С точки зрения биологических особенностей, определяющих возможности лечения, все больные РМЖ делятся на три группы:
1) больные с гормоночувствительными опухолями, содержащими РЭ, РП; в лечении этих больных, как правило, используется гормонотерапия;
2) больные, опухоль которых характеризуется гиперэкспрессией HER2; этим больным показан трастузумаб (Герцептин);
3) больные РМЖ, у которых опухоль не содержит ни рецепторов стероидных гормонов, ни HER2 (так называемые трижды негативные опухоли); при лечении таких больных наиболее перспективна цитотоксическая химиотерапия (XT).
Эти клинические группы соответствуют молекулярным подтипам рак молочной железы (люминальный А и Б HER2-позитивный, базальный нормоклеточный).
Гормонотерапия — один из важнейших методов лечения РМЖ. Около 60% больных РМЖ (а среди пожилых больных до 80%) имеют гормонозависимые опухоли, т.е. опухоли, содержащие РЭ и РП.
Существует прямая корреляция между наличием и уровнем рецепторов стероидных гормонов и эффективностью гормонотерапии. Эффективность лечения РЭ-положительных опухолей составляет 50-60%, тогда как при РЭ-отрицательных злокачественных опухолях молочной железы положительный эффект гормонотерапии отмечается лишь у 5-10% больных. Около 30% больных с неизвестным рецепторным статусом отвечают на гормональные воздействия.
К методам гормонотерапии относятся: хирургическая, лучевая и химическая (с помощью суперагонистов LH-RH) кастрация у женщин с сохранной менструальной функцией, применение антиэстрогенов, ингибиторов ароматазы, прогестинов, андрогенов и их аналогов, кортикостероидов.
В принципе в основе всех методов гормонотерапии рака молочной железы лежит попытка воспрепятствовать стимулирующему воздействию стероидных гормонов (эстрогенов) на клетки опухоли.
У женщин в пременопаузе это может быть достигнуто путем овариэктомии или облучения яичников либо с помощью применения суперагонистов LH-RH, под влиянием которых функционируют яичники. Такая химическая кастрация носит обратимый характер и достигается применением гозерелина (Золадекс) или лейпрорелина, бусерелина.
У женщин в менопаузе синтез эстрогенов происходит в основном в жировой ткани путем реакции ароматизации андрогенов, продуцируемых корой надпочечников, а следовательно, использование ингибиторов ароматазы снижает содержание эстрогенов.
К селективным ингибиторам ароматазы относятся нестероидные — летрозол (Фемара), анастрозол (Аримидекс) — и стероидный ингибитор экземестан (Аромазин).
Антиэстрогены блокируют РЭ в опухоли. В эту группу входят селективные модуляторы эстрогенных рецепторов (SERM) — тамоксифен и торемифен и селективный супрессор эстрогенных рецепторов (SERD) — фульвестрант (Фазлодекс). Эти препараты активны как в пре-, так и в менопаузе.
Менее ясен механизм противоопухолевого действия прогестинов (мегестрол, медроксипрогестерон), которые также используются в гормонотерапии РМЖ.
РМЖ — опухоль, чувствительная к большинству современных противоопухолевых цитотоксических препаратов, прежде всего к антрациклинам — доксорубицину, который эффективен у 40% больных. Аналогичная эффективность и у эпирубицина, митоксантрона, циклофосфамида (35%), метотрексата (35%), фторурацила и тегафура (25 %). В 1990-е годы в клиническую практику вошли таксаны: паклитаксел (Таксол), эффективность 56-60%, доцетаксел (Таксотер) — 57-75%, винорелбин (Навельбин) — 41-51 %, капецитабин (Кселода) вторая линия — 20-36%, гемцитабин (Гемзар) вторая линия — 25%. У больных с гиперэкспрессией HER2 эффективен таргетный препарат трастузумаб (Герцептин) — гуманизированное МКА к EGFR — и лапатиниб (Тайверб, Тайкерб) — двойной ингибитор тирозинкиназы рецепторов EGF (HER2/HER1).
Больные с операбельным раком молочной железы нуждаются в дополнительной (адъювантной) лекарственной терапии, улучшающей отдаленные результаты лечения, снижающей риск рецидива заболевания и увеличивающей выживаемость больных. Исключение составляет лишь небольшая прогностически благоприятная группа больных старше 35 лет с высокодифференцированной (G1) гормоночувствительной (РЭ+, РП+) опухолью размером до 1 см, без метастазов в лимфоузлах (T1aN0M0) и без гиперэкспрессии HER2.
Важнейшими прогностическими факторами являются наличие и число пораженных лимфоузлов, размер первичной опухоли, степень злокачественности, определяемая по дифференцировке опухоли (G), возраст больной и состояние ее менструальной функции, содержание РЭ и/или РП в опухоли, а также гиперэкспрессия HER2 (табл. 9.18).
Таблица 9.18. Распределение больных раком молочной железы на категории риска
Рекомендации по выбору методов лечения в зависимости от чувствительности РМЖ к гормонотерапии приведены в табл. 9.19 и 9.20.
Таблица 9.19. Рекомендации по выбору методов лечения в зависимости от чувствительности к гормонотерапии (ГТ)
Примечание: При необходимости назначения XT и тамоксифена прием последнего должен быть начат после завершения XT (ХТ->ГТ) Вопрос относительно последовательности назначения ингибиторов ароматазы и XT (XT + ГТ или ХТ->ГТ) остается дискутабельным У больных в пременопаузе применение аналогов гонадотропин-рилизинг гормона может быть начато одновременно с XT для максимально быстрого достижения менопаузы.
Таблица 9.20. Рекомендации по лечению больных с гормоночувствительными опухолями
Примечание: В круглых скобках указаны лечебные опции, являющиеся предметом дискуссий и оцениваемые в соответствующих клинических исследованиях. Т — тамоксифен; ИА — ингибиторы ароматазы, ГТ — гормонотерапия; ОС — овариальная супрессия
При высоком риске N0 и отсутствии гормональных рецепторов послеоперационно проводится 4-6 курсов химиотерапии с включением антрациклинов (AC, FAC) или 6 курсов CMF. Больным в пременопаузе с положительными рецепторами и N0 после XT назначается тамоксифен на 5 лет. Альтернативой у этой категории пациенток служит выключение функции яичников с назначением тамоксифена.
У больных с низким риском в пременопаузе с N0 используется выключение функции яичников с помощью агонистов LH-RH в течение 2 лет, изучается целесообразность более длительного применения этих препаратов.
У больных в постменопаузе с N0 и положительными рецепторами используются ингибиторы ароматазы либо тамоксифен в течение 5 лет или прием тамоксифена в течение 2-3 лет с последующим переходом на ингибиторы ароматазы (до 5 лет). У больных в постменопаузе адъювантная гормонотерапия на любом этапе ее проведения может включать ингибиторы ароматазы. В ряде исследований было показано, что лечение тамоксифеном неэффективно у НЕR2-позитивных больных, что служит показателем резистентности к тамоксифену.
При высоком риске и N0 даже в менопаузе считается целесообразным назначение химиотерапии, а затем гормонотерапии ингибиторами ароматазы или тамоксифеном. У больных старше 70 лет основой адъювантной лекарственной терапии является тамоксифен.
При N+ в пременопаузе и при количестве метастазов в подмышечных лимфоузлах менее 4 показано проведение 6 курсов антрациклинсодержащих комбинаций CAF, FAC, АС или 6 курсов классического режима CMF с пероральным приемом циклофосфамида. При наличии 4 метастазов и более считается целесообразным назначение более длительной химиотерапии с дополнительным использованием таксанов. Далее при положительных рецепторах назначается тамоксифен на 5 лет.
У больных с сохранной менструальной функцией при поражении не более 3 лимфоузлов и положительных рецепторах допустимо выключение функции яичников с одновременным приемом тамоксифена.
У больных в постменопаузе с положительными рецепторами основой адъювантного лечения считается гормонотерапия (ингибиторы ароматазы или тамоксифен), но при поражении 4 лимфоузлов и более показано на I этапе проведение XT с последующей гормонотерапией. При отрицательных рецепторах в постменопаузе рекомендуется только XT.
Комитет экспертов конференции (St. Gallen, 2009) предложил упростить вопрос выбора показаний к применению гормонотерапии при операбельном РМЖ: все больные, у которых обнаружены РЭ+ (независимо от их уровня), должны получать гормонотерапию. РЭ-положительными считаются все опухоли, в которых при иммуногистохи-мическом исследовании обнаруживается даже минимальное количество РЭ-положительных клеток. При окрашивании более 50% клеток опухоль рассматривается как высокочувствительная к гормонотерапии.
Стандарт гормонотерапии для больных в пременопаузе — это применение тамоксифена либо тамоксифена + выключение функции яичников; ингибиторы ароматазы пациенткам в пременопаузе противопоказаны и могут применяться лишь в случае противопоказаний к использованию тамоксифена, при условии надежного выключения функции яичников по показателю содержания эстрадиола в сыворотке крови (верификация выключения функции яичников желательна даже при назначении ингибиторов ароматазы пациенткам в менопаузе моложе 60 лет). Для женщин в менопаузе предпочтительна гормонотерапия ингибиторами ароматазы, хотя у отдельных больных возможно использование тамоксифена. У больных с высоким риском предпочтительны ингибиторы ароматазы.
Показано, что у больных в менопаузе при рецептор-положительном раком молочной железы длительное применение летрозола (Фемара) по 2,5 мг/сут после окончания 5-летнего приема тамоксифена улучшает эффективность адъювантной гормонотерапии, снижая к 4 годам наблюдения относительный риск рецидива на 42 %.
Современный выбор оптимальных режимов адъювантной химиотерапии достаточно широк и включает использование антрациклинов и таксанов.
Применение антрациклинсодержащих комбинаций позволяет по сравнению с CMF уменьшить риск рецидива на 12%, риск смерти — на 11 % и увеличить 5-летнюю безрецидивную выживаемость на 3,2%, 5-летнюю общую выживаемость — на 2,7%. В США в адъювантном лечении у больных с плохим прогнозом используется паклитаксел после нескольких курсов антрациклинсодержащих комбинаций, в Европе активно ведутся исследования по использованию доцетаксела в адъювантной терапии, показавшие его высокую активность.
У больных с HER2+ РМЖ в рандомизированных исследованиях показано значение адъювантного применения трастузумаба (Герцептин).
На основании предварительного анализа результатов этих исследований международным консенсусом в 2007 г. рекомендовано использование трастузумаба при ранних стадиях HER2+ РМЖ в течение 1 года. Остается неясным вопрос о длительности его применения, целесообразности назначения при N0 и Т 5 лет);
• пожилой возраст;
• метастазы в костях, локорегионарные метастазы, минимальные метастазы в легких;
• гистологически установленная I-II степень злокачественности (G1-G2);
• большая длительность полученной ранее ремиссии в результате предшествовавшей гормонотерапии.
Ответ на гормонотерапию маловероятен в следующих случаях:
• короткий период без метастазирования (
источник