«Результаты УЗИ молочных желез выявили образование, подозрительное на онкологию», «результаты маммографии не позволяют однозначно исключить наличие злокачественного образования», «биопсия показала наличие раковых изменений в молочной железе и требуется расширенное обследование». Это лишь немногие из самых страшных слов, которые женщина может услышать от своего врача.
Молочные железы состоят из трех основных типов тканей — жировой, соединительной и железистой. Раком молочной железы (РМЖ) называют злокачественные опухоли, развивающиеся именно из клеток железистой ткани. Вопреки расхожему мнению, РМЖ заболевают как женщины, так и мужчины, однако у женщин он встречается примерно в 100 раз чаще.
Рак груди развивается так же, как и любая другая злокачественная опухоль в организме. Одна или несколько клеток железистой ткани в результате произошедшей в них мутации начинают аномально быстро делиться. Из них образуется опухоль, способная прорастать в соседние ткани и создавать вторичные опухолевые очаги — метастазы.
Мутации, которые приводят к РМЖ, бывают наследственными и приобретенными.
Распространенными наследственными генетическими причинами рака молочной железы становятся мутации в генах BRCA1 и BRCA2. Носительницы мутации BRCA1 имеют риск заболеть раком молочной железы 55–65%, а носительницы BRCA2 — 45%. Такие генетические дефекты передаются по наследству от родителей детям, они становятся причиной рака молочной железы примерно в 15% случаев.
Намного чаще опухоль возникает из-за приобретенных мутаций: они возникают в клетках молочной железы и не передаются по наследству. Например, в 20% случаев увеличено количество копий гена, кодирующего HER2 — белок-рецептор, который находится на поверхности клеток и стимулирует их размножение.
«Молекулярно-генетический портрет» опухоли имеет важное значение при выборе оптимального лечения.
Чаще всего опухоли молочных желёз развиваются из клеток молочных протоков — в этом случае врачи говорят о протоковом раке молочной железы или протоковой карциноме. Довольно часто злокачественные опухоли вырастают из клеток долек молочной железы, этот тип рака называют инвазивной лобулярной карциномой (инвазивный рак молочной железы). Стоит отметить, что рост опухоли возможен и из других клеток железистой ткани.
К сожалению, полной информации о причинах возникновения рака молочной железы у ученых пока нет. Существует список факторов риска, влияющих на вероятность появления опухоли, однако у некоторых болезнь диагностируют при отсутствии этих факторов, другие же остаются здоровыми при наличии сразу многих из них. Тем не менее, ученые все же связывают развитие рака груди с определенными обстоятельствами, наиболее часто предваряющими его появление. К ним относятся:
- Возраст. Большинство случаев РМЖ приходятся на женщин в возрасте 55 лет и старше.
- Наследственность. Если РМЖ диагностирован у кого-то из близких родственников, риск повышается вдвое.
- Рак молочной железы в анамнезе.
- Повышенная плотность ткани молочной железы по результатам маммографии.
- Некоторые доброкачественные новообразования в молочной железе.
- Раннее начало менструаций — до 12 лет.
- Поздняя менопауза — после 55 лет.
- Отсутствие детей или поздние (после 35 лет) первые роды.
- Воздействие радиации, например, в ходе лучевой терапии, проводимой для лечения другого типа рака.
- Курение и злоупотребление алкоголем. Если женщина ежедневно потребляет 28–42 г этилового спирта, ее риски повышаются на 20%.
- Лишний вес и низкая физическая активность.
- Использование гормональных препаратов: оральные контрацептивы, заместительная гормональная терапия в постменопаузе.
- Травмы молочных желез.
- Сахарный диабет.
- Работа по графику с ночными сменами.
Довольно часто на ранних стадиях рак молочной железы протекает бессимптомно. Но в ряде случаев признаки, указывающие на наличие заболевания, все же есть, и их можно заметить.
В первую очередь, к симптомам, которые должны насторожить, относят уплотнения в молочных железах, рядом с ними или в подмышечной впадине. В 9 случаях из 10 уплотнения бывают доброкачественными, однако установить это наверняка можно только на осмотре у маммолога.
К симптомам рака молочной железы относят:
- Отвердение кожи
- Участок втяжения кожи
- Эрозия кожи
- Покраснение кожи
- Выделения из соска
- Деформация молочной железы по типу ряби
- Припухлость кожи
- Увеличенные в размерах вены
- Втяжение соска
- Нарушение симметрии молочных желез
- Симптом лимонной корки
- Пальпируемый узел внутри молочной железы.
При появлении указанных симптомов, а также любых других изменений в молочных железах (например, необычных или болезненных ощущений) нужно немедленно проконсультироваться с маммологом.
В Европейской клинике ведёт консультативный приём и выполняет операции известный российский хирург-маммолог, доктор медицинских наук Сергей Михайлович Портной (автор более 300 печатных работ, член правления Российского общества онкомаммологов, автор трех патентов на изобретения).
Сергей Михайлович выполняет весь объем оперативных вмешательств на молочной железе, включая органосохраняющие и реконструктивные пластические операции.
Самостоятельно проверять грудь на наличие узелков или каких-либо других изменений стоит раз в месяц, по окончании менструации. Домашнюю диагностику удобнее всего проводить, принимая ванну или находясь под душем. О любых изменениях, которые удалось обнаружить, стоит как можно быстрее рассказать врачу.
Порядок проведения самообследования молочных желез:
- Разденьтесь выше пояса и встаньте перед зеркалом.
- Поднимите руки вверх и заведите их за голову. Внимательно осмотрите грудь. Повернитесь правым, левым боком.
- Ощупайте молочные железы в положении стоя сложенными указательным, средним и безымянным пальцем. Начинайте с верхней наружной части груди и двигайтесь по часовой стрелке.
- Сожмите сосок двумя пальцами. Проверьте, выделяется ли из него что-нибудь.
- Снова ощупайте молочные железы — теперь в положении лежа.
70% случаев рака молочной железы выявляются пациентами самостоятельно в результате самообследования груди.
О роли биопсии в диагностике рака молочной железы рассказывает врач Европейской клиники Портной С.М.:
Для подтверждения или исключения диагноза в первую очередь проводится мануальное обследование груди. Затем, при наличии подозрений или в качестве скрининговой процедуры, может быть назначена маммография, рентгенологическое исследование молочных желез. Как правило, женщинам до 35 лет ее выполнение не рекомендуется, в молодости ткань молочных желез особенно чувствительна к радиоактивному облучению.
Ультразвуковое исследование (УЗИ) молочных желез позволяет оценить структуру их ткани и отличить, например, опухоль от кисты, наполненной жидкостью.
Если результаты маммографии или УЗИ указывают на наличие новообразований в молочной железе, врач, как правило, назначает биопсию, лабораторное исследование образца тканей из молочной железы. Биопсия позволяет выяснить, является ли опухоль злокачественной, а также определить ее тип и стадию. Кроме того, исследование биопсийного материала дает ответ на вопрос, является ли опухоль гормонозависимой, что также влияет на схему лечения.
При необходимости могут использоваться и другие диагностические методы, например, магнитно-резонансная томография (МРТ).
После постановки диагноза основной задачей лечащего врача является определение стадии онкологического заболевания, то есть размера опухоли, ее расположения, наличия метастазов и агрессивности. От этих факторов зависит прогноз лечения и подбор оптимальных методов терапии. Как правило, для уточнения стадии проводятся анализы крови, маммография другой молочной железы, сканирование костей, а также компьютерная или позитронно-эмиссионная томография. В некоторых случаях определить стадию опухоли можно только при проведении операции.
Стратегия лечения рака молочной железы зависит от многих факторов — типа рака, стадии, чувствительности клеток опухоли к гормонам, а также общего состояния здоровья пациентки.
Основной метод лечения рака груди — хирургическая операция. Если болезнь удалось диагностировать на ранней стадии, хирург может выполнить лампэктомию, удаление тканей опухоли и небольшой части окружающей ее здоровой ткани. При более крупных опухолях молочная железа удаляется целиком (такая операция называется мастэктомией), равно как и ближайшие к ней лимфатические узлы. Если по оценке врача риск развития рака во второй молочной железе достаточно высок, пациентке может быть рекомендовано удаление обеих молочных желез сразу.
Чтобы разобраться, распространились ли раковые клетки в лимфатические узлы, и определиться с объемом хирургического вмешательства, может быть проведена сентинель-биопсия, или биопсия сторожевого лимфоузла. Во время операции в опухоль вводят радиофармпрепарат или флуоресцентный краситель — это помогает визуализировать лимфоузел, который первым принимает лимфу от ткани молочной железы. Его удаляют и проводят гистологическое исследование. Если в сторожевом лимфоузле не обнаруживают опухолевых клеток, можно ограничиться удалением очага в молочной железе. В противном случае показано иссечение регионарных лимфоузлов.
Лучевую терапию (то есть воздействие на опухоль ионизирующим излучением) при раке молочной железы, как правило, используют после проведения хирургической операции. Терапия проводится с целью уничтожения раковых клеток, которые могли остаться в организме.
Химиотерапия, то есть использование препаратов, убивающих раковые клетки, может проводиться после операции по удалению опухоли, как и лучевая терапия. В некоторых случаях химиотерапию проводят до оперативного лечения для того, чтобы уменьшить размер слишком крупной для удаления опухоли.
В Европейской клинике для лечения рака молочной железы применяются наиболее современные, оригинальные европейские и американские химиопрепараты. У нас есть возможность составить «молекулярный отпечаток» опухоли, подобрать на основании его анализа наиболее эффективные и безопасные комбинации лекарств.
Для лечения рака молочной железы, чувствительного к гормонам, используют гормональную терапию — к ней относится несколько разных методов, останавливающих выработку гормонов в организме или блокирующих их поступление к опухоли. Гормональная терапия позволяет снизить вероятность рецидива опухоли, а также, в случае выявления неоперабельной опухоли, помогает контролировать ее рост.
Для лечения рака молочной железы применяют также таргетную терапию — препараты, поступающие непосредственно к тканям опухоли и минимально воздействующие на здоровые клетки организма. Таргетную терапию используют либо отдельно, либо в комбинации с другими методами лечения — в зависимости от того, какая схема лучше всего подойдет пациенту.
Если рак молочной железы диагностирован на ранних стадиях (0-I), пятилетняя выживаемость приближается к 100%. То есть, можно сказать, что удается вылечить практически всех женщин. Далее, в зависимости от стадии, прогноз относительно пятилетней выживаемости ухудшается:
- На II стадии — 93%.
- На III стадии — 72%.
- На IV стадии — 22%.
Совокупность имеющихся в арсенале онкологов методов лечения рака молочной железы позволяет в большинстве случаев добиться ремиссии заболевания или, как минимум, продлить жизнь с сохранением ее качества. Однако следует помнить, что эффективность лечения в целом напрямую зависит от того, было ли лечение начато своевременно, то есть на ранних стадиях заболевания.
Максимальная эффективность противоопухолевого лечения достигается только в том случае, если оно проводится в соответствии с международными протоколами, при этом учитываются индивидуальные особенности каждого пациента. Именно так назначают лечение онкологи Европейской клиники.
источник
А) Первичная профилактика — система социальных, медицинских, гигиенических и воспитательных мер, направленных на предотвращение заболеваний путем устранения причин и условий их возникновения и развития, а также на повышение устойчивости организма к воздействию неблагоприятных факторов окружающей природной, производственной и бытовой среды. В отличие от вторичной профилактики , нацеленной на раннее выявление заболевания, предупреждение рецидивов, прогрессирования болезненного процесса и возможных его осложнений, целью первичной профилактики является сохранение здоровья, предотвращение воздействия вредных факторов природной и социальной среды, способных вызывать патологические изменения в организме.
К первичной профилактике рака молочной железы относится:
Профилактика избыточного веса и гиподинамии.
Отказ от вредных привычек
Питание с преимущественным потреблением растительных продуктов
Естественное репродуктивное поведение
Природой женщине предначертано рожать и кормить грудью нескольких детей. В современном мире многодетные семьи – редкость, а период грудного вскармливания либо минимален, либо вообще отсутствует. А между тем, самый низкий уровень заболеваемости раком молочной железы — в странах с высокой рождаемостью. Уменьшение числа абортов и сохранение грудного вскармливания хотя бы до полугода значительно снижает риск развития рака груди.
Сокращение стрессовых ситуаций
Ограниченное применение гормонозаместительной терапии
В) Вторичная профилактика— ранее выявление и лечение предопухолевых заболеваний молочных желез – различные формы мастопатии, фиброаденом, других доброкачественных опухолей и заболеваний, а также нарушений эндокринной системы, заболеваний женских половых органов, нарушение функции печени.
К вторичной профилактике рака молочной железы относится:
Методы самообследования молочных желез
Самообследование — один из дополнительных методов выявления опухолей молочной железы. Самообследование молочных желез необходимо проводить 1 раз в месяц, на 6-12-й день от начала менструации. Неменструирующие женщины должны проводить самообследование в произвольно установленный ими самими определенный день каждого месяца. Самообследование состоит из осмотра и ощупывания молочных желез и подмышечных областей. Обследование необходимо проводить при вертикальном (стоя) и горизонтальном (лежа на спине) положении тела. Необходимо осмотреть соски: нет ли их втяжения, не изменились ли их цвет и форма, нет ли изъязвлений. Важно осмотреть кожу желез: нет ли изменений цвета, отека, втяжений, изъязвлений. Самообследование молочных желез должна проводить каждая женщина, это поможет раньше диагностировать РМЖ и получить более хорошие результаты при лечении.
Особенно внимательными должны быть женщины, у которых присутствуют следующие факторы риска:
•рождение первого ребенка в возрасте старше 30 лет;
•раннее начало менструаций;
•онкологические заболевания груди в семье;
•преобладание в питании высококалорийной, жирной пищи;
•нередкое употребление алкоголя;
•продолжительное лечение гормональными препаратами и использование КОК.
диагностика и лечение заболеваний, которые считаются предраковыми (мастопатии, фиброаденомы и т.д.)
Скрининг — массовое периодическое обследование здорового населения с целью выявления скрыто протекающего онкологического заболевания.
Скрининг предусматривает применение методики выявления скрытой патологии у большой группы практически здоровых лиц и поэтому должен отвечать следующим требованиям:
•высокая чувствительность метода или теста (благодаря чему обнаруживается большинство злокачественных опухолей в обследуемой группе при минимальном числе ложноотрицательных заключений);
•высокая специфичность метода (позволяет исключить большинство здоровых женщин у которых нет рака молочной железы, и свести к минимуму число ложноотрицательных заключений);
•приемлемая средняя стоимость одного выявленного случая рака; минимальный вред для здоровья обследуемой;
•простота эксплуатации и содержания оборудования.
Во всем мире «золотым стандартом» скрининга рака молочной железы является маммография, позволяющим снизить смертность на 30-50%.
В понятие качественного маммографического скрининга ВОЗ вкладывает соблюдение следующих принципов:
1.Иметь парк современного диагностического оборудования: комплексы для стереотаксической биопсии непальпируемых опухолей, высокочувствительные ультразвуковые аппараты.
2.Активное участие в скрининге женского населения (не менее 75% популяции).
3. Возраст обследуемых: 40-69 и ли 50-69 лет.
4. Наличие канцер-регистра, для учета показателей заболеваемости и смертности.
Женщинам после 45 лет маммографию рекомендуется делать ежегодно. Более молодым можно проходить её реже, если только они не относятся к группе риска.
С) третичная профилактика— предупреждение, ранняя диагностика и лечение рецидивов, метастазов и метахронных новообразований.
1. постановка пациентов на диспансерный учет
При диспансеризации больных раком молочной железы контрольный осмотр осуществляется: в первые 2 года — 1 раз в 3 мес, до 5 лет — 1 раз в 6 мес, в последующие годы — 1 раз в год.
2. поддерживающая гормонотерапия тамоксифеном или ингибиторами ароматазы при раке молочной железы.
«Хирургические болезни» под редакцией М.И. Кузина, Москва, «Медицина», 2002 г.
«Онкология» под редакцией В.И.Чиссова, Москва, «Гоэтар-медиа», 2012 г.
Национальное руководство «Маммология» под редакцией В.П. Харченко, Москва, «Гоэтар-медиа», 2009 г.
«Рак молочной железы» под редакцией Е.П. Куликова, Рязань, 2013 г.
«Онкология» по редакцией Ш.Х. Ганцева, Москва, 2010 г.
источник
В клинической медицине стадии онкологических заболеваний, в том числе стадии рака молочной железы, четко определены, поскольку развитие болезни происходит поэтапно, а методы лечения должны быть адекватны интенсивности и характеру патологического процесса.
Ответ на вопрос, сколько стадий рака молочной железы различают онкологи, дает международная классификация злокачественных опухолей TNM Classification of Malignant Tumours. В соответствии с ней, рак молочной железы имеет пять стадий.

TNM Classification of Malignant Tumours (последняя 7-я редакция, 2009 год) касается раковых опухолей любой локализации, и, таким образом, это и есть классификация стадий рака молочной железы. Она систематизирует основные симптомы рака: T — Tumor (опухоль), N — Nodus (узлы, то есть поражение лимфоузлов) и M — Metastasis (метастазы). В зависимости от степени их проявления определяет стадии развития заболевания.
Обозначение Тis (Tumor in situ) применяется в случае наличия компактной опухоли, которая не затрагивает другие, расположенные в непосредственной близости ткани. Обозначения Т1-Т4 относятся к определению размера злокачественного новообразования, а также уровню поражения тканей и органов, расположенных рядом с опухолью. Это стадии рака молочной железы 1, 2, 3 и 4.
Кроме того, если патологический процесс не затронул регионарные лимфатические узлы, применяется обозначение N0. Поражение лимфоузлов — их размеры, общее число и локализация — обозначаются N1-N3. А процесс метастазирования рака имеет следующие градации: Мх (обнаружить метастазы невозможно), М0 (отдаленные метастазы отсутствуют) и М1 (отдаленные метастазы есть).
Соответственно, 0 стадия рака молочной железы представляет собой совсем небольшую опухоль, которая не успела поразить другие ткани и затронуть лимфатические узлы.
Если диагностируется 1 стадия рака молочной железы, то это означает, что размер опухоли не превышает 2 см в поперечнике, а ее клетки уже проникли в окружающие ткани, то есть идет процесс опухолевой инвазии. Но при этом лимфатические узлы не затронуты.
2 стадия рака молочной железы характеризуется увеличением неоплазии до 5 см и началом ее распространения на клетки гиподермы — нижнего (жирового) слоя кожи. Эта стадия имеет варианты — 2А и 2В. При 2А метастазы отсутствуют, а при 2В в области подмышек со стороны опухоли обнаруживаются единичные метастазы, не соединенные ни между собой, ни с соседними тканями.
Исходя их клинической картины онкопатологии, 0, 1 и 2А – это ранние стадии рака молочной железы. 2В, 3 – более поздние, а 4 считается самой поздней стадией данного заболевания.
3 стадия рака молочной железы также имеет две «подстадии» — 3А и 3В. В случае 3А поперечный размер опухоли составляет более 5 см, отмечается наличие нескольких метастазов (в подмышечную область) и увеличение лимфоузлов, которые спаяны друг с другом или близлежащими тканями. Сосок может втянуть, из него могут быть серозные или кровянистые выделения.
На стадии 3B опухоль становится еще больше, при этом могут быть поражены внутригрудные лимфоузлы и стенка грудной клетки. Онкологи отличают так называемую воспалительную форму рака молочной железы, которая развивается очень быстро и нередко «маскируется» под мастит. Характерные признаки такого рака – видоизменение кожи на груди, ее гиперемия и гипертермия.
4 стадия рака молочной железы определяется, когда поражение охватывает всю железу, а также все лимфатические узлы (подмышечные, внутригрудные, подключичные и более отдаленные). Кожа и подкожные ткани груди изъязвляются, а метастазы опухоли, распространенные лимфотоком, могут обнаруживаться в легких, надпочечниках, печени, костных тканях и даже в головном мозге.

Диагностика рака молочной железы проводится с использованием следующих методов:
- клинический анализ крови (в том числе биохимический и на онкомаркеры);
- маммография (рентген молочной железы);
- УЗИ молочной железы, грудной клетки, брюшной полости;
- дуктография (рентген груди с контрастным веществом, проводится при деструкции молочных протоков, с которыми связаны серозные или кровянистые выделения из сосков);
- биопсия (пункционная, тонкоигольная аспирационная, стереотаксическая или хирургическая) молочной железы и лимфоузлов;
- гистологическое и иммуногистохимическое исследования биоптата;
- магнитно-резонансная томография (МРТ);
- рентгенография легких;
- УЗИ или компьютерная томография (КТ) органов грудной клетки, брюшной полости и малого таза;
- остеосцинтиграфия (радиоизотопное исследование костей).
Необходимо подчеркнуть особую важность для диагностики рака молочной железы иммуногистохимического исследования образцов тканей опухоли. Это так называемый FISH-тест, дающий онкологу информацию о количестве генов в опухолевых клетках, которые принимают участие в синтезе рецептора HER2/neu. Установлено, что при онкологических опухолях молочных желез существует высокая вероятность повышения активности гена HER2 – мембранного белка-фосфотрансферазы рецептора эпидермального фактора роста. Именно активизация синтеза данного белка приводит к гиперэкспрессии — росту числа рецепторов HER2 на внешней оболочке клеток опухоли и их повышенному размножению путем деления.
Благодаря определению количества рецепторов HER2/neu в опухолевых клетках можно спрогнозировать дальнейшее развитие неоплазии и применить нужные химиотерапевтические препараты для остановки деления патологических клеток.

Лечение стадий рака молочной железы зависит от результатов обследования пациенток и состояния ее здоровья и должно учитывать все факторы развития патологии. На сегодняшний день в онкологии молочных желез применяются такие методики лечения, как:
- химиотерапия;
- хирургическое удаление опухоли;
- лучевая терапия (радиотерапия);
- гормональная терапия;
- таргетная (целевая) терапия;
- комбинированная терапия.
Химиотерапия проводится с помощью цитотоксических (цитостатических) препаратов, которые нарушают механизм деления патологических клеток и тем самым приводят к прекращению их пролиферации. К таким препаратам относятся: препараты платины (Цитопластин, Цисплатин, Карбоплатин, Триплатин и др.); препараты группы таксонов (Паклитаксел, Таксан, Паклитакс, Паксен и др.); препараты группы алкалоидов барвинка (Винкристин Винорельбин, Винбластин, Маверекс); производные оксазафосфоринов (Эндоксан, Мафосфамид, Трофосфамид и др.); производные фторпиримидина карбамата (Капецитабин, Кселода) и др.
При этом химиотерапия рака молочной железы может проводиться в качестве единственного метода лечения, а также с целью уменьшения размеров опухоли перед ее хирургическим удалением и остановки образования метастазов после операции.
Хирургическое вмешательство — удаление опухоли и части окружающих ее тканей (лампэктомия) или удаление всей молочной железы (мастэктомия) – проводится в большинстве клинических случаев онкологии груди, особенно если диагностированы ранние стадии рака молочной железы.
Лучевая терапия при раке молочной железы, как и в случае опухолей другой локализации, призвана вызвать мутацию и гибель раковых клеток под воздействием радиоактивного облучения. Лучевая терапия может дополнять химиотерапию и хирургическое удаление опухоли молочной железы.
Как утверждают специалисты, гормональную терапию опухолей молочных желез целесообразно проводить после их удаления только пациенткам с гормонозависимыми новообразованиями, то есть при наличии у раковых клеток рецепторов к эстрогенам и прогестерону. В этом случае назначаются лекарственные препараты группы ингибиторов ароматазы (цитохром Р450-зависимого фермента) — Анастрозол, Летрозол или Эксеместан.
Таргетная терапия, нацеленная на опухоль и ее метастазы, базируется на способности рекомбинантных моноклональных антител класса IgG1 (подобных вырабатываемых иммунными клетками человека) селективно связываться с молекулярными рецепторами HER2/neu на внешней оболочке раковых клеток и останавливать их рост. В числе наиболее широко используемых препаратов данной группы онкологи называют Трастузумаб и Эпратузумаб.
Комбинированное лечение стадий рака молочной железы предполагает индивидуальный подбор и одновременное или поочередное использование всех методов, перечисленных выше.
В лечении 0 стадии рака молочной железы применяется удаление пораженного патологией сектора молочной железы (секторальная резекция) либо лампэктомия (см. выше). Данные операции могут сопровождаться лимфодиссекцией — удалением близлежащих лимфатических узлов.
Кроме того, обязательно назначают курс лучевой терапии, а при повышенной опухолевой экспрессии HER2 – таргетная терапия с помощью рекомбинантных моноклональных антител.
При лечении 1 стадии рака молочной железы проводится лампэктомия с удалением подмышечного лимфоузла. Чтобы ликвидировать оставшиеся клетки опухоли и избежать ее повторного возникновения, после хирургического вмешательства назначается адъювантная (послеоперационная) лучевая, гормональная или химиотерапия. А в случае опухолевой гиперэкспрессии HER2 должна применяться адъювантная таргетная терапия.
Обязательный этап лечения 2 стадии рака молочной железы – частичное удаление тканей пораженного органа (лампэктомия) или полное удаление железы (мастэктомия), что зависит от индивидуальной клинической картины заболевания. При этом удалению подлежат и пораженные регионарные лимфатические узлы. Курс химиотерапии пациентки с опухолями более 5 см проходят дважды: до оперативного вмешательства и после него.
По показаниям проводятся послеоперационные курсы лучевой или гормональной терапии.
В случае мастэктомии со временем проводится эндопротезирующая пластическая операция груди.
Началом лечения 3 стадии рака молочной железы является комплексная атака на раковые клетки с помощью цитотоксических препаратов (химиотерапия) и онкологической гормонотерапии. И только после положительных результатов принимается решение о проведении операции. Положительный результат хирургов закрепляется повторным курсом химиотерапии или прицельного ионизированного облучения.
Однако при некрозе опухоли, кровоточивости или образовании абсцесса лечение начинают с операции (паллиативной радикальной мастэктомии). А уже после этого применяется химио- и лучевая терапия.
При гормонозависимых новообразованиях показан длительный прием ингибиторов ароматазы (гормонотерапия), а при опухолевой гиперэкспрессии рецепторов HER2 (подробнее см. раздел Диагностика рака молочной железы) – применение моноклональных антител.
По общему признанию онкологов, лечение 4 стадии рака молочной железы – рецидивирующего и метастазирующего опухолевого процесса – в большинстве случаев является паллиативным, то есть направлено на облегчение состояния пациенток. Однако полноценная комплексная терапия при данной стадии заболевания способна продлить жизнь.
В первую очередь, чтобы снизить уровень интоксикации организма, необходима санационная мастэктомия, которая заключается в максимально полном удалении некрозных и изъязвленных тканей. А для борьбы с метастазами используется весь арсенал противораковых методов: комплексная химиотерапия, лучевая и гормональная терапия.
Кроме того, в обязательном порядке должно быть поддерживающее лечение сопутствующих патологических процессов. Так, при анемии и тромбоцитопении показаны прием соответствующих медпрепаратов и переливание крови; при метастазах в кости — назначение препаратов группы бифосфонатов и т.д.
Развитие болезни проходит несколько этапов, и стадии рака молочной железы четко определены. Поэтому следует вовремя обращаться за медицинской помощью и не допускать неподдающихся лечению стадий онкологических заболеваний.
Разнообразие морфологических признаков, вариантов клинических проявлений и реакций на терапевтическое воздействие дает все основания определять рак молочной железы как заболевание неоднородное.
источник
По распространенности рак молочной железы (РМЖ) занимает первое место среди онкологических заболеваний. Он поражает ежегодно 1 млн. 600 тыс. женщин в мире и свыше 66 тыс. в Российской Федерации.
В ближайшие 20 лет во всех странах прогнозируется почти двукратное увеличение заболеваемости женщин раком груди, что объясняется увеличением продолжительности жизни и улучшением методов диагностики.
За последние годы, благодаря более раннему выявлению опухолей, смертность от рака груди у женщин снижается. В развитых странах, где применяется маммографический скрининг населения, этот показатель снизился на 30–50%.
Рак молочной железы – это не единообразное заболевание. При лечении клиницисты учитывают принадлежность опухоли к конкретному подтипу. Генетическое тестирование и иммуногистохимический метод, позволяют надежно определить биологические подтипы РМЖ. Эти подтипы сами по себе включают многие факторы риска и предсказывающие признаки, что позволяет выбрать наиболее эффективную терапию для больного.
Доказанное с помощью молекулярно-генетического анализа и иммуногистохимического исследования патогенетическое разнообразие РМЖ позволяет индивидуализировать лечение.
Увеличение выживаемости при раке молочной железы связано не только с широкомасштабным внедрением маммографического скрининга, но и адекватным использованием системных видов лечения.
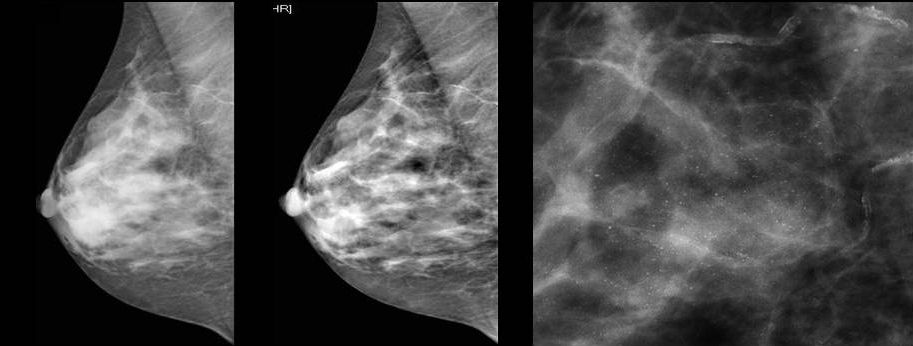
Для выявления злокачественных опухолей молочной железы существует определенный алгоритм диагностики, и его первичный элемент — маммографический скрининг. Чувствительность этого метода диагностики для опухолей от 2 мм до 5 мм составляет около 85%. Маммографическое исследование выполняют в двух проекциях.
Молодым женщинам с плотным строением молочной железы необходимо включение в программу наблюдения методов УЗИ и МРТ.
Поскольку традиционный маммографический скрининг у женщин до 40 лет малоэффективен, для скрининга может понадобиться альтернативная методика — МРТ. Современная контрастная магнитно-резонансная томография — высокочувствительный метод диагностики заболеваний молочной железы.
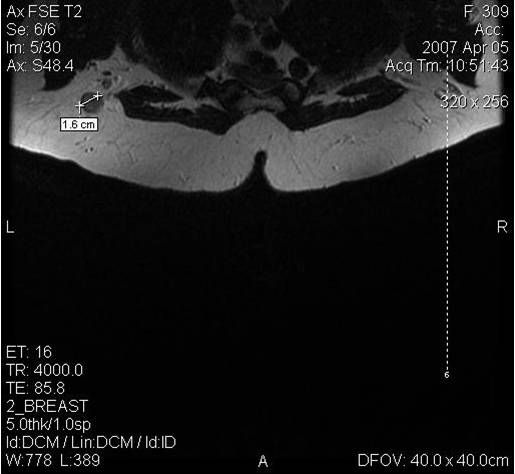
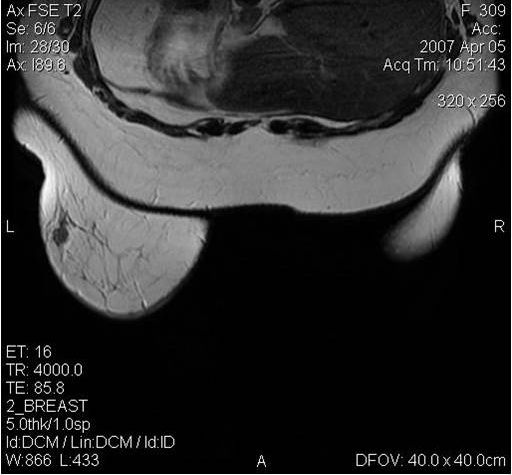
МРТ-диагностика рака молочной железы
У женщин с мутациями BRCA1 или BRCA2 при проведении МРТ возможно диагностировать рак молочной железы на самых ранних стадиях.
При ряде показаний женщинам назначается биопсия молочной железы под контролем УЗИ. Это исследование позволяет прицельно брать биологический материал для гистологического исследования, определения уровня экспрессии стероидных гормонов и статуса Her-2.
Известно множество факторов, повышающих риск возникновения рака молочной железы. На некоторые из них повлиять невозможно:
- семейная история по РМЖ,
- раннее менархе (начало месячных),
- позднее наступление менопаузы.
В то же время существуют и модифицируемые факторы, такие как:
- избыточный вес в постменопаузе,
- использование заместительной гормонотерапии,
- потребление алкоголя,
- курение
Стратегические шаги, направленные на снижение риска возникновения РМЖ включают контроль веса и борьбу с ожирением, регулярную физическую активность, уменьшение потребления алкоголя.
Большинство факторов риска рака молочной железы связано с действием гормонов на ткань молочной железы (раннее менархе, позднее наступление менопаузы, ожирение, применение гормональных препаратов). Считается, что именно женские половые гормоны, стимулируют процессы клеточного роста и повышают риски повреждения ДНК, что может привести к развитию злокачественного новообразования.
Только 5–10% случаев рака молочной железы обусловлены унаследованными мутантными генами BRCA. Но при этом, среди носителей мутаций риск возникновения заболевания может достигать 80%.
Чем младше возраст выявления первичного заболевания рака груди, тем выше вероятность заболеть контралатеральным раком, т.е. противоположной молочной железы.
Семейная история с наличием заболеваний раком молочной железы у кровных родственников, даже без ассоциации с мутациями BRCA, также повышает риск возникновения РМЖ.
Ожирение
Различными исследованиями доказано существование связи между заболеваемостью первичным РМЖ в постменопаузе и ожирением. Есть подтверждение связи между избыточным весом и низкой выживаемостью при всевозможных видах РМЖ.
Алкоголь
Алкоголь — также установленный фактор риска возникновения первичного РМЖ. Достоверность его отрицательного воздействия на пациентов, перенесших рак молочной железы, убедительна, так как он влияет на увеличение количества циркулирующих эстрогенов.
Только врач может оценить значимость различных симптомов. Однако каждой женщине необходимо знать, при каких симптомах надо обращаться к маммологу:
- «Образование», уплотнения, узел, инфильтрат, опухоль, «шарик» — что-то подобные этому вы обнаружили. Это еще не повод решить, что у вас РМЖ, но повод показаться специалисту.
- Деформация контура молочной железы, ареолы или соска (втяжение кожи или наоборот выбухание)
- Втяжение соска; особенно, если появилось недавно
- Выделение крови из соска
- Отек кожи всей молочной железы или ее локального участка
- Появление раздражения, мокнутые «ранки», язвочки, корочки на соске или ареоле
- Изъязвления (длительные, без видимой причины) на коже груди
- Дискомфорт в подмышечной области и обнаружение лимфоузлов ( «шариков» ) в подмышечной области
- Изменение цвета кожи молочной железы — покраснение, повышение температуры кожи в этой области.
Все эти симптомы могут быть проявлениями различных заболеваний (их насчитывается несколько десятков), возможно, не злокачественной природы. Однако, это может решить только специалист по заболеваниям молочной железы.
Признаки и симптомы рака молочной железы
0 стадия
Это стадия, когда не выявлена первичная опухоль, или она не может быть оценена, а также в случае неинвазивного рака молочной железы (что означает опухоль не выходит за границы своего появления, так называемый рак in situ).
1 стадия
Раковые клетки в этой стадии инвазируют или прорастают в соседние ткани. Опухолевый узел не более 2 см, лимфоузлы при этой стадии не поражены.
2 стадия
В этой стадии опухолевый узел превышает 2см и может достигать до 5см. При этой стадии могут быть поражены лимфоузлы, но поражение лимфоузлов носит одиночный характер, они не спаяны друг с другом и находятся на той же стороне, что и опухоль. В случае поражения лимфоузлов размер опухоли может быть и менее 2см.
3 стадия
Инвазивный рак, более 5 см или с явным и значительным поражением лимфатических узлов. При этом лимфоузлы могут быть спаяны между собой.
4 стадия
На этой стадии опухоль прорастает в кожу груди, грудную стенку либо во внутренние грудные лимфатические узлы. Она может быть любых размеров.
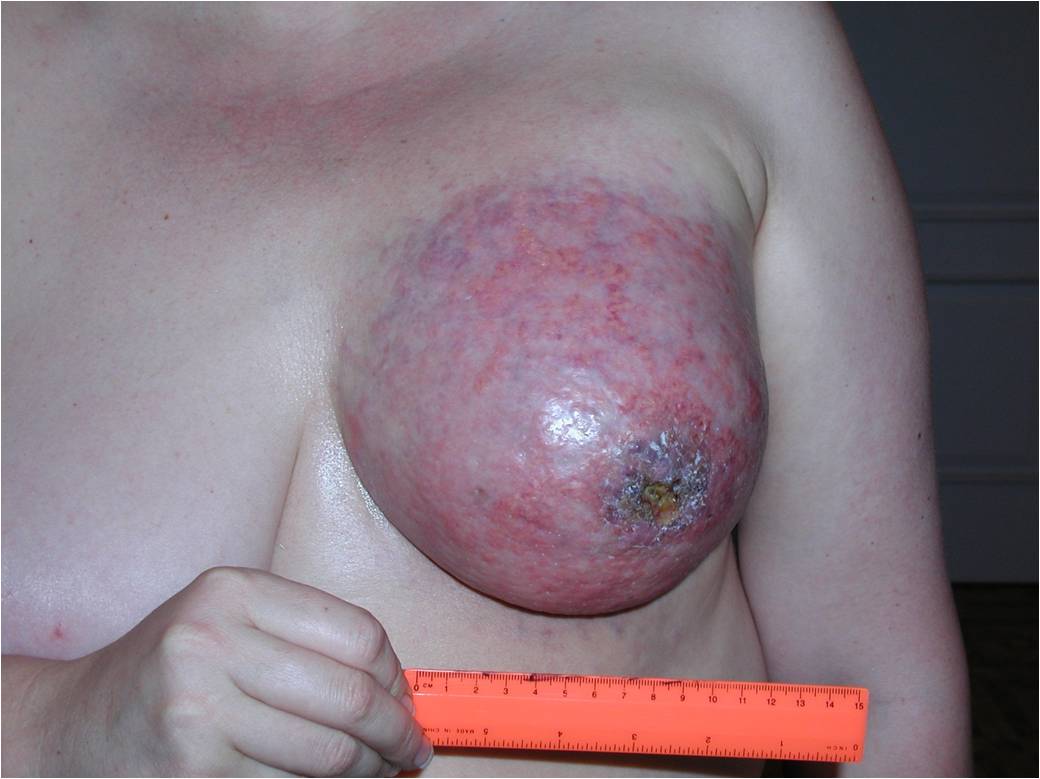
К 4 стадии рака молочной железы относится воспалительный рак, он встречается до 10 % всех случаев. Симптомы воспалительной формы рака груди это покраснение кожных покровов, железа становится теплой, отмечается увеличение и/или уплотнение части либо всей молочной железы. Кожа приобретает вид апельсиновой корки. Эту форму рака надо дифференцировать с воспалением молочной железы – маститом.
Также при 4 стадии опухоль может распространяться за пределы грудной клетки, в подмышечную область, внутренние грудные лимфатические узлы. Возможны метастазы в надключичные лимфатические узлы, а также в легкие, печень, кости или головной мозг.
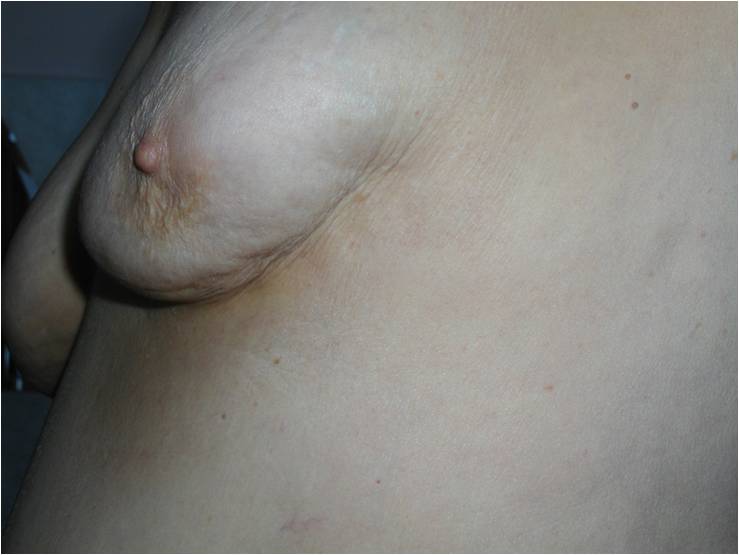
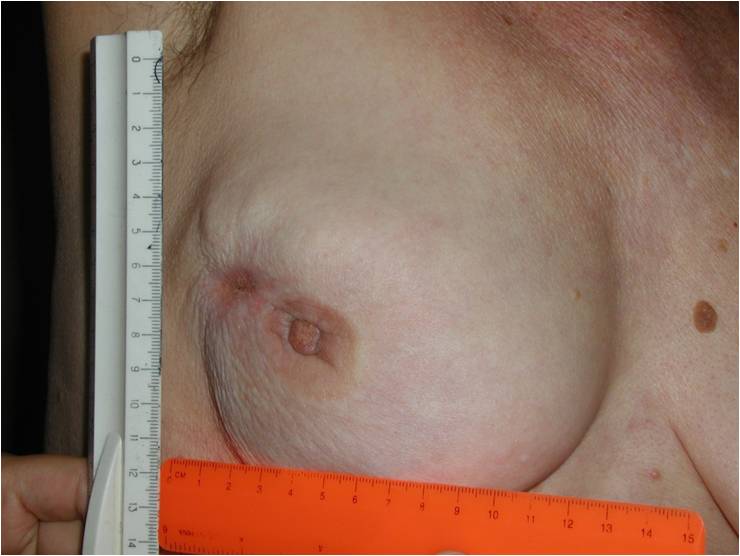
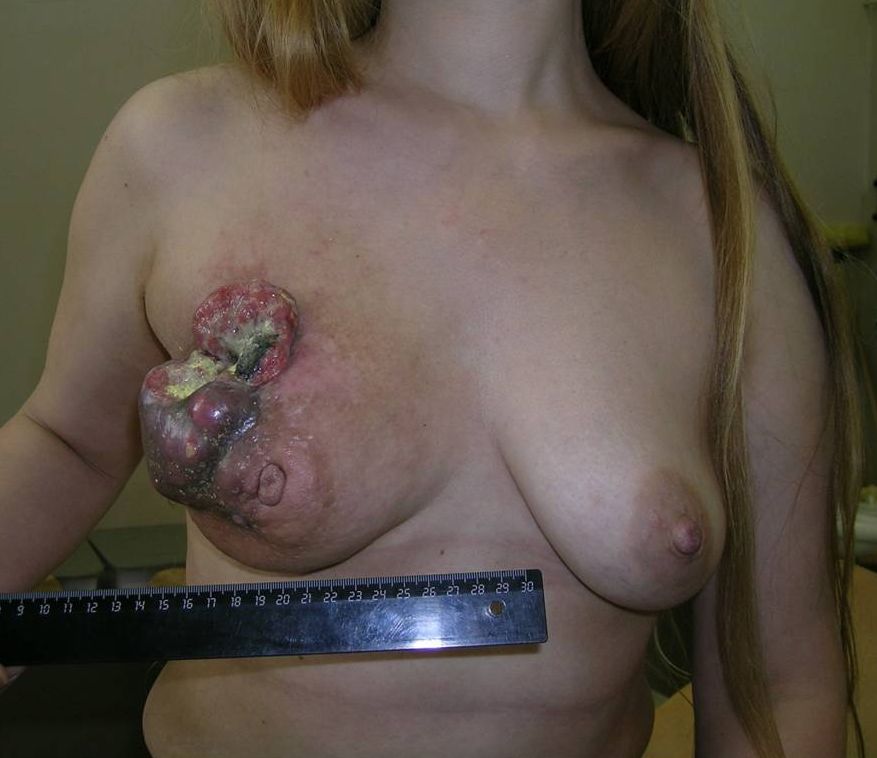
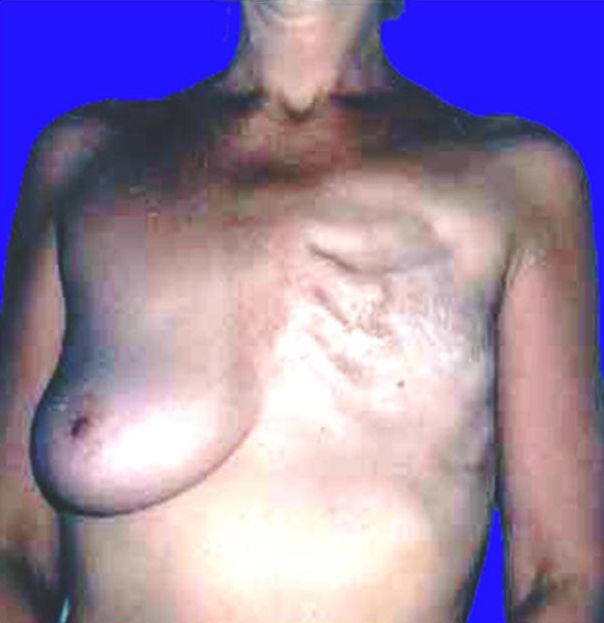
Как выглядит рак груди в разных стадиях:
Хирургическая операция — основной метод лечения при опухолях груди, и от качества его проведения во многом зависит исход заболевания. По данным некоторых штатов Индии, в которых по религиозным мотивам не проводится хирургическое лечение, показатели заболеваемости практически равняются показателям смертности. Обычно смертность от РМЖ в два — четыре раза уступает заболеваемости.
Однако, после хирургического лечения чаще всего следует лучевое. Местное лечение без послеоперационной лучевой терапии часто приводит к локально-регионарным рецидивам заболевания. Дело в том, что после завершения хирургической операции невозможно исключить существования скрытых отдаленных метастазов. Даже у больных с опухолями менее 1 см в диаметре в 10% случаев возможен рецидив заболевания.
Локализация отдаленных метастазов при РМЖ
Сейчас во всем мире наблюдается тенденция к сокращению объема хирургического вмешательства без потери эффективности. Хирургическое и лучевое лечение РМЖ развивается и совершенствуется в направлении органосохранения.
Благодаря внедрению маммографического скрининга, резко возросло число больных с ранней стадией заболевания, когда лимфоузлы не поражены метастазами. В этом случае «классическое» удаление всех уровней лимфоузлов было бы избыточной калечащей процедурой. На помощь хирургам пришел метод биопсии сигнальных (сторожевых) лимфатических узлов.
Поскольку, метастазы в подмышечных лимфоузлах появляются последовательно от первого ко второму, затем к третьему уровню, то достаточно определить наличие метастазов именно в первом лимфоузле. Его назвали «сигнальным»: если сигнальный лимфатический узел не содержит метастазов, то другие лимфоузлы также не метастатические.
Благодаря этому органосохраняющему методу, тысячи пациенток избежали избыточной полной хирургической диссекции, удаление раковой опухоли не привело к удалению груди.
Последние результаты клинических испытаний, в том числе и при участии НИИ онкологии им. Н.Н. Петрова, подтвердили безопасность отказа от полной подмышечной диссекции. Биопсия сигнальных (сторожевых) лимфатических узлов постепенно вытесняет подмышечную диссекцию как стандартную процедуру стадирования РМЖ.
Концепция биопсии сигнальных лимфатических узлов приобретает все большее признание и введена для многих локализаций опухолей в стандарты хирургического лечения Европейской Организацией по Изучению и Лечению Рака (EORTC).
Химиотерапия, наряду с хирургическим вмешательством, является одним из основных методов терапии рака. Послеоперационная химиотерапия улучшает результаты хирургического лечения, как и прогноз заболевания.
Ранее решение о назначении химиотерапии основывалось на двух факторах:
- стадия заболевания
- состояние регионарных лимфоузлов.
Благодаря многочисленным исследованиям ученых изменяются представления о биологии рака молочной железы, и выбор режимов химиотерапии значительно расширяется. И сегодня химиотерапевтическое лечение назначают даже при отсутствии метастазов в лимфоузлах, если небольшие по размеру опухоли обладают агрессивными биологическими характеристиками.
Люминальный А рак
При люминальном А раке избегают назначать проведение химиотерапии, особенно при негативных лимфоузлах, и применяют одну эндокринотерапию.
Люминальный В рак
Люминальные В опухоли характеризуются высокой агрессивностью. В этом случае чаще всего будет назначена химиотерапия, а выбор лечения основывается на оценке риска развития рецидива.
HER2-позитивный рак молочной железы
Лечение HER2-позитивного рака молочной железы основано на применении стандартных схем химиотерапии – трастузумаб и ХТ, основанная на антрациклинах и таксанах. Однако, только небольшой процент пациентов выигрывает от лечения, но все подвержены связанной с этим токсичностью.
Трижды негативный РМЖ
Трижды негативный рак молочной железы обычно ассоциируется с плохим прогнозом. Из-за редкой встречаемости особых типов РМЖ нет достаточных данных о роли адъювантной химиотерапии.
Химиотерапия при РМЖ у очень молодых женщин
Рак молочной железы в молодом возрасте обычно протекает агрессивно, часто встречаются гормонорезистеные и HER2-позитивные опухоли с иными свойствами, чем у более пожилых женщин. Для таких пациенток, моложе 35 лет, адъювантная полихимиотерапия почти всегда является необходимым методом лечения.
Химиотерапия пожилых пациенток
У пожилых пациенток (старше 65 лет) при решении вопроса о назначении адъювантной химиотерапии обязательно учитываются общее состояние организма и наличие сопутствующих хронических заболеваний.
В идеале пожилые пациенты должны подвергаться гериатрической оценке для определения их «пригодности» к адъювантому лечению. Потенциальный эффект лечения должен быть сбалансирован с теми рисками для организма, которые несет химиотерапия. Врач определяет наиболее эффективный и при этом наиболее безопасный специфический режим, основываясь на подтипе опухоли и индивидуальных характеристиках пациента.
Гормонотерапия
Молодые женщины с гормоноположительным раком молочной железы сохраняют риск рецидива заболевания на протяжении по крайней мере 15 лет после первичного заболевания. Онкологи должны определить, кто из пациентов нуждается в долгосрочной адъювантной терапии тамоксифеном или ингибиторами ароматазы.
Неоадъюватная (предоперационная) терапия
Неоадъюватная терапия занимает ведущую роль в лечении женщин с неоперабельным раком молочной железы, а также имеет важное значение при операбельных опухолях, когда выполняются органосохраняющие операции.
Эффект неоадъювантного лечения ДО (слева) и ПОСЛЕ (справа)
Лучевое лечение после проведенного хирургического вмешательства играет важную роль в терапии рака молочной железы и прогнозе заболевания. В НМИЦ онкологии им. Н.Н. Петрова было проведено исследование роли лучевой терапии после органосохраняющих операций (секторальная резекция с аксиллярной лимфоаденэктомией) у пациенток с минимальным РМЖ.
Анализ десятилетней безрецидивной выживаемости доказал более высокую эффективность лечения в группе больных, где применялась послеоперационная лучевая терапия.
Использование лекарственных препаратов для снижения риска заболевания называется химиопрофилактикой. На сегодняшний день одобренными препаратами для профилактики рака молочной железы являются тамоксифен и ралоксифен.
Тамоксифен может использоваться как пременопаузальными, так и постменопаузальными женщинами. Прием тамоксифена приводит к снижению риска РМЖ на 38% на более чем 10 летний период. Наиболее распространенными нежелательными явлениями на фоне приема препарата являются приливы.
В настоящее время клинические исследования изучают роль другого класса препаратов – ингибиторов ароматазы для оценки эффектов снижения риска РМЖ, которые сегодня используются только для лечения РМЖ. Предварительные результаты оказываются многообещающими. Ингибиторы ароматазы действуют только у женщин с нефункционирующими яичниками.
Профилактические хирургические операции по удалению молочных желез проводятся только в одном случае – если женщина является носителем мутаций в генах BRCA1 и BRCA2, известных как «синдром Анджелины Джоли». Мировой практикой доказано, что при удалении ткани обеих молочных желез риски РМЖ снижаются более чем на 90%. Такие операции выполняются в клиниках США и Израиля. В Европе подход к этому вопросу более консервативный.
В НМИЦ онкологии им. Н.Н. Петрова при проведении хирургического лечения женщинам с мутациями BRCA1 предлагается профилактическое удаление и реконструкция молочной железы.
«Справочник по онкологии»
Под редакцией доктора медицинских наук Б. Е. Петерсона.
Издательство «Медицина», Москва, 1964 г.
OCR Wincancer.Ru
Приведено с некоторыми сокращениями
Рак молочной железы является наиболее частой формой опухоли этого органа и встречается преимущественно у женщин. Рак молочной железы у мужчин составляет 1-2%. Частота распространения рака молочной железы на земном шаре неравномерна. В ряде стран рак молочной железы занимает первое — второе место среди всех форм рака у женщин, составляя 20—24% (США, Швеция). Заболеваемость раком молочной железы на 100 000 женского населения составляет: в США — 25; Дании — 23; Италии — 14,7; СССР — 12,3; Японии — 3,7. Заболеваемость и смертность от рака молочной железы в ряде стран за последние десятилетия возрастают.
Распространение рака молочной железы в различных районах СССР также неравномерно. На 100 000 городского населения в прибалтийских республиках в 1961 г. регистрировалось 13—14 новых заболеваний раком молочной железы; в УССР — 10,6; в РСФСР — 8,6; в республиках Средней Азии — 3,9—4,3. Отмечается более высокая заболеваемость среди женщин крупных городов по сравнению с сельским населением. Частота распространения рака молочной железы совпадает с частотой распространения предопухолевых заболеваний этого органа. К предопухолевым заболеваниям молочной железы относятся дисгормональные гиперплазии диффузного и узлового характера, объединяемые под общим названием мастопатии (фиброаденоматоза).
Большую роль в этиологии и патогенезе предопухолевых заболеваний и рака молочной железы играют дисгормональные расстройства, возникающие в результате функциональных нарушений и заболеваний в женской половой сфере, что ведет к патологической пролиферации эпителия молочных желез. К этим факторам относятся: малое число родов и последующих лактаций, непродолжительность и неполноценность последних, большое число абортов, заболевания женских половых органов и др.
Показательна в этом отношении высокая заболеваемость раком молочной железы в США и ряде стран Европы и нарастание ее в последние годы. В этих странах значительно реже вскармливают детей грудью или последнее продолжается всего 2—3 месяца. В СССР, в тех республиках, где рак молочной железы встречается редко, регистрируется значительно большая рождаемость, отмечается продолжительное повторное кормление детей грудью и очень малое число абортов.
Большое значение в этиологии рака молочных желез у мышей придается «фактору молока». Этот фактор выявлен у мышей чистых линий и передается с молоком матери. Спонтанные опухоли молочных желез у мышей этой линии в половозрелом возрасте достигают 60% и более. Ряд ученых считает этот «фактор» вирусом. Другие ученые считают его химическим веществом (отделимым от клетки белковым веществом). Так или иначе одного «фактора молока» (вируса) недостаточно для возникновения рака молочных желез у подопытных животных, и для этого необходим определенный дисгормональный фон. В эксперименте вызвать рак молочных желез у различных видов животных можно воздействием эстрогенов, канцерогенов, повторными беременностями без лактации, прижиганием соска, различными воздействиями на яичники и пр.
Во всех случаях удается проследить динамические морфологические изменения в молочных железах подопытных животных, закономерно проходящие все стадии от развития кист из расширенных молочных ходов и альвеол на фоне фиброза и гиалиноза стромы до появления пролиферации эпителия в них. Пролиферация эпителия может носить характер солидных или сосочковых разрастаний. На более поздних стадиях возникают начальные признаки злокачественного роста в виде атипии эпителия и прорыва основной мембраны с внедрением пролиферирующего эпителия в строму. Аналогичные морфологические изменения обнаруживаются при гистологическом изучении различных форм мастопатии у женщин.
Молочные железы женщин в силу своих физиологических особенностей находятся в состоянии постоянной смены и инволюции, связанной с фазами менструальных циклов и соответствующим им различным уровнем половых гормонов. На процессы пролиферации эпителия молочных желез оказывают влияние эстрогены и прогестерон, вырабатываемые яичниками и корой надпочечников, и гонадотропные гормоны передней доли гипофиза, в первую очередь фолликулостимулирующий гормон (ФСГ). В период беременности на процессы гиперплазии молочных желез большое влияние оказывают гормоны, вырабатываемые плацентой.
Деятельность желез внутренней секреции, влияющих на процессы физиологической пролиферации эпителия молочных желез, коррелируется диэнцефало-гипофизарной системой и корой головного мозга. В процессе жизни женщин встречается большое число разнообразных вредных воздействий, нарушающих эту стройную нейро-гуморальную регуляцию (аборты, воспалительные заболевания половых органов, функциональные и органические заболевания нервной системы и пр.) и ведущих к развитию дисгормональных расстройств, резкому колебанию гормонального равновесия, повышению и снижению секреции половых и гонадотропных гормонов.
Эти причины способствуют развитию фолликулярных кист, персистирующих фолликулов в яичниках, развитию ановуляторных циклов, нарушению гормонального равновесия, в первую очередь в сторону гиперэстро-генизации. Под влиянием гормональных сдвигов нарушаются процессы физиологической эволюции и инволюции в молочных железах, развиваются очаги патологической пролиферации эпителия на фоне коллагеноза и гиалиноза стромы и образования кист.
Суммируясь на протяжении многих лет, эти изменения ведут к развитию различных форм мастопатии, а в ряде случаев на их фоне развивается малигнизация.
Синонимы: мастопатия, фиброаденоматоз, мастальгия, мазоплазия, хронический кистозный мастит, болезнь Реклю, болезнь Минца, болезнь Шиммельбуша, кровоточащая молочная железа и др. Фактически эти названия отражают различные формы и стадии единого патологического — дисгормонального — процесса в молочных железах. Термин мастопатия наиболее распространен в нашей стране. Он объединяет большую группу различных по морфологическому строению, но общих по этиологии и патогенезу заболеваний молочных желез, являющихся по своему существу дисгормональными пролифератами.
Патологическая анатомия. Разделение мастопатии на диффузную и узловую формы удобно для клиницистов. При морфологическом исследовании молочных желез по поводу мастопатии это разделение не имеет значения, так как обнаруживаемые изменения идентичны для обеих форм. В основе морфологических изменений при мастопатии лежит разрастание мелких внутридольковых протоков, железистых пузырьков и соединительной ткани. При этом происходят резкое сдавление и перегибы отдельных петель одних протоков и кистозное расширение других. В дальнейшем в расширенных протоках и кистах возникает пролиферация эпителия.
При диффузной мастопатии в одной или обеих молочных железах появляются очаги уплотнения разных размеров. На разрезах они состоят из белесоватой блестящей соединительной ткани с кистами разных размеров, заполненных прозрачным, сероватым или серовато-коричневым содержимым. При микроскопическом исследовании наряду с участками нормального строения имеются резко гиперплазированные и атрофичные дольки, окруженные соединительной тканью с участками гиалиноза. Среди соединительной ткани видны кисты размерами от микроскопических до нескольких сантиметров в диаметре. Преобладание гиперплазии железистых долек, развития фиброза или кист позволяет разделить мастопатию на железистую (дольковую), фиброзную и фиброзно-кистозную формы.
В некоторых кистах эпителий становится высоким цилиндрическим с очень светлой эозинофильной протоплазмой (апокринизация эпителия), иногда он располагается в несколько слоев. В других кистах пролиферирующий эпителий вместе со стромой образует ветвящиеся сосочки — так называемые внутрипротоковые папилломы. При отрыве их возникает кровотечение, причем кровь выделяется через сосок («кровоточащая молочная железа»). Пролиферирующий эпителий выполняет протоки и кисты, образуя солидные скопления и так называемые криброзные структуры (железистоподобные ходы среди эпителиальных тяжей), папилломатозные разрастания. Появление выраженных явлений пролиферации в протоках и кистах дает основание выделить особую форму мастопатии — пролиферативную, которая может встречаться при железистой, фиброзной и фибрознокистозной мастопатии.
Интенсивная внутрипротоковая пролиферация эпителия, образование внутрипротоковых папиллом, формирование криброзных структур указывают на тенденцию мастопатии к малигнизации и поэтому расцениваются как предраковое состояние. Появление полиморфизма эпителия, фигур атипических митозов, гиперхроматоз ядер, базофилия цитоплазмы являются морфологическим проявлением малигнизации. Нарушение целостности базальных мембран и прорастание эпителия в окружающую соединительную ткань расцениваются морфологами как начало рака.
Наиболее выраженные процессы пролиферации эпителия обычно обнаруживают при микроскопическом исследовании тех участков молочных желез, которые до операции имели более четкие уплотнения и диагностировались клиницистами как узловая форма мастопатии.
При операции по поводу мастопатии хирург обычно обнаруживает, помимо узлового образования, диффузное уплотнение ткани железы и наличие большего или меньшего числа кист, что свидетельствует о диффузной мастопатии, на фоне которой появилось уплотнение узлового характера. Именно в этом участке и имеются более далеко зашедшие процессы пролиферации. Практически при операции по поводу узловой мастопатии почти никогда не удается произвести иссечение в пределах здоровых на глаз тканей.
В некоторых случаях на фоне диффузной мастопатии в одной из крупных кист или в расширенном протоке может образоваться внутрипротоковая или внутрикистозная папиллома, которая иногда достигает размеров, видимых невооруженным глазом. Появление таких папиллом ведет к клиническому симптому кровянистых выделений из соска или обильному истечению серозной жидкости.
Клиника мастопатии (фиброаденоматоза). Клинически различают две формы мастопатий: диффузную и узловую. Такое деление заболевания удобно, так как оно определяет терапевтическую тактику врача. Диффузная мастопатия является начальной стадией заболевания. Клинические проявления заболевания: болезненные набухания молочных желез, усиливающиеся в предменструальном периоде; выделения из сосков: серозные, типа молозива, грязно-зеленоватые, бурые и др.; при пальпации молочных желез определяется грубая дольчатость, тяжистость и мелкая зернистость, выраженные неравномерно в одной или обеих молочных железах. Наиболее часто эти изменения обнаруживаются в верхненаружных квадрантах молочных желез.
Боли, уплотнения в молочных железах и выделения из сосков при диффузной мастопатии бывают непостоянны и могут периодически усиливаться и уменьшаться. С течением времени болевые ощущения становятся менее интенсивными. На первый план выступают более ограниченные уплотнения, локализующиеся в одном или нескольких участках одной и той же или обеих молочных железах. Определяется увеличение и более четкое отграничение уплотнений в предменструальных периодах и уменьшение вплоть до полного исчезновения их с началом менструации.
Узловая мастопатия является следующей стадией заболевания. Узловая мастопатия характеризуется появлением постоянных очагов уплотнения в одной или обеих молочных железах. При захвате мастопатических узлов между пальцами в вертикальном положении больных они определяются более четко. При исследовании в положении лежа уплотнения исчезают или определяются не так отчетливо. Симптом Кенига отрицательный ( а) Исследование уплотнения или опухоли в молочной железе при захватывании их между пальцами и при прижатии ладонью к грудной стенке дает одинаково четкое ощущение опухоли — симптом Кенига положительный, б) Исследование уплотнения или опухоли в молочной железе при захватывании их между пальцами дает четкое ощущение узла, а при прижатии ладонью к грудной стенке опухоль исчезает — симптом Кенига отрицательный).
Как правило, кожа над мастопатическими узлами свободно подвижна, симптом морщинистости или втяжения кожи отсутствует. Пальпация молочных желез и мастопатических узлов менее болезненна, чем при диффузной форме. В области мастопатических узлов могут определяться более плотные участки, вплоть до хрящевой консистенции, выступающие в виде «шипиков». Такие участки могут служить указанием на развившуюся малигнизацию, и при появлении их необходимо производить операцию со срочным гистологическим исследованием. Так как узловая форма мастопатии возникает на фоне предшествующей диффузной, то могут иметь место и признаки последней: грубая дольчатость, зернистость и болезненность молочных желез вне узла, наличие выделений из сосков.
По отношению к мастопатии принято применять термин «предрак». Однако далеко не все формы мастопатии являются предраковыми. К предраковым формам мастопатии могут быть отнесены те формы, когда при гистологическом исследовании выявляются резко выраженные явления пролиферации эпителия в кистах и расширенных протоках. Те больные, у которых при гистологическом исследовании выявлены предраковые изменения, должны находиться под особенно тщательным динамическим наблюдением онкологов.
Лечение. При диффузной форме мастопатии допустимо наблюдение за больными и проведение консервативной терапии. Часто мастопатия развивается на фоне хронических воспалительных заболеваний придатков и матки и сопровождается функциональными расстройствами нервной системы. Выявление этого фона, лечение гинекологических заболеваний и укрепление нервной системы могут повести к значительному улучшению в течении мастопатии.
При самых начальных формах мастопатии, типа мастальгии, в ряде случаев под наблюдением опытного онколога допустимо применение легких физиотерапевтических процедур: ионтофорез с йодистым калием или новокаином, ретромаммарная новокаиновая блокада, легкие тепловые процедуры. К этим мероприятиям следует прибегать очень осторожно при полной убежденности в отсутствии явлений активной пролиферации эпителия. В этих же случаях больным могут быть даны советы о нормализации половой жизни, необходимости иметь беременность, роды и обязательное кормление ребенка грудью не менее года.
При далеко зашедших стадиях диффузной формы мастопатии и в тех случаях, когда перечисленные мероприятия не оказывают терапевтического эффекта, рекомендуется проведение лекарственной или гормональной терапии.
1. Лечение витаминами, с целью улучшения функции печени, принимающей участие в инактивации избытка эстрогенов, которые могут быть повышены у больных мастопатией. Рекомендуется применение витаминов A, B1 и Е в виде стандартных препаратов внутрь или путем инъекций в течение месяца, иногда повторно.
2. Лечение микродозами йодистого калия направлено на нормализацию лютеиновой функции яичников, нередко сниженную у больных мастопатией в связи с наличием персистирующих фолликулов или фолликулярных кист и ановуляторных циклов. Назначается 0,25% раствор йодистого калия, 1—2 чайные ложки 1 раз в день. Лечение проводится в межменструальнем периоде на протяжении 6—12 месяцев.
3. Лечение андрогенами направлено на подавление эстрогенной активности яичников в тех случаях, когда она оказывается повышенной. Контролем служит характер влагалищных мазков. Можно применять инъекции тестостерон-пропионата или неодроля, 25 мг через день внутримышечно, в течение нескольких межменструальных периодов, до получения стойкого терапевтического эффекта. Инъекции андрогенов можно заменить приемом препаратов в виде таблеток, закладываемых под язык. С этой целью применяются препараты метилтестостерон или метиланростендиол, 25—30 мг в день (2 таблетки 2—3 раза в день под язык). Лечение проводится до получения стойкого терапевтического эффекта на протяжении нескольких межменструальных периодов.
Консервативная терапия допустима лишь при диффузной форме мастопатии. При появлении на фоне диффузной мастопатии более четких уплотнений в молочных железах, не исчезающих с началом менструаций, следует производить секторальную резекцию с обязательным срочным гистологическим исследованием.
Секторальная резекция должна проводиться достаточно широко, так, чтобы был удален весь сектор молочной железы, в котором определяется узловое уплотнение, с кожей и ретромаммарной клетчаткой. Узел должен располагаться в центре иссекаемого сектора. Нередко в момент операции выявляется наличие диффузного уплотнения почти всей молочной железы и большое количество мелких кист. Памятуя о том, что наиболее далеко зашедшие процессы пролиферации локализуются в области узлового уплотнения, допустимо иссекать лишь сектор, в котором расположен узел, оставляя те участки, в которых изменения носят диффузный характер.
Однако в этих случаях вслед за секторальной резекцией следует подвергнуть больную той или иной консервативной терапии с целью воздействия на остающиеся патологические участки в молочной железе. Секторальная резекция при узловой мастопатии является одновременно лечебным и диагностическим мероприятием. В ряде случаев при секторальной резекции молочной железы при срочном гистологическом исследовании выявляются предраковые изменения или рак.
Следует во всех случаях проводить секторальную резекцию молочной железы по поводу узловой мастопатии со срочным гистологическим исследованием. В тех случаях, когда срочное гистологическое исследование обеспечено быть не может, лучше направить больную в то учреждение, где это возможно. Даже самые опытные онкологи не всегда могут макроскопически поставить правильный диагноз.
Секторальная резекция не излечивает больных окончательно. При операции удаляют лишь участок молочной железы, в котором процесс патологической пролиферации зашел наиболее далеко. Появление новых мастопатических узлов в той же молочной железе или в другой и даже развитие рака через несколько лет после операции не так редки. Развитие рака в молочных железах после секторальной резекции по поводу мастопатии, по данным различных автороз, колеблется от 3 до 10%.
Больные мастопатией должны состоять на учете и находиться под наблюдением онкологов, которым надлежит осматривать их не менее 1—2 раз в год. В промежутке между врачебным осмотром больные должны раз в месяц осматривать и ощупывать свои молочные железы сами. При обнаружении изменений, которых ранее не отмечалось (увеличение и более четкие контуры уплотнений, появлений втяжения кожи, появление кровянистых выделений из соска), больная должна обратиться к наблюдающему ее врачу, не ожидая назначенного срока.
Такое динамическое наблюдение за больными мастопатией является существенным фактором для выявления ранних форм рака молочной железы. Своевременное лечение мастопатии является профилактикой развития рака молочной железы.
Фиброаденома молочной железы является одной из форм узловых дисгормональных пролифератов. Фиброаденомы встречаются в более молодом возрасте, чем мастопатия, нередко у совсем молодых девушек. Наиболее часто фиброаденомы встречаются в возрасте 20—40 лет. В молочной железе появляется плотный, округлый, безболезненный, свободноподвижный опухолевидный узел.
Узлы фиброаденом имеют обычно гладкую поверхность, четко контурируются от окружающих участков молочной железы, не имеют признаков спаяния с кожей. При исследовании больных в положении лежа фиброаденомы не исчезают — симптом Кенига (ладони) положителен. Фиброаденомы могут быть различных размеров, вплоть до гигантских. Нередко встречаются множественные фиброаденомы в одной и той же или обеих молочных железах. Фиброаденомы часто возникают на фоне диффузной мастопатии. Диагноз фиброаденомы поставить легче, чем мастопатии или рака. Малигнизация в фиброаденомах возникает реже, чем в мастопатических узлах (не превышает 1%).
Макроскопически фиброаденомы представляют собой округлые, четко отграниченные узлы. По микроскопическому строению различают: а) периканаликулярные фиброаденомы, состоящие из железистых каналов, выстланных кубическим эпителием, окруженных новообразованной соединительной тканью, богатой клетками; б) интраканаликулярные фиброаденомы, характеризующиеся разрастанием соединительнотканных тяжей, сдавливающих железистые канальцы, превращая их в узкие щели с отходящими в стороны отростками.
В особую группу выделяются листовидные фиброаденомы, которые обладают характерным макроскопическим видом; по микроскопическому строению они являются смешанными пери-интраканаликулярными структурами.
Пролиферация эпителия в узлах фиброаденом встречается значительно реже, чем при мастопатии, малигнизация фиброаденом развивается не чаще чем в 1%. При длительном существовании фиброаденомы она может перейти в рак или фибросаркому, что наблюдается очень редко.
Лечение фиброаденом в основном хирургическое. Не следует производить вылущивания фиброаденом, особенно когда фиброаденомы развиваются на фоне мастопатии, так как вылущивание их может усилить процесс пролиферации в остающихся мастопатических участках. В случае диагностической ошибки вылущивание ракового узла, принятого за фиброаденому, может способствовать генерализации процесса. Операцию при фиброаденомах следует проводить по типу секторальной резекции, однако последняя может носить несколько более экономный характер, чем при мастопатии. В случаях сочетания фиброаденомы с диффузной мастопатией после секторальной резекции следует проводить консервативное лечение по поводу мастопатии.
Патологическая анатомия. Макроскопически различают: а) узловатый рак; б) диффузный рак; в) болезнь Пэджета. Узловатый рак представляет собой бледно-серый или сероватожелтый нечетко контурируемый плотный узел, на разрезе имеющий зернистую поверхность с желтоватыми крапинками. При надавливании может выделяться в виде червеобразных слепков детрит, состоящий из погибших раковых клеток Опухолевый узел обычно расположен среди белесоватой ткани молочной железы (на фоне мастопатии). Иногда раковые узлы имеют более мягкую консистенцию, хорошо контурируются.
Диффузный рак в виде серовато-желтых плотных тяжей или инфильтрата занимает большую часть или всю молочную железу. К диффузным относятся: инфильтрагивно-отечные, маститоподобные, эризипелоидные и панцирные формы. Макроскопически различают раки, происходящие из протоков, долек, рак Пэджета и редкие формы.
Рак протоков и долек может обладать инфильтративным и неинфильтративным характером роста. К неинфильтративным относятся внутрипротоковые и дольковые раки. Инфильтративные раки в зависимости от степени развития и характера стромы делятся на солидные и скиррозные формы. К инфильтративным относятся также железистоподобные, криброзные, коллоидные, или слизистые, раки.
Редкие формы рака: рак из апокринизированного эпителия, так называемые плоскоклеточные раки, и «воспалительноподобные формы» (эризипелоидные, маститоподобные, инфильтративно-отечные, панцирные).
Особую форму представляет рак Пэджета, развивающийся из эпителия крупных выводных протоков, проходящих через сосок. Гистологически он характеризуется наличием крупных светлых клеток, так называемых клеток Пэджета; в дальнейшем возникает картина типичного солидного рака.
Метастазирование рака молочной железы в первую очередь происходит по лимфатическим путям. Отдаленные метастазы развиваются при попадании раковых клеток с током лимфы в кровеносное русло или могут развиваться первично гематогенным путем. Наиболее частой локализацией метастазов рака молочной железы является; лимфатические узлы подмышечной, подлопаточной, подключичной и надключичной областей, загрудинные лимфатические узлы.
Чаще поражаются лимфатические узлы той же стороны, что и молочная железа, но могут быть поражены лимфатические узлы противоположной стороны (перекрестные метастазы); отдаленные метастазы локализуются наиболее часто в костях, легких, плевре, яичниках, печени, головном мозгу и в любых других органах и тканях. Микроскопическое строение метастазов обычно соответствует строению первичной опухоли, однако метастазы отличаются меньшей дифференциацией.
Клиника. Клинически различают несколько форм рака молочной железы; а) узловатую, б) диффузную, в) болезнь Пэджета. Наиболее частой формой рака молочной железы является узловатая. Клиническим проявлением этой формы является появление плотного узла в том или ином участке молочной железы. Наиболее часто поражаются верхненаружные квадранты. Поражение правой и левой молочных желез встречается почти одинаково часто.
Клинические признаки ранних форм рака молочной железы:
1) наличие четко определяемого узла в молочной железе;
2) плотная консистенция опухоли;
3) ограниченная подвижность опухоли в молочной железе;
4) наличие кожных симптомов (патологической морщинистости или втяжения кожи над опухолью, определяемые при сдвигании кожи над опухолью);
5) безболезненность опухоли;
6) наличие одиночного или нескольких плотных округлых узелков в подмышечной впадине той же стороны, метастатической природы.
Клинические признаки поздних стадий рака молочной железы:
1) заметное на глаз втяжение кожи в месте определяемой опухоли молочной железы — симптом умбиликации;
2) явления лимфостаза — симптом лимонной корки над опухолью или за ее пределами;
3) изъязвление или прорастание кожи опухолью;
4) утолщение соска и складки ареолы (симптом Краузе);
5) втяжение, фиксация соска;
6) большие размеры опухоли;
7) деформация молочной железы: уменьшение или увеличение размеров, подтягивание вверх, фиксация к грудной стенке;
8) большие метастатические, неподвижные узлы в подмышечной впадине той же стороны;
9) надключичные метастазы с той же стороны или перекрестные подмышечные н надключичные метастазы с противоположной стороны;
10) боли в молочной железе;
11) отдаленные метастазы, выявляемые клинически или рентгенологически, и симптоматика, им соответствующая.
Диффузные формы рака молочной железы. Эризипелоидный — рожистоподобный — рак молочной железы встречается редко. Отличается быстрым течением, трудно поддается лечению. Характеризуется диффузным покраснением кожи молочной железы и быстрым распространением покраснения кожи за пределы молочной железы на грудную стенку. Кожная температура может быть несколько повышена. Молочная железа диффузно, умеренно уплотнена, слегка болезненна, определяются увеличенные плотные регионарные лимфатические узлы.
Маститоподобная форма встречается так же редко, как и предыдущая. Характеризуется диффузным уплотнением всей молочной железы, увеличением ее размеров, небольшой гиперемией кожи, болезненностью, наличием регионарных метастазов. Течение заболевания быстрое. Прогноз плохой.
Болезнь Пэджета встречается в 0,5—5% всех случаев рака молочной железы. Начинается с покраснения и утолщения соска, появления сухих и мокнущих корочек и струпиков. При отпадении последних обнаруживается влажная, зернистая поверхность. Процесс медленно распространяется на ареолу. Постепенно сосок уплощается, изъязвляется, процесс распространяется на кожу молочной железы за пределы ареолы. Одновременно идет распространение процесса по крупным протокам в глубь молочной железы. Позже присоединяются метастазы в подмышечные лимфатические узлы. В начале заболевания болезнь может быть принята за экзему или псориаз. Цитологическое исследование мазка с изъязвленной поверхностью помогает правильной диагностике.
Клиническая классификация рака молочной железы по стадиям. Выбор метода лечения и прогноз заболевания при раке молочной железы зависят от клинической классификации и стадии заболевания. Рак молочной железы принято делить на четыре стадии. По новой международной классификации при определении стадии заболевания учитывается степень распространения процесса в молочной железе, регионарных лимфатических узлах и наличие отдаленных метастазов.
Т — первичная опухоль.
T1 — опухоль не более 2 см, отсутствует поражение кожи, соска (исключая болезнь Пэджета) и фиксация к грудной стенке.
Т2 — опухоль размером 2—5 см, наличие ограниченного втяжения или морщинистости кожи, ретракция соска при субареолярном расположении опухоли, болезнь Пэджета, распространяющаяся за пределы соска.
Т3 — опухоль размером 5—10 см или поражение кожи в той или иной форме — сращение с опухолью, изъязвление, инфильтрация, симптом лимонной корки или фиксация к грудной мышце.
Т4 — опухоль более 10 см или поражение кожи в той или иной форме, превосходящее размеры опухоли, но в пределах молочной железы или фиксация молочной железы к грудной стенке.
N — регионарные лимфатические узлы.
N0 — подмышечные лимфатические узлы не прощупываются.
N1 — прощупываются плотные подмышечные узелки, смещаемые.
N2 — подмышечные лимфатические узлы больших размеров, спаяны, ограниченно подвижны.
N3 — односторонние надключичные лимфатические узлы или отек руки.
М — отдаленные метастазы.
М0 — отдаленные метастазы отсутствуют.
М + отдаленные метастазы; поражение кожи за пределами молочной железы, метастазы в лимфатических узлах противоположной стороны, метастазы в другой молочной железе, метастазы в костях, легких, плевре, печени и других органах, выявляемые клинически или при рентгенологическом обследовании.
Стадия 1: T1, N0, М0, Т2, N0, М0
Стадия II: Т1, N1, М0, Т2, N1, М0.
Стадия III: T1, N2, М0, T1N3M0, T2N2M0, T3N0M0, T3N1M0, T3N1M0, T3N2M0, T3N3M0, T4N0M0, T4N1M0, T4H3M0
Стадия IV — любое сочетание Т, N и М.
Введение новой международной номенклатуры дает возможность детализировать поражение, учитывая как размеры опухоли, так и поражение лимфатической системы и отдаленное метастазирование. Введение этой классификации обеспечивает более точную оценку отдаленных результатов и возможность сравнения различных методов терапии, применяемых как отечественными, так и зарубежными авторами.
Диагностика. Диагностика рака молочной железы основывается на клинических данных и данных дополнительных методов обследования: аспирационной биопсии с цитологическим исследованием, биопсии со срочным гистологическим исследованием маммографии. К дополнительным методам обследования обычно следует прибегать при начальных стадиях заболевания. Установить диагноз рака молочной железы II и более поздних стадий удается на основании клинической картины.
В анамнез должны входить акушерско-гинекологические данные. При осмотре нужно обращать внимание на размеры и форму молочных желез, уровень стояния сосков, дефюрмацию молочной железы, состояние кожи, соска и ареолы. Вслед за осмотром производится пальпация, причем следует одинаково тщательно прощупать обе молочные железы. Вначале ощупывание молочных желез производится в положении больных стоя.
Изучается состояние сосков и ареол, утолщение или уплотнение, наличие или отсутствие выделений из сосков, их характер. Осторожно собирая кожу молочной железы в складки, выявляют наличие или отсутствие кожных симптомов — патологической морщинистости или умбиликации. После поверхностной пальпации производят более глубокое изучение состояния молочных желез.
При этом ткань молочных желез захватывают между пальцами последовательно во всех отделах, а также производят исследование кончиками пальцев. Это дает возможность выявить ограниченный участок уплотнения или опухоль в молочной железе.
После обнаружения уплотнения или опухоли этот участок молочной железы придавливают ладонью к грудной стенке (удобнее при этом стоять сзади от больной). Если уплотнение при этом приеме исследования не исчезает, то это свидетельствует о наличии рака или фиброаденомы. В положении больной стоя определяются: форма, размеры, консистенция, поверхность, отношение опухоли к окружающим тканям, подвижность ее, болезненность. После исследования в вертикальном положении больную следует уложить на кушетку и повторить исследование в положении лежа на спине в той же последовательности. Уменьшение или исчезновение уплотнения свидетельствует в пользу доброкачественной его природы. Этот симптом носит название симптома Кенига или ладони.
После осмотра и пальпации молочных желез производят осмотр и пальпацию подмышечных, подключичных и надключичных областей обеих сторон с целью выявления возможных метастазов в лимфатические узлы. Если проведенное обследование не дает уверенности в диагнозе доброкачественного процесса или рака, то следует подвергнуть больных дополнительным методам исследования.
Аспирационная биопсия и цитологическое исследование дают возможность установить диагноз рака молочной железы в 80—85% случаев. При этом исследовании могут быть выявлены атипичные клетки, комплексы клеток, принадлежность их к злокачественному новообразованию, иногда может быть определена гистологическая форма опухоли. Отрицательный ответ при цитологическом исследовании не исключает диагноза рака, который должен ставиться по всей совокупности клинических признаков и данных дополнительных методов исследования. Цитологическому исследованию подвергаются материалы, полученные при пункции участков уплотнений или опухолевых узлов в молочной железе, выделения из сосков, отпечатки с изъязвленных участков.
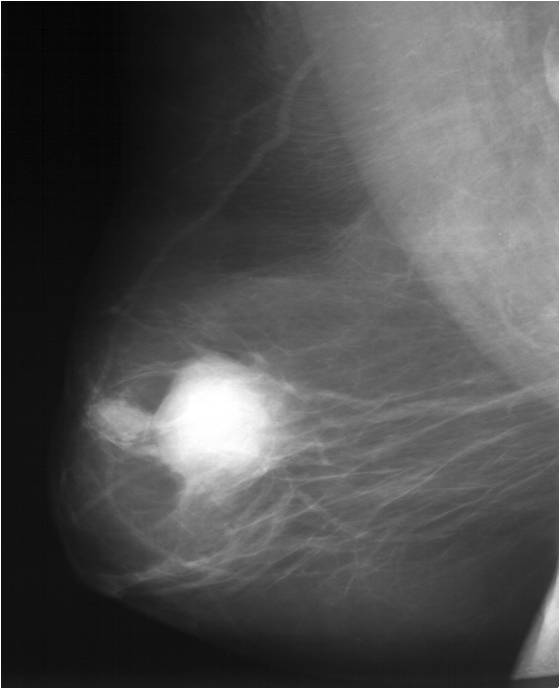
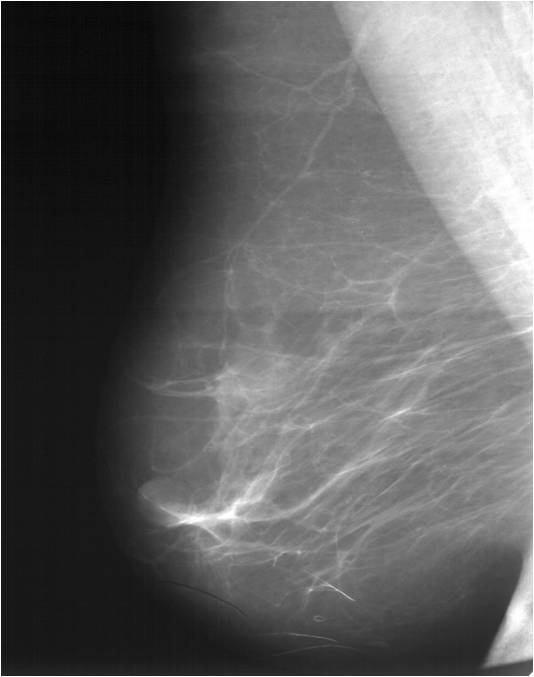
В некоторых случаях диагностике помогает маммография. Различают контрастную и бесконтрастную маммографию. При контрастной маммографии вводят контрастный раствор в выводное отверстие на соске, из которого определяют вытекание жидкости. Иголка должна иметь притупленный кончик, чтобы не повредить протока. Вводят иглу на глубину 1—3 см. В качестве контрастного вещества применяется преимущественно 40% раствор сергозина. После введения контраста производится рентгенография молочной железы в двух проекциях. Метод исследования позволяет выявить локализацию расширенного протока или кисты, из которых выделяется патологический секрет. Это дает возможность производить секторальную резекцию в тех случаях, когда при наличии выделений из соска не прощупывается четкого уплотнения в молочной железе.
Маммография простая или бесконтрастная производится в двух проекциях, в положении больной лежа на спине и на боку. Производятся рентгеновские снимки обеих молочных желез. При раковых опухолях определяется тень с наличием лучистых тяжей в окружающие ткани. При мастопатии определяется диффузное, тяжистое затемнение с мелкими очагами просветления (кистами), узлы фиброаденом дают четко ограниченные округлые затемнения. В случаях, подозрительных на рак молочной железы, когда клиническое обследование, цитологическое исследование, маммография не дают уверенности в диагнозе, следует прибегать к биопсии со срочным гистологическим исследованием.
Биопсия при раке молочной железы должна проводиться по типу секторальной резекции. Подозрительный на рак участок молочной железы иссекают вместе с кожей через всю толщу тканей до большой грудной мышцы, отступя на 3—4 см от определяемых пальпаторно границ узла. Разрез радиарный — от края ареолы до основания молочной железы. После иссечения пораженного сектора при подозрении на рак хирург должен рассечь более плотный участок и по его виду в большинстве случаев удается установить диагноз.
Для рака характерны следующие признаки: нечеткие контуры уплотнения или узла, распространение в окружающую ткань в виде тяжей, западение поверхности разреза, сохранение острой грани при рассечении уплотнения (симптом сыра), розовато-сероватый цвет с желтоватыми вкраплениями (симптом спелой груши), плотная до хрящевой консистенция. Однако пои различном гистологическом строении раковой опухоли эти признаки полностью или частично отсутствуют, и поэтому диагноз должен во всех случаях подтверждаться срочным гистологическим исследованием или цитологическим исследованием отпечатка или соскоба с поверхности рассеченного узла.
При получении гистологического ответа о наличии рака следует немедленно произвести радикальную мастэктомию. В случаях, когда срочного гистологического исследования произвести нельзя, а клинически нет подозрения на рак, ответ должен быть получен не позже чем через 2 дня; более долгий разрыв между секторальной резекцией и радикальной мастэктомией пои выявлении рака недопустим, так как может отягчить течение, заболевания и ухудшить отдаленный результат. При невозможности срочного или быстрого гистологического исследования больных нужно направлять для секторальной резекции в те лечебные учреждения, где это возможно произвести.
При редких формах рака (эризипелоидная, маститоподобная) с целью диагностики допустима «инцизионная биопсия». Производится иссечение пластинки по типу лимонной дольки из наиболее плотного участка молочной железы или измененного участка кожи. В место иссечения кусочка из опухолевого инфильтрата вкладывают марлевую салфетку, пропитанную 10% раствором формалина или спиртом. При получении гистологического заключения о наличии рака немедленно производят радикальную мастэктомию.
Дифференциальная диагностика. Кроме предопухолевых заболеваний и рака молочной железы, дифференциальная диагностика между которыми описана выше, в молочных железах могут встречаться и другие патологические процессы и опухоли. Липомы молочной железы встречаются редко, имеют нечеткие, расплывчатые контуры, мягки на ощупь, не имеют уплотнений в центре, что характррно для небольших раковых опухолей типа скирра.
Липогранулемы молочной железы встречаются редко. Возникают вследствие бывших травм или ограниченных воспалительных процессов, а также после проводившихся ранее по какому-либо поводу инъекций в молочную железу (антибиотики, новокаин). Липогранулемы не имеют четких границ, положительный симптом втяжения кожи над ними может симулировать ранние стадии скирра. Дифференциальная диагностика уточняется данными цитологического или гистологического исследования.
Крупные одиночные кисты, достигающие больших размеров, могут иногда симулировать раковые опухоли, так как обладают внешними признаками последних. Пункция, отсасывание содержимого кисты и цитологическое исследование могут облегчить дифференциальный диагноз. Если после отсасывания содержимого кисты и цитологического исследования, не подтверждающего пролиферации эпителия, уплотнение уменьшается или исчезает, врач не должен снижать онкологической настороженности, а должен оставить больную под строгим динамическим наблюдением или подвергнуть патологический очаг секторальной резекции со срочным гистологическим исследованием, так как в стенках крупных кист нередко могут развиваться процессы малигнизации.
Галактоцеле напоминает крупные кисты, развивается в период лактации и может существовать долго после ее окончания. Анамнез помогает дифференциальной диагностике; окончательное уточнение диагноза основывается на данных пункции цитологического или гистологического исследования (биопсии).
Ангиомы молочной железы встречаются редко, не имеют четких границ, уменьшаются при сдавлении. При поверхностном расположении имеют типичную голубоватую окраску или типичный багровый цвет. Значительные затруднения в диагностике возникают при туберкулезе и актиномикозе в молочных железах. Два последних заболевания встречаются в настоящее время редко. Анамнестические данные помогают диагнозу. Исследование отделяемого из свищей или содержимого, полученного при пункции, может выявить туберкулезные палочки или друзы актиномикоза.
Туберкулез молочной железы в запущенных стадиях с образованием холодных гнойников и типичными свищами при современной организации фтизиатрической службы представляет исключительную редкость. Начальные формы туберкулеза молочной железы и специфического подмышечного лимфаденита могут быть диагностированы при цитологическом исследовании или при биопсии с гистологическим исследованием.
Сифилис молочной железы встречается редко. Анамнез и серологические исследования крови в подозрительных случаях помогают направить мысль врача по правильному пути. Значительные трудности возникают при дифференциальной диагностке эризипелоидного и маститоподобного рака от острых воспалительных процессов. В этих случаях диагностические ошибки и следующее за ними неправильное лечение могут оказаться роковыми для больных. Особенно трудной стала диагностика этих форм рака в последнее время, так как широкое применение антибиотиков затушевывает клиническую картину острых воспалительных процессов и ведет к вялому течению маститов.
Острое начало, подъем температуры, сильные боли в начале заболевания, совпадение его с периодом лактации позволяют поставить дифференциальный диагноз. Если современные методы терапии острого мастита (новокаиновая ретромаммарная блокада, масляно-бальзамические повязки, противовоспалительные дозы рентгенотерапии и лечение антибиотиками), применяемые в течение нескольких дней, не снимают картины острого воспалительного процесса, то следует более детально обследовать больных, провести пункционную биопсию с цитологическим исследованием. При вскрытии предполагаемых гнойников обязательно нужно взять ткань из наиболее плотных участков для гистологического исследования.
Саркома молочной железы встречается редко, составляя 1— 3% к общему числу опухолей молочной железы. Отличается очень быстрым ростом, большими размерами, крупно-бугристой поверхностью, неравномерной плотностью, истончением, как бы растянутой кожей над опухолью, расширением подкожных вен молочной железы, легкой гиперемией кожи, отсутствием увеличенных подмышечных лимфатических узлов при больших размерах опухоли.
Дифференциальная диагностика при наличии указанных признаков нетрудна. Лечебная тактика та же, что и при раке, поэтому диагностические ошибки практически не имеют значения.
Лечение. Лечение рака молочной железы включает ряд последовательных мероприятий, поэтому обозначается как комбинированное или комплексное. В план лечения вводят: хирургические, лучевые, гормональные и химиотерапевтические методы. План лечения вырабатывается индивидуально для каждой больной в зависимости от стадии заболевания, местного распространения процесса, наличия регионарных и отдаленных метастазов, возраста, менструального цикла, общего состояния, связанного с распространением процесса или сопутствующими заболеваниями.
В зависимости от стадии заболевания могут быть рекомендованы различные схемы терапии. При I, И, III стадиях, когда процесс локализуется в молочной железе и регионарных лимфатических узлах, план лечения должен включать: а) оперативное удаление первичного очага и доступных регионарных метастазов, что достигается радикальной мастэктомией; б) профилактические мероприятия, направленные на предупреждение возникновения рецидива и отдаленных метастазов (лучевая терапия, гормонотерапия, химиотерапия).
В IV стадии заболевания при неоперабильных раках молочной железы, при рецидивах, локальном или генерализованном метастазировании лечение значительно сложнее и менее перспективно. В этих случаях на первый план выступает гормонотерапия, применение противоопухолевых химиотерапевтических препаратов или лучевая терапия. Комбинированная терапия рака молочной железы является наиболее распространенным методом при I, II, III стадиях заболевания. Она включает радикальную мастэктомию и послеоперационную лучевую терапию. Предоперационная рентгенотерапия обязательна при III стадии, но может быть применена и при II стадии, особенно у молодых женщин, у которых течение заболевания носит более злокачественный характер.
Хирургические методы лечения. Секторальная резекция. Техника операции описана выше. Показания: категорический отказ больной от радикальной операции, наличие множественных отдаленных метастазов при небольших размерах первичной опухоли, общие противопоказания к радикальной мастэктомии в связи с преклонным возрастом или сопутствующими заболеваниями. В тех случаях, когда при раке молочной железы произведена лишь секторальная резекция, необходимо вслед за ней проводить лучевую терапию, гормональную терапию или химиотерапию.
Простая мастэктомия (ампутация молочной железы) имеет те же показания, что и секторальная резекция. Операция заключается в ампутации молочной железы с фасцией большой грудной мышцы и клетчаткой подмышечной впадины, если в последней определяются увеличенные лимфатические узлы. После ампутации молочной железы обязательно проведение лучевой и гормональной терапии.
Радикальная мастэктомия — наиболее часто применяемая операция при раке молочной железы. Принцип операции заключается в удалении молочной железы единым блоком с большой и малой грудной мышцами и клетчаткой подключичной, подмышечной и подлопаточной областей. В зависимости от локализации опухоли кожный разрез варьируют, при этом следует отступить от ощутимых краев опухоли не менее чем на 5 см. Наиболее типичным разрезом является овальный, начинающийся вверху от границы наружной и средней трети ключицы, окаймляющий молочную железу с обеих сторон и заканчивающийся у края реберной дуги до сосковой линии. Кожные лоскуты отсепаоовываются медиально до середины грудины, латерально до задней аксиллярной линии, вверх до ключицы и вниз до середины подложечной области. Отсепаровка кожных лоскутов проводится в слое поверхностной фасции, на коже остается слой клетчатки не более 0,5 см.
После отслойки кожных лоскутов производится пересечение большой и малой грудных мыши возможно ближе к местам их прикреплений. При пересечении большой грудной мышцы сохраняется часть ее волокон, прикрепляющихся к ключице, для предотвращения срастания сосудистого подключичного пучка с кожным рубцом. Следующим этапом производится удаление клетчатки вдоль сосудистого пучка. Выделение начинается от места перекрещивания подключичной вены с ключицей. Тщательно выделяют все мелкие артерии и вены, пересекают между зажимами и перевязывают кетгутом.
Клетчатку удаляют последовательно вдоль сосудов из подключичной, подмышечной и подлопаточной областей, вместе с заложенными в ней лимфатическими узлами, вниз по направлению к молочной железе. Выделение латерально производят до края широкой мышцы спины, осторожно снимают фасцию, покрывающую переднюю зубчатую мышцу и верхнюю часть прямой мышцы живота, и пересекают волокна большой и малой грудной мышцы в местах начала их от грудной стенки.
В последний момент отсекают волокна большой грудной мышцы вдоль края грудины. Прободающие сосуды из внутренней грудной артерии захватывают зажимами и перевязывают кетгутом. Проводят тщательный гемостаз с помощью электрокоагуляции и кетгутовых лигатур; рану орошают 96° спиртом или противоопухолевым препаратом и края ее ушивают шелком. Через контрапертуру, по средней аксиллярной линии, в подлопаточную и аксиллярную области вводят резиновый дренаж на 1—2 суток.
Желательно присоединить дренаж к отсосу, в этом случае его следует держать до 5 суток. Если при ушивании краев раны происходит натяжение, то следует произвести послабляющие надсечки в шахматном порядке на кожных лоскутах в зоне натяжения или произвести пластику свободным кожным лоскутом. В далеко зашедших случаях кожный разрез и отсепаровку лоскутов рекомендуется производить электрохирургическим ножом.
Расширенная радикальная мастэктомия с удалением парастернальных лимфатических узлов (подмышечно-грудинная мастэктомия) показана при локализации опухоли во внутренних и центральных отделах молочной железы, когда парастернальные лимфатические узлы могут являться первым этапом метастазирования. Вначале операция проводится так же, как радикальная мастэктомия, но отсечение препарата проводится лишь до линии прикрепления волокон большой грудной мышцы к хрящевой части II—V ребер и края грудины. Удаляемую молочную железу с мышцами изолируют полотенцем и производят резекцию грудной стенки в виде пластинки, включающей край грудины, хрящи II—V ребер, соответствующие им межреберные мышцы и располагающуюся позади них клетчатку вместе с отрезком внутренней грудной артерии и лимфатическими узлами вдоль нее.
Центральный и периферический концы внутренней грудной артерии предварительно лигируют шелковыми лигатурами. Резекцию производят очень осторожно, желательно при этом не повредить плевру. Проводят тщательный гемостаз. Резецированный участок грудной стенки убирают единым блоком с молочной железой, мышцами и клетчаткой. Образовавшийся дефект в грудной стенке укрывают медиальным участком ключичной части большой грудной мышцы, свободной пересадкой куска широкой фасции бедра или аллопластическим протезом.
К расширенным радикальным мастэктомиям следует прибегать с большой осторожностью. Следует учитывать общее состояние больных, локализацию процесса, возраст и пр. Операции могут производиться при современном общем обезболивании с управляемым дыханием и соответствующим послеоперационным уходом. Вопрос о целесообразности расширенной подмышечно-грудинной мастэктомии широко дебатировался на VIII Международном противораковом конгрессе, однако точных критериев для показаний к этой операции не установлено. Операция может быть методом выбора в руках отдельных высококвалифицированных хирургов-онкологов.
Широкое иссечение одиночных рецидивов или метастазов в грудной стенке, в отдельных случаях включающее резекцию ребер и грудины, допустимо при полной убежденности в отсутствии генерализации процесса. Иссечение рецидивов и метастазов должно сочетаться с гормонотерапией, химиотерапией или лучевой терапией. При наличии одиночных метастазов в легкие иногда рекомендуют производить лобэктомию. Однако одиночные метастазы в легкие представляют очень редкое исключение, и этот метод терапии их является казуистическим.
Лучевая терапия занимает одно из ведущих мест в общем комплексе лечебных мепоприятий при раке молочной железы. Выбор той или иной схемы облучения зависит от многих ппичин: стадии, формы и характера опухоли, особенностей ее клинического течения, объема оперативного вмешательства, а также от гормонального фона, на котором проводится лучевая терапия. В большинстве случаев лучевое лечение сочетается с хирургическим; в поздних, запущенных фазах болезни оно может быть использовано как самостоятельный консервативный метод терапии.
Большое значение лучевое лечение имеет для воздействия на очаги метастазирования (общее и местное облучение), а также как фактор угнетения и выключения функции эндокринных органов (яичники, надпочечники, гипофиз). В качестве одного из этапов комбинированного лечения используется предоперационная и послеоперационная лучевая терапия и интерстициальная кюритерапия, проводимая вслед за удалением первичной опухоли молочной железы.
Предоперационная лучевая терапия преследует цель девитализации опухолевых клеток, частичное уничтожение одних и понижение жизнеспособности других с целью предупреждения их диссеминации во время операции. Облучению подвергается молочная железа и ближайшие пути лимфооттока: подмышечная, подключичная, надключичная области, а в ряде случаев парастернальная область.
В качестве источников излучения используются рентгенотерапевтические аппапаты (с напряжением генерирования от 200 до 250 kV) и телегамма-установки (с зарядом от 400 до 1000—20000 грамм-эквивалент радия). Молочную железу облучают с двух — трех полей. Разовая доза 200—300 r; суммарная доза 5000—6000 r на молочную железу и по 2000—3000 r на подмышечную, подключичную, надключичную и парастернальную области. В силу возникновения реактивных изменений кожи операция выполнима только после стихания последних, в сроки от 3 недель до 2 месяцев с момента окончания облучения.
Предоперационное облучение обычно проводят больным со II и III стадиями процесса, когда отмечается выраженный инфильтративный рост опухоли, при отеке молочной железы, при наличии инвазии лимфатических путей, при быстро прогрессирующих опухолевых формах.
Послеоперационная лучевая терапия ставит своей задачей воздействие на опухолевые элементы, оставленные во время операции и на ближайшие лимфатические барьеры, где эти элементы могли оказаться. По классической схеме облучению подлежат операционное поле, подмышечные, подключичные, надключичные и в отдельных случаях парастернальные области. Облучение проводится на рентгенотерапевтических аппаратах и телегамма-установках. Разовая доза 200—250 r; суммарная доза на каждое поле 2000—3000 r; при воздействии на парастернальную область ввиду более глубокого расположения лимфатических узлов по ходу art. mammaria interna доза должна достигать 4000—5000 r.
Интерстициальная кюритерапия возможна при ограниченных опухолях молочной железы в случае отказа больных от радикальной операции, при небольших размерах молочных желез. После иссечения опухолевого очага по типу секторальной резекции под молочную железу, в ретромаммарную клетчатку, в подмышечную, надключичную, подключичную и парастернальные области внедряются радионосные иглы, содержащие по 2—3 мг радия; всего 25—30 игл на 5—7 дней. В некоторых случаях до внутритканевого облучения проводится рентгенотерапия.
Паллиативная лучевая терапия при иноперабильных раках молочной железы складывается из сочетания различных лучевых воздействий. В основном используется наружное облучение опухоли и метастатических узлов на телегамма-установках. В случае эффекта у отдельных больных дополнительно проводится внутритканевая лучевая терапия (введение в остатки лимфатического узла радиоактивного золота, введение в область art. mammaria interna радиоактивной кобальтовой или при радиевой проволоки для облучения расположенных по ходу артерий лимфатических узлов). Методы и формы применения сочетанной лучевой терапии, так же как и величина используемых доз, строго индивидуальны. Известные перспективы для лечения запущенных форм рака молочной железы имеют источники высоких энергий (гамматроны, линейные ускорители, бетатроны).
Паллиативная лучевая терапия проводится на фоне гормонального лечения, а в отдельных случаях и химиотерапевтического лечения. При выявлении одиночных метастазов рака молочной железы большинство из них подлежит лучевому лечению. Так, при метастатическом поражении лимфатических узлов показана телегамматерапия в дозе 4000—5000 r или облучение на рентгенотерапевтическом аппарате с использованием свинцовой решетки (доза 6000—8000 r).
При локальных метастазах в кости — облучение с нескольких полей, суммарной очаговой дозой 5000—6000 г; при одиночных метастазах в коже — близкофокусная рентгенотерапия (доза 8000—10 000 r); при ограниченном рецидиве в рубце — аппликация радиоактивных препаратов или внутритканевое введение радиоактивных препаратов, или близкофокусная телегамматерапия в дозе 6000 r; при специфических плевритах — внутриплевральное введение радиоактивного золота.
При генерализованном метастазировании в кости показано тотальное облучение в виде попеременного верхней и нижней половины туловища с расстоянием 120 см, при разовой дозе 15—25 г и суммарной дозе 400—500 r. Во всех случаях метастазирования лучевую терапию следует сочетать с гормональными и химиотерапевтическими средствами. Лучевая терапия может быть использована для подавления функции эндокринных органов: яичников, надпочечников и гипофиза. Облучение яичников предпочтительно проводить на гамма-установке в очаговой дозе 2000 r на каждый яичник. При облучении надпочечников также используется очаговая доза 2000—2500 r. Для лучевого воздействия на гипофиз используется внедрение гранул радиоактивного золота или радиоактивного иттрия — радиоактивных изотопов, дающих мягкое бета-излучение, не повреждающее соседние ткани.
Кроме того, для той же цели может служить облучение на аппарате для конвергентной рентгенотерапии. Следует подчеркнуть, что хирургическая кастрация и адреналэктомия имеют ряд преимуществ перед облучением соответствующих органов; что касается гипофизэктомии, то в силу высокого числа послеоперационных осложнений лучевая терапия в данном случае является методом выбора. Для выключения функции гипофиза требуются высокие очаговые дозы порядка 10 000 r.
Гормонотерапия наиболее часто применяется в запущенных стадиях и помогает в ряде случаев перевести неоперабильные формы в операбильные, а при генерализованном метастазировании вызывает ремиссию, временно возвращая больных к обычной жизни и труду. В зависимости от отношения больных к овариальным циклам методика гормонотерапии изменяется. Соответственно с этим больные распределяются на три группы: 1) менструирующие; 2) больные в климаксе и менопаузе менее 10 лет; 3) больные в период глубокой менопаузы, более 10 лет.
У больных первой и второй групп гормонотерапия должна проводиться на фоне предварительной овариэктомии, что обеспечивает полное выключение гормонов яичникового происхождения по сравнению с облучением яичников или применением одних андрогенов. В третьей группе, когда функция яичников полностью отсутствует, в силу возрастного фактора прибегать к овариэктомии нет необходимости.
Могут быть рекомендованы четыре схемы гормонотерапии: 1) андрогены на фоне овариэктомии — метод направлен на выключение функции яичников и подавление фолликулостимулирующей функции (ФСГ) гипофиза; применяется у больных первой и второй групп; 2) кортикостероиды на фоне овариэктомии — метод направлен на выключение овариальной функции и подавление эстрогенной функции коры надпочечников, применяется у больных первой и второй групп; 3) эстрогены на фоне овариэктомии — метод направлен на выключение функции яичников и подавление ФСГ гипофиза; применяется у больных второй группы; 4) эстрогены в сочетании с кортикостероидами — метод направлен на подавление ФСГ гипофиза и функции коры надпочечников; применяется у больных третьей группы.
Применение гормональных препаратов должно проводиться длительно и непрерывно, при IV стадии заболевания — практически в течение всей жизни. Общая схема терапии следующая: в первой и второй группах больных лечение начинают с овариэктомии. Через 5—7 дней, после того как больные выйдут из послеоперационного периода, следует начинать введение гормональных препаратов. Андрогены или эстрогены согласно выбранной схеме вводят внутримышечно ежедневно в дозе 50—100 мг в масляном растворе или водно-новокаиновой суспензии.
Через 2—3 недели после начала инъекций, когда определяется переносимость препаратов, рекомендуется произвести внедрение пилюль соответствующих гормональных препаратов в подкожную клетчатку передней брюшной стенки. Общая доза пилюль должна равняться 3—б г. При этом создается депо гормонального препарата, который, постоянно всасываясь, непрерывно насыщает организм, поддерживая более или менее постоянный уровень.
Через каждые 4—5 месяцев внедрение гормональных пилюль следует повторять. Если изготовление пилюль невозможно, то больные должны получать инъекции соответствующего препарата ежедневно в дозе 50—100 мг без перерыва до получения стойкого эффекта. При получении выраженной объективной ремиссии дозу вводимого препарата можно снизить до 50 мг в день. Если в результате длительных инъекций развиваются болезненные инфильтраты, можно производить инъекции через день, а через день применять соответствующий гормональный препарат в таблетках (метилтестостерона 50 мг, или 10 таблеток в день под язык; диэтилстильбэстрола 20— 30 мг в день, или 20—30 таблеток).
Кортикостероиды применяются в виде стандартного препарата кортизона в иньекциях или в виде таблеток преднизона и преднизолона. Суточная доза кортизона 50 мг. Препарат вводят 4 раза в день по 0,5 мл. Вместо кортизона можно применять преднизон или преднизолон, адекватная доза 10 мг в сутки (полтаблетки 4 раза в сутки). Так же как андрогены и эстрогены, кортикостероиды при IV стадии заболевания следует применять без перерывов до конца жизни больных. У больных в менопаузе более 10 лет проводится лечение эстрогенами (синэстрол, диэтилстильбэстрол) без предварительной овариэктомии. Методика применения препаратов и дозировки те же, что и у больных второй группы. На фоне применения синэстрола показано периодически 2—3 раза в год проводить месячные курсы лечения кортизоном с целью подавления наступающей гиперфункции коры надпочечников.
Применение гормональных воздействий может быть рекомендовано и больным с первичным раком молочной железы в более ранних стадиях заболевания. В этих случаях оно расценивается как гормонопрофилактика рецидивов и метастазов и применяется в общем комплексе терапии.
У больных II—III стадии (международная номенклатура) лечение рекомендуется начинать с предоперационной лучевой терапии, затем произвести радикальную мастэктомию, через 2 недели после которой у менструирующих и больных в менопаузе менее 10 лет произвести овариэктомию и применять тот или иной гормональный препарат соответственно выбранной схеме; параллельно начать послеоперационную лучевую терапию.
В отдельных случаях гормонопрофилактика рецидивов и метастазов может быть рекомендована и больным с заболеванием I стадии при наличии отягчающих моментов: молодой возраст, наличие беременности, период лактации и т. п. Гормонопрофилактика проводится по тем же схемам, что и гормонотерапия. С целью профилактики рекомендуется применять гормональные препараты до 2 лет. Если на протяжении этого срока не возникает рецидивов или метастазов, гормонопрофилактику можно прекратить.
Применение различных схем гормонотерапии при далеко зашедших стадиях рака молочной железы дает выраженную объективную и субъективную ремиссию при различных локализациях метастазоз почти в одинаковом числе случаев и достигает 60—70%; средняя продолжительность ремиссии в случаях эффективности гормонотерапии достигает 2 лет, а средняя продолжительность жизни 2 года 6 месяцев. Выбор той или иной схемы для соответствующей группы больных не имеет каких-либо специальных показаний. Относительным противопоказанием к применению кортикостероидов является склонность больных к тучности, поэтому такую схему желательно применять у худых и ослабленных больных. У больных в менопаузе менее 10 лет наиболее приемлемым является лейение эстрогенами на фоне овариэктомии. Применение эстрогенов противопоказано больным с сердечно-сосудистыми заболеваниями.
При далеко зашедших формах рака молочной железы и на фоне гормонального лечения показано проведение повторных курсов терапии противоопухолевыми препаратами. Лучшие результаты получены при применении препаратов: циклофосфан, эндоксан, тиофосфамид (ТиоТЭФ). Применение противоопухолевых препаратов оказывает лучший эффект при метастазах в кожу, лимфатические узлы, плевру и легкие. При костных метастазах, особенно множественных, химиотерапия оказывается малоэффективной. В этих случаях развивается быстрое угнетение кровотворения, препятствующее доведению дозы препарата до терапевтического эффекта. При метастатических плевритах введение препаратов в плевральную полость оказывается весьма эффективным. Применение химиотерапии без гормонотерапии также ведет к терапевтическому эффекту, но он оказывается менее стойким.
Сочетанное применение гормонотерапии и химиотерапии на современном этапе, по-видимому, является лучшим методом лечения при далеко зашедших формах рака молочной железы. Гормонотерапия создает общий фон, неблагоприятный для прогрессирования опухолевого процесса, а противоопухолевые препараты на этом фоне действуют более активно на раковые клетки. Применение химиотерапевтических препаратов проводится по инструкциям, для них существующим (см. противоопухолевые препараты и гормоны).
Симптоматическая терапия больных с запущенными формами рака молочной железы при неэффективности комплексных методов терапии сводится к средствам, тонизирующим общее состояние, болеутоляющим и к общему уходу. К тонизирующим средствам следует отнести препараты: чага, таблетки КН, круцин, витамины, препараты, повышающие гемопоэз, дробные переливания небольших доз крови и др. При сильных болях следует прибегать к анальгезирующим и наркотическим средствам. Больные в запущенных стадиях требуют особенно внимательного ухода, применения сердечных средств, кислорода, облегченной, высококалорийной диеты. Целый ряд симптоматических средств зависит от характера распространения процесса и применение их должно строго индивидуализироваться.
Суммируя все изложенное выше, можно кратко рекомендовать следующие схемы комплексной терапии для каждой стадии рака молочной железы (стадии по международной классификации):
I стадия — радикальная мастэктомия и послеоперационная лучевая терапия. При отягчающих обстоятельствах — выявление рака в момент беременности или лактации, очень молодой возраст больных — следует проводить гормонопрофилактику по одной из приведенных схем.
II стадия — радикальная мастэктомия и послеоперационная лучевая терапия. При отягчающих обстоятельствах (см. выше) лечение можно начинать с предоперационной лучевой терапии, затем производить радикальную мастэктомию, овариэктомию, послеоперационную лучевую терапию и гормонопрофилактику по рекомендуемым схемам.
III стадия — лечение начинается с лучевой терапии, затем производятся радикальная мастэктомия, овариэктомия и послеоперационная лучевая терапия параллельно с применением гормональных препаратов по выбранной схеме.
Применение гормональных препаратов при I—II—III стадиях рака молочной железы проводится без перерывов на протяжении до 2 лет. Если на протяжении этого срока рецидивов и метастазов не выявлено, то гормонопрофилактику следует прекратить. Если развились рецидивы или метастазы, то болезнь, следовательно, перешла в IV стадию, и поэтому нужно продолжать комплексную терапию, включив дополнительно химиотерапию или лучевую терапию или последовательно то и другое. Строго индивидуализируя лечение больных, при неэффективности одного из гормональных препаратов допустима замена другим гормональным препаратом из той же или из другой группы.
Например, вместо тестостерон-пропионата применять неодроль, вместо синэстрола — диэтилстильбэстрол; вместо андрогенов — кортикостероиды или эстрогены и наоборот. В отдельных случаях такая смена гормонального лечения может повести к новой ремиссии. К сожалению, каждая следующая ремиссия оказывается менее выраженной и более короткой.
В вопросах трудоустройства больных раком молочной железы до настоящего времени еще нет единства мнений. При решении этого вопроса следует учитывать большое число факторов: стадию заболевания, в которой начато лечение, послеоперационные осложнения (стойкий лимфостаз, отек верхней конечности, ограничение движений в плечевом суставе), наличие сопутствующих заболеваний и характер труда. Обычно после окончания комбинированной или комплексной терапии уже через 2—3 недели больные могут приступать к работе, исключая, конечно, тяжелый физический труд или труд, связанный с большими производственными вредностями (запыленность воздуха, цеха с повышенной или пониженной температурой, цеха с наличием химической или радиоактивной вредности). Больным после радикальной мастэктомии противопоказан труд с перегрузкой для руки оперированной стороны. В зависимости от характера труда больные обычно получают третью или вторую группу инвалидности.
Вопросы трудоустройства больных с заболеванием в IV стадии еще более сложны и зависят в первую очередь от локализации степени распространения метастазирования. При эффективности гормональной терапии многие больные могут быть временно возвращены к труду, хотя последний всегда должен быть облегченным и не должен вызывать физического и умственного перенапряжения.
Прогноз. Эффективность комбинированной и комплексной терапии рака молочной железы учитывается по отдаленным результатам. Накопившийся большой клинический материал как отечественных, так и зарубежных онкологических учреждений показывает, что при комбинированных методах терапии выживаемость больных до 5 лет равна 50—60%. Эффективность терапии зависит от стадии, в которой начато лечение.
Так, по данным клиники Мэйо, из 7925 больных, начавших лечение без метастазов, 5-летняя выживаемость отмечалась у 78,3%, а из больных, начавших лечение с метастазами,— лишь у 32,5%. По данным ЛОИ АМН СССР, на 1040 больных раком молочной железы разных стадий, начавшие лечение в I стадии, прожили 5 лет в 84,7%, а больные с заболеванием в III стадии — лишь в 28%. Применение гормонопрофилактики у больных с заболеванием I—III стадии отодвигает сроки появления рецидивов и метастазов, улучшая отдаленные результаты на 10—20%. Однако накопленный в этом направлении материал еще недостаточен для окончательного суждения. Особенно показательны данные по применению гормонопрофилактики рецидивов и метастазов у больных с заболеванием в III стадии.
Лучшие результаты гормонотерапии запушенных стадий рака молочной железы получены при применении адреналэктомии или гипофизэктомии, а также при применении комплексных методов, рекомендуемых выше. Выраженная объективная и субъективная ремиссия при указанном методе достигается у 65%, у 50% средняя продолжительность ремиссии достигает 2 лет, а средняя продолжительность жизни — 2 года 6 месяцев. Средняя продолжительность жизни больных, у которых гормональная или комплексная терапия оказывается неэффективной, редко превышает 6 месяцев.
| Каким должно быть питание при онкологических заболеваниях? Какие продукты абсолютно противопоказаны при той или иной форме рака? Узнать подробности >> |
| Фитотерапия способна оказать существенную помощь не только в лечении онкологических заболеваний, но также и в их профилактике. Узнать подробности >> |
| Многих людей, имеющих у себя или у родственников онкологическое заболевание, интересует вопрос: передается ли рак по наследству? Узнать подробности >> |
| Лечение рака во время беременности является довольно сложным, ведь большинство лекарственных средств обладает токсичностью. Узнать подробности >> |
| Какие перспективы у беременности после перенесенного онкологического заболевания? Следует ли выдерживать срок после лечения рака? Узнать подробности >> |
| Профилактика является важной частью общей борьбы с онкологическими заболеваниями. Как же уменьшить вероятность возникновения рака? Узнать подробности >> |
| Что представляет из себя паллиативное лечение рака? Как оно может повлиять на качество жизни онкологического больного и изменить ее к лучшему? Узнать подробности >> |
| Учеными разработано достаточно много перспективных методов лечения рака, пока еще не признанных официальной медициной. Но все может измениться! Узнать подробности >> |
| Статистика заболеваемости раком, к сожалению, неутешительна: наблюдается рост числа заболевших, при этом болезнь «молодеет». Узнать подробности >> |
| Иногда «народными» методами удается победить рак, но тех, кто уповал только на них и в итоге покинул этот мир раньше времени — намного больше. Узнать подробности >> |
| Как найти силы для борьбы с раком? Как не впасть в отчаяние от возможной инвалидности? Что может послужить надеждой и смыслом жизни? Узнать подробности >> |
| Как помочь близкому человеку жить с диагнозом «рак»? Нужна ли «ложь во спасение»? Как вести себя, чтобы близкие люди меньше страдали? Узнать подробности >> |
| Бытует такое мнение, что постоянные стрессовые ситуации способны привести к развитию онкологических заболеваний. Так ли это? Узнать подробности >> |
| Многие онкологические больные часто страдают от резкой потери веса. Чем это вызвано и можно ли как-то справиться с этой проблемой? Узнать подробности >> |
| Правила ухода за больными, вынужденными постоянно находиться в кровати, имеют свои особенности и их нужно обязательно знать. источник |