В нашей клинике вы можете пройти анализ на выявление мутаций в генах BRCA1 и BRCA2 — данная процедура позволяет диагностировать высокую степень риска рака молочной железы .
Лечение РМЖ на различных стадиях
- У пациенток с операбельной опухолью (I-II стадий) лечение обычно начинается с операции.
- Пациенткам с первично иноперабельной опухолью (III стадии) необходимо проведение на первом этапе химиотерапии или сочетания химиотерапии с лучевой терапией или гормонотерапии. Операция становится возможной при успешном лечении.
- Пациенткам с диссеминированной опухолью (при наличии метастазов в других органах, IV стадии) предлагается проведение лекарственного лечения или сочетания лекарственного лечения с лучевой терапией, а в некоторых случаях – с операцией.
Сергей Михайлович Портной «Методы лечения рака молочной железы».
Рассмотрим основные положения местного и общего лечения не диссеминированного рака. Кратко анализируя эволюцию методов хирургического лечения рака молочной железы на протяжении ХХ века, можно выделить две противоположные тенденции:
- тенденцию к расширению объема операции,
- тенденцию к сокращению объема оперативного вмешательства.
Первая связана со стремлением к повышению радикализма за счет широкого удаления пораженных опухолью тканей и тканей, где такое поражение может быть. Для рака молочной железы характерно распространение по протокам и по лимфатическим сосудам, как в пределах молочной железы, так и за ее пределы в лимфатические узлы. Такое распространение при небольших, казалось бы, ограниченных опухолях, может быть выявлено только при микроскопии удаленной ткани, ни рентгенологически, ни при пальпации оно не выявляется. После лечения, ограниченного только удалением опухоли, закономерно возникали рецидивы рака в молочной железе или в ближайших лимфатических узлах. Именно с этим связано широкое применение операций, при которых полностью удаляется молочная железа и жировая клетчатка, в которой находятся ближайшие лимфатические узлы (радикальная мастэктомия).
Потеря молочной железы после радикального лечения по поводу рака представляет не только физический недостаток, но и является, прежде всего, серьезной психической травмой. Желание удалить опухоль и сохранить молочную железу выразилось в исторически более ранних операциях, так как радикальная мастэктомия была альтернативой таким операциям. Вместе с тем, органосохраняющее лечение, не худшее по результатам, чем радикальная мастэктомия, было разработано сравнительно недавно.
Современное представление о возможности сохранения молочной железы основано на представлении о том, что РМЖ даже 1 стадии к моменту его выявления уже имеет существенную вероятность наличия отдаленных гематогенных микрометастазов и проведение операции самого максимального объема не снижает риска реализации микрометастазов в клинически проявляемые метастазы (B.Fisher). К настоящему времени проведено большое количество рандомизированных исследований, сравнивающих, с одной стороны органосохраняющие операции в сочетании с лучевой терапией и радикальную мастэктомию с другой стороны.
Многолетние наблюдения за тысячами больных показали равноценность выживаемости и, следовательно, — адекватность органосохраняющего лечения. В то же время, органосохраняющие операции не могут применяться при всех формах роста и на всех этапах развития рака молочной железы.
Показаниями к органосохраняющим операциям являются:
- небольшой размер опухоли (не более 3-4 см),
- один очаг опухоли,
- отсутствие распространения опухоли на кожу.
Предположительно существующее микроскопическое распространение опухоли по лимфатическим сосудам и протокам в пределах молочной железы подавляется обязательным последующим облучением.
Объединение современных возможностей онкологии и пластической хирургии позволило разработать целую серию новых одномоментных операций, при которых онкологический этап операции (радикальная мастэктомия, органосохраняющая операция) дополняется реконструкцией молочной железы.
Облучение молочной железы после органосохраняющих операций позволяет добиться такой же низкой частоты развития местных рецидивов, как и после радикальной мастэктомии. Важно отметить, что проведение правильного органосохраняющего лечения не повышает риск развития отдаленных метастазов, вероятность и скорость их появления остается такой же, как и после радикальной мастэктомии. Пресечь или затормозить этот процесс может только системное профилактическое лечение.
Предполагается, что у значительной части больных на раннем этапе развития рака происходит рассеивание опухолевых клеток током крови по тканям организма. Здесь они могут погибнуть, но, если первичная опухоль не удалена, им на смену придут следующие партии клеток, которые могут сформировать микроскопические колонии.
Современные методы выявления метастазов рака молочной железы не идеальны, с их помощью можно выявить очаг поражения тогда, когда он достиг, по крайней мере, 0,5 см в диаметре. После удаления первичной опухоли дальнейшее поведение микрометастазов определяет судьбу больной:
- Если микрометастазов вообще нет или они настолько малы, что их развитие блокируется естественными силами организма, наступает длительное излечение.
- Если микрометастазы малы и растут медленно, рецидив болезни может развиться через десятки лет.
- Наконец, если микрометастазы относительно крупные и быстро растут, они быстро проявят себя.
При раке молочной железы наибольшую опасность представляют микрометастазы опухоли, вероятно, рассеянные по всему организму уже к моменту первого обращения к врачу. Естественно, что чем больше местное распространение опухоли (ее размер, вовлечение в опухолевый процесс регионарных лимфатических узлов, кожи молочной железы, грудной стенки), тем больше вероятность существования микрометастазов. Именно поэтому при местно-распространенном РМЖ (III стадии) часто лечение начинается не с местных воздействий на первичную опухоль, а с общего воздействия, чаще всего — с химиотерапии. Значение лекарственного лечения, предпринимаемого после радикальных операций, также чрезвычайно велико для уничтожения микрометастазов и повышения вероятности длительного выздоровления больных. Причем, чем больше стадия болезни, тем хуже прогноз и тем больше оснований к проведению профилактического системного лечения.
Химиотерапия и эндокринная терапия
Под химиопрепаратами понимаются вещества природного или синтетического происхождения, обладающие способностями убивать опухолевые клетки. Обычно они вводятся в определенных сочетаниях, позволяющих рассчитывать на успех в 50 — 70% случаев. Химиотерапия обычно проводится за несколько (от 4 до 16) курсов, с интервалами отдыха.
Из средств эндокринного лечения наибольшее применение нашли хирургическое удаление яичников, лекарственное выключение функции яичников, а также препараты, являющиеся гормонами, антигормонами, или ингибиторами образования гормонов. Эти лекарства обычно принимаются длительно и непрерывно, цель их применения — препятствовать стимуляции опухолевого роста собственными гормонами организма. Рецепторы эстрогенов (РЭ) и рецепторы прогестерона (РП) – белковые молекулы в клетках опухоли, воспринимающие воздействие соответствующих женских половых гормонов. Наличие этих молекул говорит о гормональной зависимости опухоли и о возможности снижения вероятности рецидива болезни при проведении гормонотерапии.
Рецептор эпидермального фактора роста 2 типа (HER2) – белковая молекула в опухолевой клетке, воспринимающая стимулирующее действие соответствующего фактора роста. Присутствие этого рецептора, с одной стороны, говорит об очень высокой агрессивности опухоли. С другой стороны, это позволяет применять высокоэффективные средства, по своему механизму действия являющиеся антителами к HER2.
Каким образом планировать компоненты профилактического лечения у каждой конкретной больной?
Хорошо аргументированные ответы содержатся в рекомендациях Международной конференции по адъювантной терапии рака молочной железы в Сан-Галлене (2015-2017 гг.). По современным рекомендациям, практически все больные инвазивным раком молочной железы после операции нуждаются в проведении профилактического лекарственного лечения.
Для составления индивидуального прогноза и выбора лечения больной принимаются во внимание:
- возраст,
- размер опухоли,
- степень злокачественности опухоли,
- наличие опухолевых клеток в перитуморальных сосудах,
- экспрессия РЭ, РП, HER2 и Ki67,
- наличие метастазов в лимфатических узлах.
Решение вопроса о предоперационной и послеоперационной лекарственной терапии решается консультантами-химиотерапевтами так же, как и вопрос о лучевой терапии решается консультантами лучевыми терапевтами.
Особенности лечения наследственного РМЖ
Органосохраняющие операции у больных наследственным раком молочной железы имеют значение для лечения существующей на данный момент болезни, но они не защищают от развития последующих опухолей.
В одном из наблюдений сообщается, что частота вторых раков молочной железы у таких больных составила:
- в оперированной молочной железе – 49%,
- в противоположной молочной железе – 42%.
Эти результаты резко отличаются от результатов таких операций в общей популяции, где частота местных рецидивов может составлять 5-10%.
Выполнение двусторонней мастэктомии у женщин носителей мутаций BRCA1 или BRCA2 при раке одной молочной железы более оправдано, такая операция уносит ткань-мишень, в которой могут формироваться новые опухоли; то есть операция имеет и лечебный, и профилактический смысл.
Тактика лечения наследственного РМЖ основывается на анализе общепринятых для РМЖ характеристик:
- возраста,
- соматического состояния,
- репродуктивного статуса,
- распространённости опухоли, её молекулярно-биологического портрета,
- пожеланий пациентки.
Особенностью тактики является возможность проведения одновременных мер по профилактике второго рака. В частности, при планировании хирургического лечения следует иметь ввиду, что, чем больше оставляется железистой ткани, тем больше вероятность развития второй опухоли как в ипсилатеральной, так и в контралатеральной молочной железе.
Отказ от органосохраняющей операции в пользу мастэктомии на стороне болезни и выполнение контралатеральной профилактической мастэктомии снижает вероятность развития второго РМЖ на 90-100%!
Лечение больных наследственным РМЖ направлено на решение следующих задач:
- непосредственное лечение имеющегося заболевания (РМЖ),
- профилактика второго РМЖ,
- профилактика рака яичников (при мутациях генов BRCA1 и BRCA2).
Обширные профилактические операции могут быть непереносимы по соматическому состоянию или по психологической неготовности пациентки. Решение второй и третьей задач может осуществляться одновременно с проведением лечения первичного заболевания или быть отсрочено.
источник
Когда человеку говорят, что у него злокачественная опухоль, возникает ощущение, что рушится мир. Женщины должны знать, что рак молочной железы, симптомы которого выявлены на ранней стадии, поддается лечению и имеет благоприятный прогноз. Почему развивается заболевание, какие первые признаки патологии, как происходит оздоровление – необходимо разобраться в этих вопросах, чтобы избежать страшных последствий.
Женский организм устроен сложно, причин, по которым в нем происходят гормональные перестройки, множество. Молочные железы очень чувствительны к изменениям. В них начинают развиваться патологические процессы. Происходит неконтролируемый рост агрессивных опухолевых клеток, что приводит к возникновению опасного новообразования. Высокий процент заболеваемости раком наблюдается у женщин старше 50 лет, но не исключены случаи патологий у молодых. Опухоль разрастается, дает метастазы в:
- лимфатические узлы;
- кости таза, позвоночника;
- легкие;
- печень.
Чтобы своевременно начать лечение рака молочной железы, нужно знать, как он проявляется. Опасность в том, что на ранней стадии процессы протекают без видимых признаков. Это усложняет лечение и прогнозы – женщины обращаются к специалистам, когда требуются радикальные способы вмешательства. Для развития рака характерны симптомы:
- образование уплотнений в груди;
- утолщение или втяжение соска;
- появление над очагом «лимонной корки»;
- покраснение кожи.
При выявлении одного или нескольких симптомов, необходимо пройти обследование у врача. Злокачественная опухоль молочной железы характеризуется образованием признаков:
- уплотнение загрудинных, подмышечных лимфатических узлов;
- непропорциональное увеличение размера одной груди;
- появление болей;
- деформация груди;
- образование отека;
- возникновение язв, корочек;
- наличие выделения из соска;
- повышение температуры;
- слабость;
- головокружение;
- резкое похудение;
- проявления боли в костях, печени при метастазах на поздней стадии рака.
Необходимо знать, что развитие рака не всегда сопровождает возникновение боли, особенно при раннем выявлении патологии. На появление симптома влияет место расположения опухоли. Молочные железы, как и другие органы, имеют нервы. При увеличении размеров новообразования:
- возникает отек;
- происходит оттеснение здоровых тканей;
- идет давление на нервные окончания;
- появляется постоянная ноющая боль.
Этот симптом возникновения рака наблюдается на ранней стадии болезни. Он сигнализирует, что в глубине молочной железы развивается инфильтративный процесс, вызывающий фиброз тканей. При умбиликации:
- связки органа подтягиваются к опухоли;
- над очагом воспаления наблюдается небольшое углубление;
- отмечается втягивание поверхности кожи внутрь;
- аналогичный процесс может проходить в соске.
Возникновение этого симптома онкологического заболевания молочной железы характерно для последних стадий рака. Явление зачастую наблюдается в нижней части груди. При увеличении опухоли изменяется форма молочной железы, на коже образуются изъязвления и «лимонная корка». Причины этого явления:
- при увеличении лимфатических узлов нарушается отток лимфы;
- возникает отек тканей;
- кожа утолщается;
- поры увеличиваются по размеру;
- на поверхности кожи наблюдается «лимонная корка».
На одном из этапов развития рака груди, в злокачественный процесс вовлекаются лимфатические и венозные сосуды. Происходит уменьшение эластичности тканей молочной железы. При симптоме Кернига:
- в толще железистых тканей возникает уплотнение;
- размеры опухолевого образования – до нескольких сантиметров;
- участок плотный, подвижный, безболезненный.
Чтобы избежать риска осложнений, женщины должны ежемесячно проводить самостоятельный осмотр груди. При регулярном наблюдении можно заметить изменения, обнаружить рак на ранней стадии и успешно вылечиться. Обнаружив первые симптомы болезни, необходимо обратиться к маммологу для проведения клинического обследования. Вполне возможно, что это будет доброкачественная опухоль или фиброаденома, но при отсутствии лечения все может перерасти в рак.
Как начинается рак груди? Женщины обнаруживают при самостоятельном обследовании:
- уплотнения в груди;
- поражение подмышечных впадин;
- расширение подкожных вен;
- возникновение язв;
- втяжение кожи соска;
- изменение формы груди;
- появление на коже «лимонной корки»;
- покраснение;
- утолщение кожи соска, ареол вокруг;
- увеличение лимфоузлов грудины подмышек;
- втягивание кожи над местом очага;
- выделения из соска.
Нельзя однозначно сказать, что вызывает рак груди у женщин. Существует множество провоцирующих факторов для развития патологических новообразований. Онкология молочной железы может прогрессировать по причинам:
- запущенные доброкачественные заболевания;
- наличие родственников, больных раком;
- травмы груди;
- возраст старше 40 лет;
- злоупотребление алкоголем;
- курение;
- ожирение;
- раннее начало менструального цикла;
- сахарный диабет;
- гинекологические воспалительные заболевания.
Злокачественное новообразование в груди может возникнуть как следствие:
- нередких абортов;
- поздних первых родов;
- короткого периода кормления грудью;
- отсутствия детей;
- гормональной терапии в анамнезе;
- поздней менопаузы;
- воздействия химических канцерогенов;
- нерегулярности менструального цикла;
- стрессовых ситуаций;
- бесплодия;
- кисты яичников;
- опухолей мозга;
- карциномы кору надпочечников;
- диеты с большим количеством жиров;
- воздействия облучения.
В медицине используются несколько классификаций раковых опухолей груди. Они отличаются характеристиками, особенностями строения новообразования, макроскопическими формами. При рассмотрении гистотипов встречаются:
- неинвазивный рак – злокачественные клетки находятся в пределах протока или дольки грудной железы;
- инвазивная карцинома – инфильтрирующий рак – берет начало в одной структуре, постепенно переходит на другие.
Существует классификация злокачественных опухолей грудной железы по макроскопическим формам. Она включает:
- диффузный рак – отличается скоростью развития, поражением лимфоузлов, отеками, увеличением размера молочных желез, образованием изъязвлений;
- узловой вид – располагается снаружи и вверху груди, захватывает жировые ткани, мышцы, кожу;
- рак Педжета – сопровождается увеличением соска, появлением на поверхности корочек и язв, опухоль диагностируется поздно – симптомы похожи на экзему.
Для удобства диагностики, подбора методик воздействия, принято разделять развитие патологических новообразований по стадиям. Для каждой характерны определенные признаки. Выделяются четыре стадии:
Прорастание в соседние ткани
Не проникают в кожу, жировую ткань
Прорастают в мышцы, ткани, кожу
Окологрудинных, подключичных, подмышечных
Разрастание злокачественной опухоли груди может происходить с различной скоростью. Это зависит от своевременности лечения, гормональной чувствительности, агрессивности раковых клеток. Одни женщины живут после выявления злокачественных новообразований долгие годы, другие – погибают за несколько месяцев. По скорости роста различают рак:
- быстро растущий – за три месяца количество злокачественных клеток увеличивается вдвое;
- со средним развитием – аналогичные изменения бывают за год;
- медленно растущий – разрастание опухоли в 2 раза происходит за больше чем 12 месяцев.
Основа результативного лечения рака груди – своевременная диагностика. После обнаружения симптомов болезни при самоосмотре, женщины идут в клинику к маммологу. Методы обследования для выявления рака включают:
- визуальный осмотр;
- пальпацию;
- опрос о вероятности заболевания наследственным раком;
- биопсию – исследование клеток;
- маммографию – рентгеновский метод, выявляет кисты, фиброаденомы, место расположения опухоли.
Для уточнения состояния рекомендуется проводить:
- ультразвуковое сканирование подмышечных впадин, груди, на выявление метастазов, поражений тканей;
- иммуногистохимический анализ – определение устойчивости злокачественного новообразования к гормональной терапии;
- цитологическое исследование – оценка структуры клеток;
- анализы на онкомаркеры – определение белков, которые вырабатываются только при наличии злокачественной опухоли;
- компьютерная томография для выявления метастазов в органы.
На выбор схемы лечения влияют стадия болезни, возраст и состояние здоровья женщины. Играет роль локализация и размер опухоли, первичный рак или вторичный. Существуют лучевые, медикаментозные методы воздействия и хирургическое удаление. Эффективные способы лечения:
- ампутация груди с сохранением лимфоузлов;
- секторальная резекция молочной железы – иссечение части груди с подмышечной клетчаткой;
- эмболизация опухоли – остановка питания раковых клеток;
- лучевая терапия – для исключения рецидивов заболевания.
- применяется радикальное удаление лимфатических узлов вместе с молочной железой, клетчаткой, мышцами – расширенная подмышечно-грудинная мастэктомия;
- практикуется иссечения яичников как источника выработки половых гормонов эстрогенов;
- химиотерапия проводится после удаление опухоли;
- при больших очагах поражения выполняется гормональная терапия;
- возможно сочетание двух последних методик.
Российскими учеными разработана методика воздействия на злокачественные новообразования электромагнитным излучением с определенной частотой – НИЭРТ. При влиянии на раковую клетку происходит ее нагрев и разрушение. Способ лечения позволяет избежать операций. Во время процесса:
- воздействию подвергаются агрессивные клетки по всему организму;
- здоровые ткани, имеющие другую резонансную частоту, не изменяются.
Альтернативой хирургическому вмешательству становится гормональная терапия. Ее задача – уменьшить влияние эстрогенов на рост опухолевых клеток. Метод эффективен при чувствительности злокачественных новообразований к гормонам. Лечение производится как профилактическая мера, применяется на ранних стадиях развития рака, после операций. Терапия предполагает:
- употребление препаратов для подавления функции эндокринной системы;
- введение антагонистов гормонам на клеточном уровне – Бромокриптина, Тамоксифена.
Когда опухоль имеет небольшие размеры и есть возможность сохранить грудь, используются органосохраняющие операции. Происходит щадящее вмешательство в организм женщины. Эффективностью отличаются 3 вида воздействия:
- эмболизация опухоли – в крупный сосуд, около новообразования вводится специальное вещество, происходит нарушение питания, гибель раковых клеток;
- квандрантэктомия – удаляется четверть груди и подмышечные лимфоузлы;
- радикальная резекция – иссекается только пораженный сектор, лимфоузлы, оболочка большой грудной мышцы.
При обнаружении огромных очагов поражения, распространении метастазов, проводится мастэктомия. Операция включает резекцию груди, окружающих тканей и органов. Существует 4 методики проведения вмешательства:
- простая – удаляется только грудь, мышцы и узлы не трогаются;
- радикальная модифицированная – иссекается молочная железа, лимфоузлы, оболочка большой грудной мышцы;
- мастэктомия по Холстреду – удаляется жировая клетчатка, все лимфатические узлы, мышцы и полностью грудь;
- двусторонняя – иссекаются обе железы.
Облучение злокачественного новообразования применяется при комплексном лечении рака груди. Это помогает избежать распространения агрессивных клеток, исключить рецидивы. Лучевая терапия применяется:
- после органосохраняющих операций;
- при риске развития рецидивов;
- если размеры первичной опухоли более 5 см;
- после радикальной резекции инвазивного рака;
- при наличии нескольких опухолей;
- обнаружение раковых клеток в 4 и более лимфоузлах.
Применение для лечения химических препаратов практикуется после проведения операции или до ее начала с целью уменьшения размеров опухоли. При панцирном, метастатическом раке, когда метастазы распространяются по всему телу, метод улучшает качество жизни пациента. Длительность курса – 2 недели, повторяется ежемесячно. Химиотерапия помогает:
- понизить стадию рака;
- улучшить итоги операции;
- способствует осуществлению контроля симптомов.
Прогнозирование результатов лечения злокачественной опухоли зависит от ее распространенности, агрессивности, наличия метастазов. Положительным итогом считается отсутствие рецидивов в течение пяти лет. Частота трагичных исходов из-за позднего обнаружения опухоли достигает 30%. Через некоторое время после выздоровления не исключено возобновление ракового процесса. Пятилетняя выживаемость пациенток в зависимости от стадии заболевания составляет в процентах:
- первая – до 95;
- вторая – 50-80;
- третья – до 40;
- четвертая – 5-10.
Не существует методов, способных полностью защитить женщину от рака груди. Есть средства, которые помогают снизить риск развития патологии. Особенно внимательными нужно быть женщинам, имеющим родственников, болевших раком, содержащим ген, провоцирующий онкологию. Им рекомендуют удаление яичников. К способам первичной профилактики относятся:
- самостоятельный осмотр;
- регулярное прохождение маммографии;
- планирование беременности;
- контроль веса;
- кормление ребенка грудью;
- профилактика мастита;
- прием гормональных препаратов после обследования.
источник
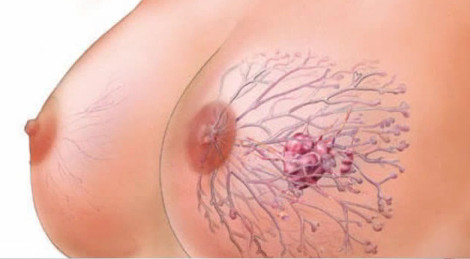
Многочисленные наблюдения установили, что в молочных железах замужних, но не рожавших или прерывавших беременность женщин, а также имеющих некоторые отклонения от нормальной деятельности половых органов, нередко возникают различные болезненные процессы, многие из которых сопровождаются развитием опухолеподобных уплотнений. Нередко в молочной железе возникают также доброкачественные опухоли — фибромы, кисты и др. Некоторые из них, будучи вначале совершенно невинными, после многих лет существования претерпевают злокачественное превращение и переходят в настоящий рак. Разобраться в каждом отдельном случае и определить характер имеющейся опухоли может только опытный врач-специалист.
Само слово «рак молочной железы» для большинства звучит как приговор. В этот период очень важно понять, что очень многое зависит от тебя. Это не пустые слова. Ни один врач не может вылечить больного, который не борется за свою жизнь. Современная онкологическая наука располагает большим арсеналом высокоэффективных препаратов, совершенствуются методики хирургических вмешательств, огромный вклад в процесс познания биологических особенностей опухолевого процесса привносят данные молекулярной биологии. Существующие сейчас возможности диагностики позволяют выявлять заболевание на начальных этапах. Современная хирургия делает возможным сохранение молочной железы или ее реконструкции с помощью пластических операций. Прогресс лекарственной терапии привел к созданию и широкому внедрению
препаратов, непосредственно действующих на биологические мишени. Милые женщины, поверьте, после постановки диагноза жизнь не заканчивается, а просто переходит к новому этапу. Самое главное не замыкаться в себе и не «уходить» в заболевание. Женщина может и должна полноценно жить, невзирая на болезнь.
• Точная причина болезни неизвестна, но вероятность возникновения рака груди связана со следующими факторами:
• Возраст. Риск возникновения рака груди возрастает с возрастом. Наиболее часто он развивается после 50 лет.
• Наследственные факторы. Примерно у 10 процентов женщин, страдающих раком груди, в семье были случаи заболевания этой болезнью. Женщины, у которых родственники по крайней мере второго порядка имели диагноз рака груди в возрасте до 50 лет или рака яичников в любом возрасте, могут унаследовать один-два гена, которые увеличивают риск их заболевания как раком груди, так и яичников.
• Рождение детей в позднем возрасте или отсутствие детей. Женщины, у которых нет детей, у которых первый ребенок родился в возрасте за 30 лет или которые никогда не кормили грудью, более подвержены раку груди.
• Раннее наступление менструаций (до 11 лет).
• Позднее наступление менопаузы (непрохождение менопаузы в возрасте слегка за 50 лет).
• Доброкачественные кисты или опухоли в груди.
• Пища с большим содержанием животного жира.
• Умеренное или сильное употребление алкоголя (более трех раз в день).
• Возможно, токсины в окружающей среде.
• Длительное (более 5 лет) использование заместительной гормональной терапии (сочетание эстрогена и прогестина).
• Длительное нахождение под светом по ночам (например, при посменной работе).
Рак молочной железы – «многоликая патология», но чаще всего либо сама пациентка, либо специалист обращает внимание на плотное ограниченно подвижное образование. При пальпации можно нащупать увеличенные подмышечные лимфатические узлы. Узловая форма рака – самая распространенная. Именно ее сопровождают кожные симптомы – втяжение, деформация, морщинистость.
Иногда женщина жалуется на кровянистые выделения из соска.Однако в некоторых случаях опухоль не формируется. Процесс диффузно распространяется по ткани молочной железы, не образуя узлов. В подобных клинических случаях наблюдается отек кожи железы, гиперемия, повышается температура. Такие клинические варианты рака
молочной железы называются диффузными или воспалительными.
Схожесть симптомов воспаления и «специфического процесса» иногда приводит к постановке ошибочных диагнозов и, как следствие, назначению неверного лечения.
Своеобразными симптомами отличается рак Педжета – редкая клиническая форма, на долю которой приходится не более 4% случаев.
Начало заболевания очень похоже на экземоподобные изменения на соске или ареоле, часто сопровождающиеся зудом. При посещении дерматолога назначаются мази, содержащие кортикостероиды и способствующие эпителизации компоненты. После их использования возможно даже улучшение состояния, однако вскоре процесс продолжает
развиваться, захватывая большую часть ареолы, может появиться узловое образование в различных отделах молочной железы. В этом случае уже нет сомнения в недоброкачественности процесса, и женщину направляют на полноценное обследование.
• Обычно безболезненное вздутие или опухоль в груди или под мышкой (чаще в верхней или наружной части груди).
• Изменение внешнего вида кожи груди, уплощение, вдавливание, покраснение или шелушение груди.
• Изменение соска, включая вдавливание, ощущение зуда или жжения, темные или кровянистые выделения.
• Изменение размера или асимметричное развитие груди.
• Боль или дискомфорт в груди при выраженном развитии болезни.
Чаще всего рак молочной железы начинается в виде небольшого узелка или ограниченного уплотнения, возникающего в толще железы и нередко долгое время остающегося незамеченным самой больной. Большей частью случайно, при мытье или одевании, женщина обнаруживает у себя в груди плотное образование с вишню или лесной орех величиной, с нерезкими границами, подвижное, безболезненное, иногда со слегка втянутой над ним кожей.
Реже рак молочной железы начинается без ясно ощутимого опухолевого узла, а в виде разлитого уплотнения, распространяющегося во все стороны, вызывающего отек и покраснение кожи.
Еще реже болезнь начинается с кровянистых выделений из соска или экземы его, с последующим образованием опухолевого узла в толще железы.
Возникнув в той или иной форме, раковая опухоль то быстро, то медленно, но неуклонно увеличивается в размерах, оставаясь безболезненной и ничем себя не проявляя, кроме узловатого затвердения в груди. Между тем, опухолевый процесс постепенно распространяется, что чаще всего выражается незначительным втягиванием кожи над опухолью.
Но дело не ограничивается лишь местным разрастанием ткани. Уже очень скоро, особенно у более молодых женщин, опухолевые клетки проникают в лимфатические пути и с током лимфы уносятся дальше, оседая в близлежащих лимфатических железах (подмышкой, над ключицей). При наличии благоприятных условий из них вырастают дочерние опухолевые узлы — метастазы, что проявляется припуханием и уплотнением желез, совершенно безболезненным. Обычно к этому времени наличие рака можно обнаружить даже при осмотре, в виде шаровидного выпячивания, чаще кнаружи и кверху от соска, или сморщенного и втянутого участка кожи, соответственно глубжележащей опухоли.
Такое постепенное и безболезненное развитие болезни без резко выраженных внешних признаков усыпляет бдительность больных, которые не торопятся обратиться к врачу, выжидая самопроизвольного исчезновения опухоли. Однако этого не происходит, опухоль увеличивается в размерах, спаивается с кожей и изъязвляется; в то же время идет развитие новых метастатических узлов на шее, подмышкой другой стороны и в других местах. Прорыв опухоли в кровяное русло приводит к появлению множественных опухолей в легких, печени, костях и других органах и, таким образом, весь организм оказывается пораженным болезнью.
Поэтому особенно важно обнаружить опухоль своевременно, в первом периоде ее существования, т. е. тогда, когда она еще целиком помещается в толще железы и не выходит за ее пределы, не дает метастазов подмышкой.
Правильно проведенное радикальное лечение в этих случаях обеспечивает выздоровление.
• Наличие бугорка в груди может быть выявлено путем обследования или маммографии.
Маммография – метод визуализации, использующий рентгеновские лучи. Лучевая нагрузка при маммографии незначительна, а диагностическая точность велика — 80-95%. Поэтому «вредным» это исследование назвать нельзя. С помощью маммографии удается не просто увидеть уплотнение, но и определить его локализацию, понять «взаимоотношение» уплотнения со здоровой тканью. Так, при росте опухоли в сторону центрального отдела молочной железы (соска и ареолы), органосохранная операция (радикальная резекция) не всегда показана. Маленькие, не достигшие 1см (в наибольшем измерении) узлы можно диагностировать только на маммограммах. Это же касается скопления солей кальция или микрокальцинатов, зачастую являющихся признаком самой ранней (преинвазивной) стадии рака.
Для выявления располагающихся внутри протока образований с клиникой серозных или кровянистых выделений из соска, необходимым методом диагностики является рентгенологическое исследование с введением контрастного вещества – дуктография.
Казалось бы – идеальное исследование. Тем не менее, маммография имеет свои недостатки, которые нельзя игнорировать. У женщин до 30 лет «информативность» маммографии снижается из-за плотной структуры ткани. Это не касается пациенток с силиконовыми имплантами. Нельзя не учитывать дискомфорт во время процедуры, связанный со сдавливанием железы
• Необходима биопсия бугорка, чтобы определить, присутствуют ли в нем раковые клетки. Из бугорка с помощью иглы берется ткань или жидкость; образец ткани может быть также взят во время небольшой операции.
Так как в самых ранних стадиях болезни при помощи обычных методов исследования — осмотра и ощупывания — не всегда удается поставить точный диагноз, а выжидание может быть опасным и привести к распространению процесса, то нередко приходится прибегать к пробной операции удаления опухоли и выяснению ее характера с помощью микроскопического исследования. Такое срочное исследование может быть произведено в течение нескольких минут, и хирург узнает результаты его еще в операционной. Благодаря этому удается без проволочки произвести нужное вмешательство, если опухоль оказывается раковой, и, с другой стороны, избежать больших операций там, где доброкачественный характер опухоли делает их излишними.
• Могут быть выполнены ультразвуковое обследование, термография или компьютерная томография.
Ультразвуковое исследование (УЗИ) также дает максимум информации. Этот метод основан на получении изображения при помощи высокочастотных звуковых колебаний. Наибольшей информативностью УЗИ обладает для обследования молодых (до 35 лет) женщин. С возрастом, в силу инволюции (жировое перерождение) ткани, информа-
тивность снижается.
УЗИ более четко позволяет дифференцировать кисты и солидные образования, весьма схожие при маммографии, а также внутрикистозные разрастания. Цветное допплеровское картирование – метод, визуализирующий патологические сосуды, всегда сопровождающие опухолевый рост. Ультразвуковое исследование позволяет одновременно с визуализацией проводить диагностическую тонкоигольную биопсию небольших или глубоко расположенных образований с их последующей маркировкой. И, наконец, УЗИ дает представления о состоянии регионарных лимфатических узлов (гиперплазия, специфическое поражение).
Несмотря на все достоинства, УЗИ не может заменить маммографию, которая дает возможность «увидеть» мелкие кальцификаты, иными словами, детализировать исследование.
Метод магнитно-резонансной томографии (МРТ) основан на использовании отраженных сигналов магнитного поля. Преобразованные компьютером в цифровое изображение ткани любого органа, в том числе и молочной железы, хорошо видны на экране. Часто при выполнении МРТ применяют контрастные вещества, внутривенное введение
которых с последующим избирательным накоплением позволяет увидеть обычно невизуалиризуемые ткани. Показаниями к назначению МРТ в комплексном обследовании пациенток с патологией молочных желез обычно служат:
– уточнение результатов маммографии и УЗИ у молодых (до 35 лет) женщин;
– оценка состояния имплантов в протезированной железе;
– прорастание опухолью структур грудной стенки;
– диагностика рецидива рака в оперированной (сохранная операция + лучевая терапия) молочной железе.
Во всех остальных ситуациях метод может применяться, но значительных преимуществ перед маммографией и УЗИ он не имеет.
Данные гисто- или цитологического исследования – необходимая и решающая составляющая диагноза «рак». Пациентам, у которых на первом этапе планируется операция, обычно достаточным выполнить тонкоигольную или стереотаксическую биопсию. Если опухоль определяется хорошо, биопсия выполняется «под контролем пальца». При глубоком расположении образования используется ультразвуковой метод. Определить злокачественная опухоль или нет до операции чрезвычайно важно.
Во-первых, это связано с возможностью медицинского учреждения в выполнении срочного интраоперационного исследования. Если такой возможности нет, ответ морфолога будет получен минимум через 7-10 дней.
При диагнозе «рак» такая операция не может считаться радикальной.
Во-вторых, это влияет на продолжительность операции, что при определенных сопутствующих заболеваниях неблагоприятно.
Для больных, у которых на первом этапе планируется консервативное лечение, морфологическое исследование просто необходимо. С одной стороны, лечить рак без гистологически подтвержденного диагноза юридически неправомочно, с другой –результаты биопсии позволяют сделать правильные прогнозы.
Чаще всего в этих целях используют кор-биопсию, иногда трепан-биопсию. Оба варианта выполняются амбулаторно, под местной анестезией.
• Для удаления опухоли необходима операция. Больной должна быть оказана необходимая хирургическая помощь при биопсии или при последующей операции. В зависимости от того, насколько развилась болезнь, может быть удален только бугорок или опухоль, или вся грудь (мастэктомия). При каждой операции могут быть удалены соседние лимфатические узлы. Если опухоль захватила мышечную ткань под грудью, может быть произведено удаление груди и расположенной ниже мышечной ткани (радикальная мастэктомия).
Решающими факторами для подобного хирургического вмешательства являются стадия опухолевого процесса и локализация новообразования в молочной железе. Возраст женщины значения не имеет. В объем удаляемых тканей включается сектор ткани молочной железы с опухолью и все уровни лимфатических узлов. Во время операции проводится срочное исследование удаленного сектора. Если морфолог по краю находит опухолевые клетки – нужна расширенная операция. Бывают ситуации, когда врач даже не обсуждает вопрос об объеме операции. Это означает, что у конкретной больной имеются абсолютные противопоказания для сохранения молочной железы. Современные
противопоказания к выполнению радикальной резекции – следующие:
– расположение опухоли в подсосковой (центральной) части молочной железы;
– несколько опухолей, расположенных в разных отделах молочной железы;
– отечная и воспалительная (например, маститоподобная) формы опухолевого процесса;
– ожидаемый плохой косметический результат (очень маленький размер железы).
• После операции может потребоваться лучевая терапия, чтобы предотвратить дальнейшее распространение рака, особенно если были задеты лимфатические узлы.
Весьма вероятно, что в оставшейся части ткани молочной железы могут быть микроопухоли, зона микрокальцинатов, из которых в последующем снова разовьется злокачественное образование. Подобное сомнение иногда приводит к отказу пациентки от данной операции. В связи с этим встает вопрос: не является ли радикальная мастэктомия,
при которой удаляется вся ткань молочной железы, правильной и радикальной операцией? Мы готовы согласиться с этим утверждением, если после органосохранной операции не предлагается лучевая терапия на оставшуюся часть молочной железы, иногда с включением в поле облучения зон регионарного лимфооттока.
В данном случае лучевая терапия решает основную задачу –профилактика возникновения местного рецидива заболевания.
Причем ее применение необходимо даже при пальпаторно неопределяемых до операции образованиях. В отсутствии послеоперационного облучения число пациенток, у которых может развиться рецидив в рубце, увеличивается в два и более раза.
Современные методики облучения, индивидуальный расчет полей облучения для каждой пациентки позволяют почти полностью избежать постлучевых изменений. Как правило, каждой женщине даются рекомендации по уходу за кожей во время проведения лечения, контролю показателей крови. Современные препараты местного использования в виде мазей: актовегиновая, метилурациловая, солкосерил-гель, бальзам «Спасатель», пантенол, димексид весьма эффективны. Обычно больная наблюдается у лечащего врача-хирурга и лучевого специалиста, которые совместно подбирают необходимое лечение. Благодаря этому значительных деформаций сохраненной молочной железы лучевая терапия не вызывает.
Существует еще один вариант, когда облучение молочной железы зон регионарного лимфооттока является компонентом лечебной программы – индукционная терапия местнораспространенного рака.
В этом случае задача лучевой терапии – сокращение объема первичной опухоли для последующего выполнения хирургического этапа.
• До и после операции может потребоваться химиотерапия, чтобы предотвратить дальнейшее распространение рака. Такое лечение обычно длится от шести месяцев до года.
Химиотерапия – основной и эффективный вариант лекарственного лечения злокачественных опухолей.
В результате воздействия химиотерапии на опухолевую ткань, размеры первичного образования (а также возможно имеющихся метастазов) сокращаются и помимо
этого идет активная профилактика развития метастазов.
При раке молочной железы химиотерапия может проводиться до операции в целях уменьшения размера опухоли и воздействия на регионарные лимфоузлы. В процессе этого реализуется так называемый непосредственный эффект лечения, свидетельствующий о:
– адекватности и эффективности выбранной схемы;
– чувствительности опухоли;
– достижении операбельного состояния.
Обычно используют несколько (в среднем 4-6) циклов химиотерапии.
Необходимость назначения химиотерапии после операции диктуется результатами гистологического исследования удаленной опухоли и лимфатических узлов. Помимо этого, исследуется содержание рецепторов к эстрогенам и прогестерону, а также HER-2/neu статус (в зависимости от особенности опухоли подбирают лечение в послеоперационном периоде). Основной задачей в этом случае является профилактика возникновения отдаленных метастазов (профилактика метастатической болезни). При необходимости проведения химиотерапии стандартом считается 4-6 курсов с интервалом в 3-4 недели.
В ряде случаев химиотерапия назначается как до, так и после операции. В этой ситуации лечащий врач подробно разъясняет женщине необходимость подобной комбинации. Химиотерапия может использоваться как основной метод лечения без операции, когда опухолевый процесс уже распространенный и есть отдаленные метастазы.
Современные схемы химиотерапии обычно включают в себя препараты либо разнонаправленного действия, либо взаимно усиливающие друг друга. Наиболее эффективные из них антрациклины (адриамицин, адриабластин, доксорубицин, фармарубицин и т.д.) и таксаны (Таксотер®, паклитаксел).
В настоящее время Таксотер® – один из наиболее эффективных химиотерапевтических препаратов, применяемых для лечения рака молочной железы.
В зависимости от особенностей рака молочной железы и состояния пациента выбирают тот или иной режим назначения Таксотера®.
Таксотер® можно назначать как с антрациклинами (одновременно или последовательно), так и в комбинированной химиотерапии без антрациклинов, в монорежиме (самостоятельно), а также использовать в комплексе с трастузумабом при гиперэкспрессии HER-2/neu.
Как известно, при использовании любых медицинских препаратов, могут возникать нежелательные явления и химиотерапия не является исключением. Наиболее распространенные – тошнота, рвота. Это связано с тем, что противоопухолевые агенты повреждают не только опухолевые, но и нормальные клетки желудочно-кишечного тракта. У некоторых начинается обезвоживание, анорексия. В этом случае интервал между курсами необходимо увеличить, либо полностью отказаться от этого метода лечения. Однако есть больные, у которых подобные эффекты вообще не возникают.
Существует ряд рекомендаций, позволяющих не только уменьшить, но иногда и полностью избежать побочных эффектов. Необходимо учитывать, что у некоторых больных, помимо истинной (острой или отсроченной), тошнота и рвота носят психогенный характер и начинаются только от одного вида процедурного кабинета или разведенного препарата.
Современная противорвотная терапия предлагает широкий спектр препаратов, благодаря которым у 90% больных эти явления можно предупредить заранее. Наиболее часто применяются: навобан, зофран, китрил, эменд.
Помимо этого, пациентке должны дать практические рекомендации о режиме питания при проведении химиотерапии:
– есть чаще, маленькими порциями;
– исключить приторно-сладкие и острые блюда, отдавая предпочтение продуктам с кислым и слегка соленым вкусом;
– не следует употреблять тяжелую, трудно перевариваемую пищу, на 2-3 дня перейти на легкую, но с достаточным количеством калорий.
В интервалах между курсами химиотерапии можно применять гепатопротекторы (гептрал, эссенциале, карсил и т.д.), способствующие восстановлению печеночной паренхимы.
Многих пациенток волнует выпадение или потеря волос (алопеция) – один из наиболее частых побочных эффектов. Как скоро он начинается и прекращается, зависит от конкретной ситуации. Обычно в течение года волосы полностью восстанавливаются, а иногда становятся даже лучше.
Чрезвычайно важно при проведении химиотерапии контролировать показатели крови, в частности, лейкоциты.
Исследование проводится в динамике, обязательно перед каждым следующим введением. При резком падении лейкоцитов (ниже 2,5 тыс.) свободный интервал может быть продлен, либо лечение включает поддержку колониестимулирующими факторами. Считается, что способствуют этому грецкие орехи, печень, красная икра, красное сухое вино,
гранаты и их сок. Специальной диеты, которая увеличивает количество лейкоцитов, нет. В любом случае каждая конкретная ситуация должна обсуждаться с лечащим врачом
• После операции опухолей с положительной реакцией на эстроген может потребоваться гормонотерапия.
Эндокринотерапия, как метод лечения, насчитывает более чем столетнюю историю. Впервые овариэктомию (удаление яичников) выполнил Г. Беатсон у пациенток с запущенным раком молочной железы. В результате из 10-ти прооперированных, в 3-х случаях полностью исчезли все проявления болезни. Позже были открыты основные стероидные гормоны и описаны их взаимоотношения в женском организме между собой и тканями-мишенями.
Этот опыт не стал достоянием истории. Овариэктомия – наиболее частый способ эндокринной терапии для женщин, относящихся к репродуктивному возрасту. Альтернативой хирургическому вмешательству сейчас стало использование агонистов рилизинг-гормонов (золадекс) в комбинации с антиэтрогенами.
В 70-е годы прошлого века на поверхности опухолевой клетки были обнаружены гормональные рецепторы. Именно благодаря им клетка способна воспринимать гормональную стимуляцию, отвечая на нее специфическим действием (деление, созревание и т.д.) Для «женского» рака молочной железы очень важен положительный статус опухоли по рецепторам к эстрогенам и прогестерону (РЭ+, РП+). Только при наличии рецепторов имеет смысл использовать эндокринотерапию. Рецепторопозитивностью отличаются около 2/3 опухолей молочных желез, поэтому в этой группе гормонотерапия – один из самых эффективных вариантов лечения.
Следует отметить, что в разных возрастных группах применяются несколько различные методы эндокринотерапии, поскольку пути образования гормонов у менопаузальных больных и пациенток с сохранной менструальной функцией неодинаковы.
Долгое время «золотым стандартом» независимо от возраста были антиэстрогенные препараты, широкое применение которых началось с 70-х годов прошлого века. Основным механизмом их действия является конкурентное связывание рецепторов эстрогенов с блокадой возможных сигналов, что приводило к снятию эстрогенной стимуляции клеточной пролиферации. Наиболее широко и часто использовался тамоксифен и его аналоги (зитазониум, нольвадекс, торемифен). Эти лекарственные препараты до сих пор остаются
основными в гормонотерапии пациенток репродуктивного возраста.
При сохранной менструальной функции циркулирующие эстрогены активно продуцируются яичниками. Стимуляция их осуществляется гормонами центрального звена (фолликулостимулирующим, лютеинизирующим). Поэтому, помимо связывания рецептора, необходимо добиться максимального снижения уровня циркулирующих женских
гормонов. Для этого сейчас используют: хирургическое удаление яичников (овариэктомия), лучевое воздействие на их ткань, или так называемую «химическую кастрацию». Последняя осуществляется введением препаратов, тормозящих выработку «центральных» гормонов –фолликулостимулирующего и лютеинизирующего. После процедуры
наблюдается резкое снижение функциональной активности яичников, уровень циркулирующих эстрогенов приближается, по абсолютным значениям, к менопаузальному состоянию. Привлекательность данного способа овариэктомии состоит в его обратимости, т.е. при отмене препарата восстанавливается менструальный цикл и репродуктивный статус женщины. Комбинация золадекса и тамоксифена – наиболее часто используемый вариант эндокринотерапии, который позволяет на 50% снизить вероятность повторного заболевания и на 25% – показатель смертности от рака молочной железы.
Продолжительность приема тамоксифена в дозе 20 мг/сут. – не менее 5 лет.
Естественно, что любую женщину, которой рекомендована эндокринотерапия, будет волновать вопрос: какие наиболее частые побочные эффекты могут возникнуть в процессе лечения?
В отношении золадекса к наиболее частым побочным эффектам относят: приливы, изменение настроения (кастрационный синдром), сухость слизистой влагалища. Тамоксифен индуцирует развитие атипической гиперплазии эндометрия, сопровождающейся дисфункциональными маточными кровотечениями, вплоть до карциномы эндометрия.
В этом случае препарат отменяется!
Принимая гормональную терапию, женщина должна не реже одного раза в полгода консультироваться у гинеколога и регулярно проводить ультразвуковое исследование органов малого таза, помимо стандартного обследования.
Говоря об антиэстрогенах, в XXI веке нельзя не сказать несколько слов о перспективе этого класса соединений, что прежде всего связано с фазлодексом (ICI 182, 780. Fulvestrant).
Препарат, в отличие от тамоксифена, не обладает теми побочными эффектами, которые иногда приводят к отмене последнего. Фазлодекс не просто блокирует, он полностью разрушает эстрогеновые рецепторы, а это ведет к остановке пролиферации. В экспериментальных исследованиях было показано, что фульвестрант тормозит развитие не
только опухолей молочной железы, устойчивых к действию тамоксифена, но и опухолей тела матки.
Фазлодекс в целом хорошо переносится. Побочные эффекты регистрируются редко (менее 1%). Приблизительно у 5% больных отмечены боли в суставах, нарушения в системе свертывания крови и местные (препарат вводится инъекционно) реакции. Несколько чаще регистрировались желудочно-кишечные расстройства, приливы (около 20%).
Ожидаемое повышение риска сосудистых реакций и остеопороза не отмечено, именно поэтому препарат особенно рекомендуется группе менопаузальных больных.
Сочетание хорошей переносимости и выраженной эффективности способствует все более широкому внедрению фульвестранта в клиническую практику, особенно при прогрессировании на фоне предшествующего лечения.
Последнее время проводятся исследования применения фазлодекса вместо тамоксифена совместно с золадексом в качестве послеоперационного лечения молодых больных с рецепторопозитивными опухолями.
Скорее всего, все имеющиеся положительные качества в самом ближайшем будущем сделают фульвестрант «золотым стандартом» эндокринотерапии XXI века, каким в XX веке был тамоксифен.
У женщин в период менопаузы источником эстрогенов являются не яичники, а надпочечники и жировая ткань. В этих органах под действием ароматазы (ключевой фермент реакции ароматизации) продуцируются эстрогены. Поэтому сейчас назначение антиэстрогенов при рецепторопозитивном раке молочной железы у женщин менопаузального возраста считается менее правильным, чем использование ингибиторов ароматазы. Классическими представителями этой группы являются фемара (летрозол) и аримидекс (анастрозол).
Ингибиторы ароматазы не должны назначаться молодым женщинам, поскольку снижение продукции эстрогенов, в частности, в жировой ткани, неминуемо приведет к их увеличению в функционирующих яичниках (эффект обратной связи).
Многочисленные исследования показали: применение ингибиторов ароматазы достоверно снижает риск возникновения рецидива заболевания и на 12% риск смертности.
Частота возникновения контрлатерального рака молочной железы при использовании анастрозола приблизительно в 4 раза ниже, чем при применении тамоксифена.
Препараты этой группы практически лишены тех побочных эффектов и осложнений, которые развиваются при приеме тамоксифена: не отмечается патологии эндометрия, системы коагуляции (свертывания крови), а также кастрационный синдром.
Ингибиторы ароматазы сейчас используются в качестве послеоперационного лечения при непереносимости или прогрессировании на фоне антиэстрогенов, а также до хирургического этапа при неоперабельных опухолях.
Современная эндокринотерапия – наиболее щадящий и эффективный метод лекарственной терапии для больных раком молочной железы с гормонально чувствительной опухолью.
Оказывая выраженный противоопухолевый эффект, гормонотерапия сохраняет хороший уровень качества жизни, не вызывает характерных для химиотерапии побочных эффектов – тошноту, рвоту, выпадение волос, анемию и лейкопению (снижение количества лейкоцитов.)
• Женщины, у которых удалена часть груди или вся грудь, могут воспользоваться пластической хирургией. Пластическая операция может быть произведена во время операции по удалению груди или позже.
Современные экзопротезы учитывают все анатомо-топографические особенности проведенной операции. В комплект, который предлагается женщине, включено эстетическое белье, топы, купальники.
Все это делает дефект практически незаметным.
Опытные консультанты подбирают для каждой женщины подходящий именно ей по форме, цвету, размеру и весу экзопротез. Правильно подобранный протез должен отвечать не только эстетическим задачам, но и являться лечебно-профилактическим средством, обеспечивающим наиболее быструю послеоперационную адаптацию и заживление
тканей. Такой протез предупреждает нарушение осанки, искривление позвоночника, опущение плеч и т.д.
Основные правила выбора экзопротеза:
1. масса протеза должна максимально соответствовать массе другой молочной железы;
2. размер экзопротеза подбирается по чашечке бюстгалтера;
3. экзопротез должен максимально компенсировать возникший после мастэктомии дефект;
4. во время примерки женщине лучше не брать протез в руки. Если ей все же любопытно, то необходимо сразу разъяснить, что его тяжесть только видимая. На самом деле молочная железа весит ровно столько же;
5. форма экзопротеза должна соответствовать форме молочной железы.
Современные протезы разнообразны по форме – овальные, треугольные, каплевидные. Они весьма сходны по своим свойствам с женской грудью. Экзопротезы имеют мягкую и нежную структуру, быстро принимают температуру тела.
В последних моделях экзопротезов предусмотрена система фиксации непосредственно к поверхности грудной клетки. Протез лучше облегает, с большей точностью корректирует дефекты. Тем не менее, носить его более 12 час. в день не рекомендуется.
Помимо этого, современные экзопротезы разрабатываются еще и с учетом их функциональных задач. Послеоперационные протезы –легкие, не мешающие заживлению раны. Их можно носить практически сразу после удаления дренажа.
Облегченные – при большой молочной железе, при лимфатическом отеке на стороне операции. Эти протезы особенно удобны в жаркую погоду.
Специальные протезы, предназначенные для занятий плаванием и посещений физкультурного зала.
Экзопротезы не доставляют женщине много хлопот в гигиеническом плане. Их рекомендуется ежедневно мыть в теплой воде с мылом, после чего вытирать мягким полотенцем. Ночью хранят в специальной упаковке, чтобы форма оставалась неизменной. После посещения бассейна, где вода может быть хлорированной или морской, нужно тщательно вымыть протез. По возможности его необходимо оберегать от булавок и длинных ногтей, поскольку возможна травма протеза.
И все же у части женщин полноценная психологическая реабилитация возможна лишь после выполнения реконструктивно-пластической операции.
В зависимости от того, какой «материал» используется в пластической операции, методики бывают:
1. Использующие только силиконовый материал – экспандер-протез.
2. Использующие комбинацию силиконового материала и собственные ткани – торако-дорзальный лоскут (донорская зона- широчайшая мышца спины) и силиконовый эндопротез;
В основном используются силиконовые протезы.
3. Реконструкция собственными тканями – различные виды кожно-мышечных лоскутов.
Без сомнения, каждая из методик может сопровождаться послеоперационными осложнениями. Об этом больную также предупреждают.
Наиболее частые из них: образование вокруг импланта фиброзной (констрикторной) капсулы, отторжение протеза, кожный некроз.
Завершающий, окончательный этап любой реконструкции – создание сосково-ареолярного комплекса, относящийся к вторичным реконструктивным процедурам. Выполнение его также в значительной степени решается больной, равно как и методика восстановления.
Таким образом, восстановление утраченной в процессе лечения молочной железы – вовсе не заоблачная перспектива, а вполне реальный шаг, сделать который под силу многим женщинам.
1. Размер опухоли в молочной железе.
2. Количество пораженных метастазами регионарных лимфатических узлов.
Принципиально важным является:
• их отсутствие;
• метастазы в 1-3-х лимфатических узлах;
• метастазы в 4-х и более лимфатических узлах.
Качество жизни, ее продолжительность, проводимое лечение – все находится в прямой зависимости. Чем меньше диаметр опухоли, тем больше продолжительность жизни. Чем меньше лимфатических узлов поражено, тем менее агрессивной будет терапия.
3. Рецепторы к стероидным гормонам в опухоли.
Женские половые гормоны (эстрогены и прогестерон) могут стимулировать рост и развитие опухолевой популяции. Однако это происходит далеко не со всеми опухолями. Для осуществления данного эффекта необходимо, чтобы на поверхности опухолевой клетки находился «замочек» или воспринимающий гормональную стимуляцию аппарат – рецептор к соответствующему гормону. Такие рецепторы находятся практически в 2/3 опухолей молочных желез. Определяют их биохимическим или иммуногистохимическим способом. Последний –наиболее предпочтителен. Причем материалом может служить как ткань опухоли, так и «готовые послеоперационные(парафиновые) блоки». В процессе изучения рецепторопозитивных опухолей выяснили, что они обычно высокодифференцированы и хорошо реагируют на один из вариантов лекарственного лечения –эндокринотерапию. Гормональные препараты, применяемые в этом случае, способны блокировать соответствующие рецепторы, делая невозможной их связь с циркулирующими гормонами.
4. Рецептор эпидермального фактора роста HER2.
Около 30% женщин, страдающих раком молочной железы, имеют HER2- положительные опухоли. Помимо гормонов, на поведение клеток в организме влияют еще и так называемые ростовые факторы.
Имеющийся на поверхности клеток HER2-рецептор определяет ее реакцию на ростовые факторы. Причем экспрессируется он любой клеткой, но в разных количествах. В некоторых опухолях его так много, что это приводит к ускорению и без того быстрого деления и пролиферации. Сейчас HER2-рецептор можно определить тремя методами:
– иммуногистохимически;
– флюоресцентной in situ гибридизацией;
– хромогенной гибридизацией in situ
Считается, что HER2-положительные опухоли – особая форма рака, отличающаяся неблагоприятным прогнозом, требующая более агрессивного лечения. В этих случаях обязательно применение таргетной терапии, или терапии мишеней. Применение моноклональных антител –блокаторов HER2-рецептора у таких больных значительно интенсифицирует системное лекарственное лечение и увеличивает безрецидивный интервал.
Одним из основных препаратов этой группы является герцептин (трастузумаб). Препарат блокирует HER2-рецептор, снижает способность клеток к активной пролиферации, повышает чувствительность к химиотерапии. Он применяется во всех случаях установленной гиперэкспрессии или амплификации HER-2/neu (т.е. при HER2-позитивных
опухолях). Современная наука активно развивает это направление.
Сейчас уже есть лекарственные формы блокаторов HER1 и HER2 – лапатиниб, а также VEGF(фактор роста опухолевых сосудов) – авастин (бевацизумаб). На фоне приема авастина прекращается опухолевый ангиогенез, т.е. опухоль не получает питательные вещества и погибает.
В последние годы начато совместное применение герцептина и авастина, результатом которого является разнонаправленное воздействие на опухолевую ткань, приводящее к большей эффективности лечебной программы.
• Очень мелкие опухоли, которые невозможно почувствовать, можно определить с помощью маммографии. Женщины в возрасте более 50 лет должны проходить маммографию ежегодно, а женщины в возрасте от 40 до 50 лет должны обсудить с врачом свои факторы риска, чтобы определить, когда следует начинать делать маммографию.
• Обследование должно проводиться радиологом, специализирующимся в области маммографии, или в маммологическом центре.
• Женщины должны ежегодно проходить обследование груди у врача.
• Женщины должны ежемесячно обследовать грудь (лучше всего через два-три дня после менструаций). Ткань груди обычно немного бугристая и неровная, поэтому важно привыкнуть к нормальному контуру и текстуре груди. Тогда легче будет определить изменения текстуры и внешнего вида.
• Регулярные упражнения и поддержание нормального веса могут снизить риск возникновения рака груди после менопаузы.
• Женщины, у которых велик риск возникновения рака груди, могут прибегнуть к химической профилактике болезни, принимая тамоксифен в течение пяти лет. Решение о принятии тамоксифена должно быть принято после обсуждения риска заболевания и перспектив лечения с врачом.
• Женщины, у которых в семье есть случаи заболевания раком груди, могут пройти генетический тест на наличие генов рака груди. Женщины с положительным результатом теста должны находиться под усиленным наблюдением с целью выявления как рака груди, так и рака яичников, или рассмотреть возможность превентивного удаления грудей или яичников.
• Обратитесь к врачу, если вы обнаружили бугорок в любом месте груди или под мышкой. Большинство бугорков не являются канцерогенными, но необходима биопсия, чтобы поставить окончательный диагноз.
• Свяжитесь с врачом, если вы заметили любые изменения размера, формы или внешнего вида груди, или если у вас есть какие-либо выделения из соска.
источник