Хирургическое лечение опухолей и кист средостения
Больные с различными опухолями и кистами средостения составляют, по различным статистическим данным, от 0,5 до 3% всех больных опухолями. Существует много различных классификаций опухолей и кист средостения. Мы делим их на четыре основные группы: первая — злокачественные опухоли, вторая — доброкачественные опухоли, третья — кисты, к четвертой группе относим загрудинный и внутригрудной зоб.
Деление опухолей средостения на злокачественные и доброкачественные является условным, так как иногда точную границу между ними провести нельзя. Например, при тератоме или тимоме вообще трудно определить границу перехода доброкачественного новообразования в злокачественное.
В нашей клинике оперировано свыше 300 больных с различными новообразованиями средостения. При этом злокачественные опухоли были у четверти больных, что не отражает истинного соотношения различных опухолей средостения, так как большинство больных со злокачественными опухолями поступает в специализированные онкологические и радиологические стационары для лучевого и химиотерапевтического лечения.
Диагностика. Основными методами диагностики опухолей и кист средостения в настоящее время являются различные рентгенологические методы. Всем больным необходимо производить прямую и боковую рентгенографию грудной клетки. У ряда больных очень показательные данные удается получить путем томографии. Для более рельефного выявления различных новообразований средостения большую ценность имеет так называемая пневмомедиастинография, т. е. рентгенография после введения в клетчатку средостения воздуха или кислорода, который вводят под местной анестезией за рукоятку грудины, под мечевидным отростком или около края грудины в одном из межреберных промежутков в количестве от 500 до 1000 см 3 . При анализе пневмомедиастино- или пневмомедиастино-томограмм, который должен быть произведен квалифицированным рентгенологом, в большинстве случаев удается достаточно точно определить локализацию, размеры и другие особенности имеющегося новообразования.
От ряда более сложных методов исследования (ангиография, азигография, торакоскопия, пункционная биопсия через грудную стенку, чрезбронхиальная биопсия) в настоящее время мы почти отказались. Окончательное уточнение диагноза происходит, как правило, на операционном столе. Во время операции при всех относительно неясных случаях участок опухоли должен быть взят для срочного гистологического исследования с целью установления ее природы и уточнения операбельности.
Рассмотрим первую группу — злокачественные опухоли средостения. Наиболее частыми разновидностями этих опухолей являются лимфогранулематоз, лимфосаркома, ретикулосаркома, относящиеся к системным злокачественным опухолевым формам лимфоретикулоза, а также различные виды тимом, злокачественных внутригрудных и загрудинных струм.
Лимфогранулематоз нередко трудно дифференцировать от лимфосаркомы и ретикулосаркомы. Согласно исследованиям Скотта, различие этих трех опухолевых форм заключается главным образом в степени дифференциации клеток. Поэтому некоторые авторы объединяют их под общим названием «лимфомы», или опухолевые формы ретикулоза.
У больных лимфогранулематозом имеется определенная, подчас весьма сложная клиническая симптоматика, выражающаяся повышением температуры, изменениями крови с лейкоцитозом, эозинофилией и ускоренной РОЭ и нередко кожным зудом. В связи с тем что эти симптомы у многих больных бывают выражены слабо, они не привлекают к себе должного внимания. Главным признаком, с которым приходится сталкиваться в хирургической клинике, являются рентгенологические симптомы. Компрессионный синдром развивается позже. Диагноз лимфогранулематоза бывает относительно прост в тех случаях, когда наряду со средостением поражаются различные группы периферических лимфатических узлов; при поражении только медиастинальных лимфатических узлов диагноз весьма труден и просто невозможен без биопсии.
Для взятия биопсии раньше приходилось прибегать к торакотомии. В настоящее время у ряда больных материал для гистологического исследования может быть получен более простым способом — при медиастиноскопии. Способ медиастиноскопии, предложенный Карленсом, состоит в следующем. Под наркозом делают небольшой разрез над яремной вырезкой. Затем с помощью ларингоскопа, бронхоскопа или специально сконструированного инструмента медиастиноскоиа — тупо расслаивают клетчатку позади грудины и проникают в переднее средостение. Кусочки ткани из лимфатических узлов или непосредственно из опухоли берут бронхоскопическими цапками или специальными щипцами.
При подтверждении диагноза лимфогранулематоза средостения хирургическое вмешательство обычно целесообразно при ограниченных поражениях; при распространенных — более эффективно лучевое и в некоторых случаях — химиотерапевтическое лечение или их последовательное сочетание.
Особенно эффективна лучевая терапия при лимфосаркоме средостения. У больных с лимфосаркомой опухоль иногда буквально «тает» под влиянием облучения и может даже исчезнуть совсем. У нас имеется одно наблюдение выздоровления больного с гистологически доказанной лимфосаркомой средостения после лучевого лечения, причем больной прослежен на протяжении 8 лет. Обычно же, однако, у этих больных возникают рецидивы. В случаях рецидива опухоли, исходящей из лимфоидной ткани, повторное лучевое лечение гораздо менее эффективно, применение химиотерапии (допан, хлорбутан, дегранил и др.) может сопровождаться более длительными ремиссиями.
Опухоли, исходящие из зобной железы, называют тимомами. В отечественной литературе мы описали первую операцию по поводу тимомы в 1954 г. Обычно тимомы имеют злокачественный характер. Несмотря на медленный рост, малигнизация тимом раньше или позже наступает почти всегда. Макроскопически тимомы представляют собой относительно большие округлые или уплощенные образования, которые на разрезе имеют так называемое бахромчатое строение. В отдельных случаях опухоль может иметь кистозный характер. Дифференциальная диагностика между тимомами, лимфосаркомами и лимфогранулематозом весьма трудна. Тимомы, как правило, располагаются непосредственно за рукояткой или телом грудины и только в запущенных случаях сдавливают или смещают трахею либо пищевод. Однако сосуды средостения и особенно плечеголовные вены при тимоме все же сдавливаются, что затрудняет отток по венозной системе головы и шеи. В таких случаях лицо больного бывает цианотично, отечно, вены на шее напряжены, венозное давление повышается и может достигать 150-200 мм вод. ст. и более, иногда отмечаются кровоизлияния в склеры.
Больной Л, 42 лет, поступил с жалобами на умеренные боли в правой половине грудной клетки. Больным себя считает 3 месяца. Стал отмечать боли в правой половине грудной клетки. Обратился к врачу и при рентгенологическом обследовании была обнаружена опухоль средостения. Ранее ничем не болел. Работает кузнецом.
Общее состояние при поступлении вполне удовлетворительное. Физически развит хорошо. Одышки нет. Поверхностные лимфатические узлы не увеличены. Перкуторно над легкими ясный легочный звук, аускультативно — дыхание везикулярное, хрипов нет. Границы сердечной тупости расширены вправо на 2-3 см. Тоны сердца ясные, шумов нет. Артериальное давление 125/75 мм рт. ст. Другие органы без патологии.
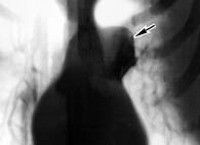
Рентгенологически (обычное исследование, томография, пневмомедиастинография): наличие патологической тени размером 6×8 см, неправильно-округлой формы, располагающейся в переднем средостении; тень имеет бугристые неровные контуры, однородна (рис. 112). На томограммах в условиях пневмомедиастинума определяется конгломерат увеличенных лимфатических узлов в области корня правого легкого. Легочный рисунок диффузно усилен. Правый купол диафрагмы несколько деформирован. Левое легкое без изменений. Срединная тень не смещена.
Заключение; новообразование переднего средостения, по-видимому, тимома, не исключена возможность озлокачествления новообразования.
Клинические анализы крови и мочи без отклонения от нормы.
Диагноз: новообразование переднего средостения, расположенное больше справа, по-видимому, тимома. Противопоказаний к операции нет.
Сделана торакотомия справа по пятому межреберью. В плевральной полости выпота, спаек нет. Правое легкое без признаков патологии. Непосредственно за грудиной в переднем средостении располагается большая бугристая, плотная на ощупь опухоль, продолговатая по форме, интимно спаянная с перикардом, дугой аорты и верхней полой веной, но без признаков прорастания этих органов. Поражения лимфатических узлов не обнаружено. Острым путем опухоль постепенно, со значительными техническими трудностями отделена от перикарда, дуги аорты и верхней полой вены, после чего удалена. Гемостаз. Плевральная полость промыта антибиотиками. Введен один дренаж. Рана грудной стенки ушита наглухо.
Препарат: опухоль размером 11x6x6 см, весом 200 г, на разрезе буровато-мясистая, с двумя очагами распада. При гистологическом исследовании удаленная опухоль оказалась тимомой с признаками озлокачествления. Послеоперационный период протекал без осложнений.
В хирургической клинике нам более часто приходится встречаться с доброкачественными опухолями средостения, прежде всего с так называемыми неврогенными опухолями.
Неврогенные опухоли практически оказываются почти у каждого пятого больного, оперированного по поводу опухоли средостения. В зависимости от гистологического строения среди неврогенных опухолей различают ганглионеврому, ганглионейробластому, невриному.
Клиника неврогенных опухолей отличается некоторыми особенностями, обусловленными тем, что опухоль исходит либо из симпатического нервного ствола, либо из межреберных нервов или из нервных корешков спинного мозга. Все симптомы мы делим на три основные группы.
Первая группа — это неврологические признаки: боли в груди, синдром Хорнера, положительная проба Минора, изменение чувствительности кожи на стороне поражения, а в редких случаях — парезы верхних или нижних конечностей. Вторая группа симптомов обусловлена сдавлением сосудов и органов средостения, третья группа — деформацией костей грудной клетки.
При рентгенологическом исследовании больных с неврогенными опухолями обнаруживают округлую интенсивную гомогенную тень, которая имеет ровные контуры и располагается в задних отделах средостения, примыкая к позвоночнику или к задним отрезкам ребер. Она особенно хорошо контурируется после наложения пневмомедиастинума или пневмоторакса.
Существенное практическое значение имеют некоторые варианты неврогенных опухолей, обусловленные особенностями их роста. Так, некоторые опухоли имеют форму песочных часов. При этом одна часть такой опухоли располагается в позвоночном канале, а другая — в грудной полости. У ряда больных с неврогенными опухолями ввиду вовлечения в процесс симпатического ствола отмечаются различные секреторные, вазомоторные и трофические расстройства кожи, верхней половины туловища, верхней конечности, шеи, лица на стороне опухоли. В связи с этим подобных больных следует консультировать со специалистом-невропатологом.
Своевременное хирургическое вмешательство при неврогенных опухолях средостения очень эффективно. Операция дает минимальную летальность и сопровождается практически полным и стойким выздоровлением оперированных больных. В то же время длительное откладывание операции или отказ от оперативного лечения у таких больных могут приводить к очень тяжелым последствиям.
Больной Ш., 41 года, поступил с жалобами на резкую слабость, отсутствие движений в нижних конечностях, потерю чувствительности в них, нарушение мочеиспускания. Опухоль средостения диагностирована 12 лет назад. Полгода назад в одной пз клиник сделана безуспешная попытка удалить опухоль. При обследовании в нашей клинике диагностирована невринома заднего средостения справа с деструкцией II, III грудных позвонков и II ребра и явлениями сдавления спинного мозга (на уровне Д3), а также правой подключичной, плечеголовной и частично верхней полой вены (рис. 113 и 114).
Произведена операция под эндотрахеальным наркозом из бокового правостороннего доступа по четвертому межреберью. При срочном гистологическом исследовании кусочка опухоли установлен диагноз нейрофибромы. Опухоль размером 12x10x8 см, весом 315 г выделена острым путем и удалена, сдавление спинного мозга устранено. Послеоперационное течение гладкое. На 5-й день отмечено самостоятельное мочеиспускание. Через месяц после операции больной начал ходить. Через 6 месяцев ходит свободно по 2-3 км, боли в ногах не беспокоят, чувствительность не нарушена, тазовых расстройств нет. Наступило полное выздоровление.
Другими частыми доброкачественными новообразованиями средостения являются так называемые тератоидные образования, к которым относят эпидермоидные и дермоидные кисты и тератомы.
Дермоидные кисты образуются вследствие отщепления частиц эктодермы и погружения их в средостение при слиянии кожных покровов в процессе эмбрионального формирования передних отделов грудной клетки. Практически дермоидные кисты состоят из различных тканей: соединительной, эпителия, сальных желез и т. д. Поэтому их относят к так называемым органоидным образованиям. Характерная локализация дермоидных кист — передневерхний отдел средостения. У ряда больных кисты располагаются и в нижних отделах средостения.
Наиболее достоверным клиническим симптомом дермоидной кисты является откашливание больным кашицеобразных масс с примесью жира и волос, что наблюдается в связи с прорывом кисты в бронх. Этот симптом встречается примерно у 30% больных. До прорыва могут наблюдаться кашель, кровохарканье, боли в груди. У ряда больных при длительно протекающих доброкачественных опухолях средостения, в частности тератоидных, отмечается выпячивание грудной клетки в области расположения опухоли. У половины больных опухоль вызывает различные нарушения со стороны сердечно-сосудистой системы: приступы грудной жабы, сжимающие боли в области сердца, учащение пульса.
Рентгенограммы больного с дермоидной кистой переднего средостения приведены на рис. 115.
При всех дермоидных кистах и тератомах средостения показано радикальное оперативное вмешательство с удалением опухоли. Операция нередко представляет большие технические трудности, так как в результате длительного существования опухоли и воспалительного процесса происходит обширное спаяние ее с окружающими органами и тканями. Поэтому полное удаление новообразования не всегда оказывается возможным. В этих случаях рекомендуется часть капсулы образования оставить, обработав ее острой ложкой и настойкой йода.
Более редкими доброкачественными новообразованиями средостения являются липомы, лимфангиомы, бронхогенные или эпителиальные кисты, целомические перикардиальные кисты. Эти новообразования, как правило, протекают доброкачественно. Но и при них в отдельных случаях может наблюдаться малигнизация со всеми вытекающими отсюда последствиями. Поэтому радикальное оперативное вмешательство рекомендуется при всех доброкачественных новообразованиях средостения.
Все операции при опухолях средостения в настоящее время производятся под эндотрахеальным наркозом с мышечными релаксантами и управляемым дыханием. Раньше мы пользовались различными доступами к органам средостения, но в настоящее время основным стал стандартный боковой межреберный разрез по четвертому, пятому или шестому межреберью. Он обеспечивает хороший доступ ко всем отделам грудной полости и практически позволяет удалить любую операбельную опухоль. В отдельных случаях может быть использована срединная стернотомия, а также комбинированный доступ со стороны плевральной полости и со стороны шеи. Последний приходится изредка применять при некоторых формах внутригрудного зоба.
Послеоперационное ведение больных, оперированных по поводу новообразований средостения, не имеет каких-либо специфических особенностей и является общим для торакальной хирургии.
Однако необходимо констатировать, что при доброкачественных опухолях средостения достижения современной анестезиологии и торакальной хирургии позволяют радикально излечивать почти всех больных. В то же время при злокачественных опухолях средостения оперативное удаление их возможно относительно редко, а лучевая терапия и химиотерапия остаются относительно малоэффективными. Чрезвычайно важно своевременно оперировать больных доброкачественными опухолями средостения. Эта тактика предотвращает переход ряда доброкачественных опухолей в злокачественные, ликвидирует опасность прогрессирующего сдавления органов и в целом значительно улучшает исходы лечения больных с различными новообразованиями средостения.
- Баранова А. Г. Диагностика интраторакальных опухолей. Л., 1959.
- Гамов В. С. Однокамерный эхинококк органов грудной полости. Л., 1960.
- Зворыкин А. И. Кнсты и кпстоподобные образоваппя легких. Л., 1959.
- Многотомное руководство по хирургии. Т. 2, кн. 1. М., 1966.
- Осипов Б. К. Хирургические вмешательства на средостении и его органах. М., 1953.
- Петровский Б. В. Хирургия средостения. М., 1960.
Источник: Петровский Б.В. Избранные лекции по клинической хирургии. М., Медицина, 1968 (Учеб. лит. для студ. мед. ин-тов)
источник
Оперативные вмешательства при различных повреждениях и заболеваниях средостения часто являются весьма сложными и ответственными ввиду глубины залегания и наличия в нем большого количества жизненно важных органов, сосудов, нервов. Поэтому каждой такой операции должно предшествовать тщательное обследование больного, обсуждение показаний и противопоказаний к хирургическому лечению и необходимая предоперационная подготовка.
При травматических повреждениях и различных заболеваниях средостения показания к хирургическому лечению устанавливаются индивидуально.
При травме средостения и ее последствиях могут встретиться весьма срочные показания к операции : нарастающая медиастинальная эмфизема, гематома, сдавление органов средостения осколком или пулей, двусторонний пневмоторакс. Менее срочные показания имеются при большинстве слепых ранений средостения, наличии не-инфицированного инородного тела в клетчатке средостения, повреждении грудного лимфатического протока и т. д. Так же различны по срочности показания к операции при воспалительных процессах в средостении. Острый гнойный и в особенности гнилостный медиастинит требует неотложного вмешательства, тогда как подострые и хронические медиастиниты обычно заканчиваются благополучно при консервативном лечении.
Злокачественные опухоли средостения оперируют редко ввиду быстрого роста опухоли и прорастания ею окружающих жизненно важных органов. Так, из 26 больных с первичными злокачественными опухолями средостения нам удалось оперировать только 9, причем радикальная операция была выполнена у 7 больных. Примерно такие же данные приведены в работах других авторов [Зейболд (Seybold, 1949); Б. К. Осипов, 1953, и др.].
Чаще удается выполнить операцию при начальных фазах малигнизации доброкачественных опухолей и кист средостения.
В литературе приводятся многочисленные истории болезни, при анализе которых можно сделать вывод о часто встречающихся осложнениях, наблюдающихся при доброкачественных медиастинальных опухолях и кистах. Они прежде всего зависят от роста опухоли и сдавления его сосудов, трахеи, сердца, а также от инфицирования содержимого кисты [Ю. Ю. Джанелидзе, 1929; Гойер и Эндрас (Goyer, Andrus, 1940); Кей (Key, 1954) и др.]. По данным Г. Б. Быховского (1899), при дермоидных кистах средостения, леченных консервативно, прогноз плохой в 100% случаев (наблюдалось 24 больных).
Аналогичные данные о фибромах средостения сообщают Гойер и Эндрас (1940). Следует отметить высокий процент малигнизации доброкачественных кист и опухолей. Так, по Кенту (Kent, 1944), она составляет 37—41%.
Таким образом, опыт большинства хирургов говорит о наличии прямых показаний к операции у всех больных, имеющих доброкачественные опухоли и кисты средостения.
Аналогичные показания приняты и при загрудинном зобе, опасности которого особенно отчетливо выявляются в верхней апертуре грудной клетки, где опухоль ущемляется. В таких случаях трахея, как правило, смещается в сторону или сдвигается растущим новообразованием.
Вместе с тем успехи хирургии последних лет в значительной степени уменьшают риск оперативного вмешательства при инородных телах, опухолях и кистах средостения. Летальность после подобных операций составляла к 1956 г. 7—10%, а в настоящее время еще больше снизилась.
Все сказанное также подтверждает необходимость расширения показаний к хирургическому лечению заболеваний средостения.
источник
Средостение, которое является центральной частью грудной клетки, находится между правой и левой плевральной полостью и простирается от грудины спереди до позвоночного столба сзади. Это пространство содержит все органы грудной полости, за исключением легких. Поскольку многие опухоли и кисты средостения имеют характерную локализацию, средостение можно искусственно разделить на различные отделы, чтобы облегчить локализацию специфических патологических образований. Большинство авторов подразделяют средостение на 3 отдела: переднее, среднее и заднее. Передним отделом средостения называют область, которая находится сзади от грудины, спереди от сердца и крупных сосудов и содержит тимус, лимфатические узлы средостения и жировую клетчатку. В среднем отделе средостения находятся сердце, перикард, легочная артерия и вены, восходящии отдел и дуга аорты, брахиоцефальные сосуды, полая вена, трахея, бронхи и лимфатические узлы. Задний отдел средостения находится сзади от сердца и содержит пищевод, нисходящий отдел аорты, непарную вену, ганглии и нервы автономной нервной системы, грудной проток, лимфатические узлы и жировую ткань.
Образования средостения имеют различную природу: от медленно растущих доброкачественных образований, имеющих минимальные симптомы, до агрессивных инвазивных опухолей, которые могут активно метастазировать. Образования средостения наиболее часто отмечаются в переднем средостении (56%), реже — в заднем (25%) и еще реже — в среднем (19%) средостении. Хотя в некоторых сериях приведены различия в относительной распространенности опухолей и кист средостения, чаще всего встречаются опухоли из нервной ткани (20%), тимомы (19%), первичные кисты (18%), лимфомы (13%) и герминальноклеточные опухоли (10%).
Пациенты с опухолями средостения могут не иметь каких-либо клинических симптомов заболевания, и диагноз устанавливают случайно, при обычной рентгенографии грудной клетки. И наоборот, у пациентов могут отмечаться системные симптомы или связанные с механическими эффектами инвазии или компрессии. К наиболее распространенным симптомам относятся боль в грудной клетке, лихорадка, кашель и диспноэ. Симптомы, связанные с компрессией или инвазией органов средостения, например синдром верхней полой вены, синдром Горнера, охриплость голоса или сильные боли, обычно более характерны для злокачественной патологии, хотя могут отмечаться и у пациентов с доброкачественными заболеваниями.
Основная цель диагностической оценки пациентов с образованиями средостения — постановка точного гистологического диагноза, что позволит подобрать оптимальную терапию. Для гистологической диагностики можно провести чрескожную игольную биопсию, особенно пациентам с образованиями переднего средостения. Однако низкодифференцированные злокачественные опухоли переднего средостения, в частности тимомы, лимфомы, герминогенные опухоли и первичный рак, могут иметь в значительной мере схожие цитологические и морфологические признаки. Если игольная биопсия противопоказана или не дала достаточного количества ткани для установления гистологического диагноза, нередко может возникнуть необходимость в более инвазивных процедурах — медиастиноскопии и торакоскопии. Медиастиноскопия — полезная методика для оценки и проведения биопсий при образованиях среднего отдела средостения. Для биопсии и резекции разных образований средостения у тщательно отобранных пациентов используют торакоскопические операции. Хотя большинству пациентов можно безопасно проводить хирургические операции, больные с образованиями средостения средних и крупных размеров, в частности дети, имеют повышенный риск развития тяжелых кардиореспираторных осложнений во время общей анестезии. Пациенты с постуральным диспноэ и синдромом верхней полой вены относятся к группе повышенного риска. У пациентов с обструкцией дыхательных путей или верхней полой вены риск общей анестезии значительно возрастает, и попытки верифицировать диагноз гистологически должны быть ограничены игольными биопсиями или открытыми операциями под местной анестезией. Большая часть этих образований — злокачественные и нерезектабельные.
Видеоторакоскопия — полезный диагностический и терапевтический метод, применяемый при работе с образованиями переднего средостения. Дифференциальную диагностику при лимфоме, тимоме или герминально-клеточной опухоли трудно провести на основании одного только цитологического исследования. В связи с тем что тонкоигольная аспи- рационная биопсия образований переднего отдела средостения часто неинформативна, видеоторакоскопия может играть важнейшую роль в получении адекватного количества ткани для постановки точного гистологического диагноза. Более того, видеоторакоскопия позволяет диагностировать опухолевую инвазию или метастатическое распространение, которое не было обнаружено при предоперационном обследовании, и позволяет провести непосредственное удаление опухолей, имеющих выраженную капсулу. У пациентов с инвазивными опухолями, требующими резекции, видеоторакоскопия помогает выяснить, какой из доступов будет наиболее оптимальным при конверсии: торако- или стернотомия.
Для большинства пациентов с опухолями переднего отдела средостения видеоторакоскопию применяют в первую очередь для диагностики. Хотя с ее помощью возможно проведение резекции некоторых опухолей (например, мелких тимом) переднего отдела средостения, стандарт лечения в таких ситуациях в настоящее время — открытая резекция. У пациентов с кистами переднего средостения или генерализованной миастенией без тимомы с помощью видеоторакоскопии можно проводить полную резекцию образования.
Техника торакоскопической операции на средостении
Оперативное лечение пациентам с образованиями переднего отдела средостения обычно проводят в латеральном положении. Общую анестезию осуществляют через двухпросветную эндотрахеальную трубку для коллабирования легкого на стороне поражения. Первый 10-миллиметровый порт устанавливают по срединно-подмышечной линии в шестом или восьмом межреберье. Плевральную полость исследуют с помощью 30-градусной оптики. Остальные порты используют в зависимости от того, какие инструменты необходимы для ретракции и диссекции. Эти порты устанавливают несколько ближе кпереди, чтобы образовалась фигура треугольника с портом для камеры. После рассечения плевры над опухолью делают биопсию или удаляют образование. Если предполагается, что образование имеет сосудистое происхождение, можно провести его аспирационную биопсию. После тщательного гемостаза вводят дренажную трубку для кратковременного контроля выделений.
ВИДЕОТОРАКОСКОПИЧЕСКАЯ ТИМЭКТОМИЯ ПРИ ГЕНЕРАЛИЗОВАННОЙ МИАСТЕНИИ
У пациентов с нетимоматозной генерализованной миастенией видеоторакоскопию используют все чаще в качестве эффективной терапевтической опции. Этот доступ приносит симптоматическое улучшение большинству пациентов с минимальными периоперационной смертностью и частотой послеоперационных осложнений. Видеоторакоскопическую тимэктомию можно провести из лево-, право- и двустороннего доступа. Левосторонний видеоторакоскопический доступ обеспечивает превосходный обзор левого диафрагмального нерва, который повреждают чаще, чем правый, и позволяет провести обширное удаление перитимоидной ткани в аортолегочном окне и левом перикардио-диафрагмальном углу. Приверженцы правостороннего доступа при видеоторакоскопии утверждают, что важное преимущество этого метода — увеличенное операционное поле в более широкой плевральной полости. Кроме того, слияние двух брахиоцефальных вен, формирующих верхнюю полую вену, четче визуализируется справа. Право- и левосторонний доступы имеют очень сходные результаты вмешательства.
Правостороннюю видеоторакоскопическую тимэктомию осуществляют в положении пациента лежа на боку, под углом 45° к горизонтальной плоскости, с валиком или подушкой из пенорезины, подложенными под правую половину грудной клетки. Первичный 10-миллиметровый порт устанавливают по срединно-ключичной линии
в седьмом межреберье. Два других порта используют для введения рабочих инструментов. Эти 5-миллиметровые порты устанавливают в третьем и пятом межреберном промежутке по передней подмышечной линии. Затем мобилизуют правый нижний полюс тимуса в краниальном направлении с помощью электрокоагулятора и диссекции острым и тупым путямм. С помощью осторожной тракции можно обнажить и рассечь ножницами ткани, соединяющие тимус с щитовидной железой. Артерии тимуса, входящие в верхние полюса, — это ветви внутренних маммарных артерий, которые клипируют и пересекают. Безымянная вена четко идентифицируется, и венозные притоки от тимуса также клипируют и пересекают. Затем проводят диссекцию правого цервикального рога вместе с перитимической тканью вблизи безымянной и верхней полой вен. После этого идентифицируют левый край тимуса от задней поверхности железы и отделяют его от париетальной плевры слева. Необходимо действовать с осторожностью, чтобы не повредить левый диафрагмальный нерв. Теперь левый нижний полюс полностью мобилизован, и грудинная диссекция завершена. Тимус помещают в защитный контейнер и извлекают через отверстие переднего порта. После этого проверяют гемостаз в средостении и оставшейся жировой ткани переднего средостения. Для кратковременного дренирования устанавливают один плевральный дренаж.
Образования среднего средостения — чаще всего доброкачественные кисты и лимфаденопатия. Биопсию лимфатических узлов для исключения злокачественной опухоли обычно удается провести с помощью шейной или передней медиастиноскопии, однако при более сложных случаях может понадобиться видеоторакоскопия. К кистам средостения относятся бронхогенные, кишечные (дупликационные) и перикардиальные кисты, которые могут вызывать такие симптомы, как боли в грудной клетке, диспноэ, кашель и стридор. Бронхогенные кисты выглядят, как гладкие плотные узлы на уровне карины, которые могут сдавливать пищевод, что можно определить при исследовании с глотанием бария. Дупликационные кисты средостения происходят из заднего отдела первичной кишки, из которой образуется верхний отдел желудочно-кишечного тракта. Эти кисты встречаются реже, чем бронхогенные или перикардиальные, и обычно имеют связь с пищеводом. Для профилактики возможных осложнений бронхогенные и дупликационные кисты необходимо удалять. Перикардиальные кисты, для которых характерно расположение в переднем реберно-диафрагмальном углу, резецируют при симптомах, вызывающих подозрение на их малигнизацию, или при рецидивировании кист после аспирации.
Торакоскопические операции при образованиях среднего отдела средостения проводят в положении пациента латерально. Общую анестезию проводят с помощью двухпросветной эндотрахеальной трубки для одностороннего коллабирования легкого. По средней подмышечной линии в восьмом межреберном промежутке устанавливают 10-миллиметровый порт и осматривают грудную клетку с помощью 30-градусной оптики. Второй разрез (длиной примерно 3 см) делают в четвертом или пятом межреберном промежутке спереди. Легкое отводят в сторону от кисты, которая наиболее часто имеет паратрахеальную или субкаринальную локализацию. Кисту мобилизуют от окружающих структур с помощью тупой и острой диссекций. Аспирация кисты может облегчить ее мобилизацию. Иногда плотное прилегание кисты к жизненно важным органам может препятствовать ее полному иссечению. В этих трудных случаях электрокоагуляция слизистой оболочки остатков стенки кисты должна снизить риск рецидивирования.
Наиболее распространенные внелегочные патологические образования заднего средостения — нейрогенные опухоли [нейролеммомы или нейрофибромы симпатической нервной цепочки либо межреберного нерва]. Эти опухоли могут характеризоваться корешковыми болями или просто патологическими изменениями на рентгенограмме грудной клетки. Было показано, что видеоторакоскопия — эффективный хирургический метод удаления доброкачественных нейрогенных опухолей, который отличает более быстрое выздоровление пациента после операции (по сравнению с открытой резекцией). Обычно торакоскопически можно резецировать опухоли диаметром менее 5 см.
Операции при опухолях заднего средостения проводят в латеральном положении пациента. Общую анестезию осуществляют с помощью двухпросветной эндотрахеальной трубки для одностороннего коллабирования легкого. Десятимиллиметровый порт вводят по срединно-подмышечной линии в шестом или восьмом межреберном промежутке в зависимости от расположения опухоли. Грудную клетку осматривают с помощью 30-градусной оптики. Передний разрез делают в четвертом межреберном промежутке. Диссекцию начинают с рассечения плевры вокруг опухоли. Опухоль мобилизуют, ее сосуды находят, клипируют и пересекают. Нервы, выходящие из опухоли, также находят, клипируют и пересекают. Затем опухоль помещают в эндоскопический контейнер и извлекают через торакотомию. Проверяют надежность гемостаза и устанавливают плевральный дренаж через отверстие порта для кратковременного дренирования.
источник
Ведение послеоперационного периода связано с определенными трудностями.
После операции больные получают увлажненный кислород, ингаляции антибиотиков, соды и химотрипсина, камфору, строфантин, корглюкон (в зависимости от частоты сердечных сокращений), 40% раствор глюкозы с витаминами С и В внутривенно, обезболивающие средства (2% раствор промедола, 50% раствор анальгина), антибиотики парентерально с учетом чувствительности микрофлоры. Таким образом, при гладком течении послеоперационного периода лечебные мероприятия ограничиваются профилактикой сердечно-сосудистых и дыхательных расстройств, инфекции, борьбой с болями.
При нарушении водноэлектролитного баланса, щелочного резерва соответственно назначают препараты калия, хлориды, соду. Учет количества выпитой и выведенной жидкости позволяет своевременно производить коррекцию водного баланса. При явлениях олигурии исследуется содержание остаточного азота, мочевины и электролитов крови. Лечение проявлений почечной недостаточности заключается в повторных вливаниях 20% раствора глюкозы по 200 мл с витаминами B, С, маннитола, гидрокортизона.
Основное внимание уделяется состоянию легких после операции (В. С. Карпенко, А. М. Тарнопольский, В. М. Кравец, 1966). С этой целью в плевральной полости создается эффективное разрежение с помощью вакуум-аппарата. Дренаж из плевральной полости извлекают на следующие сутки, если разрежение стойко удерживается. В этот же день производят рентгеноскопию грудной клетки. Рентгенологический контроль в последующие сутки начинают в зависимости от общего состояния больного, данных аускультации. При наличии в плевральной полости воздуха и экссудата производят пункцию плевральной полости с аспирацией содержимого и введением антибиотиков.
У некоторых больных в послеоперационном периоде усиливается секреция в трахеобронхиальных путях, что приводит к дыхательной гипоксии. В этих случаях мы широко пользовались эндотрахеальным введением антибиотиков на физиологическом растворе путем прокола трахеи. При неэффективности этих мероприятий и рентгенологических признаках ателектаза мы немедленно применяем лечебную бронхоскопию под наркозом.
При этом наряду с тщательным туалетом бронхиального дерева производим раздувание легких через бронхоскоп. Так, у одного больного лечебную бронхоскопию мы применили 2 раза, пока не было достигнуто полное расправление легких и не восстановилось самостоятельное дыхание и кашлевой рефлекс. Обычно очищение трахеобронхиального дерева от секрета удается с помощью внутритрахеального введения антибиотиков и аппарата «Искусственный кашель» путем усиления активного выдоха. Ингаляции с хемотрипсином способствуют разжижению бронхиального секрета.
Кровопотерю восполняют во время операции, поэтому переливание крови обычно применяем для стимуляции в послеоперационном периоде. Повышение температуры в первые трое суток — обычное явление, однако если температура становится выше, чем в предыдущие 2 дня после операции, и удерживается в последующем, это свидетельствует о присоединении инфекции. Поэтому мы производили ревизию раны, рентгеноскопию грудной клетки, осматривали вены, через которые вливали жидкости или проводили анестезию.
При исключении экстраторакальных причин повышения температуры основное внимание уделялось лечению начинающейся пневмонии, рентгенологические признаки которой могут отсутствовать в первые дни. Важное значение приобретают данные аускультации, частота дыхания и пульса, состояние кожных покровов, адинамия. Пневмония, как осложнение после операции по поводу новообразований средостения, имела место у 9 больных.
Флебиты и тромбофлебиты вен нижних конечностей мы наблюдали у 4 больных. Среди осложнений, связанных с техническими погрешностями при укладке больных на операционном столе, мы наблюдали плекситы (6 больных). Травматические плекситы отличаются торпидным течением, что нередко несколько задерживает выздоровление больных несмотря на полный благополучный исход хирургического лечения основного заболевания. Лечение плекситов заключалось в назначении прозерина, витаминов, алоэ и стекловидного тела, пирабутола (бутадиона, реопирина), массажа, ЛФК. В среднем лечение плексита занимает 3—4 недели.
У 18 больных после перенесенной операции мы наблюдали явления астенизации. У таких больных нарушается сон, появляется раздражительность, быстрая утомляемость, отсутствие аппетита, подавленное настроение и другие проявления психогенного дискомфорта. Лечение заключалось в назначении седативных средств (бромиды, андаксин и др.), переливаний крови, плазмы, применении гормональных анаболитов (метиландростендиол), препаратов китайского лимонника, женьшеня, пантокрина, витаминов группы В, лечебной физкультуры. В последующем после выписки из больницы показано санаторно-курортное лечение.
После заживления раны у 7 больных имела место длительная экссудация в плевральную полость на стороне операции (реактивный плеврит). Обычно в экссудате количество лейкоцитов не превышает 10—20 в поле зрения. Введение антибиотиков в плевральную полость усиливает экссудацию. Наилучшие результаты дает десенсибилизирующая терапия (вливание 10% раствора хлористого кальция, супрастина). Местно в плевральную полость мы вводили по 50—100 мг гидрокортизона 1 раз в неделю, что привело к значительному уменьшению экссудации в ближайшие дни, а затем к ее ликвидации.
Нагноение раны имело место у 5 больных в связи с незамеченной серомой или гематомой. При этом мы снимали частично швы и производили обкалывание краев раны раствором антибиотиков.
Тяжелые осложнения послеоперационного периода наблюдались у 5 больных и явились одной из причин смертельного исхода.
У одной больной во время операции имело место повреждение безымянной вены и двусторонний пневмоторакс в связи с повреждением обеих медиастинальных плевр. Это осложнение не было распознано в послеоперационном периоде. Состояние больной было крайне тяжелым и расценивалось как результат массивной кровопотери и сердечно-сосудистого коллапса.
Другой больной умер от тромбоза сосудов головного мозга на 6-е сутки после операции. При вскрытии обнаружен атеросклероз с преимущественным поражением сосудов головного мозга и обширный очаг серого размягчения левой гемисферы.
У третьего больного во время операции была повреждена верхняя полая вена, что сопровождалось массивной кровопотерей. После лигирования сосуда появился острый венозный застой в головном мозгу; больной умер спустя 1 час после оперативного вмешательства. На секции установлено наличие огромной двусторонней нейрогенной саркомы передне-нижнего средостения с прорастанием сердечной сорочки, легких и метастазами в легкие, выраженный отек легких мозговых оболочек и вещества мозга.
У четвертой больной смерть наступила от легочно-сердечной недостаточности спустя 2 суток после дренирования больших размеров нагноившейся тератоидной медиастинальной кисты.
На вскрытии выявлена незрелая тератома средостения с некрозом и метастазами в легкие, лимфоузлы средостения и оба яичника. Кроме того, обнаружены фибринозный перикардит, зернистая дистрофия миокарда, печени, почек, левосторонний гидроторакс. У пятого больного внезапно развилась острая сердечно-сосудистая и легочная недостаточность, закончившаяся летальным исходом. Непосредственными причинами смерти 3 больных с тяжелой миастенией, умерших после тимэктомии на 3-й, 5-и и 17-е сутки, оказались: обширные ателектазы легких, двусторонняя аспирационная пневмония, ограниченный медиастинит на фоне часто повторяющихся миастенических и холинэргических кризов.
Как видно из приведенных данных, у 8 (3,5%) из 225 больных, оперированных по поводу опухолей и кист средостения, в ближайшем послеоперационном периоде наступила смерть.
Анализируя послеоперационные осложнения, закончившиеся летальным исходом, следует подчеркнуть, что у 2 из 8 умерших во время операции и на секции были выявлены злокачественные медиастинальные и внемедиастинальные опухоли с метастазами в отдаленные органы. Иноперабельное их состояние, к сожалению, до операции не было выявлено, а оперативное вмешательство предпринималось по жизненным показаниям. Разумеется, в этих случаях операция была паллиативной. Прогрессирующий рост опухоли, бластоматозная интоксикация, усугубившаяся операционной травмой, явились теми отягощающими моментами, которые привели к тяжелым осложнениям, повлекшим за собой смертельный исход.
Таким образом, ведение послеоперационного периода после удаления опухолей и кист средостения преследует цели своевременного распознавания тех или иных осложнений и своевременной их ликвидации.
источник
Больная Б., 30 лет, поступила в ту же клинику 18/XI 1948 г. Жалобы на сильную одышку во время физической работы, значительное снижение трудоспособности.
В апреле 1948 г. больная перенесла правостороннюю крупозную пневмонию, по поводу которой находилась в терапевтическом стационаре, где при просвечивании грудной клетки была обнаружена опухоль переднего средостения. Больная чувствовала себя удовлетворительно. В дальнейшем стала беспокоить одышка, усиливающаяся при ходьбе, подъеме по лестнице. Появился сухой кашель, слабость.
Больная удовлетворительного питания. Правая половина грудной клетки отстает при дыхании. Перкуторно определяется участок притупления от верхнего края III ребра до нижнего края V ребра, занимая пространство между правым краем грудины и передней аксиллярной линией. Дыхание соответственно участку притупления ослаблено. Границы сердца в пределах нормы. Тоны приглушены, чистые. Пульс 72 удара в минуту. Рентгеноскопия: большое, округло-овальной формы, однородное затемнение с ровными, гладкими контурами, располагающееся в средней зоне правого легочного поля. Симптом Неменова отрицательный. Диагноз: киста правого легкого.
8/ХII 1948 г. операция. Под местной анестезией в шестом межреберье справа с пересечением реберной дуги широко открыта правая плевральная полость. Разделены шварты. Обнаружена опухоль размером 10х13х8 см, исходящая из переднего средостения. Опухоль плотная, бугристая, с кистозными участками. При пункции получен белый детрит (посев стерилен). Из-за спаяния опухоли с корнем правого легкого, дугой аорты и верхней полой веной она с большим трудом была отделена от этих элементов (местами острым путем), а затем удалена. Грудная клетка зашита наглухо. Вес опухоли 575,5 г.
Гистологически: опухоль типа тератомы с разрастанием хрящевой ткани и слизистых желез. Заживление первичным натяжением. Больная выписана 30/ХII 1948 г.
Больная Е., 53 лет, поступила в ту же клинику 6/ХII 1948 г. Жалобы на кашель с отхождением значительного количества мокроты с резким запахом, одышку и утомляемость.
В 1921 г. при рентгеноскопии легких у больной была обнаружена опухоль левого легкого. Больная чувствовала себя удовлетворительно, продолжала работать. В 1929 г. вновь была отмечена та же опухоль, но несколько больших размеров. Больная продолжала считать себя здоровой. В 1946 г. перенесла эксгудативный плеврит, в декабре 1947 г. воспаление легких и вторично левосторонний экссудативный плеврит. С этого времени у больной появился кашель с гнойно-слизистой мокротой (количество мокроты временами достигало 500 мл в сутки), имевшей резкий запах, одышка, утомляемость.
Рентгенологически установлено спадение стенок кисты. К декабрю 1948 г. самочувствие больной ухудшилось, усилилась одышка, утомляемость, кашель. Больная похудела. Рентгенологически отмечено наполнение полости кисты жидкостью. Киста достигла вновь значительных размеров.
При обследовании больной в легких соответственно левой лопаточной области прослушиваются сухие и большое количество влажных средне- и крупнопузырчатых хрипов. Границы сердца в пределах нормы. Тоны несколько приглушены, чистые. Пульс 88 ударов в минуту.
Кровь: л. 9 500; РОЭ 17 мм в час. Моча нормальная. Реакции Вассермана и Каццони отрицательные. Мокрота слизисто-гнойная, в ней туберкулезных палочек, эластических волокон и клеток новообразования нет.
Рентгенологически: в левой плевральной полости большая, овальной формы полость с газом и жидкостью, уровень которой находится на II ребре. Верхний отдел полости заходит в верхушку левого легкого, нижний — на уровне III ребра. Полость расположена более кзади, стенки ее толстые.
С предположительным диагнозом нагноившейся’ кисты левого легкого больная оперирована 22/ХII 1949 г. Под местной анестезией разрез по внутреннему краю левой лопатки. Резекция II, III и IV ребра от головки до задней подмышечной линии. Париетальная и висцеральная плевра спаяны. Пункцией кисты получен гной. Разрез электроножом по игле. Через тонкий слой легочной ткани в 0,3 см вскрыта плотная стенка кисты, которая оттесняет верхнюю долю левого легкого кпереди и книзу.
Медиальная поверхность кисты прилежит к средостению. Отчетливо видны: дуга аорты, корень левого легкого, левая общая сонная и левая подключичная артерия. Верхний и задний полюсы кисты прилежат к задней грудной стенке. После дополнительной анестезии ложа аорты и корня левого легкого острым путем произведено иссечение стенок кисты. На нижней поверхности кисты обнаружен бронхиальный свищ 0,5 см в диаметре. Последний ушит кетгутом. Частичное ушивание ложа кисты по типу капитонажа и тампонада ее мышечными лоскутами на ножке по Абражанову. Два дренажа. Швы.
При микроскопическом исследовании стенка кисты выстлана многорядным кубическим эпителием, в подэпителиальном слое круглоклеточная инфильтрация.
Дренажи удалены на тринадцатый день. Рана полностью покрылась грануляциями спустя 2% месяца. При контрольной рентгеноскопии после операции отмечается понижение прозрачности легочной ткани слева, соответственно местоположению удаленной кисты.
Больная выписана 28/III 1949 г. с бронхиальным свищом. Через месяц состояние больной хорошее, одышки нет, свищ полностью закрылся.
источник
Mediastinal Tumor Resection
Это операция по удалению опухоли в области грудной клетки, которая отделяет легкие от остальных органов.
Злокачественная (раковая) опухоль должна быть удалена, чтобы предотвратить распространение рака. Без удаления или лечения рак может распространиться на другие части тела. Рак может также начать сжимать органы грудной клетки, такие как сердце, легкие, или пищевод.
Пациенты, проходящие операцию по удалению опухоли средостения, часто имеют лучший прогноз, чем те, кто проходит курс лучевой или химиотерапии.
Осложнения встречаются редко, но процедура не гарантирует отсутствие риска. Если планируется удаление опухоли средостения, нужно знать о возможных осложнениях, которые могут включать:
- Повреждение органов, прилегающих к опухоли, в том числе сердца, легких и спинного мозга;
- Накопление жидкости между покровом легочной ткани и стенкой грудной полости;
- Дренаж, инфекции или кровотечения.
Факторы, которые могут увеличить риск ослонений:
Перед операцией врач может провести или назначить следующее:
- Медицинский осмотр;
- Анализы крови;
- Рентген — это тест, который использует излучение, чтобы выполнить снимки структур внутри тела;
- МРТ — тест, который использует магнитные волны, чтобы выполнить снимки структуры внутри тела;
- Компьютерная томография брюшной полости — типа рентгена, который использует компьютер, чтобы сделать снимки органов тела;
- Позитронно-эмиссионная томография — тест, который использует радиационные метки, которые показывают активность в тканях организма.
- Обратитесь к врачу по поводу принимаемых лекарств. За неделю до операции вас могут попросить прекратить принимать некоторые препараты:
- Противовоспалительные препараты (например, аспирин);
- Разжижающие кровь (например, клопидогрель);
- Антитромбоцитарные препараты (например, варфарин);
- Можно съесть легкую пищу вечером перед операцией. Не ешьте и не пейте ничего на ночь;
- Нужно организовать возвращение домой из больницы. Кроме того, нужно организовать помощь на дому.
Применяется общая анестезия, которая блокирует боль и поддерживает пациента в состоянии сна во время операции.
Перед началом операции пациенту вводят дыхательную трубку и внутривенный катетер. Катетер используется для введения лекарств и жидкостей во время операции.
Чтобы удалить опухоль, врач выполняет один большой, разрез в центральной части груди или несколько маленьких разрезов. Если выполняется несколько маленьких надрезов, в один из них будет вставлена камера. Камера позволяет врачу видеть область операции на мониторе. Через другие разрезы будут вставлены хирургические инструменты. Опухоль и по необходимости окружающие ткани будут удалены.
Врач может вставить в грудь дренажные трубки, которые помогут удалить жидкость и воздух из грудной полости. Разрез будет закрыт с помощью скоб или швов.
Дыхательная трубка будет удалена. Вы будете направлены в послеоперационную палату для наблюдения за состоянием здоровья.
Около 1-4 часов (в зависимости от типа операции).
Анестезия облегчит дискомфорт после операции. Область операции может обладать повышенной чувствительностью. Врач предоставит обезболивающие лекарства для снятия дискомфорта.
Эта операция проводится в условиях стационара. Обычно длительность пребывания составляет четыре дня. Врач может продлить срок пребывания, если возникают осложнения.
После операции дополнительно может потребоваться химиотерапия и/или лучевая терапия.
В больнице вы будете принимать жидкую пищу. Нужно практиковать глубокое дыхание и кашель, чтобы помочь легким восстановиться.
Когда вы находитесь дома, обязательно следуйте указаниям врача, в том числе:
- Избегайте подъема объектов тяжелее, чем 3 кг;
- Не садитесь за руль в течение 4-6 недель;
- Выполняйте несложные упражнения. Это поможет вам восстановиться.
Необходимо уточнить у врача, когда можно безопасно принимать душ, ванну или подвергать место операции воздействию воды.
После выписки из больницы нужно обратиться к врачу, если появились следующие симптомы:
- Признаки инфекции, включая лихорадку и озноб;
- Покраснение, отек, усиление боли, кровотечение, или любые выделения из операционного разреза;
- Боль, которая не проходит после приема назначенных обезболивающих лекарств;
- Кашель, затрудненное дыхание или боли в груди;
- Боль, жжение, частое мочеиспускание или постоянное наличие крови в моче;
- Постоянная тошнота и/или рвота;
- Потеря аппетита;
- Боль и/или отек ног, икр и ступней;
- Любые другие болезненные симптомы.
источник
Кисты средостения – многочисленная группа полостных образований медиастинального пространства врожденного и приобретенного характера. Кисты средостения могут иметь бессимптомное течение или сопровождаться признаками компрессии окружающих органов (бронхов, пищевода, предсердий, артерий), нарушая их функцию. Диагностика кист средостения подразумевает проведение полипозиционной рентгеноскопии и рентгенографии грудной клетки, пищевода, сердца; томографии; бронхоскопии, пневмомедиастинографии, медиастиноскопии, тонкоигольной аспирационной биопсии, УЗИ средостения, парастернальной медиастинотомии. Лечение кист средостения может включать их открытое или торакоскопическое удаление, трансторакальную пункцию кисты с дренированием и склерозированием и др.
Кисты средостения составляют от 14 до 18,5% всей медиастинальной патологии. К кистами средостения относят полостные образования различного генеза, происходящие из разнородных тканей и объединенные анатомо-топографическими особенностями расположения. Преимущественно обнаруживаются у пациентов в возрасте 20-50 лет, при этом с одинаковой частотой у женщин и мужчин.
Кроме кист, в средостении могут развиваться истинные доброкачественные и злокачественные опухоли: тимомы, тератомы, липомы, нейрогенные опухоли, лимфомы, саркомы, лимфогенные метастазы злокачественных опухолей различных органов и др. Проблема диагностики и лечения кист средостения относится к числу наиболее сложных и актуальных разделов пульмонологии и торакальной хирургии.
Под средостением (mediastinum) понимают сложное в анатомическом отношении пространство, расположенное в грудной полости. Спереди границами средостения служат грудина, позадигрудинная фасция и реберные хрящи; сзади — предпозвоночная фасция, передняя поверхность грудного отдела позвоночника и шейки ребер; по бокам — листки медиастинальной плевры; снизу – диафрагма; сверху — условная горизонтальная плоскость, проходящая по верхнему краю рукоятки грудины. Т.о., в медиастинальном пространстве выделяют 3 отдела (переднее, среднее и заднее средостение) и 3 этажа (верхнее, среднее и нижнее средостение).
В средостении сосредоточены жизненно важные органы и анатомические образования (крупные сосуды, нервные стволы и сплетения, лимфатические протоки, бифуркация трахеи и главные бронхи, пищевод, перикард и др.). Поэтому компрессия или инвазия этих структур может сопровождаться различными по проявлениям и нередко угрожающими жизни симптомокомплексами. Кисты средостения могут выявляться в любых отделах и этажах медиастинального пространства.
Кисты средостения классифицируются по происхождению и локализации. Среди множества кист средостения различают истинные (врожденные, первичные), вторичные (приобретенные).
Врожденные кисты средостения развиваются из мезодермальных образований — целома или передней кишки. К ним относятся целомические, энтерогенные, бронхогенные, дермоидные кисты, кисты тимуса и др. Приобретенные кисты средостения происходят из лимфатических сосудов, различных органов средостения и пограничных областей. В число приобретенных кист средостения входят лимфатические, тимусные, паразитарные (эхинококковые), менингеальные.
Являются своеобразным врожденным пороком развития и составляют 3,3-14,2% всех медиастинальных новообразований. Наиболее часто кисты перикарда (60%) развиваются в правом кардиодиафрагмальном углу, реже (30%) – в левом кардиодиафрагмальном углу и других отделах средостения (10%). Такие кисты средостения являются полыми тонкостенными образованиями, сходными по строению с тканями перикарда, имеют гладкую поверхность серо-желтого или серого цвета.
Кисты перикарда содержат прозрачную серозную или серозно-геморрагическую жидкость. Целомические кисты перикарда могут достигать диаметра от 3 до 20 и более см. Целомические кисты средостения могут быть однокамерными или многокамерными, сообщаться с полостью перикарда, быть связанными с перикардом посредством ножки или плоскостного сращения. Приобретенные кисты перикарда встречаются редко; обычно имеют воспалительное и травматическое происхождение. Также описаны паразитарные (эхинококковые) кисты перикарда.
Встречаются в 30-35% наблюдений. Они также являются пороками эмбрионального развития и формируются из участков дистопированного бронхиального эпителия. Макроскопически представляют тонкостенные образования, заполненные прозрачной, реже бурой жидкостью. При гистологическом исследовании в них обнаруживается хрящевая ткань, соединительнотканные и гладкомышечные волокна слизистые железы.
Полость бронхогенной кисты средостения изнутри выстлана эпителием цилиндрического или реснитчатого типа. Внутри кисты содержится прозрачная или мутноватая желатинообразная, вязкая масса, которая, при наличии связи кисты с бронхиальным деревом, может нагнаиваться. Бронхогенные кисты средостения обычно располагаются позади бифуркации трахеи и тесно соприкасаются с трахеей или главными бронхами, иногда — пищеводом. Обычно они имеют однокамерное строение и достигают размеров 7-10 см в диаметре.
Энтерокистомы являются эмбриональными производными из первичной кишки. С учетом микроскопического сходства их структуры с отделами ЖКТ, выделяют пищеводные, желудочные и кишечные кисты. Гастроэнтерогенные кисты средостения встречаются в 0,7-5% случаев. Они представляют собой однокамерные округлые или овоидные образования, с толстыми стенками и ножкой; локализуются преимущественно в заднем средостении. Гастроэнтерогенные кисты средостения содержат мутноватую слизевидную массу. Желудочные кисты могут продуцировать соляную кислоту, что приводит к изъязвлению стенок, кровотечению, язвам и перфорации стенок кисты средостения. В редких случаях в стенке кисты может развиваться рак.
Кистозные тератомы содержат в своей структуре элементы эктодермы и возникают в процессе нарушения эмбриогенеза. В медицине встречаются дермоидные кисты яичников, брюшной стенки, кожи, забрюшинной клетчатки, печени, почек и др. органов и тканей. Дермоидные кисты обычно расположены в передневерхнем отделе средостения. Величина дермоидных кист средостения может достигать 15-25 см. Форма кистозных тератом обычно неправильная овальная; консистенция эластическая или мягкая. Стенки кисты могут содержать хрящевые и известковые включения. Внутри кисты заключена густая кашицеобразная жирная масса с множеством различных включений (волос, чешуек эпидермиса, кристаллов холестерина, аморфных жиров, зубов).
Могут иметь врожденное и приобретенное (воспалительное, опухолевое) происхождение. Они преимущественно выявляются у детей и людей молодого возраста.
Особенности клинических проявлений кисты средостения обусловлены типом и расположением образования, его величиной и скоростью роста. В большинстве случаев симптоматика развивается на том этапе, когда увеличение кисты средостения вызывает компрессию других органов и неизбежное нарушение их функций.
Течение кист перикарда в большинстве случае бессимптомное, гладкое. Нередко они являются находкой при прохождении профилактической флюорографии. Иногда наблюдаются сердцебиение, одышка, сухой кашель, возникающие при перемене положения туловища и физической нагрузке. При осложненном течении целомических кист средостения может иметь место провыв содержимого кисты перикарда в бронх, нагноение и разрывы кисты.
Развитие бронхогенных кист средостения нередко сопровождается надсадным кашлем, одышкой, дисфагией, тупой болью в грудной клетке. При сдавлении кистой дыхательных путей развивается стридорозное дыхание. В случае прорыва бронхогенной кисты средостения в бронх может появиться кровохарканье. При одновременном прорыве кисты в плевральную полость и в бронх, развивается гидропневмоторакс и бронхоплевральный свищ.
Гастроэнтерогенные кисты средостения проявляют себя кашлем, одышкой, тахикардией, дисфагией, болью в груди. Энтерокистомы могут прорываться в трахею, бронхи, плевральную полость, средостение, вызывая развитие кровохарканья, эмпиемы плевры, частых пневмоний, лихорадки неясного генеза, бронхоэктазов, медиастинита.
Более чем в половине случаев дермоидная киста средостения сопровождается различными сердечно-сосудистыми нарушениями: приступами стенокардии, болью в области сердца, тахикардией. У 30% больных признаком дермоидной кисты средостения служит появление продуктивного кашля с выделением кашицеобразной массы, содержащей примесь волос и жира, что наблюдается при прорыве кисты в бронх. У части пациентов отмечается выпячивание грудной стенки в проекции расположения опухоли.
Симптоматика кист вилочковой железы может быть разнообразной – от бессимптомного течения до осложненного. Достигнув известных размеров, кисты могут вызывать медиастинальный «компрессионный» синдром. В некоторых случаях на первый план выходит миастенический синдром. Опасность кист вилочковой железы заключается в риске нагноения, прорыва в плевру, кровотечения.
Наиболее грозным осложнением кист средостения служит так называемый синдром медиастинальной компрессии, частота которого колеблется от 27 до 39%. Сюда может входить компрессия дыхательных путей, синдром верхней полой вены (СВПВ), сдавление пищевода, сердца, возвратного нерва.
При компрессии дыхательных путей развивается стридорозное дыхание, одышка, дыхательная недостаточность. Синдром ВПВ проявляется цианозом кожи лица, видимых слизистых оболочек, шеи, верхних конечностей и грудной клетки; отечностью мягких тканей этой зоны; расширением и напряжением вен шеи; повышением давления в системе ВПВ. Сдавление кистами различных структур средостения может сопровождаться дисфагией, дисфункцией надгортанника, дисфонией, компрессией и дислокацией сердца.
К прочим осложнениям кист средостения относятся их прорывы в полости плевры, бронхи и легкое, кровотечения в средостение и плевральную полость (гемоторакс). Осложненное течение кист средостения несет в себе потенциальную угрозу жизни пациента.
Методы выявления кист средостения включают рентгенологическую, ультразвуковую, томографическую, эндоскопическую, морфологическую диагностику.
- Рентгенологические исследования. Полипозиционная рентгеноскопия и рентгенография грудной клетки, рентгенография пищевода и сердца, пневмомедиастинография позволяют определить локализацию, форму и размеры кисты, ее связь с соседними органами, изменение положения при дыхательных движениях.
- Томографическая диагностика. Для более детальной оценки структуры, толщины стенок кисты, характера содержимого и взаимоотношения с соседними анатомическими образованиями, производится КТ и МРТ средостения.
- Эхография. При медиастинальных новообразованиях в диагностической практике широко используется УЗИ средостения. В диагностике кист перикарда существенно помогает ЭхоКГ, позволяющая дифференцировать кисту средостения от кист легкого, дермоидных кист средостения, аневризмы аорты.
- Бронхологическое обследование. При кистах средостения, демонстрирующих интимную связь с трахеей или бронхами, прибегают к выполнению бронхоскопии и бронхографии.
Если названные методы диагностики не позволяют определиться с нозологией образования, целесообразен переход к инвазивным диагностическим исследованиям:
- Биопсия. Проведение аспирационной тонкоигольной биопсии кисты средостения позволяет осуществить цитологическое исследование полученного пунктата и верифицировать морфологию образования в 80-90% случаев. Тонкоигольная биопсия может выполняться чрескожным, чрестрахеальным, чрезбронхиальным, чреспищеводным доступом.
- Диагностические операции. С целью визуализации и открытой эксцизионной биопсии опухоли средостения может быть предпринята медиастиноскопия, диагностическая торакоскопия, парастернальная медиастинотомия.
Лечебная тактика в отношении кист средостения сводится к их хирургическому удалению в возможно ранние сроки. Такой подход является профилактикой развития компрессионного синдрома, разрыва и малигнизации кист средостения.
- Открытое удаление кисты средостения может проводиться путем продольной стернотомии (при расположении кисты в переднем средостении), с помощью переднебоковой торакотомии на стороне поражения (при боковом расположении образования), боковой торакотомии (при локализации опухоли в среднем средостении), заднебоковой торакотомии (при расположении кисты в заднем средостении). Открытые операции обеспечивают возможность наибольшей свободы действий и полноценной интраоперационной ревизии раны. При развитии осложнений может потребоваться проведение медиастинотомии.
- Торакоскопическое удаление кист средостения также широко и успешно применяется не только для диагностики, но и для удаления медиастинальных образований. В некоторых случаях используется миниторакотомия с видеоподдержкой.
- Пункционная аспирация. У соматически отягощенных пациентов с низкими функциональными резервами методом выбора служит трансторакальная пункция с дренированием и склерозированием кисты средостения. В качестве склерозантов обычно используется раствор спирта с йодом, глюкозы.
источник