Протоковый рак молочной железы (сокращенно ПКИС) — патология, являющаяся одним из опаснейших онкологических заболеваний груди. Чаще всего представлен карциномой — внутрипротоковой неинвазивной опухолью.
Протоковый рак может поражать всю железу, занимать ее большую область или несколько областей. Эта форма патологии характеризуется усиленными пролиферативными свойствами и клеточной атипией.
По численности онкологических заболеваний, протоковый рак молочной железы встречается не очень часто, нежели другие разновидности рака груди. Стоит отметить, что последние годы статистика заболеваемости этим видом рака существенно выросла.
Отличие протокового рака в том, что он начинается с внутренних стенок млечных каналов, не затрагивая при этом дольки, и иные ткани молочных желез.
Протоковый рак молочной железы
Причины и факторы риска развития протокового рака молочной железы:
- беременность после 35 лет, либо отсутствие ее вообще;
- ранее половое созревание;
- поздняя менопауза;
- генетика, также является неотъемлемой частью заболеваемости (онкология молочной железы по семейной линии у мамы либо бабушки);
- длительный прием гормональных препаратов для лечения половых органов;
- предрасположенность к росту злокачественных опухолей.
По мужской части, протоковый рак молочной железы появляется у носителей мутированного гена BRCA2.
Неинвазивный рак молочной железы или начальные стадии протокового рака молочных желез обнаруживают, довольно часто при плановом профилактическом осмотре либо на УЗИ. Инвазивный протоковый рак молочной железы проявляется симптомами, которые пациентки могут обнаружить у себя сами.
Симптомы проявляются в виде:
- плотных шишек либо уплотнений в молочной железе, при этом уплотнения не уменьшаются, а скорее всего наоборот стремительно увеличиваются в размерах;
- изменения цвета и структуры кожи молочных желез;
- изменения очертания и формы груди;
- изменения формы и цвета соска. Изменение соска проявляется в виде покраснения, изменения формы и втянутости соска. Также образуются чешуйки я язвочки в околососковой зоне;
- выделений из сосков различного характера;
- чувства дискомфорта в молочной железе, болями.
При выявлении женщиной, хотя бы одного из симптомов перечисленных выше необходимо немедленно обратиться к докторам маммологу или гинекологу для проведения своевременной диагностики молочных желез.
Внутрипротоковый рак молочной железы — симптомы
Главным симптомом внутрипротокового рака молочной железы является наличие злокачественного опухолевого очага, который находится в тканях молочных желез. Также важным признаком болезни является выделения из соска. Стоит отметить, что на ранних стадиях онкологии эти важные признаки болезни могут отсутствовать, с этим, и связана поздняя диагностика рака молочных желез.
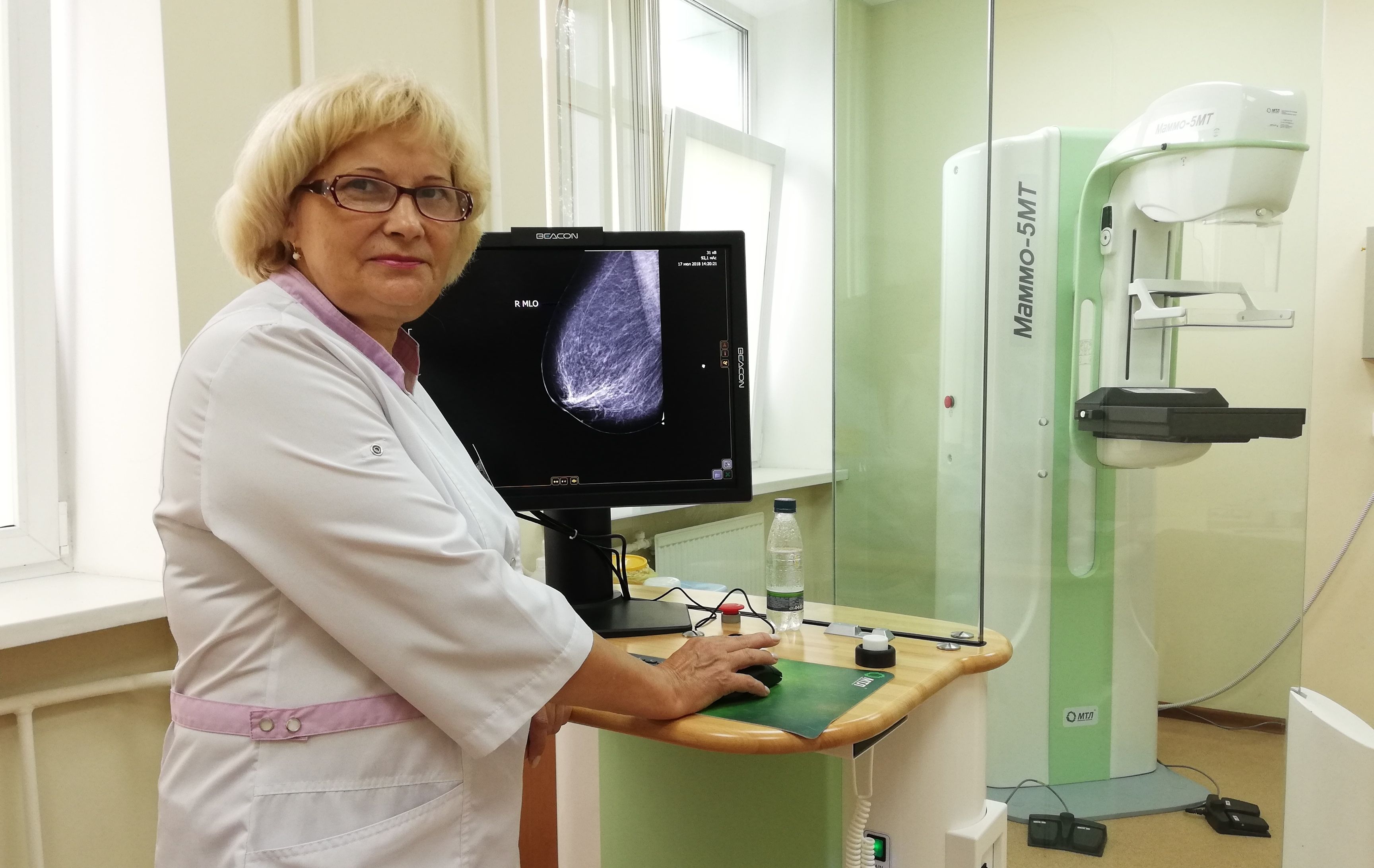
Диагностировать злокачественное образование можно при помощи современных методом исследования молочных желез: это маммография и ультразвуковое исследование (УЗИ). Симптомы протокового рака молочной железы на рентгене определяются как микрокальцинаты – пропитанные солями кальция участки железистой ткани, образовавшиеся в результате распада карциномы.
Если в процессе проведения УЗИ либо маммографии есть подозрение на рак молочной железы, пациентку дополнительно направляют на проведение биопсии. Биопсия – это извлечение части подозрительного участка ткани с последующим гистологическим исследованием. Проведение биопсии – это неотъемлемая часть в диагностировании рака молочных желез.
Неинвазивный внутрипротоковый рак — этот вид рака считается неопасным для жизни и здоровья женщины, так как он развивается только в локальном месте и только в протоковом просвете. Карциному удаляют при помощи оперативного вмешательства, и для избегания рецидивов проводят лучевую терапию, а также гормональное лечение при необходимости.
Инвазивный протоковый рак молочной железы или его еще называют: инфильтрирующий рак молочной железы, или инфильтрирующая карцинома молочной железы.
Характеризуется данный вид онкологии молочных желез агрессивностью болезни следственно и несет опасность для жизни и здоровья пациентки.
Инфильтрирующая протоковая карцинома молочной железы — самый распространённый вид злокачественного образования молочных желез. Именно этот рак встречается в 80% случае всех онкозаболеваний грудной железы.
Отличие инвазивной формы от неинвазивной в том, что процесс при инвазивном раке, выходи за пределы млечного канала и поражает другие ткани молочной железы.
Инвазивная протоковая карцинома молочной железы характеризуется следующими симптомами:
- очаговое уплотнение с равными границами;
- припухлость в подмышечных впадинах;
- втянутость соска или околососковой зоны;
- при образовании метастазов может появиться головная боль, приступы эпилепсии, асцит, боль спины и конечностей.
Злокачественное образование при инвазивном протоковом раке молочной железы имеет разнообразные размеры и скорость роста. Довольно часто при диагностике на снимках обнаруживают небольшого размера хаотично расположенные уплотнения извести в ткани (от 50 до 600 мкм). Такие отложения представляют собой результат некротического процесса в клетках с последующим пропитыванием омертвевших структур кальциевыми солями.
Для определения такого заболевания, как рак молочной железы необходимо пройти ряд исследований, для подтверждения либо опровержения диагноза.
Диагностика протокового рака молочной железы включает в себя следующие диагностические процедуры:
- маммография – самый распространённый метод диагностики, который представляет собой рентгеновское исследование грудной железы. Достоверность данного исследования достигает 90-95% даже без существенно видимых симптомов и признаков болезни. Проводят маммографию при помощи специального рентгеновского аппарата, при помощи которого можно просветить молочную железу с двух ракурсов: фронтального и бокового. Современные маммографические аппараты оснащены специальными стереотаксическими компьютерными устройствами, благодаря которым можно провести точную пункцию с последующей биопсией. Маммография гарантирует точное диагностирование болезни на начальных этапах ее развития, когда отсутствуют более видимые симптомы. Также стоит отметить, что такой метод диагностики как маммография рекомендуют проводить женщинам старше 40 лет. Что касается более молодого поколения, в этом случае используется УЗИ;
- УЗИ – метод диагностики, который по популярности исследования стоит вторым после маммографии. Как упоминалось ранее УЗИ, проводят более молодым женщина и девушкам для избегания облучения при проведении маммографии. Процедура проводится достаточно быстро. Про помощи ультразвукового исследования можно выявить расположение, размер и форму опухолевого образования. Проводить УЗИ можно в любом возрасте и в неограниченном количестве;
- термография – метод диагностики, при помощи которого определяется температура кожных покровов груди. Здоровая ткань и поражённая, имеет разную температуру. Объяснить это можно таем, что в опухоли присутствует большее количество сосудов, которые выделяют тепло и тем самым позволяют термографом выявить опухоль;
- световое сканирование – осмотр тканевого просвета или диафаноскопия. Процедуру проводят при помощи инфракрасного просвечивания тканей груди. Метод не очень распространен ввиду слабой чувствительности и сложности дифференцировки заболеваний;
- дуктография – галактофорография или контрастное маммографическое исследование. В млечный проток вводят специальную жидкость, после чего делают снимок, который показывает изменения в протоках;
- биопсия – из пораженной молочной железы изымают элемент ткани для последующего исследования. Ткань берется при помощи пункции — небольшого прокола в области опухолевого очага. В последующем материал отправляется в лабораторию для проведения разного рода исследований и выявления в нем раковых клеток. Пункционную биопсию делают не во всех случаях, иногда биопсию проводят во время оперативного вмешательства по удалению опухоли. Данный вид биопсии проводят для постановки заключительного диагноза;
- в качестве дополнительных исследований можно использоваться МРТ и КТ, сканирование костной системы и пр.
Лечение протоковой карциномы молочной железы наиболее эффективно, когда оно применяется в комплексе, то есть с применением оперативного вмешательства, химиотерапии, гормональной и лучевой терапии.
Схему и метод лечебной терапии назначает лечащий врач после глубоко изучения симптомов и признаков болезни, проведя при этом тщательную диагностику, а также после консилиума с участием специалистов, разного профиля: маммолога, хирурга-онколога, химиотерапевта и специалиста по радиологии. Лечение зависит от многих факторов: локализации опухоли, ее размера, распространённости в окружающие ткани и органы, наличия метастаз. Возраст и общее состояние здоровья пациента, также играют немаловажную роль в выборе того или иного комплекса терапий.
Как правило, необходима радикальная терапия – это полное удаление опухолевого очага. Также использую паллиативную хирургию, она направлена на продление жизни пациента. При паллиативном вмешательстве не удается удалить опухоль в полном объеме, а только ее часть.
- лампэктомию — частичное удаление тканей молочной железы;
- квадрантектомию – удаление большей части тканей молочной железы;
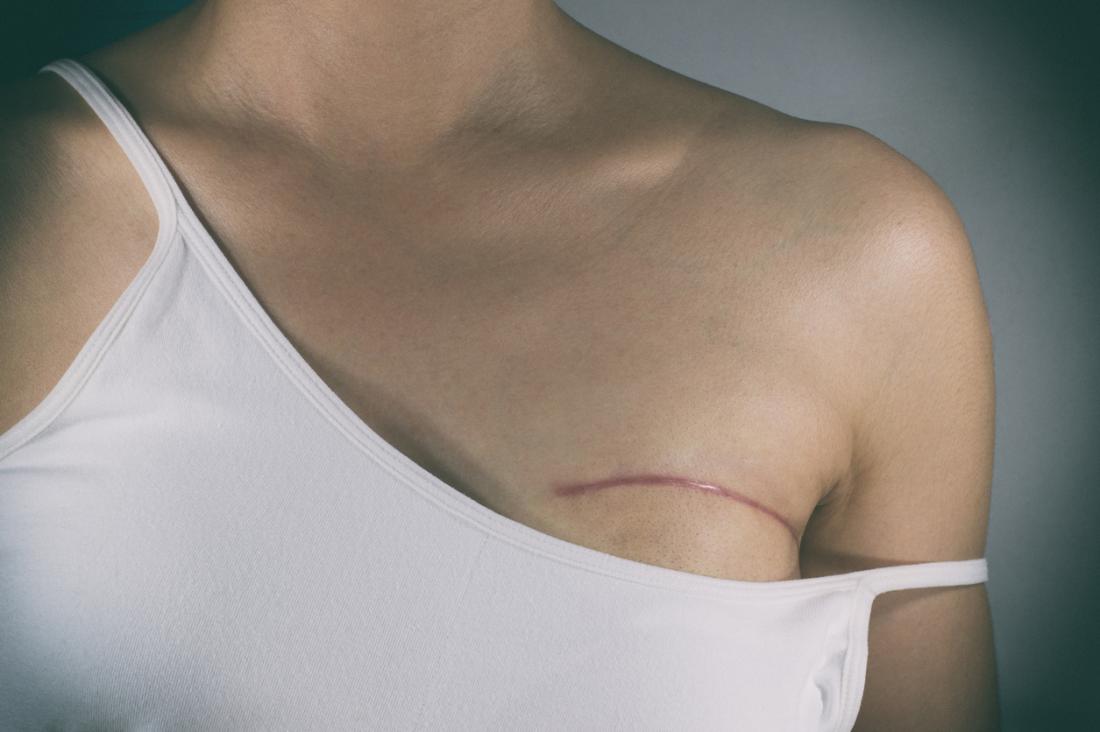
- мастэктомию — удаление молочной железы в полном объёме с вблизи лежащими лимфатическими узлами.
Пластическую операцию по восстановлению груди проводят, как правило, во время мастэктомии либо через 1 год, после окончания полного комплекса лечения и финального обследования.
Лучевая терапия при раке молочной железы, проводится в тех случаях, когда невозможно провести оперативное вмешательство либо непосредственно перед ним для локализации злокачественного очага. Также ее используют в целях профилактики рецидивов опухоли. Невозможно проведение облучения при расстройствах кровообращения мозга, нарушениях обмена веществ и заболеваниях печени.
Химиотерапия при раке груди, особенно в начале болезни позволяет остановить рост злокачественных клеток, что в дальнейшем дает возможность для проведения органосохраняющей операции. Химиотерапия тормозит рост и распространение раковых клеток, так сказать блокирует их деление и тем самым существенно улучшает прогноз выживаемости. Химиопрепараты используются в комплексе, то есть вводятся внутривенно либо внутримышечно одновременно несколько видов препаратов, это так называется комбинированное лечение, оно особенно эффективно при региональных метастазах. Применяют Антрациклины, Таксаны, в том числе и Моноклональные препараты, такие как: Трастузумаб, Герцептин.
Гормональное лечение подразумевает по собой использование препаратов, которые понижают уровень эстрогенов в организме, что и тормозит в свою очередь рост опухоли. Наиболее чаще,препаратом выбора становится «Тамоксифен».
При комплексе всех вышеперечисленных методов лечения протокового рака, специалисты стремятся добиться положительных результатов в лечении и тем самым улучшить прогноз на полное выздоровление.
Если вы нашли ошибку просто выделите ее и нажмите Shift + Enter или нажмите здесь. Большое спасибо!
Спасибо за ваше сообщение. В ближайшее время мы исправим ошибку
источник
Рак молочной железы – самое частое злокачественное заболевание среди женщин. Ежегодно его частота возрастает на 1.79%. Заболеваемость увеличивается с возрастом и достигает максимума к 60-65 годам.
Не так давно раки молочной железы подразделяли на протоковые и дольковые. Считалось, что протоковые возникают из озлокачествленных клеток протоков, а дольковые, соответственно, из самой железистой ткани. Со временем обнаружилось, что это деление не имеет смысла, так как большая часть новообразований разрастается из так называемой дольково-протоковой единицы. В 2012 году из классификации ВОЗ был удален термин «протоковый рак». Понятие «инвазивный протоковый рак молочной железы» на сегодня отсутствует в международной классификации онкологических заболеваний. Сохранилось лишь понятие «протоковый рак in situ» или «протоковая карцинома in situ». Это означает, что первичный очаг не вышел за пределы базальной мембраны – структуры, являющейся основой для клеток эпителия.
«In situ», в переводе с латыни, означает «на месте». То есть это ранняя стадия развития злокачественного новообразования, развивающегося до тех пор, пока его клетки не прорастут стенку протоков. При протоковой карциноме на этой стадии опухоль может достигать нескольких сантиметров в диаметре.
Раньше такое состояние обнаруживали довольно редко: опухоль успевала разрастись до того, как женщина попадала к врачу. Но после того, как маммография стала рутиным методом профилактического обследования, выявление таких опухолей стало происходить гораздо чаще. В США ежегодно диагностируется примерно 64 тысячи случаев протоковой карциномы in situ (данные по РФ неизвестны). В 90% случаев она определяется на маммографии как подозрительный кальцинат.
Факторы риска возникновения протокового рака in situ такие же, как и у любых злокачественных опухолей молочной железы.
Прежде, чем отнести рак к тому или иному подвиду, его изучают под микроскопом, так как в основу классификации положена выраженность изменений на клеточном уровне. Чем сильнее клетки отличаются от нормальных, тем выше степень злокачественности опухоли и, соответственно, хуже прогноз.
- низкая степень злокачественности: клетки почти не отличаются от нормальных и относительно медленно растут;
- средняя степень – клетки имеют значительные отличия и растут быстрее;
- высокая степень злокачественности: клетки сильно отличаются от обычных и быстро растут. Высокая степень злокачественности повышает вероятность рецидива опухоли после удаления.
По строению выделяют форму комедо, или угреподобную и некомедо.
Опухоль комедо, обычно, правильной круглой формы, в центре неё – погибшие клетки (очаг некроза). Отличается более благоприятным течением.
При форме некомедо клетки опухоли образуют сложные структуры. Такая форма реже встречается и прогностически менее благоприятна.
В популярной литературе известный как «инфильтрирующий протоковый рак молочной железы». Как уже упоминалось, этот термин означает всего лишь то, что рак пророс стенку протока и начал распространяться в окружающие ткани. На этой стадии появляется тенденция к метастазированию, если опухолевые клетки прорастают лимфатический или кровеносный сосуд. На этой стадии рак груди выявляется в 75% случаев.
С целью прогнозирования рецидива после органосохраняющей операции используют Ноттингемские критерии. Они учитывают активность, с которой делятся клетки опухоли и то, насколько разнообразны их видоизменения. Чем активней делится опухоль и чем сильнее изменены ее клетки, тем хуже прогноз.
Говорить о каких-то специфических симптомах протокового рака полочной железы бессмысленно. На стадии карциномы in situ опухоль чаще всего не имеет никаких симптомов. При относительно большом объеме женщина может обнаружить узел в молочной железе. Но классическая клиническая картина раковой опухоли, к сожалению, возникает уже на поздних стадиях ее развития. При этом симптомы уже не зависят от того, росла ли опухоль изначально внутрь протока или в железистую ткань.
- изменяется структура кожи, приобретая вид лимонной корки;
- появляется втянутость определенного участка кожи груди;
- нарушается симметричность молочных желез, в том числе расположения сосков;
- изменяется форма соска;
- в груди появляется уплотнения, которое одинаково хорошо прощупывается сидя и лежа (при мастопатиях узел обычно «исчезает» если изменяется положение тела);
- выделения из соска;
- покраснение, изъязвление кожи.
Именно потому, что все эти изменения становятся заметны уже на поздних стадиях, врачи все чаще говорят о том, самодиагностика для протоковой формы теряет свое значение. Маммография – доступный и точный метод, позволяющий обнаружить рак молочной железы до того, как опухоль начнет прорастать окружающие ткани. На этом этапе есть возможность не только полностью излечиться, но и сохранить грудь, ограничившись удалением лишь пораженного опухолью сектора.
Чаще всего опухоль обнаруживается при маммографии. После нее обязательно проводят биопсию выявленного новообразования, чтобы определить его характер. Опухоль пунктируют (прокалывают) специальной иглой под контролем УЗИ и забирают часть для изучения под микроскопом.
Далее пациентка полностью обследуется для того, чтобы узнать распространенность опухоли, поражены ли лимфоузлы, есть ли отдаленные метастазы и т.д.
Основной метод лечения – операция. Объем операции врач определяет индивидуально. Учитывается степень злокачественности опухоли, вероятность рецидивов. Кроме того, важна и распространенность рака по системе TNM – то есть объем карциномы, поражение лимфоузлов и наличие отдаленных метастазов.
После операции может быть назначена лучевая терапия. Несмотря на то, что объем операции рассчитывают так, чтобы оставить после нее заведомо здоровые ткани, единичные опухолевые клетки могут остаться. Лучевая терапия назначается для того, чтобы уничтожить их и предупредить вероятность рецидива.
Часто операцию дополняют химиотерапией. Чтобы выбрать конкретное лекарство и схему лечения, учитывают биохимические особенности опухоли. Поскольку обмен веществ в ней, как и во всем организме, кодируется генами, изучив гистохимические (тканевые) особенности можно предсказать реакцию на тот или иной химиопрепарат. Если опухоль оказывается чувствительной к гормонам, применяют и гормональную терапию.
Ни в коем случае нельзя пытаться самостоятельно вылечить рак гомеопатией или народными средствами. Все, чего можно добиться таким образом – переход болезни на более позднюю стадию, когда вероятность излечения резко падает.
Прогноз относительно благоприятен, но зависит от стадии, на которой обнаружена болезнь. Если при карциноме in situ вероятность выздоровления приближается к 100%, то после появления отдаленных метастазов она не превышает 27%.
источник
Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
В списке женских онкологических заболеваний протоковый рак молочной железы встречается не менее часто, чем другие виды рака груди. При этом за последние годы заболеваемость таким видом рака существенно увеличилась.
Протоковый рак отличается от других видов злокачественных опухолей груди, прежде всего, тем, что начинает свое развитие с внутренних стенок млечных каналов, не затрагивая доли и другие ткани железы.

Среди причин и факторов риска развития протокового рака молочной железы необходимо выделить следующие:
- отсутствие беременностей в анамнезе;
- запоздалая первая беременность (если женщине более 35 лет);
- раннее половое созревание;
- запоздалое начало климактерического периода;
- случаи онкологии молочной железы у ближайших родственников (мамы, сестры, дочки);
- продолжительное лечение препаратами женских половых гормонов (5-6 лет);
- наличие предрасположенности к росту злокачественных образований (аномальные гены).
Протоковый рак молочной железы может появляться и у мужчин – носителей мутированного гена BRCA2.

Начальные и неинвазивные стадии протокового рака обнаруживают, как правило, случайным образом, при профилактическом осмотре или плановом УЗИ.
Инвазивный протоковый рак молочной железы может проявляться некоторыми симптомами, на которые пациентка может обратить внимание самостоятельно:
- обнаруживаются плотные или шишковидные участки в молочной железе, которые можно прощупать. Такие уплотнения не исчезают, а только увеличиваются со временем в размерах;
- на кожных покровах груди появляются участки с измененным цветом, структурой;
- одна из молочных желез приобретает другие очертания, изменяется её форма и контуры;
- наблюдаются изменения в области одного из сосков. Это может быть появление красноты, изменение формы и втянутость соска, формирование чешуек и язвочек в околососковой области;
- при надавливании, либо самостоятельно, из млечных протоков появляются выделения различного характера (с кровью, с гноем или светлые, в зависимости от стадии процесса);
- появляется чувство наполненности и давления с одной из грудей.
Если женщина обнаруживает у себя хотя бы один из вышеперечисленных симптомов, то ей следует непременно обратиться к доктору для того, чтобы своевременно провести дополнительную диагностику молочных желез. Можно записаться на консультацию к гинекологу, маммологу или специалисту УЗИ.

Инвазивную форму протокового рака ещё называют инфильтрирующим раком, или карциномой молочной железы.
Инфильтрирующий протоковый рак молочной железы – это самый распространенный вид злокачественного образования груди. Такой рак встречается в 80% случаев онкологических заболеваний грудной железы.
От обычной неинвазивной формы инфильтрирующий рак отличается тем, что злокачественный процесс не ограничивается только лишь стенками млечного канала, а выходит за его пределы и поражает другие близлежащие ткани грудной железы.
Характерным признаком инвазивного рака считается достаточно плотная опухоль с «рваными» границами, не флюктуирующая (как бы «склеена» с ближайшими тканями). Сосок или вся околососковая зона чаще всего втягивается внутрь.
Зачастую на диагностических снимках в зоне новообразования обнаруживают небольшие, хаотично расположенные отложения извести в ткани (от 50 до 600 мкм). Такие отложения представляют собой результат некротического процесса в клетках с последующим пропитыванием омертвевших структур кальциевыми солями.
Новообразование при инвазивном протоковом раке молочной железы может иметь разные размеры и скорость развития, что зависит от особенностей злокачественных клеток в каждом конкретном случае.

Для того чтобы точно определить заболевание молочной железы, необходимо пройти определенный ряд обследований. Диагностика протокового рака молочной железы может включать следующие процедуры:
- Маммография – наиболее распространенный диагностический метод, представляющий собой рентген-исследование грудной железы. Точность данного обследования достигает 90-95%, даже при условии отсутствия визуальных и пальпаторных симптомов опухоли. Процедуру проводят при помощи специального рентген-аппарата, который позволяет осмотреть левую и правую молочную железу с двух ракурсов – фронтального и бокового. Маммографические аппараты последнего поколения имеют специальные стереотаксические компьютерные устройства, благодаря которым проводится точная пункция с последующей биопсией. Наличие современного аппарата практически гарантирует распознавание протокового рака в начальном периоде заболевания, а также значительно облегчает течение оперативного вмешательства. Правда, есть и некоторые ограничения для использования данного метода диагностики: большинство специалистов не советуют проводить маммографическое исследование молодым девушкам и женщинам до 50 лет, так как маммография – это разновидность рентгенологической процедуры, во время которой грудная железа принимает на себя пусть небольшое, но все-таки облучение.
- Термография – метод определения температуры кожных покровов груди. Дело в том, что здоровые ткани и ткани опухоли имеют разную температуру. Это объясняется тем, что в опухоли содержится большее количество мелких сосудов, которые выделяют тепло и легко обнаруживаются термографом. Правда, данный метод не слишком популярен: его погрешность в определении злокачественных процессов все же очень велика.
- Метод светового сканирования – это усовершенствованный вариант диафаноскопии (осмотра тканевого просвета). Процедура основана на инфракрасном просвечивании тканей железы. Метод не очень распространен ввиду слабой чувствительности и сложности дифференцировки заболеваний.
- УЗИ – второй по популярности метод (после маммографии). Процедура довольно быстрая, безвредная и достаточно информативная: предоставляет исчерпывающие данные о злокачественном процессе, его расположении, размерах и формах. УЗИ разрешено использовать в любом возрасте неограниченное количество раз.
- Дуктография (галактофорография, либо контрастное маммографическое исследование). Эту процедуру часто применяют при наличии отделяемого из млечных протоков. Специальную контрастную жидкость вводят в млечный канал, после чего делают снимок, который указывает на изменения по ходу протоков.
- Биопсия – изъятие небольшого элемента ткани опухоли на исследование. Ткань берется при помощи пункции – незначительного прокола тканей в области предполагаемого расположения опухоли. В дальнейшем изъятый элемент ткани рассматривают под микроскопом на предмет наличия в нем атипичных клеточных структур. Пункцию для биопсии делают не всегда: иногда ткань для исследования берут уже во время операции по удалению опухоли. Это делается для постановки заключительного диагноза пациенту.
В качестве дополнительных исследований может использоваться МРТ и компьютерный метод томографии, сканирование костной системы и пр.

источник
Рак протоков в молочной железе — одно из наиболее опасных заболеваний. Зачастую появляется онкологическое неинвазивное новообразование. Раковые протоки могут воздействовать на всю железу, занимать большую площадь, либо несколько зон. Для этой патологии характерно разрастание ткани путём деления клеток. Протоковый рак молочной железы нередко начинается незаметно и женщине трудно определить болезнь самостоятельно.
Протокарцинома отличается от иных типов злокачественных опухолей в груди тем, что она начинает формироваться от внутренних стенок молочных каналов, не задевая лепестков и иных материй железы.
Классификация форм опухоли:
- Прединвазивная форма — внутрипротоковый рак груди. Рак диагностируют, когда он вырастает в протоках, не пробираясь в иные органы и материи. Эта форма — исходная ступень опухоли. Если формирование осложнений минимально, признаки заболевания не проявляются. Поэтому диагностика на раннем этапе весьма затруднительна. Однако, если болезнь выявлена на этом этапе, то прогноз довольно благоприятный.
- Инвазивная форма или инфильтративный протоковый рак груди. Диагностируется ориентировочно в 80% рака груди. Под воздействием провоцирующих его факторов, увеличивается вероятность быстрого прогрессирования и метастазирования в другие органы.
Основным элементом, определяющим развитие рака под воздействием провоцирующих факторов в организме женщины, является время. Поэтому возраст женщины является основным фактором риска. Точные причины рака груди трудно установить, однако есть ряд неблагоприятных условий, которые могут стать своего рода катализатором.
Можно выделить следующие причины развития болезни:
- Значительный возраст женщины. Угроза формирования карциномы существенно возрастает после 40-45 лет, когда месячный цикл прекращается.
- Генетическая склонность. В случае если бы у близких членов семьи по женской линии (в особенности мамы и бабушки) был диагностирован рак, угроза их формирования в последующем поколении существенно увеличивается.
- Поздние роды в 35-40 лет, а кроме того абсолютное отсутствие беременности.
- Несколько абортов и сильная после них менструация.
- Раннее начало полового созревания у девочек может вызвать злокачественное образование.
- Поздний климакс. Чем позднее менструальный цикл прекратится, тем более проявленным и негативным будет влияние гормонального фона на ткани груди.
- Карцинома способна сформироваться вследствие долгого употребления гормональных веществ (более 5-6 лет последовательно может вызвать расстройство в организме).
- Генетические дисфункции, такие как присутствие модифицированных либо мутированных генов в коде ДНК.
На начальной стадии опухоли чаще всего не имеют симптоматики. В редких случаях женщина сама может выявить симптомы внутрипротокового рака молочной железы. Однако обычная медицинская картина карциномы, к сожалению, видна на поздней стадии формирования. В поданном случае признаки больше не зависят от того, росли опухолевые клетки внутри каналов или в железистой материи.
Часто случаются следующие признаки:
- видоизменяется строение кожи, принимая форму лимонной цедры
- существует ретракция установленной области кожи
- есть проявление симметрии желез, в том числе сосков
- в груди есть скиррозное уплотнение, что хорошо чувствуется сидящей и лежащей женщиной
- есть течение жидкости из сосков
- могут распространяться покраснения кожи
Именно потому, что все такие перемены становятся видны в наиболее тяжелых степенях, доктора чаще заявляют о сложной самодиагностике протоковой конфигурации. Маммография — это недорогой метод выявления рака железы, и выявить наличие болезни можно прежде, чем новообразование начнет разрастаться в тканях. На этом шаге можно сберечь собственную грудь, удалив пораженную область. Если вовремя не обратиться к врачу, то прогноз рака протоков молочных желез будет неутешительным.
Как правило болезнь не возникает и не раскрывается сразу в физических проявлениях. Тем не менее, небольшое число женщин может иметь опухолеподобное формирование либо выделения из сосков, что подтверждает заболевание.
Чаще всего новообразование протоков выявляется при маммограмме. Проблема в том, что клетки умирают, не успевая целиком обновиться, возникают микрокальцинаты. Микрокальцификация может быть показана при маммографии. Точность этого осмотра достигает 90-95%. Также проводят УЗИ. В случае если итоги скрининга рассматриваются доктором как сомнительные, последующим шагом в диагностике карциномы является биопсия.
В эпизоде карциномы протоков производятся минимум две инвазивные биопсии:
- Биопсия малой иглой. В этом случае тонкую долгую иглу вводят в толщину раковой сомнительной сферы ткани груди. Шприц накачивает незначительную часть материи, после этой операции нет рубцов.
- Биопсия толстой иглой. Это инъекция иглы наибольшего диаметра дольковой части и забор наибольшего числа материи из сомнительных сфер. Оставляет незначительный след, но через несколько месяцев он становится практически невидим.
После этого образцы исследуются под микроскопом и выявляются характеристики. Как правило, количество материи, что берется во время биопсии, является необходимым для выполнения клинической диагностики.
Чаще всего, терапия карциномы протоков состоит в удалении опухоли груди с последующей терапией лучами. Протокол лечения рака молочной железы зависит от персональных особенностей пациента. Лечить болезнь должен специалист.
Могут проводиться разные операционные методы для удаления новообразований. Как правило это:
- лампэктомия — удаляется лишь часть молочной железы, в которой расположена опухоль и небольшой объем нормальной ткани
- резекцию (рассечение) — удаляется сектор молочной железы, в котором локализована опухоль
После лампэктомии либо вторичной резекции материи как правило назначают лучевую терапию. Она не проводится, если у женщин весьма незначительный риск возобновления.
Лучевая терапия может проводиться двумя методами:
- методическое облучение всей груди
- частичное облучение груди
Химиотерапевтическое лечение карциномы — один из элементов комплексного лечения. Его сущность состоит в назначении больным цитотоксических веществ, которые ингибируют формирование опухоли и рушат опухолевые клетки в груди. Химиотерапия рака груди может использоваться как независимый способ, а также перед и после операции. В обоих случаях химиотерапия имеет различные цели.
При применении химиотерапии в период подготовки к хирургическому воздействию карциномы груди цитотоксические препараты могут помочь сократить воспаление и новообразование. Это дает возможность подкреплять здоровую ткань груди. Послеоперационная химиотерапия помогает остановить метастазы и избежать рецидива.
Грудь считается весьма восприимчивой к влиянию отдельных гормонов, которые контролируют увеличение и формирование клеток, являющихся главными элементами абсолютно всех тканей организма. Итогом их воздействия считаются стабильные позитивные изменения в материи молочной железы.
Гормональную терапию относят к системному методу устранения рака. Это значит, что вещества (гормоны) проявляют огромное воздействие на организм поступательно. Лечебные средства используются для лечения гормонально-положительного рака либо рецидивирующего состояния. Онкологическая терапия отличается от заместительной гормональной терапии для менопаузы.
Целью гормонотерапии микропрепаратами считается устранение онкологических клеток уже после первого хирургического вмешательства, и других способов лечения. Для конкретных пациентов с гормоно-положительным раком груди терапия так же существенна, что и другие процедуры. Практически, гормональное лечение может быть более эффективно, чем химиотерапия. В зависимости от определенного случая лечение применяется совместно или в комплексе с химиотерапией.
Нет таких методов, которые гарантированно защитят от рмж. Однако, благодаря современным способам лечения и диагностики, вполне возможно восстановить здоровье, несмотря на негативную статистику в общем. Ведущие международные клиники благополучно справляются даже с наиболее сложными случаями неинвазивной опухоли в молочной железе.
При любых подозрениях на новообразование необходимо обратиться к врачу, иначе прогноз будет неутешительный. Профилактика онкологии молочной железы включает в себя любые действия, обращённые на снижение рисков развития карциномы.
Важно помнить, что рак лечится. Отзывы и непосредственные описания с фото многих людей говорят об эффективности лечения.
источник
Инфильтративная форма рака молочной железы — это злокачественное новообразование, которое развивается из атипичных эпителиальных клеток ее протоков и/или ткани долек. Злокачественные клетки достаточно быстро распространяются в соседние ткани и с током лимфы и крови — в лимфоузлы и различные органы. Этот тип рака является одной из самых неблагоприятных форм в плане метастазирования и агрессивности течения.
Рак груди среди злокачественных новообразований у женщин находится на первом месте и составляет около 20%, причем число случаев с 1985 года постоянно растет. Злокачественные опухоли все чаще выявляются среди молодых женщин и даже девушек подросткового возраста. Особенностью инфильтративного рака является и длительное сохранение раковых клеток после лечения скрытых (неактивных) метастазов, способных рецидивировать на протяжении 10 лет.
Существуют различные теории развития этого патологического процесса. В их основе лежит, преимущественно, представление о накоплении на протяжении жизни клеточных повреждений, в результате которых происходят мутация клеточной ДНК и стимуляция пролиферации поврежденных клеток.
Это происходит на фоне сложного взаимодействии эндокринной и иммунной систем, на фоне избыточной продукции эстрогенов, оказывающих влияние на трансформированные под действием канцерогенных факторов клетки. Однако конкретные причины и механизмы развития не установлены.
Основными факторами риска заболевания раком груди являются:
p, blockquote 8,0,1,0,0 —>
- 50-летний и более возраст женщины;
- отсутствие родов или их наличие в 30-летнем и более возрастном периоде;
- поздний менопаузальный период (после 50 лет);
- наличие в семье, особенно у ближайших родственников, рака груди или яичников и/или наличие у женщины в прошлом этой патологии;
- атипичный характер гиперплазии ткани органа, выявленный в результате биопсии;
- характер питания и избыточная масса тела; многими исследованиями подчеркивается определенная связь заболевания с избыточным употреблением жиров животного происхождения, а также с дополнительным синтезом жировой клетчаткой (при ожирении) эстрогенов;
- наследование мутированных генов-супрессоров роста опухолей молочной железы (гены BRCA).
Выделяют следующие клинико-гистологические формы инвазивной опухоли груди:
p, blockquote 9,0,0,0,0 —>
- Отечную.
- Протоковую.
- Дольковую.
- Неспецифическую.
Встречается в двух разновидностях:
p, blockquote 11,0,0,0,0 —>
- первичной, или истинной (диффузной);
- вторичной, или узловой.
Регистрируется относительно редко и составляет около 2% всех злокачественных новообразований молочной железы. С самого начала она проявляется признаками воспаления — отечностью и увеличением объема органа, покраснением кожи в виде «языков пламени» или подобным рожистому воспалению.
В месте покраснения отмечается повышение кожной температуры, симптом «лимонной корки» (характерные втяже6ния), диффузное (распространенное) уплотнение тканей молочной железы в этой области. Характерным является и отсутствие самой опухоли как при пальпации, так и при маммографическом исследовании.
При вторичной форме отечно-инфильтративного рака груди развитие инфильтрации и отека происходит постепенно. Наряду с вышеперечисленной симптоматикой на маммограмме и, нередко, пальпаторно определяется опухолевой узел. Его величина и темпы роста различны, однако после появления отека железы клиническое течение патологического процесса, включая и характер метастатических процессов, приобретают такую же агрессивность, как и в случае первичного варианта.
Ранние метастазы, что характерно для отечно-инфильтративной формы, выявляются у 95% пациентов, из которых в среднем у 35% — это метастазы в надключичные лимфоузлы. В соответствии со статистикой к моменту установления диагноза в среднем у 32,5% больных пациентов в отечно-воспалительный процесс вовлечена вся молочная железа, что является плохим прогностическим признаком. Кроме того, для этих форм свойственно отсутствие какого-либо определенного гистологического варианта.
Является наиболее распространенной (около 80%) формой в числе всех злокачественных новообразований груди. Чаще встречается среди женщин старших возрастов.
Он характеризуется множеством типов морфологической структуры и развивается из эпителиальных клеток молочных протоков, но затем способен распространяться на остальные ткани. Эта форма макроскопически представляет собой плотный овальный узел с неровными звездчатыми очертаниями, спаянный с окружающими тканями. Его наибольший диаметр может составлять от 0,5 до 10 см. Внутри узла возникают некротические участки, в результате чего формируются кистозные образования, и отложение кальциевых солей (микрокальцинаты).
Длительное время опухоль ничем себя не проявляет и не определяется пальпаторно. Со временем в процессе роста она достигает ареолы или соска, что приводит к деформации или втяжению последнего, а также к появлению из него выделений, имеющих различный характер, как по консистенции, так и по цвету. Возможно формирование симптома «лимонной корки». Основные гистологические варианты опухоли: высокодифференцированная, низкодифференцированная, наиболее опасная в плане рецидивирования и метастазирования, и промежуточная.
Составляет до 10% всех инфильтрирующих опухолей груди. Чаще встречается в пожилом возрасте, причем у половины больных имеет симметричное двухстороннее расположение. Наиболее частая локализация — верхний наружный квадрант железы.
Опухоль развивается из молочных долек, безболезненна, имеет неровные контуры и плотную консистенцию. На поздних стадиях развития она приводит к втяжению и сморщиванию кожи и метастазирует в яичники и в матку.
Включает очень редкие формы инвазивных опухолей (плоскоклеточная метаплазия, листовидная опухоль, папиллярный рак, коллоидная форма и др.), не имеющие специфической морфологической картины, а также те случаи заболевания, которые из-за низкой клеточной дифференцировки вызывают затруднения в выводах патоморфолога.
В зависимости от поражения лимфоузлов различают распространенность опухоли:
p, blockquote 26,0,0,1,0 —>
- 1 степени, когда поражены от 1 до 3 лимфоузлов в подмышечной области или увеличены окологрудинные лимфоузлы;
- 2 степени — раковые клетки распространились на 4-9 подмышечных лимфатических узла или увеличены лимфоузлы в грудной полости;
- 3 степени — наличие 10 и больше пораженных подмышечных лимфоузлов или распространение поражения на подключичные лимфоузлы.
Лечение инфильтративного рака молочной железы заключается в комплексной терапии. В неё входят:
p, blockquote 29,0,0,0,0 —>
- Хирургическое лечение.
- Применение химиотерапевтических средств в высоких дозах.
- Лучевая терапия.
- Гормональная терапия современными препаратами, включая инактиваторы и ингибиторы ароматаз (Летрозол, Анастрозол и др.), а также аналоги гормонов гипоталамуса (Трипторелин, Бусерелин и др.).
- Таргетная терапия.
Значительные разногласия вызывает хирургическое лечение отечно-инфильтративного рака молочной железы. Даже сочетание оперативного лечения с лучевой терапией являются недостаточными. Многие авторы предлагают использовать только симптоматическую терапию, поскольку существующие методы не предотвращают появление метастазов у 80% больных в те же сроки, что и при отсутствии лечения, а процент выживаемости в течение 5 лет при применении этих методов не превышает 5%.
В то же время, определенные обнадеживающие результаты получены при сочетании хирургического и/или лучевого метода с, так называемым, неоадъювантным химиотерапевтическим воздействием до операции. Основными целями последнего являются уменьшение величины опухоли и степени ее биологической активности, обеспечение условий для оперативного лечения и лучевого воздействия, а также для увеличения возможности предотвращения рецидивов и метастазирования.
На прогноз при инфильтративном раке молочной железы во многом влияет его форма и степень распространенности опухоли, то есть стадия заболевания. Так, например, 5-летняя выживаемость при первой стадии рака в среднем составляет 70-94%, при второй — 51-74%, при третьей — 10-51%, при четвертой — менее 11%.
Для отечно-инвазивной формы заболевания характерно очень агрессивное, быстрое течение клинического процесса. От времени появления первых симптомов до момента обращения к специалисту обычно проходит в среднем до 2-х месяцев. К этому времени у 95% больных уже обнаруживаются метастазы в регионарных лимфоузлах, а у 30-55% — в отдаленных органах.
Итак, диагностика и лечение злокачественного новообразования на ранней стадии способны значительно увеличить сроки выживаемости.
p, blockquote 34,0,0,0,0 —> p, blockquote 35,0,0,0,1 —>
источник
Тотальная мастэктомия (ТМ) может выполняться с одномоментной реконструкцией или без таковой.
Наиболее существенным современным достижением в реконструкции молочных желез является мастэктомия с сохранением кожного покрова, при которой ТМ, включая комплекс соска и ареолы, выполняется через периареолярный разрез.
Крупные ретроспективные исследования не показали увеличения частоты местных рецидивов рака молочной железы.
Хотя вмешательства с сохранением комплекса ареолы и соска исследуются применительно к протоковому раку (ПР) in situ, к настоящему времени доступны только ограниченные данные относительно местного рецидивирования (примерно 3-5%). Лимфаденэктомия подмышечных лимфатических узлов не является необходимой в лечении большинства пациенток с ПР in situ, поскольку частота метастазирования в лимфатические узлы при чистом протоковом раке in situ составляет всего лишь 0-1%.
Применение органосохраняющего хирургического вмешательства (ОСХВ) остается спорным и должно рассматриваться в контексте клинических испытаний. Клинически подозрительные лимфатические узлы и хирургически удаленные сторожевые лимфатические узлы следует подвергать гистологическому исследованию с приготовлением препаратов методом мазков-отпечатков или замороженных срезов.
Положительный результат исследования должен приводить к завершению первоначального вмешательства лимфаденэктомией лимфатических узлов уровня. Такой подход особенно эффективен в случаях, когда планируется одномоментная реконструкция молочной железы.
Ключевым для исходов органосохраняющих методов лечения (ОМЛ) является скрупулезное иссечение опухоли в пределах здоровых тканей с одновременным достижением приемлемого косметического результата. Выявляемые маммографически непальпируемые образования иссекают после дооперационного установления локализации патологии путем установки проводника при помощи визуализирующих методов исследования.
Точность иссечения можно улучшить за счет обозначения границ крупных образований проводниками. Точное расположение кончика проводника оценивается путем триангуляции с помощью маммографии в двух проекциях, выполняемой после введения проводника. Изогнутый разрез кожи делают как можно ближе к кончику проводника, а чрезмерного туннелирования следует избегать.
Опухоль предпочтительнее удалять одним блоком, пользуясь для точной анатомической ориентации скобками, узелками или шестицветной схемой окрашивания края резекции. Такое окрашивание крайне важно для точного анализа края резецированных тканей и значительно облегчает повторное иссечение.
Рекомендуется дополнительное иссечение краев для того, чтобы избежать выявления ложноположительных краев резекции при использовании систем окраски и для уменьшения частоты повторного иссечения. Рекомендуется выполнять интраоперационные мазки-отпечатки в качестве меры профилактики повторного иссечения по поводу обнаружения по краю резекции опухолевых клеток.
Частота повторного иссечения по поводу обнаружения по краю резекции или вблизи него (менее 1 мм) опухолевых клеток оценивается в 55%, а повторное иссечение обычно ухудшает косметический результат. Повторное сопоставление биопсийной полости и использование более совершенных онкопластических методик обеспечивает достижение лучшего косметического результата.
Хирург и рентгенолог должны взаимодействовать в использовании периоперационных рентгенографических методов для выполнения интраоперационной рентгенографии операционного материала. В то время как рентгенография образца не позволяет адекватно определить полноту удаления опухоли, увеличение изображения в двух проекциях усиливает разрешение изображения и может помочь в выявлении микрокальцификатов (или объемных образований), распространяющихся за пределы края резекции. После этого резекция может быть завершена.
Рентгенография операционного материала должна сопровождать гистологическое исследование, чтобы помочь в точном взятии образца патологических изменений. Исследование замороженных срезов иссеченных образцов не рекомендуется, поскольку атипичная протоковая гиперплазия (АПГ) или ПР in situ могут быть неразличимы на таких срезах, мелкие очаги микроинфильтрации могут быть пропущены. Металлические скобки следует размещать в операционной ране, чтобы помочь точно определить опухолевое ложе для адъювантной лучевой терапии на область молочной железы.
Подвергшимся простой (тотальной) мастэктомии пациенткам, которые не подлежат одномоментной реконструкции, устанавливают дренаж по Бюлау, удаляемый, когда объем отделяемого уменьшается до уровня ниже 30 мл/сутки.
При ОМЛ дренирование требуется редко. Ведение после одномоментной реконструкции основывается на типе реконструктивного вмешательства, при этом методики перемещения тканей требуют более тщательного наблюдения за жизнеспособностью перемещенных тканей.
Частота рецидивов после мастэктомии составляет 0-2%, тогда как при органосохраняющих методах лечения регистрируемая частота варьирует от 10% до 40%. Критическим для оптимального ведения пациенток, подвергающихся ОМЛ, является минимизация риска местного рецидива. Факторы, приводящие к местному рецидиву, многообразны и включают технические, связанные с опухолью, и связанные с пациенткой факторы, играющие роль в местном рецидиве после органосохраняющих методов лечения.
Основным техническим моментом местного устранения опухоли является ее удаление в пределах здоровых тканей — адекватный край опухоли, который представляет собой расстояние между протоковыму раком in situ и краем удаленного блока тканей. Послеоперационная маммография и состояние края равнозначны в отношении оценки полноты иссечения.
Поскольку ПР in situ лишен инфильтрирующей и метастатической способности, полное иссечение опухоли должно приводить к излечению. До второй половины 1980-х годов не существовало стандартизированных методов оценки тканей края резекции. В этой связи в ранних исследованиях не удалось продемонстрировать, что состояние края резекции является значимым фактором в отношении местного устранения опухоли.
Сильверштейн (Silverstein) опубликовал ретроспективный анализ влияния ширины края на местный рецидив при протоковом раке in situ по сведениям из проспективной базы данных. Пациенток распределяли в группы по ширине края резекции (более 10 мм, 1-9 мм и менее 1 мм). У пациенток с краем резекции свыше 10 мм добавление к лечению лучевой терапии не снижало частоту рецидивирования, при этом расчетная вероятность рецидива к 8 годам после операции составляла 4%.
Однако статистическая достоверность для выявления различий в этой группе была низкой. В группе 1-9 мм к 8 годам частота местного рецидива равна 20% без адъювантной лучевой терапии и 12% с лучевой терапией (p не определялось).
Кроме того, облученные образования были существенно больше и с большей вероятностью имели угревидные некрозы, а также наблюдались в дальнейшем на 20 месяцев дольше по сравнению с группой, в которой лучевая терапия не проводилась. Последующие проспективные исследования этой благоприятной в отношении прогноза группы не смогли подтвердить низкую частоту рецидивирования у пациенток, лучевая терапия которым не проводилась.
ПР in situ с краем резекции менее 1 мм приводил к статистически значимому снижению частоты рецидивирования с 58% до 30% при дополнении лечения лучевой терапией. Однако это не имело клинического значения, поскольку обе частоты обладали слишком высоким значением для органосохраняющих методов лечения.
Работа Холланда (Holland) и др. продемонстрировала, что ПР in situ может иметь отстоящие от основной опухоли образования размером до 10 мм или более, что также поднимает вопрос об адекватности края резекции в пределах 1-2 мм. В настоящее время идет включение пациенток в проспективные протоколы (исследования RTOG 98-04 и ECOG E-5194), в которых будет оцениваться изолированное применение иссечения опухоли у отдельных пациенток.
Длительное время признаки некроза при гистологическом исследовании ПР in situ ассоциировались с неблагоприятным прогнозом и более высокой частотой рецидивов. Лишь недавно было установлено, что клеточная архитектура и степень полиморфизма ядер оказывают влияние на местный рецидив более прогнозируемо, чем только угревидный некроз.
Рецидивы в группе низкодифференцированных опухолей возникают значительно раньше, чем в группе высокодифференцированных опухолей или с промежуточной степенью дифференцировки. Солин (Solin) зафиксировал, что 5-летняя частота рецидивирования составляет 12% при низкодифференцированных опухолях, по сравнению с 3% при высокодифференцированных, однако 10-летняя частота рецидивирования не различалась статистически и составляла 18% и 15% соответственно.
Это указывает на различия по времени прогрессирования, а не на различия в самой способности к рецидивированию. Размер опухоли, подобно ширине края резекции, отражает распространение опухоли и способность хирурга адекватно иссечь протоковый рак in situ.
Сильверштейн (Silverstein), используя прогностические факторы — степень полиморфизма ядер и угревидного некроза вместе с размером опухоли и шириной края резекции, разработал USC/VNPI. Этот индекс выявляет подгруппы пациенток, у которых в случае выбора в качестве метода лечения ОМЛ не требуется проведение лучевой терапии.
В табл. 4.1 описана система USC/VNPI с общей оценкой по трем показателям для каждого прогностического фактора — от наименьшего значения, равного 4, до наибольшего, равного 12.
Таблица 4.1. Шкала оценки прогноза USC/Ван-Найса.
источник
В странах с развивающейся экономикой карцинома, то есть злокачественное образование молочных желез, — самая частая опухоль, несущая опасность для жизни женщины. В государствах с развитой системой здравоохранения, где имеется система профилактики заболевания, например, в США, эта опухоль занимает сейчас 2-е место по встречаемости среди населения женского пола, а на 1-е выходит рак легкого.
Часто карцинома в начале заболевания никак себя не проявляет. Неприятные ощущения в молочной железе обычно сопровождают другие заболевания. Нередко опухоль обнаруживается сначала на рентгеновском снимке – маммограмме, а уже затем определяется пациенткой или медицинским работником.
Распознавание карциномы основано на осмотре, маммографии или ультразвуковом исследовании (УЗИ) и на пункционной биопсии. Улучшение информированности общества и оптимизация скрининга приводят к большей выявляемости карциномы на раннем этапе, когда операция имеет наивысшую эффективность. Эти факторы приводят к постепенному удлинению продолжительности жизни пациенток с опухолевым заболеванием.
Главные способы лечения карциномы грудной железы – хирургический и лучевой. Они нередко дополняются гормональными лекарствами и химиотерапией. При ранней стадии рака нередко проводится только операция и местное облучение тканей железы.
При наличии микрометастазов используется адъювантная терапия. Она может вызвать снижение смертности на 30-70%.
За прошедшие три десятилетия постоянное изучение карциномы помогло лучше понять заболевание. Появились целенаправленные и менее токсичные методы терапии.
По-прежнему важную роль играет обучение пациентов, периодическое прощупывание молочных желез и ежегодное рентгенологическое исследование.
Женские молочные железы расположены на передней поверхности грудной клетки. Они лежат на большой грудной мышце и удерживаются связками, прикрепляющимися к грудине. Железа включает около 20 долей, располагающихся секторально. Жировая ткань, покрывающая доли, создает форму груди. В каждой доле имеется большое количество мелких долек, заканчивающихся железами, способными секретировать молоко при соответствующей гормональной стимуляции.
Грудь, как и любой орган, состоит из множества микроскопических клеток. Они упорядоченно размножаются: новые клетки заменяют погибшие. При раке клетки размножаются бесконтрольно, их становится больше, чем в норме. Во время своей жизнедеятельности они выделяют большое количество отравляющих веществ, отрицательно влияющих на состояние всего организма. Опухолевые клетки по сосудам распространяются в другие органы, где также образуют очаги карциномы со сходным микроскопическим строением.
Рак железы чаще всего начинается изнутри молочных долек (дольковая карцинома) или протоков, через которые выводится молоко (протоковая карцинома). Иногда развивается бифазная карцинома молочной железы, при которой микроскопические свойства объединяют инвазивную дольковую и инвазивную протоковую формы.
Что такое карцинома молочной железы?
Это опухоль груди со злокачественным течением, характеризующаяся изменениями органа на уровне клеток. Они приводят к неконтролируемому размножению и практически бессмертию клеток, выстилающих дольки и протоки железы.
Изучение генетики этих клеток подтвердило, что имеются молекулярные подтипы болезни с определенными особенностями развития и проявлениями. Число молекулярных подтипов еще не установлено, но они, как правило, соотносятся с наличием рецепторов эстрогенов (РЭ), рецепторов прогестерона (РП) и рецептора 2 типа человеческого эпидермального фактора роста (ЭФР 2).
Такой взгляд на патологию – не как на совокупность случайных мутаций, а как на набор отдельных болезней, имеющих разное происхождение – изменил представления о причинах карциномы, типоспецифических провоцирующих факторах и значительно повлиял на формирование современных представлений о лечении заболевания.
В зависимости от генетических нарушений различают 4 основных подтипа болезни:
p, blockquote 18,0,0,0,0 —>
- Люминальная А.
- Люминальная В.
- Базальная.
- ЭФР 2-положительная.
Люминальная А:
p, blockquote 19,0,0,0,0 —>
- самый частый подтип;
- менее агрессивная;
- хороший прогноз;
- хороший ответ на гормоны;
- учащается с возрастом;
- РЭ + и/или РП +, ЭФР -.
Люминальная В:
p, blockquote 20,0,0,0,0 —>
- похожа на подтип А, но с худшим прогнозом;
- более часто РП -;
- РЭ + и/или РП +, ЭФР +.
p, blockquote 21,0,0,0,0 —>
- агрессивный подтип;
- высокая частота деления клеток;
- появляется до 40 лет;
- ЭФР +.
ЭФР 2 – положительная:
p, blockquote 22,0,0,0,0 —>
- довольно редкий, агрессивный подтип;
- появление до 40 лет.
Базальный подтип имеет сходные свойства с опухолью яичников, в том числе и на генетическом уровне. Это означает, что у них может быть общая причина. Существуют убедительные данные, что пациенты с базальной опухолью поддаются такой же терапии, как и при раке яичников.
Типы опухоли
p, blockquote 24,0,1,0,0 —>
- Инвазивная протоковая карцинома молочной железы – склонна к мигрированию по лимфатическим путям, составляет ¾ всех случаев рака. За прошедшую четверть века частота развития болезни увеличилась в два раза и сейчас достигла 2,8 случаев на 100 тысяч женщин. Наиболее опасный возраст – от 40 до 50 лет.
- Инфильтративная дольковая карцинома молочной железы имеется в 15% случаев прорастающей (распространяющейся) опухоли.
- Медуллярная карцинома молочной железы характерна для молодых пациенток, регистрируется в 5% случаев.
- Муцинозная карцинома молочной железы диагностируется менее чем в 5% случаев заболевания.
- Тубулярная карцинома молочной железы бывает в 1-2% всех злокачественных образований органа.
- Папиллярная карцинома молочной железы наблюдается в возрасте более 60 лет и составляет 1-2%.
- Метапластическая карцинома диагностируется редко, после 60 лет и наиболее характерна для представительниц негроидной расы.
- Болезнь Педжета развивается в среднем в 60 лет и составляет до 4% всех случаев.
При инвазивной карциноме раковые клетки прорастают за границы долек или протоков и проникают в близлежащие ткани. Они могут попадать в лимфатические узлы, а оттуда распространяться по всему организму, образуя метастазы. Неинвазивная карцинома еще не распространилась на окружающие ткани, ее еще называют раком «на месте», или in situ. В дальнейшем она превращается в инвазивный рак.
Для оценки агрессивности патологические ткани предложена гистологическая классификация, в которой используется обозначение g (Х-4), где gX – сложно определить структуру клеток, g1 и g2 – высокодифференцированные, постепенно увеличивающиеся опухоли, g3 и g4 – низкодифференцированные агрессивные образования.
Имеются факторы, увеличивающие вероятность заболевания. Они были выявлены с помощью крупных эпидемиологических исследований.
Инвазивная карцинома молочной железы преимущественно наблюдается у пожилых женщин. Заболеваемость имеет два пика: в 50 и 70 лет. Низкодифференцированная карцинома молочной железы развивается у более молодых пациенток, а опухоли, чувствительные к гормонам, растут постепенно и проявляются в более старшем возрасте.
Признанный фактор риска – наличие болезни у кровных родственниц. Если больны мать или сестра, вероятность опухоли у женщины возрастает в 4 раза, особенно если болезнь у родственницы была определена в возрасте до 50 лет. Если же больны 2 и больше ближайших родственниц, риск возрастает в 5 раз.
Если у ближайшей родственницы имеется рак яичников, вероятность карциномы удваивается. В этих случаях определяются молекулярные нарушения – изменения в генах brca 1 и brca2.
Также вероятность возникновения онкопатологии связана с наличием мутации таких генов, как PTEN, ТР53, MLH1, MLH2, CDH1 или STK11.
Генетическое исследование для выявления риска карциномы – быстро развивающееся направление, которое должно шире внедряться в нашей стране по примеру крупнейших государств. Оно включает определение вероятности болезни, генетическую консультацию и генетическое исследование для выявления опасных мутаций. На основе этих данных строятся современные представления о лечении и профилактике карциномы.
p, blockquote 35,0,0,0,0 —>
- первая беременность в возрасте после 30 лет;
- бездетность;
- раннее менархе;
- раннее прекращение менструаций.
Также на частоту опухоли влияет повышенный уровень женских гормонов, в частности, эстрадиола.
У женщин, использующих оральные контрацептивы, возможность карциномы груди выше на 25%. При их отмене риск постепенно снижается и спустя 10 лет сравнивается с общим по популяции.
Научные данные говорят о неблагоприятном влиянии заместительной гормонотерапии в постменопаузальном периоде. Риск увеличивается одновременно с продолжительностью применения. Наиболее высок он для таких форм, как дольковая, смешанная и протоковая — дуктальная карцинома молочной железы. С другой стороны, после ампутации матки применение эстрогенов в постменопаузе вызывает даже незначительное снижение риска. Поэтому назначение заместительной терапии гормонами должно быть строго индивидуальным.
Считается, что комбинированные препараты эстрогена и прогестерона не должны использоваться у пациенток с отягощенным семейным анамнезом или перенесших такую опухоль, как инфильтрирующая карцинома молочной железы. Довольно часто в этом случае возникает проблема лечения пациенток, страдающих от тяжелых проявлений климакса.
Более безопасны в этом отношении вагинальные формы эстрогенов. Доказательств безопасности и эффективности препаратов цимицифуги, витамина Е, пищевых добавок в этом отношении нет.
Перенесенная инвазивная карцинома молочной железы неспецифического типа в несколько раз повышает возможность появления рака в другой железе. Дольковое образование in situ (неинвазивная карцинома молочной железы) увеличивает риск до 10 раз.
Гиперплазия, папилломы увеличивают возможность болезни в 2 раза. Если же очаги гиперплазии имеют атипию (неправильно сформировавшиеся клетки), вероятность опухоли увеличивается в 5 раз, прежде всего у молодых пациенток, и в 10 раз при нескольких атипичных очагах, подтвержденных биопсией железы.
Мастопатия, фиброаденома, фиброзно-кистозные изменения и другие доброкачественные изменения не увеличивают риск карциномы.
Заболеваемость карциномой сильно различается в развивающихся странах и государствах с сильной экономикой. Общая закономерность такова, что в более бедных странах люди придерживаются питания, богатого злаковыми культурами, растениями, с малым уровнем животных жиров, калорийности и спиртных напитков. Это помогает защититься от рака многих органов: молочных желез, кишечника, простаты (у мужчин).
В постменопаузе увеличивается роль таких факторов риска, как:
p, blockquote 45,0,0,0,0 —>
- увеличение веса на 20 кг по сравнению с тем, что был в 18 лет;
- западный тип питания (высокая калорийность за счет жиров и очищенных углеводов, то есть сахара);
- гиподинамия;
- употребление спиртного.
Увеличивают вероятность опухоли груди:
p, blockquote 46,0,0,0,0 —>
- активное и пассивное курение;
- употребление жареных продуктов;
- действие пестицидов, ионизирующей радиации и пищевых эстрогенов;
- лучевая терапия по поводу других опухолей.
Первый признак карциномы — уплотнение в железе. Большинство таких участков не являются злокачественными, однако при их появлении пациентка должна обратиться к врачу.
Среди ранних признаков карциномы можно отметить следующие:
p, blockquote 50,0,0,0,0 —>
- плотный узел в железе;
- ограниченная подвижность его в ткани;
- при сдвигании кожи обнаруживается втяжение ее над опухолью;
- безболезненность поражения;
- округлые образования в подмышечной впадине.
Медицинскую консультацию также необходимо получить при наличии таких симптомов:
p, blockquote 51,0,0,0,0 —>
- болезненность в области груди или под мышкой, не связанная с менструальным циклом;
- изъязвление или сильное покраснение кожного покрова, вид «апельсиновой корочки»;
- высыпания в околососковой области;
- отечность или опухоль в одной из подмышечных областей;
- чувство утолщения тканей груди;
- ненормальное отделяемое из соска, иногда кровянистое;
- нарушение формы сосковой зоны, его втяжение;
- изменение размеров или форм груди;
- отслоение, шелушение кожного покрова железы и ареолы.
Карцинома обычно распознается во время скрининга или при появлении симптомов. Если женщина обнаружила у себя один из перечисленных выше признаков, она должна обратиться к врачу-маммологу или гинекологу. После необходимого обследования специалист решит, нужна ли пациентке консультация онколога.
p, blockquote 54,0,0,0,0 —>
- Осмотр. Врач осматривает обе груди пациентки, обращая внимание на уплотнения и другие нарушения, такие как втянутый сосок, выделения из него или изменения кожи. При этом пациентке предлагают поставить руки на пояс, затем завести их за голову. Проверяются подмышечные области, зоны над и под ключицами.
- Рентгенологические исследование – маммография. Обычно она используется для скрининга карциномы в возрасте от 40 лет. В некоторых случаях маммография дает ложноположительные результаты, то есть обнаруживает очаги, на самом деле являющиеся безвредными образованиями.
- Для повышения диагностической точности наряду с обычной двухмерной сейчас в крупных центрах применяют трехмерную маммографию. Этот метод более чувствителен и позволяет избежать ложноположительных данных.
- Ультразвуковое исследование более информативно у женщин до 40 лет. Оно помогает отличить карциному от другого образования, например, кисты.
- Биопсия. Если обнаружены патологически измененные ткани, они удаляются хирургическим путем и отправляются в лабораторию для анализа. Если клетки оказываются злокачественными, специалисты лаборатории определяют тип рака и степень его злокачественности. Для повышения точности диагностики лучше брать образцы из нескольких участков опухоли.
- Магнитно-резонансная томография помогает определить стадию заболевания и оценить поражение лимфоузлов и отдаленных органов.
Стадия новообразования определяется в зависимости от размера опухолевого узла, его инвазивности, поражения лимфатических узлов и распространения в другие органы. Стадия описывается согласно классификации TNM, где T – описание образования, N – вовлечение лимфатических узлов, М – метастазы.
В частности, при 2 степени имеется опухолевое образование с поражением подмышечных лимфоузлов. В 3 стадии определяются крупные размеры образования. В 4 стадии есть метастазы. В зависимости от определенной стадии назначается лечение.
В лечении пациентки с карциномой принимают участие многие специалисты. В такую команду входит онколог, хирург, радиотерапевт, рентгенолог, специалист по гистологическим исследованиям, пластический хирург. Нередко в лечении участвуют психолог, диетолог, физиотерапевт.
При выборе наилучшего метода лечения учитываются такие факторы:
p, blockquote 60,0,0,0,0 —>
- тип карциномы;
- стадия опухоли, то есть ее распространенность и метастазирование;
- чувствительность раковых клеток к гормонам;
- возраст и состояние пациентки;
- предпочтения и пожелания пациентки.
Лечение карциномы молочной железы включает такие варианты:
p, blockquote 61,0,0,0,0 —>
- лучевое лечение (радиотерапия);
- хирургическое вмешательство (операция);
- биологическая терапия (таргетные, лекарственные средства целенаправленного действия);
- гормональные средства;
- химиотерапия.
p, blockquote 62,0,0,0,0 —>
- лампэктомия: извлечение опухоли и небольшого участка здоровой ткани вокруг нее; используется при небольшом размере образования; это органосохраняющая операция;
- мастэктомия – удаление груди; простая форма вмешательства сопровождается удалением долей и протоков, участков жира, соска и части кожного покрова; при расширенной удаляются также часть мышц и подмышечные лимфоузлы;
- биопсия узла – хирургическое удаление одного из лимфатических узлов и определение в нем раковых клеток; при их обнаружении может выполняться подмышечная лимфодиссекция – удаление всех подмышечных лимфоузлов;
- реконструктивная хирургия груди – ряд операций, направленных на воссоздание первоначальной формы железы, может проводиться одновременно с мастэктомией с использованием имплантов.
Многие онкологи считают диффузные формы рака (отечно-инфильтративную, панцирную, маститоподобную) неоперабельными. В этом случае на первый план выходит радиотерапия.
Врачи применяют дозы контролируемой радиации, направленные на карциному для разрушения ее клеток. Лечение назначается после удаления железы или химиотерапии для борьбы с оставшимися вокруг злокачественными клетками. Как правило, радиотерапию проводят спустя 4 недели после первичного вмешательства. Длительность воздействия составляет несколько минут, необходимо до 30 сеансов.
p, blockquote 66,0,0,0,0 —>
- действие на оставшуюся ткань органа после частичного удаления железы;
- действие на грудную стенку после удаления железы;
- увеличенные дозировки используются при большом размере органа;
- облучение лимфоузлов под мышками.
Неблагоприятные эффекты радиотерапии включают слабость, потемнение и раздражение кожи грудной клетки, лимфедему (лимфатический застой из-за повреждения соответствующих сосудов).
Для уничтожения злокачественных клеток назначаются цитостатические препараты. Адъювантная химиотерапия назначается при высоком риске рецидива опухоли или ее распространении в других частях организма.
Если опухоль большая, химиотерапию проводят до операции с целью уменьшить размер очага. Это неоадъювантная химиотерапия. Это лечение также назначается при метастазах, для уменьшения некоторых симптомов, а также для прекращения выработки эстрогенов.
Химиотерапия при инвазивной карциноме может вызвать тошноту, рвоту, отсутствие аппетита, слабость, выпадение волос, увеличение восприимчивости к инфекциям. У женщин может наступить ранний климакс. Многие из этих эффектов облегчаются лекарствами.
Это лечение помогает при РЭ- и РП-положительных формах карциномы. Цель лечения – предотвращение рецидива. Терапия назначается после операции, но иногда используется и до нее для уменьшения размера образования.
Если пациентка по состоянию здоровья не может перенести операцию, химио- или лучевую терапию, гормональное лечение может стать единственным видом помощи, который она получает.
Гормональная терапия не влияет на опухоли, не чувствительные к гормонам, то есть не имеющие РЭ или РП.
Лечение длится до 5 лет после операции и может включать:
p, blockquote 74,0,0,1,0 —>
- Тамоксифен, который предотвращает связывание эстрогена с РЭ в раковых клетках. Неблагоприятные эффекты: нарушение цикла, приливы, ожирение, тошнота и рвота, боли в суставах и голове, слабость.
- Ингибиторы ароматазы применяются у женщин в постменопаузе. Ароматаза способствует выработке эстрогенов в женском организме после завершения менструаций, а эти препараты (Летрозол, Экземестан, Анастрозол) блокируют ее действие. Неблагоприятные эффекты: тошнота и рвота, слабость, сыпь на коже, боль в конечностях и голове, приливы, потливость.
- Агонист гонадотропин-рилизинг фактора гозерелин подавляет функцию яичников. Месячные у пациентки прекращаются, но после завершения лечения этим препаратом возобновляются. Неблагоприятные эффекты: перепады настроения, проблемы со сном, потливость и приливы.
Таргетная терапия – это новое направление в лечении с использованием таргетных (целевых) препаратов:
p, blockquote 75,0,0,0,0 —>
- Трастузумаб (Герцептин) – это антитело, присоединяющееся к клеткам, имеющим ЭФР, и разрушающее их. Используется при ЭФР-положительных опухолях. Неблагоприятные эффекты: кожные высыпания, головные боли и/или патология сердца.
- Лапатиниб — этот препарат нацелен на белок ЭФР 2. Он также используется для лечения метастатического рака и при неэффективности Герцептина. Неблагоприятные эффекты: боли в конечностях, кожная сыпь, язвы во рту, повышенная утомляемость, диарея, рвота и тошнота.
- Бевацизумаб (Авастин) останавливает рост кровеносных сосудов в опухоли вызывая нехватку в ней питательных веществ и кислорода. Неблагоприятные эффекты: застойная сердечная недостаточность, гипертония, поражение почек и сердца, образование тромбов, головные боли, язвы в полости рта. Он не одобрен для такого использования, однако иногда все же назначается. Вопрос о его применении при карциноме остается спорным.
Существуют некоторые исследования, показывающие, что прием низких доз Аспирина может приостановить рост карциномы. Хотя результаты обнадеживающие, работа находится на очень ранней стадии, и еще не доказана эффективность такого лечения у людей.
Способы снижения риска появления карциномы:
p, blockquote 79,0,0,0,0 —>
- женщины, употребляющие не более одной порции спиртного в день или вообще не пьющие, менее подвержены риску заболеть;
- физические тренировки 5 дней в неделю снижают вероятность рака, однако если все же сохраняется избыточный вес, положительный эффект нагрузок исчезает;
- у женщин, употребляющих жирную морскую рыбу не менее раза в неделю или принимающих добавки с содержанием омега-3 жирных кислот, риск карциномы груди снижается на 14%;
- некоторые гормональные препараты в постменопаузе способны уменьшить вероятность болезни; это необходимо обсудить с лечащим врачом;
- нормальная масса тела – фактор снижения риска, поэтому диета при карциноме молочной железы направлена на снижение веса до нормы;
- у женщин с высоким риском, в том числе подтвержденным генетически, может назначаться профилактический прием лекарств (в частности, Тамоксифена) или даже проводиться удаление груди;
- грудное вскармливание ребенка в течение полугода снижает риск этого заболевания или отдаляет его развитие на несколько лет.
Достаточно важное значение придается ежегодному медосмотру и проведению профилактической маммографии у женщин старше 40 лет, хотя целесообразность этих мер широко обсуждается во врачебном сообществе.
Если у больной с карциномой возникает беременность, на ранних сроках часто показано прерывание. При более позднем сроке и жизнеспособности плода проводят досрочное родоразрешение. Затем лечение опухоли продолжают по обычным протоколам.
Показатели смертности от рака молочной железы постоянно снижаются. Это связано с прогрессом в ранней диагностике и совершенствованием способов лечения. Наибольшее снижение смертности регистрируется у женщин до 50 лет.
Факторы, от которых зависит прогноз болезни:
p, blockquote 84,0,0,0,0 —>
- состояние подмышечных лимфоузлов;
- размер опухоли;
- прорастание в лимфатические и/или кровеносные сосуды;
- возраст пациента;
- гистологический класс онкопатологии;
- подтип (тубулярная, муцинозная или папиллярная карцинома);
- ответ на терапию;
- статус РЭ/РП;
- наличие гена ЭФР 2.
Вовлеченность подмышечных лимфоузлов – показатель того, что опухоль распространяется в соседние органы. Если они не поражены, 10-летняя выживаемость равна 70%. При вовлечении лимфоузлов частота 5-летнего рецидива выглядит так:
p, blockquote 85,0,0,0,0 —>
- от 1 до 3 узлов – 30-40%;
- от 4 до 9 узлов – 44-70%;
- более 9 узлов – 72-82%.
Опухоли, имеющие рецепторы к эстрогенам и/или прогестерону, как правило, развиваются медленнее и реагируют на гормональную терапию. Эти рецепторы определяются с помощью иммуногистохимического анализа.
Ранее наличие ЭФР 2 считалось предвестником более агрессивного течения и худшего прогноза независимо от других факторов. Сейчас прогноз улучшился в связи с использованием целевых препаратов, действующих на ЭФР 2 (Трастузумаб, Пертузумаб, Лапатиниб, Трастузумаб-энтансин).
У 10-20% женщин с неинвазивной карциномой через 15 лет возникает инвазивный рак — неспецифическая карцинома молочной железы.
Инфильтративный протоковый – самый частый тип опухоли. Он склонен к распространению по лимфатическим сосудам. Инфильтративный дольковый рак тоже распространяется в лимфоузлы, однако у него есть склонность и к отдаленным метастазам. Тем не менее, его прогноз сопоставим с таковым при протоковой карциноме.
Медуллярная (аденогенная) карцинома молочной железы и атипичный медуллярный рак часто имеют неблагоприятный прогноз в связи с высокой степенью злокачественности.
Пациенты с муцинозной и трубчатой карциномой имеют хороший прогноз: их 10-летняя выживаемость составляет 80%. Вследствие этого больных с таким типом опухоли лечат с использованием органосохраняющих операций и облучения.
Кистозно-папиллярный рак растет медленно, с хорошими шансами на излечение. Однако прогноз ухудшается при микропапиллярной инвазивной дольковой карциноме, так как она нередко метастазирует в лимфоузлы.
При метапластическом раке трехлетняя выживаемость без рецидива составляет всего 15-60%. Прогноз ухудшается при большом размере опухоли.
Заболеваемость мужчин в 100 раз меньше, чем женщин. Опухоль может возникнуть на фоне увеличения желез (гинекомастии), но это не обязательное условие. Микроскопические характеристики рака такие же, как у женщин.
Население мало осведомлено о возможности такого заболевания. Поэтому мужчины нередко обращаются за помощью уже в запущенных случаях. Из-за этого у половины больных к моменту распознавания опухоли имеются язвы на коже груди, метастазы в лимфоузлы и отдаленные органы.
Клинические проявления характеризуются наличием за соском плотного образования, которое рано прорастает сквозь кожный покров и изъязвляется. Для лечения применяют операцию, облучение, химиопрепараты.
Большинство карцином у мужчин имеют рецепторы к эстрогенам и прогестерону, поэтому в течение 2 лет после операции пациентам назначают антиэстрогеновые препараты. При прогрессировании болезни показано удаление яичек с последующей терапией кортикостероидами или другими гормональными средствами.
p, blockquote 98,0,0,0,0 —> p, blockquote 99,0,0,0,1 —>
источник